Ναφθαλίνιο
| Προτείνεται το λήμμα με τίτλο «Ναφθαλίνιο» να μετακινηθεί υπό τον τίτλο «Ναφθαλένιο». Παρακαλούμε δείτε τη σχετική συζήτηση στη σελίδα συζήτησης του λήμματος. → (μετονομασία) |
| Ναφθαλίνιο | |||
|---|---|---|---|

| |||

| |||

| |||

| |||
| Γενικά | |||
| Όνομα IUPAC | Ναφθαλίνιο | ||
| Άλλες ονομασίες | Διμεθυλοδικυκλο[4.4.0](-1,3,5,7,Δ4α,8α-)δεκαπενταένιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C10H8 | ||
| Μοριακή μάζα | 128,17 amu | ||
| Αριθμός CAS | 91-20-3 | ||
| SMILES | c1cccc2c1cccc2 | ||
| InChI | 1S/C10H8/c1-2-6-10-8-4-3-7-9(10)5-1/h1-8H | ||
| Αριθμός EINECS | 214-552-7 | ||
| Αριθμός RTECS | QJ0525000 | ||
| PubChem CID | 931 | ||
| ChemSpider ID | 906 | ||
| Δομή | |||
| Διπολική ροπή | 0 D | ||
| Μοριακή γεωμετρία | επίπεδη | ||
| Ισομέρεια | |||
| Ισομερή θέσης | >100 | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | 78,2°C | ||
| Σημείο βρασμού | 217,97°C | ||
| Πυκνότητα | 1.145 kg/m³ (15°C) 1.025,3 kg/m³ (20°C) 962,5 kg/m³ (100°C) | ||
| Διαλυτότητα στο νερό |
19 g/m³ (10°C) 31,6 g/m³ (25°C) 43,9 g/m³(34,5°C) 80,9 g/m³ (50°C) 238,1 g/m³ (73,4°C) | ||
| Διαλυτότητα σε άλλους διαλύτες |
113 kg/m³ (25°C, EtOH) 131 kg/m³ (21,5°C, AcOH) 355 kg/m³ (21,5°C, CHCl3) 175 kg/m³ (25°C, C6H14) 221 kg/m³ (25°C, PrCOOH) | ||
| Ιξώδες | 0,964 cP (80°C) 0,761 cP (100°C) 0,217 cP (150°C) | ||
| Δείκτης διάθλασης , nD |
1,5898 | ||
| Τάση ατμών | 8,64 Pa (20°C) 23,6 Pa (30°C) 0,93 kPa (80 °C) 2,5 kPa (100°C) | ||
| Χημικές ιδιότητες | |||
| Ελάχιστη θερμοκρασία ανάφλεξης |
80°C | ||
| Σημείο αυτανάφλεξης | 525°C | ||
| Επικινδυνότητα | |||
   
| |||
| Εύφλεκτο (F) Ευαισθητοποιητής Πιθανό καρκινογόνο Εκκρηκτικά μείγματα | |||
| LD50 | 1.800 mg/kg (αρουραίοι, στοματική λήψη) 1.200 mg/kg (ινδικά χοιρίδια, στοματική λήψη) 533 mg/kg (ποντίκια, στοματική λήψη) | ||
| Κίνδυνοι κατά NFPA 704 |
|||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Το ναφθαλίνιο ή ναφθαλίνη[1] (αγγλικά naphthalene) είναι αρωματική οργανική χημική ένωση, που περιέχει άνθρακα και υδρογόνο, δηλαδή είναι αρωματικός υδρογονάνθρακας, με μοριακό τύπο C10H8. Πιο συγκεκριμένα, ανήκει στα αρένια, με δομή δυο συμπυκvωμένων (δηλαδή με κοινή πλευρά και δυο κοινά άτομα) βενζολικών δακτυλίων. Αποτελεί τον απλούστερο πολυκυκλικό αρωματικό υδρογονάνθρακα. Το χημικά καθαρό ναφθαλίνιο, στις κανονικές συνθήκες περιβάλλοντος, δηλαδή σε θερμοκρασία 25°C και υπό πίεση 1 atm, είναι λευκό κρυσταλλικό στερεό, με χαρακτηριστική οσμή, ανιχνεύσιμη (από τους ανθρώπους) μέχρι και σε συγκεντρώσεις της τάξης των 80 ppb, κατά βάρος[2]. Κυκλοφορεί στο εμπόριο κυρίως σε μορφή σφαιριδίων. Εξαχνώνεται εύκολα, ακόμη και στις συνθήκες δωματίου. Ο όρος ναφθαλίνιο επεκτείνεται και πέραν της «μητρικής» ένωσης και σε μια σειρά «θυγατρικών» παραγώγων αυτής, που ονομάζονται συλλήβδην ναφθαλίνια.
Ιστορία
[Επεξεργασία | επεξεργασία κώδικα]Στις αρχές της δεκαετίας του 1820, τουλάχιστον δυο χημικοί ανέφεραν ότι ένα (νέο για τότε), λευκό στερεό, με αποπνικτική οσμή μπορεί να απομονωθεί από τη λιθανθρακόπισσα. Το ονόμασαν «λευκή πίσσα». Το 1821 ο Τζον Κιντ (John Kidd) περιέγραψε πολλές από τις ιδιότητες της νέας (για τότε) ένωσης και κάποιες νέες (για τότε) μεθόδους παραγωγής της. Οι μέθοδοι αυτοί συμπεριελάμβαναν, μεταξύ άλλων, και την απομόνωσή της από τη νάφθα και γι' αυτό πρότεινε το όνομα «ναφθαλίνη»[3]. Ο χημικός τύπος του ναφθαλίνιου ανακαλύφθηκε από τον Μάικλ Φαραντέι (Michael Faraday) το 1826. Η δε δομή των δυο συμπυκνωμένων βενζολικών δακτυλίων πρωτοπροτάθηκε από τον Εμίλ Ερίενμέγιερ (Emil Erlenmeyer) το 1866[4] και επιβεβαιώθηκε από τον Καρλ Γκραμπ (Carl Gräbe), το 1869.
Δομή
[Επεξεργασία | επεξεργασία κώδικα]Το μόριο της ναφθαλίνης αποτελείται από ένα ζευγάρι συμπυκνωμένων βενζολικών δακτυλίων. Επομένως ανήκει στους πολυκυκλικούς αρωματικούς υδρογονάνθρακες (PAC: Polycyclic Aromatic Hydrocarbons). Υπάρχουν δυο ομάδες από ισοδύναμα μεταξύ τους άτομα υδρογόνου: η ομάδα «α», που αποτελείται από τα υδρογόνα #1, 4, 5 και 8, και η ομάδα «β», που αποτελείται από τα υδρογόνα #2, 3, 6 και 7 (όπως δείχνει το παρακάτω σχήμα):

Αντίθετα από ότι συμβαίνει στο βενζόλιο, στο ναφθαλίνιο οι δεσμοί C-C δεν έχουν όλοι το ίδιο μήκος και άρα δεν είναι ισότιμοι. Οι δεσμοί C1–C2, C3–C4, C5–C6 και C7–C8 έχουν μήκος περίπου 136 pm, ενώ οι υπόλοιποι 142 pm[5]. Αυτές οι διαφορές παρατηρήθηκαν με χρήση ακτίνων Χ. Αυτά τα δεδομένα οδήγησαν σε ένα μοντέλο δεσμολογίας σθένους και ειδικότερα στην εφαρμογή του θεωρήματος της σταυρωτής συζυγίας. Σύμφωνα με αυτό το θεώρημα, το ναφθαλίνιο μπορεί να θεωρηθεί ως μια αρωματική βενζολική μονάδα που είναι συνδεδεμένη σε ένα διένιο, αλλά όχι με εκτεταμένη συζυγία με αυτό, τουλάχιστον όχι στη θεμελιώδη κατάσταση. Ως τέτοια δομή, το ναφθαλίνιο έχει αρκετές δομές συντονισμού:

Φυσική παρουσία
[Επεξεργασία | επεξεργασία κώδικα]Εκτός από τη λιθανθρακόπισσα, ιχνοποσότητες ναφθαλινίου υπάρχουν σε ορισμένους τύπους ελαφίσιου κρέατος, καθώς επίσης και σε υπόγειους τερμιίτες της Φορμόζας[6]. Οι τερμίτες αυτοί παράγουν ναφθαλίνιο πιθανώς ως απωθητικό ενάντια σε μυρμήγκια, δηλητηριώδη φύκια και νηματώδεις σκώληκες.[7] Ακόμη, κάποιες ποικιλίες ενδοφυτικών φυκών Muscodor albus παράγουν ναφθαλίνιο ανάμεσα σε μια ποικιλία πτητικών οργανικών ενώσεων, ενώ τα Muscodor vitigenus παράγουν ναφθαλίνιο σχεδόν αποκλειστικά.[8]
Διαστημική παρουσία
[Επεξεργασία | επεξεργασία κώδικα]Το ναφθαλίνιο έχει ανιχνευθεί στο διαστρικό ενδιάμεσο στην κατεύθυνση προς το άστρο Περσεύς 52.[9][10] Πάνω από το 20% του άνθρακα στο σύμπαν μπορεί να συνδεθεί με πολυατομικούς υδρογονάνθρακες, που συμπεριλαμβάνουν το ναφθαλίνιο.[11]
Κατιόντα πρωτονιωμένου ναφθαλινίου {[C10H9]+} αποτελούν την πηγή για ένα μέρος του φάσματος των μη ταυτοποιημένων υπέρυθρων εκπομπών (UIRs: Unidentified InfraRed emissions). Το πρωτονιωμένο ναφθαλίνιο αποτελεί διαφορετικό χημικό είδος από το ουδέτερο ναφθαλίνιο (που χρησιμοποιείται για παράδειγμα στα γνωστά του σφαιρίδια), στο ότι περιέχει ένα επιπλέον άτομο υδρογόνου, αλλά και θετικό ηλεκτρικό φορτίο.
Με τη βοήθεια των UIRs ανιχνεύονται πρωτονιωμένα κατιόντα ναφθαλινίου από τους αστρονόμους. Αυτή η έρευνα δημοσιεύιθηκε με τον τίτλο "mothballs in space".[12]
Παραγωγή
[Επεξεργασία | επεξεργασία κώδικα]Το περισσότερο ναφθαλίνιο λαμβανόταν από τη λιθανθρακόπισσα. Από τη δεκαετία του 1960 ως τη δεκαετία του 1990, σημαντικές ποσότητες ναφθαλινίου παράγονταν επίσης από κλάσματα βαρέος πετρελαίου κατά τη διάρκεια της διύλισης πετρελαίου, αλλά στις μέρες μας μικρό ποσοστό του παραγώμενου ναφθαλινίου προέρχεται από το πετρέλαιο.
Από λιθανθρακόπισσα και πετρέλαιο
[Επεξεργασία | επεξεργασία κώδικα]Το ναφθαλίνιο είναι το πιο άφθονο απλό συστατικό συστατικό της λιθανθρακόπισσας. Παρόλο που η σύνθεση της λιθανθρακόπισσας ποικίλει ανάλογα με το κοίτασμα λιθάνθρακα από το οποίο παράγεται, η τυπική λιθανθρακόπισσα περιέχει περίπου 10% κατά βάρος ναφθαλίνιο. Στη βιομηχανική πρακκτική, η απόσταξη της λιθανθαρακόπισσας αποδίδει ένα έλαιο (λιθανθρακέλαιο) που περιέχει περίπου 50% ναφθαλίνιο, μαζί με άλλες δώδεκα (12) αρωματικές ενώσεις. Αυτό το λιθαναθρακέλαιο εκπλύνεται με υδατικό διάλυμα υδροξειδίου του νατρίου (NaOH), για να απομακρυνθούν τα όξινα συστατικά (κυρίως διάφορες φαινόλες) και μετά με θειικό οξύ (H2SO4), για να απομακρυνθούν τα βασικά συστατικά.
Μετά ακολουθεί κλασματική απόσταξη για να απομονωθεί το ναφθαλίνιο. Το ακατέργαστο ναφθαλίνιο που λαμβάνεται από την παραπάνω διεργασία περιέχει περίπου 95% κατά βάρος ναφθαλίνιο. Οι κύριες προσμείξεις στο ακατέργαστο ναφθαλίνιο είναι διάφορες θειούχες αρωματικές ενώσεις, όπως κυρίως το βενζοθειοφαίνιο (![]() , <2%), το ινδάνιο (
, <2%), το ινδάνιο (![]() , ~2‰), το ινδένιο (
, ~2‰), το ινδένιο (![]() , <2%) και τα μεθυλοναφθαλίνια (δηλαδή 1-μεθυλοναφθαλίνιο,
, <2%) και τα μεθυλοναφθαλίνια (δηλαδή 1-μεθυλοναφθαλίνιο, ![]() , και 2-μεθυλοναφθαλίνιο,
, και 2-μεθυλοναφθαλίνιο, ![]() , <2% συλλύβδην).
, <2% συλλύβδην).
Το ναφθαλίνιο που λαμβάνεται από το πετρέλαιο είναι συνήθως καθαρότερο από αυτό που λαμβάνεται από τη λιθανθρακόπισσα. Όταν απαιτείται ακόμη καθαρότερο ναφθαλίνιο, αυτό λαμβάνεται μετά από ανακρυστάλλωση ακατέργαστου ναφθαλίνιο, μετά από διάλυσή του σε διάφορους διαλύτες. Το ανακρυσταλλωμένο ναφθαλίνιο περιέχει περίπου 99% κατά βάρος ναφθαλίνιο, που επιβεβαίωνεται από τη θερμοκρασία τήξης του, το οποίο πρέπει να είναι 80°C, για να θεωρηθεί χημικά καθαρό ναφθαλίνιο. Περίπου 1,3 εκατομμύρια τόνοι ναφθαλινίου, παράγονται ετησίως παγκόσμια.[13]
Στη Βόρεια Αμερική, οι (κυριότεροι) παραγωγοί ναφθαλίνιου λιθανθρακόπισσας είναι οι εταιρείες Koppers Inc., Ruetgers Canada Inc. και Recochem Inc.. Αντίστοιχα, οι παραγωγοί ναφθαλίνιου από πετρέλαιο είναι η Monument Chemical Inc.. Στη Δυτική Ευρώπη οι παραγωγοί ναφθαλινίου είναι οι Koppers, Ruetgers, και Deza. Στην Ανατολική Ευρώπη, το ναφθαλίνιο παράγεται από μια ποικιλία ολοκληρωμένων μεταλλουργικών συμπλεγμάτων όπως Severstal, Evraz, Mechel, MMK. Στη Ρωσία οι εξειδικευμένοι στο ναφθαλίνιο και στη φαινόλη παραγωγοί είναι η INKOR, ενώ υπάρχει και η μονάδα Yenakievsky Metallurgy, που παράγει (και) ναφθαλίνιο στην Ουκρανία, ενώ τέλος η ArcelorMittal Temirtau παράγει (και) ναφθαλίνιο στο Καζακστάν.
Συνθετική μέθοδος Χάγουορθ
[Επεξεργασία | επεξεργασία κώδικα]
Εναλλακτικά, υπάρχει η συνθετική μέθοδος Χάγουορθ (Haworth) από βενζόλιο:
Χημική συμπεριφορά και παράγωγα
[Επεξεργασία | επεξεργασία κώδικα]
Δυο ισομερή είναι πιθανά για τα μονοϋποκατεστημένα «θυγατρικά» ναφθαλίνια, που αντιστοιχούν σε υποκατάση των ατόμων υδρογόνου στην α- και στη β- θέση. Το δικυκλο[6.2.0]δεκαπενταένιο είναι ένα δομικό ισομερές με ένα συμπυκνωμένο δικυκλικό σύστημα ενός κυκλοβουταδιενίου και ενός κυκλοοκτατετραένιου.
Γενικά, τα ηλεκτρονιόφιλα προσβάλλουν την α- θέση. Η εκλεκτικότητα της α- θέσης έναντι της β- εξηγείται άμεσα από τις δομές συντονισμού: Για την α- ηλεκτρονιόφιλη υποκατάσταση επτά (7) δομές συντονισμού μπορούν να σχεδιαστούν. Οι τέσσερεις (4) από αυτές διατηρούν έναν (τουλάχιστον) αρωματικό δακτύλιο. Για τη β- ηλεκτρονιόφιλη υποκατάσταση έξι (6) δομές συντονισμού μπορούν να σχεδιαστούν, αλλά μόνο δύο (2) από αυτές είναι αρωματικές.
Ηλεκτρονιόφιλες αρωματικές υποκαταστάσεις
[Επεξεργασία | επεξεργασία κώδικα]Ως προς τις ηλεκτρονιόφιλες αρωματικές υποκαταστάσεις το νοφθαλίνιο αντιδρά ταχύτερα σε σύγκριση με το βενζόλιο. Παραδείγματα
Αλογονώσεις
[Επεξεργασία | επεξεργασία κώδικα]
Το ναφθαλίνιο αντιδρά με το (στοιχειακό) χλώριο (Cl2) και με το (στοιχειακό) βρώμιο (Br2), δίνοντας αντίστοιχα, και χωρίς την ανάγκη καταλύτη, 1-χλωροναφθαλίνιο (![]() ) και 1-βρωμοναφθαλίνιο (
) και 1-βρωμοναφθαλίνιο (![]() ):
):
Αντίδραση Friedel-Crafts
[Επεξεργασία | επεξεργασία κώδικα]Ομοίως, το ναφθαλίνιο, όπως και το βενζόλιο, δίνει αντιδράσεις Friedel-Crafts. Όμως το ναφθαλίνιο δίνει τέτοιες ανιδράσεις όχι μόνο με αλκυλαλογονίδια (RX) ή ακυλαλογονίδια (RCOX), αλλά επίσης και με αλκένια (>C=C<) και με αλκοόλες (ROH), χρησιμοποιώντας, το θειικό οξύ και το φωσφορικό οξύ (H3PO4), ως καταλύτες. Παραδείγματα:
Σουλφούρωση
[Επεξεργασία | επεξεργασία κώδικα]Η σουλφούρωαη ναφθαλινίου δίνει, ωστόσο, ένα μείγμα από 1-ναφθαλινοσουλφονικό οξύ (![]() ) και 2-ναφθαλινοσουλφονικό οξύ (
) και 2-ναφθαλινοσουλφονικό οξύ (![]() ), με την αναλογία να εξαρτάται από τις συνθήκες. Το 1-ναφθαλινοσουλφονικό οξύ παράγεται επιλεκτικά περισσότερο στους 25 °C, ενώ το 2-ναφθαλινοσουλφονικό οξύ παράγεται επιλεκτικά στους 160 °C. Σε κάθε περίπτωση παράγεται γρήγορα μείγμα σε διάφορες αναλογίες:
), με την αναλογία να εξαρτάται από τις συνθήκες. Το 1-ναφθαλινοσουλφονικό οξύ παράγεται επιλεκτικά περισσότερο στους 25 °C, ενώ το 2-ναφθαλινοσουλφονικό οξύ παράγεται επιλεκτικά στους 160 °C. Σε κάθε περίπτωση παράγεται γρήγορα μείγμα σε διάφορες αναλογίες:
Παρατεταμένη σουλφούρωση δίνει αντιστοίχως ναφθαλινοδισουλφονικά, ναφθαλινοτρισουλφονικά και ναφθαλινοτετρασουλφονικά οξέα.
Λιθίωση
[Επεξεργασία | επεξεργασία κώδικα]Ανάλογα με τη σύνθεση του φαινυλολίθιου (PhLi) μπορεί να γίνει και η μετατροπή 1-βρωμοναφθαλινίου σε 1-λιθιοναφθαλίνιο, με αντίδραση διπλής αντικατάστασης:
Το παραγώμενο 1-λιθιοναφθαλίνιο δίνει και δεύτερη λιθίωση, παράγοντας 1,8-διλιθιοναφθαλίνιο, σε αντιδιαστολή με τη συμπεριφορά του φαινυλολιθίου, που δεν δίνει. Το 1,8-διλιθιοναφθαλίνιο, με τη σειρά του, αποτελεί πρόδρομη ένωση για ανάλογα «θυγατρικά» περιναφθαλίνια.[14]
Αντιδράσεις οξειδοαναγωγής
[Επεξεργασία | επεξεργασία κώδικα]Με την επίδραση αλκαλιμετάλλων, το ναφθαλίνιο σχηματίζει βοθυγαλαζοπράσινα ανιονικά άλατα, όπως τιο ναφθαλινίδιο του νατρίου {Na[H10H8]-. Τα άλατα αυτά είναι ισχυρά αναγωγικά μέσα.
Το ναφθαλίνιο μπορεί να υδρογονωθεί από διυδρογόνο (H2) υπό υψηλή πίεση και την παρουσία μεταλλικών καταλυτών (συνήθως λευκοχρύσου), αρχικά τετραλίνιου (![]() ). Με επιπλέον υδρογόνωση, παράγεται τελικά δεκαλίνιο (
). Με επιπλέον υδρογόνωση, παράγεται τελικά δεκαλίνιο (![]() ):
):
Οξείδωση με διοξυγόνο (O2), παρουσία βαναδίου ως καταλύτη, δίνει φθαλικό ανυδρίτη:
Αυτή η αντίδραση είναι βασική για την κύρια εφαρμογή του ναφθαλινίου. Η οξείδωση αυτή μπορεί επίσης να επιτευχθεί και με τα συμβατικά χρωμικά (CrO42-) και υπερμαγγανικά (MnO4-) αντιδραστήρια.
Εφαρμογές
[Επεξεργασία | επεξεργασία κώδικα]Το ναφθαλίνιο χρησιμοποιείται κυρίως ως πρόδρομη ένωση για άλλα χημικά προϊόντα. Ειδικότερα, η μοναδική μεγαλύτερη εφαρμογή του ναφθαλίνιου είναι η βιομηχανική παραγωγή φθαλικού ανυδρίτη (δείτε πώς στις «αντιδράσεις οξειδοαναγωγής»), παρόλο που παράγεται μεγαλύτερη ποσότητα φθαλικού ανυδρίτη με πρόδρομη ένωση το ορθοξυλόλιο. Επίσης, πολλά αζωχρώματα παράγονται από το ναφθαλίνιο, όπως και το εντομοκτόνο (1-ναφθυλο)-N-μεθυλοκαρβαμικό οξύ. Ακόμη, χρήσιμα αγροχημικά συμπεριλαμάνουν ναφθοξυαιθανικά οξέα, δηλαδή και πάλι «θυγατρικά» ναφθαλίνια.
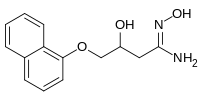
Ναφθαλινοσουλφονικά οξέα και παράγωγα αυτών
[Επεξεργασία | επεξεργασία κώδικα]Πολλά ναφθαλινοσουλφονικά οξέα και διάφορα παράγωγα αυτών αποτελούν χρήσιμα χημικά. Οι ναφθαλινοσουλφονικοί αλκυλεστέρες (ANS: Alkyl Νaphthalene Sulfonates) είναι επιφανειοδραστικές ουσίες. Τα αμινοναφθαλινοσουλφονικά οξέα, που είναι «θυγατρικά» ναφθαλίνια που εμπεριέχουν αμινομάδα (-NH2) και σουλφονική ομάδα (-SO3H), είναι πρόδρομες ενώσεις για την παραγωγή πολλών συνθετικών χρωστικών. Τετραλίνια, που είναι μερικώς υδρογονωμένα ναφθαλίνια και τα δεκαλίνια, που είναι πλήρως υδρογονωμένα ναφθαλίνια, χρησιμοποιούνται ως χαμηλής πτητικότητας διαλύτητες. Τα ναφθαλινοσουλφονικά οξέα χρησιμοποιούνται, ακόμη, για τη σύνθεση της 1-ναφθόλης και της 2-ναφθόλης, που με τη σειρά τους είναι πρόδρομα χημικά για διάφορα βερνίκια, βαφές, χημικά κατεργασίας ελαστικών, κσθώς και για σειρά άλλων χημικών, συμπεριλαμβανομένων φαρμακευτικών σκευασμάτων. [15]
Τα ναφθαλινοσουλφονικά οξέα, ακόμη, για την παραγωγή πολυναφθαλινιοσουλφονικών οξέων, που είναι πλαστικοποιητές (διασκορπιστικά), που χρησιμοποιούνται, με τη σειρά τους, για την παραγωγή ορισμένων ειδών συνθετικού τσιμέντου και γυψοσανίδων (ταμπλώ ή στεγανοτικών). Χρησιμοποιήθηκαν, επίσης, ως διασκορπιστικά για συνθετικά και φυσικά ελαστικά, ως μαυριστικά μέσα (σύντονες) σε βιομηχανίες δερμάτινων ειδών, σε αγροχημικά παρασκευάσματα (διασκορπιστικά για ζιζανιοκτόνα), χρωστικές και ως διασκορπιστικά σε πλάκες συσσωρευτών μολύβδου - οξέος.
Τα πολυναφθαλιοσουλφονικά παράγονται με επίδραση των ναφθαλινοσουλφονικών οξέων με μεθανάλη (HCHO), ακολουθούμενη με εξουδετέρωση από υδροξείδιο του νατρίου (NaOH) ή υδροξείδιο του ασβεστίου [Ca(OH)2]. Αυτά τα προϊόντα πωλούνται είτε με τη μορφή υδατοδιαλυμάτων τους είτε με τη μορφή ξηρής σκόνης.
Ως διαβροχικό μέσο και τασιενεργό
[Επεξεργασία | επεξεργασία κώδικα]Οι ANS χρησιμοποιήθηκαν σε πολλές βιομηχανικές εφαρμογές ως μη απορρυπαντικά διαβροχικά μέσα, που αποτελεσματικά διασκορπούν κολλοειδή συστήματα σε υδατικά μέσα. Οι κυριότερες εμπορικές εφαρμογές τους είναι στην αγροχημεία, που χρησιμοποιεί ANS για παρασκευάσματα με διαβροχίσιμες σκόνες και με διαβροχίσιμους κόκκους (ξηρόρευστα), καθώς επίσης στην κλωστυφαντουργία, η οποία αξιοποιεί τις διαβροχικές και απαφριστικές ιδιότητες των ANS για διεργασίες λεύκανσης και χρωματισμού.
Εργαστηριακές εφαρμογές
[Επεξεργασία | επεξεργασία κώδικα]Το τήγμα ναφθαλινίου παρέχει ένα εξαίρεται διαλυτικό μέσο για κατά τα άλλα ελάχιστα διαλυτές (σε άλλους διαλύτες) αρωματικές ενώσεις. Σε πολλές περιπτώσεις είναι πιο αποτελεσματικό σε σύγκριση και με διαλύτες υψηλής θερμοκρασίας βρασμού, όπως τα διχλωροβενζόλια, το βενζονιτρίλιο (PhCN), το νιτροβενζόλιο (PhNO2) και το ντουρένιο. Η αντίδραση μπαμινστερφουλλερένιου-60 (C60) με ανθρακένιο (![]() ) , για παράδειγμα, συμβατικά πραγατοποιείται σε τηγμένο ναφθαλίνιο με αντιρροή, δίνοντας 1:1 σύμλοκο Diels–Alder.[16] Η αρωματοποίηση των υδροπορφυρινών πραγματοποιείται, επίσης, με διάλυμα 5,6-δικυανο-2,3-διχλωρο-1,4-βενζοκινόνης σε τήγμα ναφθαλινίου.[17]
) , για παράδειγμα, συμβατικά πραγατοποιείται σε τηγμένο ναφθαλίνιο με αντιρροή, δίνοντας 1:1 σύμλοκο Diels–Alder.[16] Η αρωματοποίηση των υδροπορφυρινών πραγματοποιείται, επίσης, με διάλυμα 5,6-δικυανο-2,3-διχλωρο-1,4-βενζοκινόνης σε τήγμα ναφθαλινίου.[17]
Ως απολυμαντικό
[Επεξεργασία | επεξεργασία κώδικα]Το ναφθαλίνιο χρησιμοποιήθηκε ως οικιακό απολυμαντικό. Κάποτε ήταν το κύριο συστατικό των αντισκοριακών σφαιριδίων, παρόλο που πλέον στην εφαρμογή του αυτή αντικαταστάθηκε από εναλλακτικές ενώσεις με καλύτερη οσμή, όπως το 1,4-διχλωροβενζόλιο (![]() ). Σε κλειστό χώρο που περιέχει σφαιρίδια ναφθαλινίου, η συγκέντρωση των ατμών ναφθαλινίου φθάνει ενίοτε σε τοξικά επίπεδα για τους ενήλικες ανθρώπους, αλλά και κάποιες πρώιμες μορφές αντισκοριακών σφαιριδίων προσέβαλαν το υλικό των υφασμάτων που υποτίθεται ότι προστάτευαν. Άλλες απολυμαντικές εφαρμογές του ναφθαλίνιου συμπεριλαμβάνουν τη χρήση του ως εδαφικό απολυμαντικό και ζιζανιοκτόνο, ως απολυμαντικό για σοφίτες (ή ανάλογους χώρους), ως απωθητικό ανεπιθύμητων ζώων, συμπεριλαμβανομένων εντόμων, καθώς και σε διάφορες αποθήκες - αποξηραντές μουσείων και ντουλάπια για την προστασία των περιεχομένων από την προσβολή τους από παρασιτικά έντομα.
). Σε κλειστό χώρο που περιέχει σφαιρίδια ναφθαλινίου, η συγκέντρωση των ατμών ναφθαλινίου φθάνει ενίοτε σε τοξικά επίπεδα για τους ενήλικες ανθρώπους, αλλά και κάποιες πρώιμες μορφές αντισκοριακών σφαιριδίων προσέβαλαν το υλικό των υφασμάτων που υποτίθεται ότι προστάτευαν. Άλλες απολυμαντικές εφαρμογές του ναφθαλίνιου συμπεριλαμβάνουν τη χρήση του ως εδαφικό απολυμαντικό και ζιζανιοκτόνο, ως απολυμαντικό για σοφίτες (ή ανάλογους χώρους), ως απωθητικό ανεπιθύμητων ζώων, συμπεριλαμβανομένων εντόμων, καθώς και σε διάφορες αποθήκες - αποξηραντές μουσείων και ντουλάπια για την προστασία των περιεχομένων από την προσβολή τους από παρασιτικά έντομα.
Το ναφθαλίνιο είναι επίσης ένα απωθητικό για οπόσουμ.[18][19]
Άλλες εφαρμογές
[Επεξεργασία | επεξεργασία κώδικα]Το ναφθαλίνιο χρησιμοποιήθηκε για την παραγωγή ειδικών πυροτεχνικών εφέ, όπως η δημιουργία μαύρου καπνού και η προσομοίωση εκρήξεων. Χρησιμοποιήθκε, ακόμη, για τη δημιουργία τεχνητών πόρων για την παραγωγή τροχών άλεσης υψηλής πορότητας. Στο παρελθόν, το ναφθαλίνιο χορηγήθηκε στοματικά σε ζώα κοπαδιών για να σκοτώσει παρασιτικούς σκώληκες (στο πεπτικό τους σύστημα). Το «μητρικό» ναφθαλίνιο και τα «θυγατρικά» του αλκυλοναφθαλίνια είναι τα συστατικά του σωρισκέα. Το ναφθαλίνιο χρησιμοποιήθηκε, ακόμη, στη μηχανική, για τη μελέτη μεταφοράς θερμότητας χρησιμοποιώντας εξαχνώσιμη μάζα.
Επιπτώσεις στην υγεία
[Επεξεργασία | επεξεργασία κώδικα]Η έκθεση σε μεγάλες ποσότητες ναφθαλινίου μπορούν να προκαλέσουν βλάβη ή και να καταστρέψουν τα ερυθρά αιμοσφαίρια. Αυτό είναι πιο συνηθισμένο σε ανθρώπους που έχουν κληρονομικό κυαμισμό.[20] Η έλλειψη αυτή αφορά πάνω από 400 εκατομμύρια ανθρώπους. Οι άνθρωποι, και ειδικότερα τα παιδιά , ανέπτυξαν αιμολυτική αναιμία, μετά την κατάποση αντισκοριακών σφαιριδίων ή αποσμητικών που περιείχαν ναφθαλίνιο. Τα συμπτώματα (σχετικής δηλητηρίασης) συμπεριλαμβάνουν κόπωση, ανορεξία, ανησυχία και χλωμοδερμία Έκθεση σε μεγαλύτερες ποσότητες ναφθαλινίου μπορούν να προκαλέσουν σύγχυση, ναυτία, έμετο, διάρροια, αιματουρία και ίκτερο (δηλαδή κιτρινοδερμία εξαιτίας δυσλειτουργίας του ήπατος).[21]
Όταν το πρόγραμμα εθνικής τοξικολογίας (NTP, National Toxicology Program) των ΗΠΑ εξέθεσε αρσενικούς και θηλυκούς αρουραίους και ποντίκια σε ατμούς ναφθαλινίου τα σαββατοκύριακα για δύο (2) χρόνια,[22] οι αρσενικοί και οι θηλυκοί αρουραίοι εμφάνισαν ενδείξεις καρκινογένεσης με αυξημένα περιστατικά σε αδένωμα και νευροβλάστωμα στη μύτη, ενώ τα θηλυκά ποντίκια εμφάνισαν κάποιες ενδείξεις καρκινογένεσης με αυξημένα περιστατικά σε κυψελιδικά και βρογχιακά αδενώματα στους πνεύμονες, ενώ τα αρσενικά ποντίκια δεν εμφάνισαν καμία ένδειξη καρκινογένεσης.
Ο Διεθνής Οργανισμός Ερευνών για τον Καρκίνο (IARC, International Agency for Research on Cancer)[23] ταξινόμησε το ναφθαλίνιο στα πιθανά καρκινογόνα για ανθρώπους κιαι ζώα (Group 2B). Ο IARC επισήμανε ακόμη ότι η οξεία έκθεση σε ναφθαλίνιο προκαλεί καταρράκτη σε ανθρώπους, αρουραίους, κουνέλια και ποντίκια. Επιπλέον, ότι προκαλεί αιμολυτική αναιμία ιδιαίτερα σε παιδιά, αλλά και έμβρυα, μετά από στοματική, αναπνευστική ή άλλου είδους έκθεση κατά τη διάρκεια της εγκυμοσύνης. Σύμφωνα με την πρόταση 65 της Καλιφόρνιας, το ναφθαλίνιο μπήκε στη λίστα των «γνωστών στην πολιτεία ουσιών που προκαλούν καρκίνο».[24] Έχει ταυτοποιηθεί ένας πιθανός μηχανισμός για τις καρκινογενετικές συνέπειες από την έκθεση σε αντισκοριακά σφαιρίδια και σε κάποιους τύπους αποσμητικών χώρου που περιέχουν ναφθαλίνιο.[25][26]
Κανονισμοί ασφαλείας
[Επεξεργασία | επεξεργασία κώδικα]Οι υπηρεσίες της κυβέρνησης των ΗΠΑ έχουν θέσει όρια επαγγελματικής έκθεσης στο ναφθαλίνιο. Πιο συγκεκριμένα, η διεύθυνση επαγγελματικής ασφάλειας και υγείας έχουν θέση ως μέγιστο επιτρεπόμενο όριο συγκέντρωσης ναφθαλινίου στα 10 ppm (δηλαδή περίπου 50 mg/m³) για μέση οκτάωρη και εβδομαδιαία έκθεση. Το εθνικό ίδρυμα επαγγελματικής ασφάλειαες και υγείας (των ΗΠΑ) προτείνει επίσης ως μέγιστο επιτρεπόμενο όριο συγκέντρωσης ναφθαλινίου τα 10 ppm για την ίδια χρόνια έκθεση, αλλά επεκτείνει το όριο αυτό για βραχυπρόθεση έκθεση στα 15 ppm (75 mg/m³).[27]
Τα αντισκοριακά σφαιρίδια και τα άλλα προϊόντα που περιέχουν ναφθαλίνιο έχουν απαγορευθεί στην Ευρωπαίκή Ένωση από το 2008.[28][29]
Στην Κίνα, έχει επίσης απαγορευθεί η χρήση αντισκοριακών σφαιριδίων ναφθαλινίου.[30]
Μερικά παραδείγματα «θυγατρικών» ναφθαλινίων
[Επεξεργασία | επεξεργασία κώδικα]| Ονομασία | Μοριακός τύπος | Γραμμομοριακή μάζα [g/mol] | Θερμοκρασία τήξης [°C] | Θερμοκρασία βρασμού [°C] | Πυκνότητα [kg/m³] | Δείκτης διάθλασης |
|---|---|---|---|---|---|---|
| 1-ναφθοϊκό οξύ | C11H8O2 | 172,18 | 157 | 300 | – | |
| 1-ναφθοϋλοχλωρίδιο | C11H7ClO | 190,63 | 16–19 | 190 (35 Torr) | 1.265 | 1,6552 |
| 1-ναφθόλη | C10H8O | 144,17 | 94–96 | 278 | 1.224 | – |
| 2-ναφθόλη | C10H8O | 144,17 | 121-123 | 286 | 1.220 | |
| 1-ναφθαλδεΰδη | C11H8O | 156,18 | 1–2 | 160 (15 Torr) | ||
| 1-νιτροναφθαλίνιο | C10H7NO2 | 173,17 | 53–57 | 340 | 1.220 | – |
| 1-φθοροναφθαλίνιο | C10H7F | 146,16 | −19 | 215 | 1.323 | 1,593 |
| 1-χλωροναφθαλίνιο | C10H7Cl | 162,62 | −6 | 259 | 1.194 | 1,632 |
| 2-χλωροναφθαλίνιο | C10H7Cl | 162,62 | 59,5 | 256 | 1.138 | 1,643 |
| 1-βρωμοναφθαλίνιο | C10H7Br | 207,.07 | −2 | 279 | 1.489 | 1,670 |
| 1-μεθυλοναφθαλίνιο | C10H7CH3 | 142,20 | -30,5 | 244,4 | 1..001 | 1,61755 |
| 2-μεθυλοναφθαλίνιο | C10H7CH3 | 142,20 | 34,6 | 243,1 | 1.006 |
Δείτε επίσης
[Επεξεργασία | επεξεργασία κώδικα]- 1-μεθυλοναφθαλίνιο
- 2-μεθυλοναφθαλίνιο
- Φουλβαλένιο
- Καμφορά
- Διαλίνιο
- Τετραλίνιο
- Δεκαλίνιο
- Διαστρικά και ενδοαστρικά χημικά είδη που έχουν ανιχνευθεί
- 1-ναφθόλη
- 2-ναφθόλη
- ναφθαλινίδιο του νατρίου
- Αντίδραση Βάγκνερ-Γιούρεγκ
- Ανθρακένιο
- Φαινανθρένιο
- Ακεναφθυλένιο
- Αζουλένιο
- Πενταλένιο
- Ινδένιο
- Επταλένιο
- Διφαινυλένιο
- ας-ινδακένιο
- ς-ινδρακένιο
- Φλουορένιο
- Φαιναλένιο
- Φλουορανθένιο
- Ακεφαινανθρένιο
- Τριφαινυλένιο
- Πυρένιο
- Χρυσένιο
- Ναφθακένιο
- Πλειαδένιο
- Πενταφαίνιο
- Πεντακένιο
- Τετραφαινυλένιο
- Εξαφαίνιο
- Εξακένιο
- Ρουμπικένιο
- Κορωνένιο
- Τριναφθυλένιο
- Επταφαίνιο
- Επτακένιο
- Πυρανθένιο
- Οβαλένιο
- Θειανθρένιο
- Ισοβενζοφουράνιο
- Χρωμένιο
- Ξανθένιο
- Φαινοξαθίνιο
- Ιδολζίνη
- Ισοϊνδόλιο
- 3-υδροϊνδόλιο
- Ινδόλιο
- 1-υδροϊνδαζόλιο
- Πυρίνιο
- 4-υδροκιναζολίνη
- Ισοκινολίνη
- Κινολίνη
- Κιναζολίνη
- Φθαλαζίνη
- Ναφθυδρίνη
- Κινοξαλίνη
- Κιναζολίνη
- Κιννολίνη
- Πτεριδίνη
- 4α-υδροκαρβαζόλιο
- Καρβαζόλιο
- β-καρβολίνη
- Φαινανθριδίνη
- Ακριδίνη
- Περιμιδίνη
- 1,7-φαινανθρολίνη
- Φαιναζίνη
- Φαιναραζίνη
- Φαινοθαζίνη
- Φαινοξαλίνη
- Ισοχρωμάνιο
- Χρωμάνιο
- Ινδολίνη
- Ισοϊνδολίνη
- Κινακλιδίνη
- Πουρίνη
Πηγές
[Επεξεργασία | επεξεργασία κώδικα]- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
- MedlinePlus Encyclopedia Naphthalene poisoning.
- "NTP Technical Reports 410 and 500". NTP Technical Reports 410 and 500, available from
- Long-Term Abstracts & Reports. Retrieved March 6, 2005.
- "IARC Monographs on the Evaluation of Carcinogenic Risks to Humans". Monographs on the...
- Evaluation of Carcinogenic Risks to Humans, Some Traditional Herbal Medicines, Some Mycotoxins, Naphthalene and Styrene, Vol. 82 (2002) (p. 367). Retrieved December 25, 2008.
- Proposition 65, Office of Environmental Health Hazard Assessment
- 国务院经贸办、卫生部关于停止生产和销售萘丸提倡使用樟脑制品的通知(国经贸调(1993)64号)
- [1] Search of Chinese online shop.
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Δείτε τις εναλλακτικές ονομασίες στον παρακείμενο πίνακα πληροφοριών χημικής ένωσης.
- ↑ Amoore J E and Hautala E (1983). «Odor as an aid to chemical safety: Odor thresholds compared with threshold limit values and volatiles for 214 industrial chemicals in air and water dilution». J Appl Toxicology 3 (6): 272–290. doi:.
- ↑ John Kidd (1821). «Observations on Naphthaline, a peculiar substance resembling a concrete essential oil, which is apparently produced during the decomposition of coal tar, by exposure to a red heat». Philosophical Transactions 111: 209–221. doi:.
- ↑ Emil Erlenmeyer (1866). «Studien über die s. g. aromatischen Säuren». Annalen der Chemie und Pharmacie 137 (3): 327–359. doi:.
- ↑ Συγκρίνετε με τα μήκη 154 pm (τυπικός απλός δεσμός C-C κορεσμένων ενώσεων), 134 pm (τυπικός διπλός δεσμός C=C) και 139 pm (δεσμοί C-C στο βενζόλιο)
- ↑ BBC News
- ↑ «Termite 'mothball' keep insects at bay». Sci/Tech (BBC News). April 8, 1998. http://news.bbc.co.uk/1/hi/sci/tech/76115.stm.
- ↑ «Naphthalene, an insect repellent, is produced by Muscodor vitigenus, a novel endophytic fungus». Microbiology (Reading, Engl.) 148 (Pt 11): 3737–41. November 2002. doi:. PMID 12427963. http://mic.sgmjournals.org/cgi/content/abstract/148/11/3737.
- ↑ «Interstellar Space Molecules That Help Form Basic Life Structures Identified». Science Daily. Σεπτεμβρίου 2008.
- ↑ Iglesias-Groth, S.; Manchado, A.; García-Hernández, D. A.; González Hernández, J. I.; Lambert, D. L. (2008-09-20), «Evidence for the Naphthalene Cation in a Region of the Interstellar Medium with Anomalous Microwave Emission», The Astrophysical Journal Letters 685: L55–L58, doi: - This spectral assignment has not been independently confirmed, and is described by the authors as "tentative" (page L58).
- ↑ Hoover, Rachel (21 Φεβρουαρίου 2014). «Need to Track Organic Nano-Particles Across the Universe? NASA's Got an App for That». NASA. Αρχειοθετήθηκε από το πρωτότυπο στις 10 Μαΐου 2020. Ανακτήθηκε στις 22 Φεβρουαρίου 2014.
- ↑ «Mothballs in Space». Astrobiology Magazine. Αρχειοθετήθηκε από το πρωτότυπο στις 2 Μαρτίου 2014. Ανακτήθηκε στις 25 Δεκεμβρίου 2008.
- ↑ Gerd Collin, Hartmut Höke, Helmut Greim "Naphthalene and Hydronaphthalenes" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2003. doi:10.1002/14356007.a17_001.pub2. Article Online Posting Date: March 15, 2003.
- ↑ van Soolingen, J.; de Lang, R. J.; den Besten, R.; Klusener, P. A. A.; Veldman, N.; Spek, A. L.; Brandsma, L., "A simple procedure for the preparation of 1,8-bis(diphenylphosphino)naphthalene", Synthetic Communications 1995, 25, 1741-1744.
- ↑ Gerd Collin, Hartmut Höke, Helmut Greim "Naphthalene and Hydronaphthalenes" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2003. doi:10.1002/14356007.a17_001.pub2. Article Online Posting Date: March 15, 2003.
- ↑ K. Komatsua; Y. Murataa; N. Sugitaa; K. Takeuchib; T.S.M. Wan (1993). «Use of naphthalene as a solvent for selective formation of the 1:1 Diels–Alder adduct of C60 with anthracene». Tetrahedron Letters 34 (52): 8473–8476. doi:.
- ↑ M.A. Filatov; A.V. Cheprakov (2011). «The synthesis of new tetrabenzo- and tetranaphthoporphyrins via the addition reactions of 4,7-dihydroisoindole». Tetrahedron 67 (19): 3559–3566. doi:.
- ↑ «Summary of Possum Repellent Study». Αρχειοθετήθηκε από το πρωτότυπο στις 28 Σεπτεμβρίου 2013.
- ↑ "Removing a possums from your roof", NSW Department of the Environment and Heritage, http://www.environment.nsw.gov.au/animals/RemovingAPossumFromYourRoof.htm Αρχειοθετήθηκε 2013-09-27 στο Wayback Machine.
- ↑ «Association of naphthalene with acute hemolytic anemia». Acad Emerg Med 7 (1): 42–7. Jan 2000. PMID 10894241. https://archive.org/details/sim_academic-emergency-medicine_2000-01_7_1/page/42.
- ↑ Πρότυπο:MedlinePlusEncyclopedia
- ↑ «NTP Technical Reports 410 and 500». NTP Technical Reports 410 and 500, available from NTP: Long-Term Abstracts & Reports. Αρχειοθετήθηκε από το πρωτότυπο στις 24 Οκτωβρίου 2004. Ανακτήθηκε στις 6 Μαρτίου 2005.
- ↑ «IARC Monographs on the Evaluation of Carcinogenic Risks to Humans». Monographs on the Evaluation of Carcinogenic Risks to Humans, Some Traditional Herbal Medicines, Some Mycotoxins, Naphthalene and Styrene, Vol. 82 (2002) (p. 367). Ανακτήθηκε στις 25 Δεκεμβρίου 2008.
- ↑ Proposition 65 Αρχειοθετήθηκε 2019-07-29 στο Wayback Machine., Office of Environmental Health Hazard Assessment
- ↑ "Scientists May Have Solved Mystery Of Carcinogenic Mothballs", Physorg.com, June 20, 2006.
- ↑ «Mothballs, air fresheners and cancer». Environmental Health Association of Nova Scotia. Environmental Health Association of Nova Scotia. Ανακτήθηκε στις 24 Μαΐου 2013.
- ↑ CDC - NIOSH Pocket Guide to Chemical Hazards
- ↑ Alderson, Andrew (15 Nov 2008). «Holy straight bananas – now the Eurocrats are banning moth balls». The Telegraph. http://www.telegraph.co.uk/news/newstopics/howaboutthat/3463893/Holy-straight-bananas-now-the-Eurocrats-are-banning-moth-balls.html. Ανακτήθηκε στις 2013-11-23.
- ↑ Gray, Kerrina (17 November 2013). «Council warned against use of poisonous moth balls». Your Local Guardian (Newsquest (London) Ltd.). http://www.yourlocalguardian.co.uk/news/10813745.Council_warns_against_use_of_poisonous_mothballs/. Ανακτήθηκε στις 2012-11-23.
- ↑ 国务院经贸办、卫生部关于停止生产和销售萘丸提倡使用樟脑制品的通知(国经贸调(1993)64号)






![{\displaystyle \mathrm {{\xrightarrow[{\triangle ,\pi {\acute {\iota }}\epsilon \sigma \eta }]{Pd}}2H_{2}+} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/9a1febff2b7bfb992435a8b089acb52e54e011e9)









![{\displaystyle \mathrm {+2H_{2}{\xrightarrow[{\pi {\acute {\iota }}\epsilon \sigma \eta }]{Pt}}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/c11eaf7d5acc52dba6df38c1d41dbe71b9480646)
![{\displaystyle \mathrm {+3H_{2}{\xrightarrow[{\pi {\acute {\iota }}\epsilon \sigma \eta }]{Pt}}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/0b7f603633d63a607035613e04265f97f81d6bf8)