Βενζονιτρίλιο
| Βενζονιτρίλιο | |||
|---|---|---|---|
| |||
| |||
| Γενικά | |||
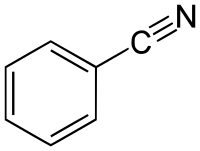
| Όνομα IUPAC | Βενζονιτρίλιο | ||
| Άλλες ονομασίες | Κυανοβενζένιο Βενζοκυανίδιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C7H5N | ||
| Μοριακή μάζα | 103,04 amu | ||
| Σύντομος συντακτικός τύπος |
PhCN | ||
| Συντομογραφίες | , | ||
| Αριθμός CAS | 100-47-0 | ||
| SMILES | N#Cc1ccccc1 | ||
| InChI | 1S/C7H5N/c8-6-7-4-2-1-3-5-7/h1-5H | ||
| PubChem CID | 7505 | ||
| ChemSpider ID | 7224 | ||
| Δομή | |||
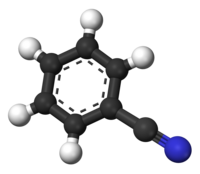
| Μοριακή γεωμετρία | επίπεδη | ||
| Ισομέρεια | |||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -13°C | ||
| Σημείο βρασμού | 188-191°C | ||
| Πυκνότητα | 1.000 kg/m3 | ||
| Διαλυτότητα στο νερό |
<5 kg/m3 (22°C) | ||
| Διαλυτότητα σε άλλους διαλύτες |
διαλυτό σε οργανικούς διαλύτες | ||
| Δείκτης διάθλασης , nD |
1,5280 | ||
| Χημικές ιδιότητες | |||
| Ελάχιστη θερμοκρασία ανάφλεξης |
75 °C | ||
| Σημείο αυτανάφλεξης | 550°C | ||
| Επικινδυνότητα | |||

| |||
| Βλαβερό (Xi) | |||
| Φράσεις κινδύνου | R21/22 | ||
| Φράσεις ασφαλείας | (S2), S23 | ||
| Κίνδυνοι κατά NFPA 704 |
|||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Το βενζονιτρίλιο ή κυανοβενζένιο ή φαινυλοκυανίδιο είναι το απλούστερο αρωματικό νιτρίλιο, με σύντομο συντακτικό τύπο PhCN. Είναι ένα άχρωμο υγρό με γλυκιά οσμή αμυγδάλου.
Παραγωγή
[Επεξεργασία | επεξεργασία κώδικα]Με αμινοξείδωση τολουολίου
[Επεξεργασία | επεξεργασία κώδικα]Με αμινοξείδωση τολουολίου παράγεται βενζονιτρίλιο:
Με κυάνωση φαινυλαλογονιδίου
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση κυανιούχου καλίου σε φαινυλαλογονίδιο (PhX)[1], παράγεται βενζονιτρίλιο[2]:
Με αφυδάτωση βενζαμιδίου
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση αφυδατικών μέσων, όπως πεντοξείδιο του φωσφόρου (P2O5) ή πενταχλωριούχο φωσφόρο (PCl5) ή θειονυλοχλωρίδιο (SOCl2), σε βενζαμίδιο παράγεται βενζονιτρίλιο[3]:
Με επίδραση φαινυλομαγνησιαλογονιδίου σε χλωροκυάνιο
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση φαινυλομαγνησιαλογονίδιου σε χλωροκυάνιο (ClCN) παράγεται βενζονιτρίλιο[4]:
Χημικές ιδιότητες και παράγωγα
[Επεξεργασία | επεξεργασία κώδικα]Υδρόλυση
[Επεξεργασία | επεξεργασία κώδικα]1. Με μερική υδρόλυση βενζονιτριλίου, παράγεται βενζαμίδιο[5]:
2. Με πλήρη υδρόλυση βενζονιτριλίου, παράγεται βενζοϊκό οξύ[5]:
Παραγωγή φαινυλοκετόνης
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση οργανομαγνησιακής ένωσης (RMgX) και έπειτα υδρόλυση, παράγεται φαινυλοκετόνη
Υδρογόνωση
[Επεξεργασία | επεξεργασία κώδικα]1. Με καταλυτική υδρογόνωση παράγεται βενζυλαμίνη:
2. Με επίδραση λιθιοαργιλιοϋδρίδιου παράγεται βενζυλαμίνη:
Παραγωγή ενώσεων συναρμογής
[Επεξεργασία | επεξεργασία κώδικα]Παράγει εύκολα διάφορες ενώσεις συναρμογής. Π.χ. με επίδραση χλωριούχου παλλάδιου παράγεται δι(φαινυλοκυανο)διχλωροπαλλάδιο:
Σημειώσεις και αναφορές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Συνήθως χρησιμοποιείται φαινυλοβρωμίδιο.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 297, §13.2.Δ1.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 302, §13.6.2. και σελ. 297, §13.2.Δ2
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 297, §13.2.Δ4
- ↑ 5,0 5,1 Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 304, §13.7.1
Πηγές
[Επεξεργασία | επεξεργασία κώδικα]- Γ. Βάρβογλη, Ν. Αλεξάνδρου: Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, Χημεία Οργανικών Ενώσεων, παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ν.Α. Πετάση: Ασκήσεις και προβλήματα Οργανικής Χημείας, 1982
- Δημήτριου Ν. Νικολαΐδη: Ειδικά μαθήματα Οργανικής Χημείας, Θεσσαλονίκη 1983.
| ||||||||
|












![{\displaystyle \mathrm {PdCl_{2}+2PhCN{\xrightarrow {}}[PdCl_{2}(PhCN)_{2}]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/259c4ed4762943ba64ff95dc628b5883158957f5)