Άνθρακας
| Άνθρακας | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ιστορία | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ταυτότητα του στοιχείου | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Όνομα, σύμβολο | Άνθρακας (C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ατομικός αριθμός (Ζ) | 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Κατηγορία | αμέταλλα | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ομάδα, περίοδος, τομέας |
14 (IVA) ,2, p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Σχετική ατομική μάζα (Ar) |
12,0107 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ηλεκτρονική διαμόρφωση |
[ He ] 2s² 2p² 2 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Αριθμός CAS | 7440-44-0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ατομικές ιδιότητες | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ατομική ακτίνα | 91,4 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ομοιοπολική ακτίνα | 77 pm (sp³) 73 pm (sp²) 69 pm (sp) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ηλεκτραρνητικότητα | 2,55 (κλίμακα Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Κυριότεροι αριθμοί οξείδωσης |
4[1], 3[2][3], 2[4], 1[5][6] 0[7], −1[8], −2[9], −3[10], −4[11][12] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ενέργειες ιονισμού | 1.086,5 kJ/mole (C → C+ + e-) 2.352,6 kJ/mole (C+ → C2+ + e-) 4.620,5 kJ/mole (C2+ → C3+ + e-) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Φυσικά χαρακτηριστικά | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Σημείο τήξης | 3.527 °C (3.800,16 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Σημείο βρασμού | 4.827 °C (5.100,16 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Πυκνότητα | 3.520 kg/m³ (0 °C, 1 atm) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Η κατάσταση αναφοράς είναι η πρότυπη κατάσταση (25°C, 1 Atm) εκτός αν σημειώνεται διαφορετικά | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ο άνθρακας (από αρχαία ελληνικά: ἄνθραξ, λατινικά: carbonium, αγγλικά: carbon) είναι το αμέταλλο χημικό στοιχείο με χημικό σύμβολο C και ατομικό αριθμό 6. Είναι μέλος της δεύτερης περιόδου και της ομάδας 14 (πρώην IVA) του περιοδικού πίνακα. Δρα σχεδόν πάντα ως αμέταλλο τετρασθενές στοιχείο, δηλαδή το άτομό του έχει τέσσερα ηλεκτρόνια διαθέσιμα για τη δημιουργία (συνήθως) ομοιοπολικών χημικών δεσμών. Υπάρχουν τρία φυσικά ισότοπα άνθρακα, από τα οποία ο 12C και ο 13C είναι σταθερά, ενώ ο 14C είναι ραδιενεργό, με ημιζωή περίπου 5.730 έτη[13]. Ο άνθρακας είναι ένα από τα λίγα χημικά στοιχεία που είναι γνωστά από την Αρχαιότητα[14].
Ο άνθρακας είναι το 15ο σε αφθονία χημικό στοιχείο (κατά μάζα) στο φλοιό της Γης και το 4ο (κατά μάζα) πιο άφθονο χημικό στοιχείο στο σύμπαν, μετά από το υδρογόνο, το ήλιο και το οξυγόνο. Είναι παρόν σε όλες τις γνωστές μορφές ζωής, ενώ στο ανθρώπινο σώμα ο άνθρακας είναι το δεύτερο (κατά μάζα) πιο άφθονο χημικό στοιχείο, περίπου 18,5%, μετά το οξυγόνο[15]. Αυτή η (σχετικά υψηλή) αφθονία του άνθρακα, σε συνδυασμό με τη μοναδική του ικανότητα να σχηματίζει τέτοια τεράστια ποικιλία οργανικών ενώσεων, που επιπλέον συχνά μπορούν και να πολυμερίζονται, σε σχετικά συνηθισμένες, για την επιφάνειας της Γης μας, συνθήκες, έκαναν αυτό το χημικό στοιχείο τη βάση κάθε γνωστής μορφής ζωής.
Υπάρχουν αρκετές αλλοτροπικές μορφές του άνθρακα, από τις οποίες οι πιο γνωστές είναι ο γραφίτης, το διαμάντι και ο άμορφος άνθρακας[16]. Οι φυσικές ιδιότητες των διαφόρων αλλομορφών του άνθρακα διαφέρουν πολύ. Για παράδειγμα, το διαμάντι είναι πολύ διαφανές, το πιο σκληρό φυσικό υλικό που είναι γνωστό και με πολύ μικρή ηλεκτρική αγωγιμότητα, ενώ ο γραφίτης (του οποίου η ονομασία προέρχεται από την ελληνική λέξη «γράφω») είναι αδιαφανής, αρκετά μαλακός για να σχηματίζει μια γραμμή πάνω σε χαρτί και ένας πολύ καλός αγωγός του ηλεκτρισμού. Υπό κανονικές συνθήκες περιβάλλοντος, το διαμάντι, ο νανοσωλήνας άνθρακα και το γραφένιο έχουν τις υψηλότερες θερμικές αγωγιμότητες από όλα τα γνωστά υλικά.
Όλες οι (γνωστές) αλλοτρομορφές του άνθρακα, υπό κανονικές συνθήκες περιβάλλοντος, είναι στερεές, με το γραφίτη να έχει την πιο θερμοδυναμικά σταθερή μορφή. Ο γραφίτης είναι μάλιστα (σχετικά) χημικά ανθεκτικός και χρειάζεται (σχετικά πάντα) υψηλή θερμοκρασία για να αντιδράσει ακόμη και με (καθαρό) οξυγόνο. Η πιο συνηθισμένη βαθμίδα οξείδωσης του άνθρακα στις ανόργανες ενώσεις είναι +4, ενώ η βαθμίδα +2 βρίσκεται (για παράδειγμα) στο μονοξείδιο του άνθρακα (CO)αι στα καρβονυλικά σύμπλοκα των μεταβατικών μετάλλων. Οι μεγαλύτερες πηγές «ανόργανου άνθρακα» (στη Γη) είναι ο ασβεστόλιθος, οι δολομίτες και το διοξείδιο του άνθρακα, (CO2)αλλά υπάρχουν και σημαντικές ποσότητες οργανικής προέλευσης αποθεμάτων κάρβουνου, τύρφης, πετρελαίου, φυσικού αερίου καθώς και μεθανυδρίτες. Ο άνθρακας σχηματίζει το μεγαλύτερο αριθμό χημικών ενώσεων από κάθε άλλο χημικό στοιχείο, εφόσον σχεδόν 10.000.000 καθαρές οργανικές ενώσεις έχουν περιγραφεί προς το παρόν, που αποτελούν (όμως) ένα πολύ μικρό κλάσμα των θεωρητικά πιθανών οργανικών ενώσεων που μπορούν να υπάρξουν, υπό κανονικές συνθήκες περιβάλλοντος[17].
Χαρακτηριστικά
[Επεξεργασία | επεξεργασία κώδικα]Οι διαφορετικές αλλομορφές του άνθρακα περιλαμβάνουν (όπως είδαμε και παραπάνω) το σκληρότερο υλικό που υπάρχει στη φύση, το διαμάντι, αλλά επίσης και ένα από τα πιο μαλακά υλικά που υπάρχουν στη φύση, τον γραφίτη. Επίσης, το άτομο του άνθρακα έχει τη χημική ικανότητα να σχηματίζει έως και τέσσερις δεσμούς με άλλα άτομα, που περιλαμβάνουν και άλλα άτομα άνθρακα, με ικανότητα μάλιστα να σχηματίζει και πολλαπλούς (δηλαδή διπλούς ή τριπλούς) ομοιοπολικούς δεσμούς με τέτοια άτομα. Ως αποτέλεσμα των παραπάνω, οι μέχρι σήμερα γνωστές ενώσεις του άνθρακα (οργανικές ενώσεις) υπερβαίνουν τα 10.000.000 χημικές ενώσεις, αποτελώντας τη μεγάλη πλειοψηφία του συνολικού αριθμού των ως σήμερα γνωστών χημικών ενώσεων[17].
Ο άνθρακας έχει ακόμη την υψηλότερη θερμοκρασία εξάχνωσης από όλα τα άλλα χημικά στοιχεία. Υπό πίεση 1 atm δεν έχει θερμοκρασία τήξης, αφού το τριπλό σημείο του βρίσκεται σε πίεση 10,8 ± 0,2 MPa και σε θερμοκρασία 4.600 ± 300 K (περίπου 4.330 ± 300 °C)[18][19], οπότε εξαχνώνεται, με τη θερμοκρασία εξάχνωσής του, που (υπό πίεση 1 atm) είναι περίπου 3.900 K (περίπου 3.627 °C). Ο άνθρακας εξαχνώνεται με ανθρακικό τόξο, που έχει θερμοκρασία περίπου 5.800 K (περίπου 5.530 °C), οπότε ο άνθρακας, ανεξάρτητα από την αλλοτροπική του μορφή, παραμένει στερεός σε υψηλότερες θερμοκρασίες ακόμη και από τις θερμοκρασίες τήξης μετάλλων όπως το βολφράμιο ή το ρήνιο. Παρόλο που θερμοδυναμικά έχει τάση για οξείδωση, ο άνθρακας αντιστέκεται στην οξείδωση πιο αποτελεσματικά από χημικά στοιχεία όπως ο σίδηρος και ο χαλκός, που είναι ασθενέστερα αναγωγικά μέσα σε θερμοκρασία δωματίου (20 °C).
Ο άνθρακας είναι η βάση όλων των γνωστών μορφών ζωής στη Γη και ο κύκλος άνθρακα - αζώτου μεταφέρει (στις μορφές ζωής της Γης) κάποια από την ενέργεια, που αρχικά παράγεται στον Ήλιο (ενώ εικάζεται ότι το ίδιο μπορεί να συμβαίνει και σε άλλα αστρικά συστήματα). Παρ' όλο που σχηματίζει μια εξαιρετικά μεγάλη ποικιλία ενώσεων, οι περισσότερες αλλομορφές του άνθρακα είναι συγκριτικά χημικά αδρανείς κάτω από κανονικές συνθήκες περιβάλλοντος. Στις κανονικές συνθήκες περιβάλλοντος, ο άνθρακας αντιστέκεται σε όλα, ακόμη και στα ισχυρότερα οξειδωτικά μέσα. Δεν αντιδρά ούτε με το θειικό οξύ (H2SO4), ούτε με το υδροχλωρικό οξύ (HCl), ούτε με το (στοιχειακό) χλώριο (Cl2), αλλά ούτε και με κάποιο από τα αλκαλιμέταλλα. Σε αυξημένες θερμοκρασίες, ο άνθρακας αντιδρά με το οξυγόνο και σχηματίζει οξείδιά του, αλλά ανάγει οξείδια μετάλλων, όπως οξείδιο του σιδήρου (FeO), στα (αντίστοιχα στοιχειακά) μέταλλα[20]. Αυτή η εξώθερμη αντίδραση αξιοποιείται από τη μεταλλουργική βιομηχανία σιδήρου και χάλυβα, για να ελεγχθεί η περιεκτικότητα του χάλυβα σε άνθρακα:
Επίσης, αντιδρά με το θείο, σχηματίζοντας διθειάνθρακα (CS2):
Ακόμη πιο σημαντική είναι η αντίδραση του άνθρακα με υδρατμούς, που παράγει «υδραέριο», δηλαδή μίγμα μονοξειδίου του άνθρακα και (στοιχειακού) υδρογόνου:
Ο άνθρακας αντιδρά με κάποια μέταλλα σε υψηλές θερμοκρασίες, σχηματίζοντας καρβίδια των (αντίστοιχων) μετάλλων, όπως είναι το καρβίδιο με το σίδηρο, που ονομάζεται σεμεντίτης και περιέχεται στο χάλυβα, το καρβίδιο του βολφραμίου (WC), που χρησιμοποιείται ευρύτατα ως λειαντικό για την κατασκευή σκληρών «δοντιών» για εργαλεία κοπής.
Από το 2009, το γραφένιο φαίνεται να είναι το ισχυρότερο υλικό που έχει δοκιμαστεί[21]. Ωστόσο, η διεργασία διαχωρισμού του από τον γραφίτη χρειάζεται κάποια (επιπλέον) τεχνολογική εξέλιξη πριν γίνει αρκετά οικονομική ώστε να χρησιμοποιείται σε βιομηχανικές διεργασίες[22].
Το σύστημα των αλλοτροπικών μορφών του άνθρακα εξαπλώνεται σε ένα εύρος από ακρότητες:
| Το συνθετικό νανοκρυσταλλικό διαμάντι είναι το σκληρότερο γνωστό υλικό.[23] | Ο γραφίτης είναι ένα από τα πιο μαλακά γνωστά υλικά. |
| Το διαμάντι είναι το κορυφαίο λειαντικό. | Ο γραφίτης είναι ένα πολύ καλό λιπαντικό, που παρουσιάζει υπερλιπαντικότητα[24]. |
| Το διαμάντι είναι ένας άριστος (ηλεκτρικός) μονωτής[25], και έχει την υψηλότερη κατανομή ηλεκτρικού πεδίου οποιασδήποτε γνωστό υλικό. | Ο γραφίτης είναι ένας αγωγός του ηλεκτρικού ρεύματος[26]. |
| Το διαμάντι είναι το καλύτερο γνωστό υλικό που βρίσκεται στη φύση σε θερμική αγωγιμότητα | Κάποιες μορφές γραφίτη χρησιμοποιήθηκαν για θερμομόνωση, αλλά κάποιες άλλες, όπως ο πυρολυτικός γραφίτης, είναι καλοί αγωγοί θερμότητας. |
| Το διαμάντι είναι πολύ διαφανές. | Ο γραφίτης είναι αδιαφανής. |
| Το διαμάντι κρυσταλλώνεται στο κυβικό κρυσταλλικό σύστημα. | Ο γραφίτης κρυσταλλώνεται στο εξαγωνικό κρυσταλλικό σύστημα[27]. |
| Ο άμορφος άνθρακας είναι τελείως ισοτροπικός. | Οι νανοσωλήνες άνθρακα είναι το πιο ανισοτροπικό υλικό που έχει ποτέ παραχθεί. |
Αλλοτροπικές μορφές
[Επεξεργασία | επεξεργασία κώδικα]
Ο ατομικός άνθρακας είναι ένα πολύ βραχύβιο χημικό είδος και γι' αυτό ο (στοιχειακός) άνθρακας σταθεροποιείται σε διάφορες πολυατομικές δομές με διάφορες μοριακές διαμορφώσεις, που ονομάζονται αλλοτροπικές μορφές του άνθρακα. Οι τρεις (3) (σχετικώς) ευρύτερα γνωστές από τις αλλοτροπικές μορφές του άνθρακα είναι ο άμορφος άνθρακας, ο γραφίτης και το διαμάντι. Υπάρχουν όμως και άλλες. Για παράδειγμα, τα φουλερένια (fullerenes) θεωρούνταν κάποτε «εξωτικές» αλλοτροπικές μορφές, αλλά αυτόν τον καιρό συχνά συντίθενται και χρησιμοποιούνται στην έρευνα. Περιλαμβάνουν τις μπακιμπάλες (buckyballs)[28][29], τους νανοσωλήνες άνθρακα (carbon nanotubes)[30], τα νάνομπαντς άνθρακα (carbon nanobuds)[31] και τα νανοανθρακονήματα (nanofibers)[32][33]. Αρκετές ακόμη εξωτικές αλλοτροπικές μορφές του άνθρακα έχουν ανακαλυφθεί, όπως ο λονσδαλεΐτης (lonsdaleite)[34], ο υαλώδης άνθρακας (glassy carbon)[35], ο νανοαφρός άνθρακα (carbon nanofoam)[36] και το καρβύνιο (carbyne) ή «γραμμικός ακετυλενικός άνθρακας» (linear acetylenic carbon)[37]
Ο άμορφος άνθρακας είναι μια αλλοτροπική μορφή στην οποία τα άτομα άνθρακα έχουν μια διευθέτηση σε μια μη κρυσταλλική, ακανόνιστη, υαλώδη κατάσταση, που είναι ουσιαστικά γραφίτης, αλλά χωρίς να έχει μια κρυσταλλική μακροδομή. Βρίσκεται ως μια (πιθανώς συγκολλημένη) σκόνη, και είναι το κύριο συστατικό ουσιών όπως το ξυλοκάρβουνο, η αιθάλη και ο ενεργός άνθρακας. Σε κανονικές πιέσεις ο άνθρακας παίρνει τη μορφή γραφίτη, στον οποίο κάθε άτομο σχηματίζει (ομοιοπολικούς) δεσμούς τριγωνικά με τρία (3) άλλα άτομα άνθρακα, σε ένα επίπεδο, που αποτελείται από «συμπυκνωμένους»[38] εξαγωνικούς δακτυλίους, ακριβώς σαν κι αυτούς στους αρωματικούς υδρογονάνθρακες[39]. Το αποτέλεσμα αυτής της σύνδεσης είναι ένα δισδιάστατο δίκτυο από επίπεδα φύλλα που στοιβάζονται (το ένα πάνω στο άλλο) και ενώνονται χαλαρά με αδύναμους δεσμούς μέσω δυνάμεων φαν ντερ Βάαλς. Αυτή η δομή δίνει στο γραφίτη τη μαλακότητά του και τις διασπαστικές του ιδιότητες (τα χαλαρά συνδεδεμένα φύλλα εύκολα γλιστρούν το ένα πάνω από το άλλο). Επίσης, εξαιτίας της διάχυσης του ενός από τα τέσσερα ηλεκτρόνια της εξωτερικής στιβάδας κάθε ατόμου άνθρακα σε ένα σχηματισμό (διάχυτου δεσμικού) νέφους π, ο γραφίτης άγει το ηλεκτρικό ρεύμα, αλλά μόνο κατά το επίπεδο κάθε σχηματιζόμενου «φύλλου» του δικτύου ομοιοπολικών δεσμών. Αυτό καταλήγει σε ένα χαμηλότερο επίπεδο ηλεκτρικής αγωγιμότητας για το γραφίτη σε σύγκριση με τα περισσότερα μέταλλα. Η διάχυση των ηλεκτρονίων επίσης συνεισφέρει στην ενεργειακή σταθεροποίηση του γραφίτη, σε σύγκριση με το διαμάντι, σε θερμοκρασία δωματίου.
Σε πολύ υψηλές πιέσεις, τα άτομα άνθρακα σχηματίζουν την πιο συνεκτική αλλοτροπική δομή του διαμαντιού, το οποίο έχει σχεδόν διπλάσια πυκνότητα σε σύγκριση με το γραφίτη. Στο διαμάντι κάθε άτομο άνθρακα σχηματίζει ομοιοπολικούς δεσμούς σε τετραεδρική δομή με τέσσερα (4) άλλα άτομα άνθρακα, σχηματίζοντας έτσι ένα τρισδιάστατο δίκτυο από συμπτυγμένους εξαμελείς δακτυλίους ατόμων. Το διαμάντι έχει την ίδια κυβική κρυσταλλική δομή που έχει το πυρίτιο και το γερμάνιο, αλλά επειδή η ισχύς των δεσμών C-C είναι πολύ ισχυρότερη, το διαμάντι είναι το σκληρότερο γνωστό υλικό που εμφανίζεται στη φύση, ως προς την αντίσταση στη χάραξη. Αντίθετα από το δημοφιλές μότο «τα διαμάντια είναι για πάντα» (diamonds are forever), στην πραγματικότητα είναι θερμοδυναμικά ασταθή στις κανονικές συνθήκες και γι' αυτό (σταδιακά) μετατρέπονται σε γραφίτη[16]. Ωστόσο, εξαιτίας του υψηλού ενεργειακού εμποδίου ενεργοποίησης της διεργασίας, η μετατροπή του διαμαντιού σε γραφίτη είναι τόσο εξαιρετικά αργή, σε θερμοκρασία δωματίου, ώστε περνά απαρατήρητη. Κάτω από ορισμένες συνθήκες, ο άνθρακας κρυσταλλώνεται σαν λονσδαλεΐτης. Στη μορφή αυτή έχει μια εξαγωνική κρυσταλλική δομή στην οποία όλα τα άτομα συνδέονται ομοιοπολικά. Γι' αυτόν το λόγο, όλες οι ιδιότητες του λονσδαλεΐτη είναι πολύ κοντά σε αυτές του διαμαντιού[34].
Τα φουλερένια έχουν μια δομή που ομοιάζει μ' αυτήν του γραφίτη, αλλά αντί να περιέχουν μόνο εξαγωνικούς δακτυλίους, περιέχουν επίσης πενταγωνικούς (ή ακόμη και επταγωνικούς). Επίσης αντί να σχηματίζουν απλά επίπεδα φύλλα, τα φύλλα τους κάμπτονται σχηματίζοντας σφαιρικές, ελλειπτικές ή κυλινδρικές επιφάνειες. Οι ιδιότητες των φουλερενίων, που διακρίνονται σε μπακυμπάλες (buckyballs), μπακυσωλήνες (buckytubes) και νάνομπαντς (nanobuds) ονομάστηκαν από το όνομα του Ρίτσαρντ Μπάκμινστερ Φούλερ (Richard Buckminster Fuller), που κοινοποίησε τις γεωδαισιακές δομές, που θυμίζουν οι δομές των φουλερενίων. Οι μπακυμπάλες είναι μετρίως μεγάλα μόρια που σχηματίζονται από άτομα άνθρακα που συνδέονται τριγωνικά, σχηματίζοντας σφαιροειδείς δομές. Το πιο γνωστό και απλούστερο από αυτά είναι το μπακμινστερφουλερένιο C60, μια δομή σε σχήμα μπάλας ποδοσφαίρου, με 60 άτομα άνθρακα ανά δομή[28]. Οι μπακυσωλήνες είναι δομικά παρόμοιες με τις μπακυμπάλες, εκτός από το ότι κάθε άτομο άνθρακα συνδέεται τριγωνικά σε ένα φύλλο που κάμπτεται σχηματίζοντας έναν κοίλο κύλινδρο[30][40]. Τα νάνομπαντς έχουν αναφερθεί για πρώτη φορά το 2007 και είναι υβριδικές δομές που περιέχουν συνδυασμούς από μπακυμπάλες και μπακυσωλήνες, συνδυάζοντας έτσι τις ιδιότητες και των δυο απλούστερων δομών[31].
Μια άλλη αλλοτροπική μορφή είναι ο «νανοαφρός άνθρακα» (carbon nanofoam), που είναι μια σιδηρομαγνητική αλλομορφή του άνθρακα, που ανακαλύφθηκε το 1997. Αποτελείται από χαμηλής πυκνότητας συγκροτήματα ατόμων άνθρακα, συγκρατημένες με ένα χαλαρό τρισδιάστατο δίκτυο, στο οποίο τα άτομα συνδέονται τριγωνικά σε εξαμελείς (ή και επταμελείς) δακτυλίους. Είναι ανάμεσα στα ελαφρύτερα γνωστά στερεά σώματα, με πυκνότητα περίπου 2 kg/m³[41]. Παρομοίως, ο «υαλώδης άνθρακας» (glassy carbon) περιέχει ένα υψηλό ποσοστό πορωσιμότητας[35], αλλά σε αντιδιαστολή με τον κανονικό γραφίτη στον οποίο τα γραφιτικά «φύλλα» είναι ενωμένα μεταξύ τους, όπως οι σελίδες σε ένα βιβλίο, στον υαλώδη άνθρακα έχουν μια πιο τυχαία διάταξη. Στο «καρβύνιο» (carbyne) ή «γραμμικό ακετυλενικό άνθρακα» (linear acetylenic carbon)[37] τα «μόρια» έχουν δομή -(C≡C)n-[37]. Ο άνθρακας σε αυτήν την αλλομορφή του έχει υβριδισμό sp και είναι ένα πολυμερές με εναλλαγή απλών και τριπλών δεσμών. Αυτή η αλλομορφή παρουσιάζει ένα αξιόλογο ενδιαφέρον για τη νανοτεχνολογία, γιατί ο συντελεστής ελαστικότητας Γιανκ (Young's modulus) γι' αυτό (δηλαδή το καρβύνιο) είναι 40πλάσιος από αυτό του σκληρότερου γνωστού φυσικού υλικού, δηλαδή του διαμαντιού[42].
Το 2015, μια ομάδα του Πολιτειακού Πανεπιστημίου της Βόρειας Καρολίνας (North Carolina State University) ανακοίνωσε την ανάπτυξη άλλης αλλομορφής άνθρακα, που ονομάστηκε άνθρακας Q (Q-carbon), δημιουργήθηκε με επίδραση υψηλής ενέργειας και χαμηλής διάρκειας παλμού λέιζερ σε σκόνη άμορφου άνθρακα. Ο άνθρακας Q αναφέρθηκε ότι παρουσιάζει σιδηρομαγνητισμό, φθορισμό και σκληρότητα ανώτερη του διαμαντιού.[43]
 |
 
|
 
|
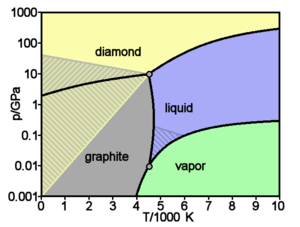
| Ο άνθρακας, χρησιμοποιώντας τη διαθέσιμη ενέργεια που παρέχουν οι κανονικές συνθήκες κρυσταλλώνεται σε γραφίτη (άνω). Σε συνθήκες υψηλής θερμοκρασίας (άνω των 3500 °C) και πίεσης, που αντιστοιχούν σε βάθη 140-190 χιλιομέτρων στο γήινο φλοιό, και διαθέσιμο χρόνο από 1 ως και 3.3 δισεκατομμύρια χρόνια, κρυσταλλώνεται με πιο πυκνή διάταξη των ατόμων του, δηλαδή σε διαμάντι (κάτω). |
Φυσική παρουσία
[Επεξεργασία | επεξεργασία κώδικα]


Ο άνθρακας είναι το τέταρτο πιο άφθονο χημικό στοιχείο κατά μάζα στο σύμπαν, μετά από το υδρογόνο, το ήλιο και το οξυγόνο. Ο άνθρακας είναι άφθονος στον Ήλιο, στα άστρα, στους κομήτες και στις ατμόσφαιρες των περισσότερων (γνωστών) πλανητών. Κάποιοι μετεωρίτες περιέχουν μικροσκοπικά διαμάντια που σχηματίστηκαν όταν το ηλιακό σύστημα ήταν ακόμη ένας πρωτοπλανητικός δίσκος. Μικροσκοπικά διαμάντια επίσης μπορούν να σχηματιστούν με τη συνύπαρξη έντονης πίεσης και υψηλής θερμοκρασίας στα σημεία σύγκρουσης μετεωριτών[44].
Το 2014 η NASA ανακοίνωσε μια πολύ αναβαθμισμένη βάση δεδομένων για τον εντοπισμό πολυκλικών αρωματικών υδρογονανθράκων (Polycyclic Aromatic Hydrocarbons, PAHs) στο σύμπαν. Περισσότερο από το 20% του άνθρακα του σύμπαντος ίσως να σχετίζεται με PAHs, που είναι σύνθετοι υδρογονάνθρακες χωρίς οξυγόνο.[45] Αυτές οι ενώσεις αποτελούν (κεντρικό) θέμα της αποκαλούμενης παγκόσμιας υπόθεσης πολυκυκλικών αρωματικών υδρογονανθράκων (PAH world hypothesis), σύμφωνα με την οποία υποτίθεται ότι έπαιξαν ρόλο στην αβιογένεση και στο σχηματισμό ζωής στο σύμπαν. Οι πολυκυκλικοί αρωματικοί υδρογονάνθρακες φαίνεται να συντέθηκαν 2 δισεκατομμύρια χρόνια ύστερα από τη Μεγάλη Έκρηξη και διασκορπίστηκαν σε όλο το σύμπαν και σχετίζονται με τον σχηματισμό νέων άστρων και με τους εξωπλανήτες.[46]
Εκτιμήθηκε ότι το στερεό τμήμα της Γης περιέχει άνθρακα σε μέση συγκέντρωση 730 ppm, με 2.000 ppm στον πυρήνα και 120 ppm συνολικά στον μανδύα και τον φλοιό του πλανήτη.[47] Εφόσον η μάζα της Γης (εκτιμήθηκε σε) 5.972·1024 kg, τα συνολικά αποθέματα άνθρακα του πλανήτη ανέρχονται σε 4.360 πετατόνους. Η ποσότητα αυτή είναι πολύ μεγαλύτερη από την (εκτιμώμενη) ποσότητα άνθρακα στους ωκεανούς ή την ατμόσφαιρα του πλανήτη (δείτε παρακάτω).
Στον συνδυασμό άνθρακα και οξυγόνου στο διοξείδιο του άνθρακα της ατμόσφαιρας της Γης περιέχονται (συνολικά) περίπου 810 δισεκατομμύρια τόνοι άνθρακα, ενώ στο διαλυμένο (διοξείδιο του άνθρακα) στα υδάτινα σώματα (ωκεανοί κ.τ.λ.) περιέχονται (συνολικά) περίπου 36 τρισεκατομμύρια τόνοι άνθρακα. Ακόμη, περίπου 1,9 τρισεκατομμύρια τόνοι άνθρακα περιέχονται στη βιόσφαιρα. Τα ορυκτά ανθρακούχα κοιτάσματα (κάρβουνο, πετρέλαιο και φυσικό αέριο) περιέχουν γύρω στα 900 δισεκατομμύρια τόνους άνθρακα. Ειδικότερα στα κοιτάσματα πετρελαίου περιέχονται περίπου 150 δισεκατομμύρια τόνοι άνθρακα. Στα βεβαιωμένα κοιτάσματα φυσικού αερίου περιέχονται περίπου άλλοι 105 δισεκατομμύρια τόνοι άνθρακα, αλλά εκτιμάται ότι υπάρχουν επίσης 900 δισεκατομμύρια τόνοι άνθρακα στα μη βεβαιωμένα (ακόμη) κοιτάσματα φυσικού αερίου, συμπεριλαμβανομένου και του σχιστολιθικού φυσικού αερίου. Ειδικότερα, στα τελευταία (δηλαδή στα κοιτάσματα σχιστολιθικού φυσικού αερίου) περιέχονται περίπου 540 δισεκατομμύρια τόνοι άνθρακα[48]. Άνθρακας παγιδεύθηκε επίσης στους μεθανυδρίτες των πολικών περιοχών και υποθαλάσσια. Έγιναν διάφορες εκτιμήσεις για τη συνολική ποσότητα άνθρακα που αντιπροσωπεύουν τα κοιτάσματα αυτά, που κυμαίνονται μεταξύ 500 και 3.000 δισεκατομμυρίων τόνων[49][50]. Στο παρελθόν οι ποσότητες των ορυκτών υδρογονανθράκων ήταν μεγαλύτερες. Σύμφωνα με μια πηγή, στη χρονική περίοδο μεταξύ 1751 και 2008 καταναλώθηκαν περίπου 347 δισεκατομμύρια τόνων ορυκτού άνθρακα και εκλύθηκαν στην ατμόσφαιρα με τη μορφή διοξειδίου του άνθρακα από τις καύσεις των ορυκτών καυσίμων[51]. Ωστόσο, μια άλλη πηγή υπολογίζει την ποσότητα άνθρακα που προστέθηκε στην ατμόσφαιρα από το 1750 σε 879 δισεκατομμύρια τόνους, ενώ συνολικά κατέληξαν στην ατμόσφαιρα, στη θάλασσα και στη γη (σε τυρφώνες) σχεδόν 2 τρισεκατομμύρια τόνοι άνθρακα[52].
Ο άνθρακας είναι ένα κύριο συνθετικό σε πολύ μεγάλες μάζες ανθρακούχων πετρωμάτων (που περιλαμβάνουν ασβεστόλιθο, δολομίτη, μάρμαρο, κ.ά.). Ο γαιάνθρακας είναι η μεγαλύτερη εμπορική πηγή ορυκτού άνθρακα, μετρώντας για περίπου 9 τρισεκατομμύρια τόνους άνθρακα ή το 80% του ορυκτού καύσιμου άνθρακα[53]. Είναι επίσης ένα πολύ πλούσιο σε άνθρακα υλικό, αφού για παράδειγμα ο ανθρακίτης περιέχει 92–98% άνθρακα[54].
Όσο για τις ανεξάρτητες αλλομορφές άνθρακα, ο γραφίτης βρίσκεται σε μεγάλες ποσότητες στις ΗΠΑ (κυρίως στις πολιτείες της Νέας Υόρκης και του Τέξας), στη Ρωσία, στο Μεξικό, στη Γροιλανδία και στην Ινδία. Τα φυσικά διαμάντια βρίσκονται σε πέτρωμα κιμπερλίτη, που βρίσκεται σε αρχαίους ηφαιστειακούς «λαιμούς» ή «σωλήνες». Τα μεγαλύτερα αποθέματα διαμαντιού βρίσκονται στην Αφρική, περισσότερο στη Νότια Αφρική, στη Ναμίμπια, στη Μποτσουάνα, στη Δημοκρατία του Κονγκό και στη Σιέρα Λεόνε. Υπάρχουν επίσης αποθέματα διαμαντιού στο Αρκάνσας, στον Καναδά, στη Ρωσική Αρκτική, στη Βραζιλία, καθώς και στη Βόρεια και Δυτική Αυστραλία. Διαμάντια έχουν επίσης ανακαλυφθεί στον ωκεάνιο πυθμένα του Ακρωτηρίου της Καλής Ελπίδος. Ωστόσο, εκτός από τα φυσικά διαμάντια, περίπου το 30% όλων των βιομηχανικά χρησιμοποιούμενων διαμαντιών στις ΗΠΑ είναι πλέον συνθετικά.
Ο άνθρακας-14 σχηματίζεται στα ανώτερα στρώματα της τροπόσφαιρας και στη στρατόσφαιρα, σε υψόμετρα 9 - 15 χιλιομέτρων, με μια αντίδραση που ενεργοποιείται από τις κοσμικές ακτίνες, και σταδιακά καθιζάνει[55]. Παράγονται θερμικά νετρόνια που συγκρούονται με πυρήνες αζώτου-14 και σχηματίζουν άνθρακα-14 και ένα πρωτόνιο:
Ισότοπα
[Επεξεργασία | επεξεργασία κώδικα]Τα ισότοπα του άνθρακα έχουν ατομικό πυρήνα που περιέχει έξι (6) πρωτόνια και επιπλέον έναν αριθμό νετρονίων, που κυμαίνονται από 2 - 16. Ο άνθρακας έχει δύο (2) σταθερά φυσικά ισότοπα[13]:
- Το ισότοπο 12C, που αποτελεί το 98,93% του άνθρακα στη Γη.
- Το ισότοπο 13C, που αποτελεί το υπόλοιπο 1,07%[13].
Η ισοτοπική συγκέντρωση του 12C αυξάνεται σε βιολογικά υλικά, επειδή οι βιοχημικές αντιδράσεις είναι (σχετικά) εκλεκτικές εναντίον της χρήσης του 13C. Το 1961, η IUPAC υιοθέτησε το ισότοπο 12C ως πρότυπο για την ατομική μονάδα μάζας, ορίζοντάς την στο 1/12 της ισοτοπικής μάζας του 12C[56]. Η ταυτοποίηση του άνθρακα σε πειράματα, με χρήση φασματοσκοπίας NMR, γίνεται χάρη στο ισότοπο 13C[57].
Ο άνθρακας-14 (14C) είναι ένα φυσικό ραδιοϊσότοπο του άνθρακα που υπάρχει σε ίχνη στη Γη, μέχρι το 1 ppt, ο περισσότερος περιορίζεται στην ατμόσφαιρα και σε επιφανειακά αποθέματα, κυρίως τύρφης και άλλων οργανικών υλικών[58]. Το ισότοπο αυτό διασπάται με εκπομπή β- ισχύος 158 keV. Εξαιτίας της σχετικά μικρής ημιζωής του, που ανέρχεται σε 5.730 έτη, ο 14C ουσιαστικά απουσιάζει από αρχαία πετρώματα, αλλά σχηματίζεται μεταξύ άνω τροπόσφαιρας και κάτω στρατόσφαιρας με την επίδραση των κοσμικών ακτίνων στο ατμοσφαιρικό άζωτο[59]. Η (σχετική) αφθονία του 14C είναι σχετικά σταθερή στην ατμόσφαιρα και στους ζωντανούς οργανισμούς, αλλά μειώνεται προβλέψιμα σε πτώματα. Αυτή η ιδιότητα αξιοποιείται από τη λεγόμενη ραδιοχρονολόγηση με άνθρακα-14, που εφευρέθηκε το 1949, και που εφαρμόστηκε εκτενώς για τον καθορισμό της ηλικίας ανθρακούχων υλικών, μέχρι περίπου 40.000 έτη[60][61].
Ακόμη, υπάρχουν 15 γνωστά βραχύβια ισότοπα του άνθρακα, από τα οποία ο 8C διασπάται μέσω εκπομπής πρωτονίου και α-διάσπασης με ημιζωή 1,98739·10−21 s[62]. Ο «εξωτικός» 19C εμφανίζει έναν πυρήνα αλογόνου, που σημαίνει ότι η ακτίνα του είναι σημαντικά μεγαλύτερη από αυτή που θα αναμενόταν, αν ο πυρήνας ήταν μια σφαίρα με σταθερή πυκνότητα[63].
Σχηματισμός στα άστρα
[Επεξεργασία | επεξεργασία κώδικα]Ο σχηματισμός του ατομικού πυρήνα του άνθρακα απαιτεί μια σχεδόν ταυτόχρονη σύγκρουση τριών (3) σωματιδίων α (δηλαδή πυρήνων ηλίου) μέσα στον πυρήνα ενός γιγάντιου ή υπεργιγάντιου άστρου, μια διαδικασία που είναι γνωστή ως διεργασία 3α (triple-alpha process), καθώς τα προϊόντα επιπλέον αντιδράσεων πυρηνικής σύντηξης ηλίου με υδρογόνο ή δύο πυρήνων ηλίου παράγουν αντίστοιχα λίθιο-5 και βηρύλλιο-8, που και τα δυο είναι πολύ ασταθή και διασπώνται σχεδόν ακαριαία πίσω σε μικρότερους πυρήνες[64]. Η τριπλή αυτή σύγκρουση συμβαίνει σε θερμοκρασίες πάνω από 100 εκατομμύρια Κέλβιν και (σχετικά υψηλή) συγκέντρωση πυρήνων ηλίου, δηλαδή συνθήκες που η ταχεία επέκταση και ψύξη του πρωτοσύμπαντος έκαναν απαγορευτικές. Γι' αυτό δεν σχηματίστηκε σημαντική ποσότητα άνθρακα κατά τη Μεγάλη Έκρηξη. Αντίθετα, τα εσωτερικά των άστρων επέτρεψαν σε οριζόντιο κλάδο τη μετατροπή τριών (3) πυρήνων ηλίου σε πυρήνα άνθρακα, με τη διεργασία 3α[65]. Για να είναι διαθέσιμος για το σχηματισμό της ζωής όπως την ξέρουμε, αυτός ο άνθρακας πρέπει στη συνέχεια να διασκορπίστηκε στο διάστημα, σε μορφή σκόνης, μάλλον σε εκρήξεις σουπερνόβα, ως μέρος του υλικού που σχηματίζει αργότερα τη δεύτερη, ή και την τρίτη γενιά αστρικών συστημάτων, που έχουν πλανήτες που φτιάχτηκαν (και από αυτήν τη) σκόνη. [66]. Το ηλιακό σύστημα είναι ένα τέτοιο τρίτης γενιάς αστρικό σύστημα. Άλλοι μηχανισμοί πυρηνικής σύντηξης που συμβαίνουν στα άστρα και σχετίζονται με τον άνθρακα είναι ο κύκλος CNO, στον οποίο ο άνθρακας δρα ως ένας καταλύτης που επιτρέπει στον κύκλο να συνεχίζεται.
Περιοδικές εκπομπές διαφόρων ισοτοπικών μορφών του μονοξειδίου του άνθρακα (για παράδειγμα 12CO, 13CO και 18CO) είναι ανιχνεύσιμες σε υποχιλιοστομετρικό εύρος μηκών κύματος, και χρησιμοποιείται στη μελέτη νεογέννητων άστρων (star formation) σε μοριακά νεφελώματα[67].
Ο κύκλος του άνθρακα
[Επεξεργασία | επεξεργασία κώδικα]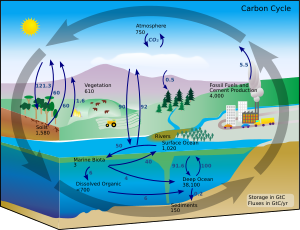
Στις γήινες συνθήκες, η μετατροπή ενός χημικού στοιχείου σε ένα άλλο είναι πολύ σπάνια. Γι' αυτό, η ποσότητα του άνθρακα στη Γη είναι ουσιαστικά σταθερή. Έτσι, διεργασίες που χρησιμοποιούν άνθρακα πρέπει να τον λάβουν από κάπου, και να αποθέσουν το προϊόν της διεργασίας κάπου αλλού. Οι διαδρομές που ακολουθεί ο άνθρακας μέσα στο (γήινο) περιβάλλον σχηματίζουν τον λεγόμενο κύκλο του άνθρακα (carbon cycle), μια διεργασία φυσικής ανακύκλωσης του γήινου άνθρακα. Για παράδειγμα, τα φυτά απορροφούν διοξείδιο του άνθρακα από την ατμόσφαιρα και το χρησιμοποιούν για να παράγουν βιομάζα, με τη διεργασία της αναπνοής άνθρακα (carbon respiration) ή τον κύκλο του Κάλβιν (Calvin cycle), μια διεργασία δέσμευσης του άνθρακα. Κάποια από αυτήν τη βιομάζα (των φυτών) καταναλώνεται από τα ζώα, όπου κάποια ποσότητα από αυτόν τον άνθρακα εκπνέεται από αυτά τα ζώα ως διοξείδιο του άνθρακα. Ο κύκλος του άνθρακα είναι σημαντικά πιο πολύπλοκος από αυτόν το μικρό κύκλο: Για παράδειγμα, κάποια ποσότητα διοξειδίου του άνθρακα διαλύεται στους ωκεανούς. Τα νεκρά φυτά και ζώα μπορεί να καταναλωθούν από βακτήρια ή και να μετατραπούν σε πετρέλαιο ή γαιάνθρακα, που μπορούν να καούν και να απελευθερώσουν διοξείδιο του άνθρακα[68][69].
Χημικές ενώσεις του άνθρακα
[Επεξεργασία | επεξεργασία κώδικα]Οργανικές ενώσεις
[Επεξεργασία | επεξεργασία κώδικα]
.

Ο άνθρακας έχει την ικανότητα να σχηματίζει πολύ μακριές αλυσίδες με δεσμούς C-C. Αυτή η ιδιότητα ονομάζεται αλυσοποίηση (catenation). Οι δεσμοί C-C είναι ισχυροί και σταθεροί. Αυτή η ιδιότητα επιτρέπει στον άνθρακα να μπορεί να σχηματίσει ένα σχεδόν άπειρο αριθμό πιθανών ενώσεων. Στην πραγματικότητα, οι γνωστές ανθρακούχες ενώσεις είναι περισσότερες από τις ενώσεις όλων των υπόλοιπων χημικών στοιχείων, εκτός από αυτές του υδρογόνου, γιατί οι περισσότερες οργανικές ενώσεις περιέχουν υδρογόνο.
Η απλούστερη μορφή οργανικών ενώσεων είναι οι υδρογονάνθρακες, μια μεγάλη οικογένεια οργανικών ενώσεων που περιέχουν μόνο άνθρακα και υδρογόνο. Το μήκος της ανθρακικής αλυσίδας, η ύπαρξη διακλαδώσεων και λειτουργικών ομάδων επηρεάζουν τις ιδιότητες των οργανικών ενώσεων.
Ο άνθρακας υπάρχει σε όλες τις γνωστές μορφές ζωής και είναι η βάση της Οργανικής Χημείας. Όταν οι ανθρακικές αλυσίδες ενώνονται με άτομα υδρογόνου σχηματίζονται οι διάφοροι υδρογονάνθρακες, που είναι σημαντικοί για τη βιομηχανία, ως ψυκτικά υγρά για ψυγεία, ως λιπαντικά, ως διαλύτες, ως πρόδρομες χημικές ουσίες για την παραγωγή πλαστικών και άλλων πετροχημικών προϊόντων, καθώς και ως καύσιμα.
Όταν συνδυάζονται άνθρακας, υδρογόνο και οξυγόνο, μπορούν να σχηματιστούν σημαντικές βιολογικές χημικές ενώσεις, που περιλαμβάνουν σάκχαρα, λιγνάνες, χιτίνες, αλκοόλες, λίπη, αρωματικούς εστέρες, καροτενοειδή και τερπένια. Μαζί και με το άζωτο σχηματίζονται αλκαλοειδή, που με την προσθήκη και θείου σχηματίζουν επίσης αντιβιοτικά, αμινοξέα και λαστιχένια προϊόντα. Μαζί και με το φωσφόρο, τα παραπάνω χημικά στοιχεία (δηλαδή ο άνθρακας, το υδρογόνο, το οξυγόνο, το άζωτο, το θείο και ο φωσφόρος) σχηματίζουν DNA και RNA, τον χημικό γενετικό κώδικα, το φορέα της ζωής, καθώς και το ATP, το σημαντικότερο μεταφορέα ενέργειας για όλα τα ζωντανά κύτταρα.
Ανόργανες ενώσεις
[Επεξεργασία | επεξεργασία κώδικα]Συνήθως ανθρακούχες ενώσεις που σχετίζονται με ορυκτά ή που δεν περιλαμβάνουν υδρογόνο ούτε φθόριο, έχουν μεταχείριση διαφορετική από τις κλασσικές οργανικές ενώσεις. Ωστόσο ο ορισμός των ανόργανων ενώσεων του άνθρακα δεν είναι άκαμπτος. Περιλαμβάνει τα πιο απλά οξείδια του άνθρακα, δηλαδή το μονοξείδιο του άνθρακα (CO) και το διοξείδιο του άνθρακα (CO2). Το τελευταίο (δηλαδή το διοξείδιο του άνθρακα) ήταν κάποτε κύριο συστατικό της παλαιοατμόσφαιρας της Γης, αλλά είναι δευτερεύον συστατικό της σημερινής ατμόσφαιρας του πλανήτη μας[70]. Όταν το διοξείδιο του άνθρακα διαλύεται στο νερό, σχηματίζει το ανθρακικό οξύ (H2CO3), αλλά οι περισσότερες ενώσεις με πολλαπλά άτομα οξυγόνου συνδεδεμένα και με απλό δεσμό σε ένα μοναδικό άτομο άνθρακα είναι ασταθείς[71]. Μέσω αυτού του ενδιάμεσου (δηλαδή του ανθρακικού οξέος) παράγονται ανθρακικά ιόντα (CO32-), που σταθεροποιούνται μέσω του φαινομένου του συντονισμού ή μεσομέρειας. Κάποια σημαντικά ορυκτά είναι ανθρακικά, όπως ο αξιοσημείωτος ασβεστίτης. Ο διθειάνθρκας (CS2) είναι παρόμοια (δομικά) ένωση. Το άλλο συνηθισμένο οξείδιο είναι το μονοξείδιο του άνθρακα (CO). Σχηματίζεται με ατελή καύση ανθρακούχων υλικών. Είναι ένα άχρωμο και άοσμο αέριο (στις κανονικές συνθήκες περιβάλλοντος). Το μόριό του περιέχει έναν τριπλό δεσμό και είναι μέτρια πολικό, με αποτέλεσμα να έχει μια τάση να σχηματίζει ένα μόνιμο δεσμό με την αιμοσφαιρίνη, εκτοπίζοντας το οξυγόνο, γεγονός που οδηγεί σε χαμηλότερη ικανότητα οξυγόνωσης του αίματος[72][73]. Τα κυανιούχα ιόντα (CN-) έχουν παρόμοια δομή, αλλά συμπεριφέρονται πολύ όμοια με τα ιόντα των αλογόνων, και γι' αυτό ονομάζονται συχνά «ψευδοαλογόνο». Για παράδειγμα σχηματίζει το δικυάνιο [(CN)2], όμοια με το σχηματισμό των διατομικών μορίων των στοιχειακών αλογόνων. Μερικά άλλα, λιγότερο συνηθισμένα και (επομένως λιγότερο) γνωστά οξείδια του άνθρακα είναι το υποξείδιο του άνθρακα (C3O2)[73], το ασταθές μονοξείδιο του διάνθρακα (C2O)[74][75], το τριοξείδιο του άνθρακα (CO3)[76][77], η κυκλοπεντανοπεντόνη (C5O5)[78], η κυκλοεξανοεξόνη (C6O6)[78] και ο μελλιτικός ανυδρίτης (C12O9).
Με δραστικά μέταλλα, όπως το βολφράμιο, ο άνθρακας σχηματίζει καρβίδια (C4-) ή ακετυλενίδια (C22-) ή και κράματα με υψηλές θερμοκρασίες τήξης. Αυτά τα ανιόντα σχετίζονται επίσης με το μεθάνιο και το αιθίνιο, που είναι και τα δυο πολύ ασθενή οξέα. Με ηλεκτραρνητικότητα ίση με 2,5[79], ο άνθρακας «προτιμά» να σχηματίζει ομοιοπολικούς δεσμούς. Λίγα καρβίδια, όμως, έχουν ομοιοπολικές δομές, όπως για παράδειγμα το καρβίδιο του πυριτίου (SiC).
Οι οργανομεταλλικές ενώσεις
[Επεξεργασία | επεξεργασία κώδικα]Ως οργανομεταλλικές ενώσεις ορίστηκαν οι ενώσεις που περιέχουν τουλάχιστον ένα δεσμό άνθρακα - μετάλλου. Υπάρχει ένα μεγάλο εύρος τέτοιων ενώσεων. Οι κύριες τάξεις τους περιλαμβάνουν απλές αλκυλομεταλλικές ενώσεις, όπως για παράδειγμα ο τετραιθυλομόλυβδος, η²-αλκενοενώσεις, όπως για παράδειγμα το άλας Ζάις (Zeise's salt), τις η³-αλλυλενώσεις, όπως για παράδειγμα το δι(αλλυλοπαλλαδιοχλωρίδιο), τα μεταλλοκένια, που περιέχουν κυκλοπενταδιενυλο- συναρμωτές, όπως για παράδειγμα το φερροκένιο, και τα καρβενοσύμπλοκα των μεταβατικών μετάλλων, όπως για παράδειγμα το τετρακαρβονυλονικέλιο, αν και αρκετοί συγγραφείς σχετικών εγχειριδίων θεωρούν ότι οι ενώσεις με το μονοξείδιο του άνθρακα ως συναρμωτή ανήκουν στις καθαρά ανόργανες ενώσεις και όχι στις οργανομεταλλικές.
Παρόλο που είναι κατανοητό ότι ο άνθρακας σχηματίζει αποκλειστικά τέσσερις (4) δεσμούς, έχει αναφερθεί μια ενδιαφέρουσα ένωση που περιέχει ένα οκταεδρικό άτομο άνθρακα με έξι (6) συναρμοτές: Πρόκειται για το σύμπλοκο κατιόν [(Ph3PAu)6C]2+. Αυτό το φαινόμενο αποδόθηκε στη χρυσοφιλία των συναρμωτών του χρυσού[80].
Ιστορία και ετυμολογία
[Επεξεργασία | επεξεργασία κώδικα]

Η αγγλική ονομασία carbon προέρχεται από τη λατινική carbo, που χρησιμοποιούνταν για το γαιάνθρακα και τον ξυλάνθρακα[81], από την οποία προήλθε επίσης η γαλλική charbon, που σημαίνει ξυλάνθρακας. Στα γερμανικά, στα ολλανδικά και στα δανικά οι ονομασίες για τον άνθρακα είναι kohlenstoff, koolstof και kulstof, αντιστοίχως, που όλες κυριολεκτικά σημαίνουν «ανθρακούχα ουσία».
Ο άνθρακας ανακαλύφθηκε κατά την Προϊστορία και ήταν γνωστό στις μορφές της αιθάλης και του ξυλοκάρβουνου από τους παλαιότερους ανθρώπινους πολιτισμούς. Τα διαμάντια ήταν γνωστά πιθανώς από το 2500 π.Χ. στην Κίνα, ενώ ο άνθρακας με τη μορφή του ξυλοκάρβουνου παραγόταν κατά τη Ρωμαϊκή Εποχή με την ίδια χημεία που παράγεται και σήμερα, δηλαδή με θέρμανση μιας πυραμίδας από ξύλα καλυμμένης με πηλό, για να αποκλειστεί η είσοδος αέρα[82][83].
Το 1722, ο Ρενέ Αντουάν Φερσώ ντε Ρεωμύρ επέδειξε τη μετατροπή του σιδήρου σε χάλυβα μέσω απορρόφησης μιας ουσίας, που τώρα είναι πια γνωστή ως άνθρακας[84]. Το 1772, ο Αντουάν Λωράν Λαβουαζιέ απέδειξε ότι τα διαμάντια είναι μια μορφή άνθρακα, αφού όταν καίγονται δείγματα ξυλοκάρβουνου ή διαμαντιού δεν παράγεται ίχνος υγρασίας και επιπλέον και τα δυο εκλύουν την ίδια ποσότητα διοξειδίου του άνθρακα, ανά γραμμάριο δείγματος[85]. Το 1779, ο Καρλ Βίλχελμ Σέελε (Carl Wilhelm Scheele) έδειξε ότι ο γραφίτης, που νόμιζαν τότε ότι είναι μια μορφή μολύβδου, είναι ομοούσιος με το ξυλοκάρβουνο, αλλά με μια μικρή πρόσμειξη σιδήρου, και ότι έδινε αέριο οξύ (aerial acid, όπως ονόμαζε τότε ο ερευνητής το διοξείδιο του άνθρακα) όταν επιδρούσε (στο γραφίτη) με νιτρικό οξύ[86]. Το 1786, οι Γάλλοι επιστήμονες Κλωντ Λουί Μπερτολέ, Γκασπάρ Μονζ και Βαντερμόντ επιβεβαίωσαν ότι ο γραφίτης αποτελείται κυρίως από άνθρακα, οξειδώνοντάς τον με τον ίδιο τρόπο που είχε χρησιμοποιήσει ο Λαβουαζιέ για το διαμάντι[87]. Κάποια πρόσμειξη σιδήρου και πάλι απέμεινε, γεγονός που οδήγησε τους Γάλλους ερευνητές επιστήμονες στη σκέψη ότι ο σίδηρος είναι απαραίτητος για τη δομή του γραφίτη. Ωστόσο, στη δημοσίευσή τους πρότειναν την ονομασία carbone (από το λατινικό carbonum) για το χημικό στοιχείο στο γραφίτη, που σχημάτιζε ένα αέριο όταν καίγονταν ο γραφίτης. Τελικά, ο Λαβουαζιέ περιέλαβε και τον άνθρακα στη λίστα των χημικών στοιχείων στο βιβλίο του το 1789[88].
Μια ένα αλλομορφή του άνθρακα, το φουλερένιο, ανακαλύφθηκε το 1985[89], που περιλαμβάνει νανοδομές μορφών όπως οι μπακισφαίρες και οι νανοσωλήνες[28]. Οι εφευρέτες τους, Ρόμπερτ Κερλ (Robert Curl), Χάρρυ Κρότο (Harold Kroto) και Ρίτσαρντ Σμώλυ (Richard Smalley), έλαβαν το Βραβείο Νόμπελ Χημείας το 1996[90]. Το αποτέλεσμα των ερευνών τους ανανέωσε το ενδιαφέρον για νέες αλλομορφές και οδήγησε στην ανακάλυψη επιπλέον εξωτικών αλλομορφών, που περιλαμβάνουν τον υαλώδη άνθρακα και τη συνειδητοποίηση ότι ο αποκαλούμενος «άμορφος άνθρακας» δεν είναι τελείως άμορφος[35].
Παραγωγή
[Επεξεργασία | επεξεργασία κώδικα]Γραφίτης
[Επεξεργασία | επεξεργασία κώδικα]Εμπορικά βιώσιμα φυσικά κοιτάσματα γραφίτη υπάρχουν σε πολλά μέρη του πλανήτη μας, αλλά οι πιο σημαντικές οικονομικά πηγές είναι στην Κίνα, στην Ινδία, στη Βραζιλία και στη Βόρεια Κορέα. Τα κοιτάσματα γραφίτη είναι μεταμορφωσιγενή. Βρίσκονται μαζί με χαλαζία, μαρμαρυγίες και άστριους σε σχιστόλιθους, γνεύσιους και μεταμορφωμένους αμμόλιθους και ασβεστόλιθους, με τη μορφή θύλακα ή φλέβας, μερικές φορές πάχους ενός μέτρου ή μεγαλύτερο. Κοιτάσματα γραφίτη στην Μπορροουντέιλ (Borrowdale), στο Κάμπερλαντ (Cumberland) της Αγγλίας είχαν στην αρχή σημαντικό μέγεθος και καθαρότητα, οπότε μέχρι το 19ο αιώνα τα μολύβια φτιάχνονταν απλά από πριονισμένα κομμάτια φυσικού γραφίτη σε λωρίδες, πριν κλειστούν μέσα σε ξύλινο πλαίσιο. Σήμερα, μικρότερα κοιτάσματα γραφίτη παίρνονται με σύνθλιψη του πετρώματος και επίπλευση του γραφίτη, που είναι ελαφρύτερος από το νερό[91].
Υπάρχουν τρεις τύποι φυσικού γραφίτη: Ο «άμορφος», ο «φυλλώδης» ή «κρυσταλλινοφυλλώδης» και η φλέβα ή σβώλος. Ο άμορφος γραφίτης είναι η πιο χαμηλή σε ποιότητα και πιο άφθονη σε ποσότητα. Σε αντίθεση με τους επιστημονικούς όρους, στη βιομηχανία ο όρος «άμορφος» αναφέρεται στο πολύ μικρό κρυσταλλικό μέγεθος και όχι στην απόλυτη απουσία κρυσταλλικής δομής. Ο άμορφος γραφίτης χρησιμοποιείται για κατώτερης ποιότητας προϊόντα γραφίτη και είναι ο πιο φθηνός γραφίτης. Μεγάλα αποθέματα αυτού του γραφίτη έχουν βρεθεί στην Κίνα, στην Ευρώπη, στο Μεξικό και στις ΗΠΑ. Ο φυλλώδης γραφίτης είναι μια λιγότερο συνηθισμένη και υψηλότερης ποιότητας γραφίτης (σε σύγκριση με τον άμορφο). Βρίσκεται σε ξεχωριστές πλάκες που κρυσταλλώθηκαν σε ένα μεταμορφωσιογενές πέτρωμα. Ο φυλλώδης γραφίτης μπορεί να έχει ως και τετραπλάσια οικονομική αξία σε σχέση με τον άμορφος. Οι καλής ποιότητας πλάκες μπορούν να επεξεργαστούν σε «επεκτάσιμο γραφίτη» για πολλές χρήσεις, όπως επιβραδυντικά φλόγας. Κοιτάσματα φυλλώδους γραφίτη έχουν βρεθεί στην Αυστρία, στη Βραζιλία, στον Καναδά, στην Κίνα, στη Γερμανία και στη Μαδαγασκάρη. Οι φλέβες ή σβώλοι γραφίτη είναι ο πιο σπάνιος και πιο ακριβός οικονομικά τύπος φυσικού γραφίτη. Βρίσκεται στις φλέβες με διακοπτόμενες επαφές με στερεούς σβώλους γραφίτη. Το μόνο οικονομικά βιώσιμο κοίτασμα τέτοιου γραφίτη που εξορύσσεται βρίσκεται στη Σρι Λάνκα[91].
Σύμφωνα με τη Γεωλογική Επιθεώρηση των ΗΠΑ (USGS), η παγκόσμια παραγωγή σε φυσικό γραφίτη ήταν 1,1 εκατομμύρια τόννοι το 2010, από την οποία η Κίνα συνεισέφερε 800.000 τόννους, η Ινδία 130.000 τόννους, η Βραζιλία 76.000 τόννους, η Βόρεια Κορέα 30.000 τόννους και ο Καναδάς 25.000 τόννους. Δεν αναφέρθηκε εξόρυξη φυσικού γραφίτη στις ΗΠΑ, αλλά αντ' αυτού παράχθηκαν το 2009 118.000 συνθετικού γραφίτη, με εκτιμώμενη αξία 998 εκατομμύρια δολάρια[91].
Διαμάντια
[Επεξεργασία | επεξεργασία κώδικα]Η αλυσίδα προμήθειας διαμαντιών ελέγχεται από έναν περιορισμένο αριθμό ισχυρών εταιρειών, και η εξόρυξή τους είναι πολύ συγκεντρωμένη σε ένα μικρό αριθμό τοποθεσιών παγκοσμίως.
Μόνο ένα μικρό κλάσμα του υλικού που εξορύσσεται από τα αδαμαντορυχεία αποτελείται από πραγματικά διαμάντια. Το εξόρυγμα συνθλίβεται, αλλά με τρόπο που αποφεύγει την καταστροφή τυχόν μεγάλων διαμαντιών, και επομένως τα υλικά προϊόντα αυτής της «προσεκτικής» σύνθλιψης ταξινομούνται κατά πυκνότητα. Σήμερα, τα διαμάντια εντοπίζονται στο πλούσιο σε διαμάντια κλάσμα πυκνότητας της παραπάνω ταξινόμησης με χρήση φθορισμού με ακτίνες Χ. Μετά τον εντοπισμό τους, τα τελικά στάδια κατάταξης γίνονται χειροποίητα. Πριν γίνει συνηθισμένη η χρήση των ακτίνων Χ, ο διαχωρισμός γινόταν με ζώνες γράσου, εφόσον τα διαμάντια έχουν μεγαλύτερη τάση να κολλάνε στο γράσο από τα υπόλοιπα υλικά που εξορύσσονται αρχικά μαζί τους στο κοίτασμα[92].
Ιστορικά, τα διαμάντια ήταν γνωστό ότι βρίσκονται μόνο στα προσχωματικά κοιτάσματα στη νότια Ινδία[93]. Η Ινδία προηγήθηκε στον κόσμο σε εξόρυξη διαμαντιών από τον καιρό της ανακάλυψής τους, περίπου κατά τον 9ο αιώνα π.Χ.[94] ως τα μέσα του 18ου αιώνα μ.Χ., αλλά η εμπορική δυναμική αυτών των κοιτασμάτων εξαντλήθηκε κατά τα τέλη του 18ου αιώνα και από τότε η Ινδία αντικαταστάθηκε (στην πρώτη θέση παραγωγής διαμαντιών) από τη Βραζιλία, όπου βρέθηκαν για πρώτη φορά διαμάντια εκτός της Ινδίας το 1725[95].
Η παραγωγή διαμαντιών από τα κύρια κοιτάσματα (κιμπερλίτες και λαμπροΐτες) άρχισε από τη δεκαετία 1870, μετά από την ανακάλυψη αδαμαντοφόρων πεδίων στη Νότια Αφρική. Η παραγωγή αυξήθηκε με το χρόνο και τώρα υπολογίστηκε ότι μέχρι σήμερα εξορύχτηκαν 4,5 δισεκατομμύρια καράτια διαμαντιών[96]. Περίπου 20% της παραπάνω ποσότητας εξορύχτηκε κατά τα τελευταία 5 χρόνια μόνο, ενώ κατά τα τελευταία 10 χρόνια 9 νέα ορυχεία άρχισαν να παράγουν και 4 επιπλέον ετοιμάζονται να ανοίξουν σύντομα. Τα περισσότερα από αυτά τα ορυχεία εντοπίζονται στον Καναδά, στη Ζιμπάμπουε, στην Ανγκόλα και στη Ρωσία[96].
Στις ΗΠΑ, διαμάντια βρέθηκαν στο Αρκάνσας, στο Κολοράντο και στη Μοντάνα[97][98]. Το 2004 έγινε μια ανακάλυψη ενός μικροσκοπικού διαμαντιού στις ΗΠΑ[99], που οδήγησε τον Ιανουάριο του 2008 στην ανακάλυψη σωλήνων κιμπερλίτη σε μια απομακρυσμένη περιοχή της Μοντάνα[100].
Σήμερα, τα πιο βιώσιμα οικονομικών κοιτάσματα διαμαντιών βρίσκονται στη Ρωσία, στη Μποτσουάνα, στην Αυστραλία και στο Κογκό[101]. Το 2005 παράχθηκε στη Ρωσία περίπου το 1/5 της παγκόσμιας παραγωγής διαμαντιών, σύμφωνα με αναφορές της Βρετανικής Γεωλογικής Επιθεώρησης. Η Αυστραλία έχει τον πλουσιότερο αδαμαντοφόρο σωλήνα με ετήσια παραγωγή που έφθασε στο μέγιστο των 42 μετρικούς τόνους στη δεκαετία του 1990[97]. Υπάρχουν ακόμη εμπορικά κοιτάσματα που εξορύσσονται στις Βορειοδυτικές περιοχές του Καναδά, στη Σιβηρία (κυρίως στη Γιακουτία, για παράδειγμα οι αδαμαντοφόροι σωλήνες Μιρ και Ουντάτσναγια), καθώς και στη Βόρεια και Δυτική Αυστραλία.
Εφαρμογές
[Επεξεργασία | επεξεργασία κώδικα]





Ο άνθρακας είναι ζωτικής σημασίας για όλες τις γνωστές μορφές ζωής, δηλαδή χωρίς αυτόν δεν εννοείται ζωή, τουλάχιστον όπως την ξέρουμε (δείτε την εναλλακτική βιοχημεία, για κάποιες υποθετικές αντιρρήσεις). Η κύρια οικονομική χρήση του άνθρακα, πέρα από τη χρήση ανθρακούχων τροφών και της ξυλείας, γίνεται με τη μορφή των υδρογονανθράκων, με μεγαλύτερη έμφαση στα καύσιμα που προέρχονται από το φυσικό αέριο και το αργό πετρέλαιο. Το αργό πετρέλαιο χρησιμοποιείται από την πετροχημική βιομηχανία για την παραγωγή, μεταξύ άλλων, βενζίνης και κηροζίνης, μέσω της διεργασίας της διύλισης, σε διυλιστήρια. Η κυτταρίνη είναι ένα φυσικό ανθρακούχο πολυμερές που παράγεται από τα φυτά, αν και συνήθως λαμβάνεται από το βαμβάκι, το λινάρι και την κάνναβη. Η κυτταρίνη χρησιμοποιείται κυρίως για τη διατήρηση της δομής των φυτών. Υπάρχουν και ζωικής προέλευσης οικονομικώς πολύτιμα φυσικά ανθρακούχα πολυμερή, όπως το μαλλί, το κασμίρι και το μετάξι. Τα πλαστικά είναι από συνθετικά ανθρακούχα πολυμερή, που συχνά περιέχουν επίσης οξυγόνο, άζωτο ή και αλογόνα. Οι πρώτες ύλες για πολλά από αυτά τα συνθετικά υλικά προέρχονται επίσης από το αργό πετρέλαιο.
Οι χρήσεις του άνθρακα και των ενώσεών του είναι εξαιρετικά ποικίλες. Μπορεί να σχηματίσει κράματα με το σίδηρο, το πιο συνηθισμένο από τα οποία είναι ο χάλυβας. Ο γραφίτης, (συχνά) μαζί με άργιλο και συνθετικά συνδετικά, χρησιμοποιείται για κατασκευή μυτών από μολύβια (κοινά και μηχανικά) για γράψιμο, σχεδίαση και ζωγραφική. Χρησιμοποιείται επίσης ως ένα λιπαντικό, ως ένα χρώμα βαψίματος, ως ένα υλικό χύτευσης για παραγωγή γυαλιού, για ηλεκτρόδια σε ξηρές μπαταρίες και σε ηλεκτροεπικάλυψη και ηλεκτροδιαμόρφωση, σε ψύκτρες για ηλεκτροκινητήρες και ως ένας επιβραδυντής νετρονίων σε πυρηνικούς αντιδραστήρες.
Το ξυλοκάρβουνο χρησιμοποιήθηκε ως ένα υλικό για σχεδίαση στη ζωγραφική, για ψήσιμο (δηλαδή στη μαγειρική), και για πολλές άλλες χρήσεις, που περιλαμβάνουν την εκκαμίνευση σιδήρου. Το ξύλο, το κάρβουνο και το πετρέλαιο χρησιμοποιήθηκαν ως καύσιμες ύλες για παραγωγή ενέργειας και για θέρμανση χώρων. Τα διαμάντια ποιότητας κοσμήματος χρησιμοποιούνται στην κοσμηματοποιία, ενώ τα βιομηχανικής ποιότητας διαμάντια χρησιμοποιούνται για διάτρηση, κοπή και λείανση εργαλείων, για επεξεργασία μετάλλων και λίθων. Τα πλαστικά γίνονται από ορυκτούς υδρογονάνθρακες και τα ανθρακονήματα γίνονται με πυρόλυση συνθετικών πολυεστερικών νημάτων και χρησιμοποιούνται για την ενίσχυση πλαστικών για την κατασκευή προχωρημένων ελαφρών σύνθετων υλικών. Ακόμη, ανθρακονήματα παράγονται και με πυρόλυση εξωθημένων και τεντωμένων νημάτων πολυακρυλονιτρίλιου (PAN = PolyAcryloNitrile) και άλλων οργανικών ουσιών. Η κρυσταλλογραφική δομή και οι μηχανικές ιδιότητες των ανθρακονημάτων εξαρτώνται από τον τύπο της πρώτης ύλης, αλλά και από την επακόλουθη επεξεργασία. Τα ανθρακονήματα που γίνονται από PAN έχουν δομή που μοιάζει με στενά φύλλα γραφίτη, αλλά η θερμική επεξεργασία μπορεί να επανοργανώσει τη δομή σε ένα συνεχόμενο ελαστικό φύλλο. Το αποτέλεσμα είναι ανθρακονήματα με υψηλότερη σχετική δύναμη εφελκυσμού ακόμη και από το χάλυβα[102].
Η αιθάλη χρησιμοποιήθηκε ως η μαύρη χρωστική ουσία του μελανιού της τυπογραφίας, για καλλιτεχνικό ελαιόχρωμα και για υδροχρώματα, για χαρτί αντιγραφής (καρμπόν), για φινίρισμα αυτοκινήτων, για ινδικό μελάνι και για κασέτα εκτυπωτή λέιζερ. Η αιθάλη χρησιμοποιήθηκε επίσης ως ένα υλικό πλήρωσης για λαστιχένια προϊόντα, όπως ελαστικοί τροχοί και σε πλαστικές ενώσεις. Ο ενεργός άνθρακας χρησιμοποιείται ως ένα προσροφητικό υλικό διήθησης σε εφαρμογές τόσο διαφορετικές μεταξύ τους όπως οι αντιασφυξιογόνες μάσκες, ο καθαρισμός νερού, οι απορροφητήρες κουζίνας και στην ιατρική για την απορρόφηση τοξινών, δηλητηρίων ή και αερίων από ένα πεπτικό σύστημα. Ο άνθρακας χρησιμοποιείται για αντιδράσεις αναγωγής σε υψηλές θερμοκρασίες. Ο οπτάνθρακας χρησιμοποιείται για την αναγωγή σιδηρούχων ορυκτών σε (μεταλλικό) σίδηρο. Η βαφή χάλυβα επιτυγχάνεται με θέρμανση τελειωμένων χαλύβδινων προϊόντων με σκόνη άνθρακα. Το καρβίδιο του πυριτίου (SiC), το καρβίδιο του βολφραμίου (WC), το καρβίδιο του βορίου (B4) και το καρβίδιο του τιτανίου (TiC) είναι ανάμεσα στα σκληρότερα γνωστά υλικά, και χρησιμοποιούνται ως «δόντια» σε εργαλεία κοπής και λείανσης. Ο ρουχισμός, φυσικές και συνθετικές υφάνσιμες ύλες καθώς και το φυσικό και το συνθετικό δέρμα, περιέχουν ανθρακούχες ουσίες, καθώς και όλες οι εσωτερικές επιφάνειες στο οικιστικό περιβάλλον, εκτός από αυτές που χρησιμοποιούν άλλα υλικά, όπως γυαλί, πετρώματα και μέταλλα.
Διαμάντια
[Επεξεργασία | επεξεργασία κώδικα]Η βιομηχανία διαμαντιών μπορεί γενικά να διαχωριστεί σε δυο βασικά διακριτές κατηγορίες: Η μία ασχολείται με τα διαμάντια επιπέδου κοσμηματοποιίας και η άλλη με τα διαμάντια επιπέδου βιομηχανίας. Παρόλο που υπάρχει ένα εκτεταμένο εμπόριο και για τους δυο τύπους διαμαντιών, οι δυο αγορές δρουν με δραματικά διαφορετικούς τρόπους.
Για τα διαμάντια επιπέδου κοσμηματοποιίας, αντίθετα από τα πολύτιμα μέταλλα, όπως ο χρυσός ή ο λευκόχρυσος, τα διαμάντια κοσμηματοποιίας δεν εμπορεύονται ως ένα (χρηματιστηριακό) προϊόν, γιατί υπάρχει μεν μια σημαντική προσαύξηση στην πώληση διαμαντιών, αλλά δεν υπάρχει μια πολύ ενεργή αγορά για μεταπώληση διαμαντιών.
Η αγορά για τα διαμάντια βιομηχανικού επιπέδου λειτουργεί πολύ διαφορετικά από αυτήν των διαμαντιών κοσμηματοποιίας. Τα βιομηχανικά διαμάντια αξιολογούνται κυρίως με βάση τη σκληρότητα και τη θερμική αγωγιμότητα που έχουν, αγνοώντας αντίστοιχα χαρακτηριστικά που αξιοποιούνται από την κοσμηματοποιία, όπως διαύγεια και χρώμα. Αυτή η διαφορά βοηθά να εξηγηθεί γιατί το 80% των εξορυσσόμενων διαμαντιών (και που αντιστοιχούν περίπου σε 100 εκατομμύρια καράτια ή 20 τόννους ετησίως) είναι ακατάλληλα για την κοσμηματοποιία και είναι γνωστά ως «μακριά» (bort) και προορίζονται για βιομηχανική χρήση[103]. Επί πρόσθετα στα εξορυσσόμενα διαμάντια, υπάρχουν και τα συνθετικά, που αξιοποιούνται αποκλειστικά σε βιομηχανικές εφαρμογές, σχεδόν αμέσως μετά από την εφεύρεσή τους τη δεκαετία του 1950. Η παραγωγή συνθετικών διαμαντιών υπολογίζεται σε σχεδόν 3 δισεκατομμύρια καράτια (= 600 τόννοι) το χρόνο, όλα για βιομηχανική χρήση[104]. Η κυρίαρχη βιομηχανική χρήση των διαμαντιών είναι για την κοπή, διάτρηση, λείανση, στίλβωση και γυάλισμα (σκληρών αντικειμένων). Οι περισσότερες από αυτές τις χρήσεις δεν απαιτούν μεγάλα διαμάντια. Στην πραγματικότητα βέβαια, και τα περισσότερα διαμάντια επιπέδου κοσμηματοποιίας θα μπορούσαν να χρησιμοποιηθούν και για βιομηχανικές εφαρμογές, ιδιαίτερα τα μικρότερα. Τα περισσότερα βιομηχανικά διαμάντια τοποθετούνται σε τρυπάνια ή λεπίδες πριονιού ή συνθλίβονται σε μια σκόνη για χρήση σε εφαρμογές λείανσης και στίλβωσης[105]. Ορισμένες εξειδικευμένες εφαρμογές διαμαντιών περιλαμβάνουν εργαστηριακές χρήσεις για πειράματα υψηλής πίεσης (δείτε για παράδειγμα το κελί διαμαντένιου αμονιού, diamond anvil cell), υψηλής απόδοσης έδρανα και περιορισμένη χρήση σε εξειδικευμένα παράθυρα[106][107]. Με τις συνεχιζόμενες προόδους στην παραγωγή συνθετικών διαμαντιών, πιθανές μελλοντικές εφαρμογές τους είναι ως ημιαγωγών για την κατασκευή μικρολοκληρωμένων κυκλωμάτων ή ως ένας απαγωγός θερμότητας σε ηλεκτρονικά συστήματα[108].
Ασφάλεια
[Επεξεργασία | επεξεργασία κώδικα]
Ο καθαρός άνθρακας έχει εξαιρετικά μικρή τοξικότητα για τους ανθρώπους και μπορεί να χρησιμοποιηθεί ακόμη και να καταπωθεί με ασφάλεια, στις μορφές του γραφίτη και του ξυλοκάρβουνου. Αντιστέκεται στη διάλυση ή σε χημικές προσβολές, ακόμη και στο όξινο περιβάλλον του πεπτικού σωλήνα. Κατά συνέπεια αν και όταν εισέλθει στους ιστούς του ανθρώπινου σώματος πιθανότατα παραμένει εκεί επ 'αόριστον. Η αιθάλη ήταν πιθανότατα μια από τις πρώτες βαφές που χρησιμοποιήθηκαν για δερματοστιξία και ο παγάνθρωπος Ότζι (Ötzi the Iceman) βρέθηκε να έχει ανθρακούχα δερματοστιξία που έμειναν επάνω του για όλη του τη ζωή και άλλα 5.200 χρόνια μετά το θάνατό του[109]. Ωστόσο, η εισπνοή καρβουνόσκονης ή αιθάλης σε μεγάλες ποσότητες μπορεί να είναι επικίνδυνη, γιατί ερεθίζει τους ιστούς των πνευμόνων και προκαλεί συμφορητική πνευμονοπάθεια ή πνευμονοκονίαση των ανθρακωρύχων. Ομοίως, η διαμαντόσκονη, που χρησιμοποιείται ως λειαντικό, μπορεί να προκαλέσει βλάβες αν καταπωθεί ή εισπνευθεί. Μικροσωματίδια άνθρακα παράγονται από τις εξατμίσεις κινητήρων ντίζελ και μπορούν να συσσωρευτούν στους πνεύμονες[110]. Σε αυτά τα παραδείγματα, όμως, τα βλαβερά αποτελέσματα μπορεί να είναι αποτέλεσμα μόλυνσης των σωματιδίων άνθρακα με οργανικά χημικά ή και βαριά μέταλλα και όχι από τον ίδιο τον άνθρακα.
Ο άνθρακας έχει μικρή τοξικότητα γενικά για όλες σχεδόν τις μορφές ζωής στη Γη, αλλά ωστόσο υπάρχουν κάποια πλάσματα για τα οποία μπορεί ο άνθρακας να είναι πραγματικά τοξικός. Για παράδειγμα, τα νανοσωματίδια άνθρακα είναι θανατηφόρα για τα δροσόφιλα (Drosophila)[111].
Επίσης, ο άνθρακας μπορεί να καεί ζωηρά και έντονα παρουσία αέρα σε υψηλές θερμοκρασίες, όπως στην πυρκαγιά του Γουίντσκεϊλ (Windscale fire), που προκλήθηκε από την ξαφνική έκλυση αποθηκευμένης ενέργειας Γουίγκνερ (Wigner energy) σε πυρήνα γραφίτη. Μεγάλες συγκεντρώσεις άνθρακα, που έχουν παραμείνει αδρανή για εκατοντάδες εκατομμύρια χρόνια, απουσία οξυγόνου, μπορεί αυθόρμητα να αναφλεγούν, αν εκτεθούν στον αέρα, για παράδειγμα σε ένα σε χωματερές ανθρακωρυχείου.
Η μεγάλη ποικιλία των ανθρακούχων ενώσεων περιλαμβάνουν θανατηφόρα δηλητήρια, όπως η τετροδοτοξίνη, η λεκτίνη ρυζίνη από σπόρους της ρετσινολαδιάς, τα κυανιούχα ιόντα (CN-) και το μονοξείδιο του άνθρακα, αλλά και ενώσεις ζωτικές για τους ζώντες οργανισμούς, όπως η γλυκόζη και οι πρωτεΐνες.
Δεσμοί
[Επεξεργασία | επεξεργασία κώδικα]| CH | He | ||||||||||||||||
| CLi | CBe | CB | CC | CN | CO | CF | Ne | ||||||||||
| CNa | CMg | CAl | CSi | CP | CS | CCl | CAr | ||||||||||
| CK | CCa | CSc | CTi | CV | CCr | CMn | CFe | CCo | CNi | CCu | CZn | CGa | CGe | CAs | CSe | CBr | CKr |
| CRb | CSr | CY | CZr | CNb | CMo | CTc | CRu | CRh | CPd | CAg | CCd | CIn | CSn | CSb | CTe | CI | CXe |
| CCs | CBa | CHf | CTa | CW | CRe | COs | CIr | CPt | CAu | CHg | CTl | CPb | CBi | CPo | CAt | Rn | |
| Fr | CRa | Rf | Db | CSg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | |||||||||||||||||
| CLa | CCe | CPr | CNd | CPm | CSm | CEu | CGd | CTb | CDy | CHo | CEr | CTm | CYb | CLu | |||
| Ac | CTh | CPa | CU | CNp | CPu | CAm | CCm | CBk | CCf | CEs | Fm | Md | No | Lr | |||
| Πυρήνας της οργανικής χημείας | Πολλές χρήσεις στη χημεία |
| Ακαδημαϊκή έρευνα, όχι ευρεία χρήση | Άγνωστοι δεσμοί |
Δείτε επίσης
[Επεξεργασία | επεξεργασία κώδικα]- Περιοδικός πίνακας
- Χημική ένωση
- Οργανική χημεία
- Ομάδα του άνθρακα
- Χαβινισμός άνθρακα
- Αποτύπωμα άνθρακα
- Οικονομία χαμηλού άνθρακα
- κάρβουνο
Παραπομπές και σημειώσεις
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Για παράδειγμα στο διοξείδιο του άνθρακα.
- ↑ Για παράδειγμα στο #1 άτομο άνθρακα του αιθανονιτρίλιου.
- ↑ "Fourier Transform Spectroscopy of the System of CP". Retrieved 2007-12-06.
- ↑ Για παράδειγμα στο #2 άτομο άνθρακα της προπανόνης.
- ↑ Για παράδειγμα στο #1 άτομο άνθρακα της αιθανάλης.
- ↑ Fourier Transform Spectroscopy of the Electronic Transition of the Jet-Cooled CCI Free Radical". Retrieved 2007-12-06.
- ↑ Για παράδειγμα στη μεθανάλη.
- ↑ Για παράδειγμα στο #1 άτομο άνθρακα της αιθανόλης.
- ↑ Για παράδειγμα στη μεθανόλη.
- ↑ Για παράδειγμα στο αιθάνιο.
- ↑ Για παράδειγμα στο μεθάνιο.
- ↑ "Carbon: Binary compounds". Retrieved 2007-12-06.
- ↑ 13,0 13,1 13,2 Carbon – Naturally occurring isotopes". WebElements Periodic Table. Retrieved 2008-10-09.
- ↑ History of Carbon". Retrieved 2013-01-10.
- ↑ "Biological Abundance of Elements". The Internet Encyclopedia of Science. Retrieved 2008-10-09.
- ↑ 16,0 16,1 "World of Carbon – Interactive Nano-visulisation in Science & Engineering Education (IN-VSEE)". Retrieved 2008-10-09.
- ↑ 17,0 17,1 Chemistry Operations (December 15, 2003). "Carbon". Los Alamos National Laboratory. Archived from the original on 2008-09-13. Retrieved 2008-10-09.
- ↑ Haaland, D (1976). "Graphite-liquid-vapor triple point pressure and the density of liquid carbon". Carbon 14 (6): 357. doi:10.1016/0008-6223(76)90010-5.
- ↑ Savvatimskiy, A (2005). "Measurements of the melting point of graphite and the properties of liquid carbon (a review for 1963–2003)". Carbon 43 (6): 1115. doi:10.1016/j.carbon.2004.12.027.
- ↑ Σημείωση: Παρόλο που ο άνθρακας έχει υψηλότερη ηλεκτραρνητικότητα από τα περισσότερα μέταλλα.
- ↑ Lee, C.; Wei, X.; Kysar, J. W.; Hone, J. (2008). "Measurement of the Elastic Properties and Intrinsic Strength of Monolayer Graphene". Science 321 (5887): 385–8. Bibcode:2008Sci...321..385L. doi:10.1126/science.1157996. PMID 18635798. Lay summary.
- ↑ Sanderson, Bill (2008-08-25). "Toughest Stuff Known to Man: Discovery Opens Door to Space Elevator". nypost.com. Retrieved 2008-10-09.
- ↑ Irifune, Tetsuo; Kurio, Ayako; Sakamoto, Shizue; Inoue, Toru; Sumiya, Hitoshi (2003). "Materials: Ultrahard polycrystalline diamond from graphite". Nature 421 (6923): 599–600. Bibcode:2003Natur.421..599I. doi:10.1038/421599b. PMID 12571587.
- ↑ Dienwiebel, Martin; Verhoeven, Gertjan; Pradeep, Namboodiri; Frenken, Joost; Heimberg, Jennifer; Zandbergen, Henny (2004). "Superlubricity of Graphite". Physical Review Letters 92 (12). Bibcode:2004PhRvL..92l6101D. doi:10.1103/PhysRevLett.92.126101.
- ↑ Collins, A.T. (1993). "The Optical and Electronic Properties of Semiconducting Diamond". Philosophical Transactions of the Royal Society A 342 (1664): 233–244. Bibcode:1993RSPTA.342..233C. doi:10.1098/rsta.1993.0017.
- ↑ Deprez, N.; McLachan, D. S. (1988). "The analysis of the electrical conductivity of graphite conductivity of graphite powders during compaction". Journal of Physics D: Applied Physics (Institute of Physics) 21 (1): 101. Bibcode:1988JPhD...21..101D. doi:10.1088/0022-3727/21/1/015.
- ↑ Delhaes, P. (2001). Graphite and Precursors. CRC Press. ISBN 90-5699-228-7.
- ↑ 28,0 28,1 28,2 Unwin, Peter. "Fullerenes(An Overview)". Retrieved 2007-12-08.
- ↑ Ebbesen, T. W., ed. (1997). Carbon nanotubes—preparation and properties. Boca Raton, Florida: CRC Press. ISBN 0-8493-9602-6.
- ↑ 30,0 30,1 Dresselhaus, M. S.; Dresselhaus, G.; Avouris, Ph., ed. (2001). "Carbon nanotubes: synthesis, structures, properties and applications". Topics in Applied Physics (Berlin: Springer) 80. ISBN 3-540-41086-4.
- ↑ 31,0 31,1 Nasibulin, Albert G.; Pikhitsa, P.V.; Jiang, H.; Brown, D. P.; Krasheninnikov, A.V.; Anisimov, A. S.; Queipo, P.; Moisala, A. et al. (2007). "A novel hybrid carbon material". Nature Nanotechnology 2 (3): 156–161. Bibcode:2007NatNa...2..156N. doi:10.1038/nnano.2007.37. PMID 18654245.
- ↑ Nasibulin, A; Anisimov, Anton S.; Pikhitsa, Peter V.; Jiang, Hua; Brown, David P.; Choi, Mansoo; Kauppinen, Esko I. (2007). "Investigations of NanoBud formation". Chemical Physics Letters 446: 109–114. Bibcode:2007CPL...446..109N. doi:10.1016/j.cplett.2007.08.050.
- ↑ Vieira, R; Ledoux, Marc-Jacques; Pham-Huu, Cuong (2004). "Synthesis and characterisation of carbon nanofibers with macroscopic shaping formed by catalytic decomposition of C2H6/H2 over nickel catalyst". Applied Catalysis A 274: 1–8. doi:10.1016/j.apcata.2004.04.008.
- ↑ 34,0 34,1 Clifford, Frondel; Marvin, Ursula B. (1967). "Lonsdaleite, a new hexagonal polymorph of diamond". Nature 214 (5088): 587–589. Bibcode:1967Natur.214..587F. doi:10.1038/214587a0.
- ↑ 35,0 35,1 35,2 Harris, PJF (2004). "Fullerene-related structure of commercial glassy carbons". Philosophical Magazine 84 (29): 3159–3167. Bibcode:2004PMag...84.3159H. doi:10.1080/14786430410001720363.
- ↑ Rode, A. V.; Hyde, S. T.; Gamaly, E. G.; Elliman, R. G.; McKenzie, D. R.; Bulcock, S. (1999). "Structural analysis of a carbon foam formed by high pulse-rate laser ablation". Applied Physics A-Materials Science & Processing 69 (7): S755–S758. doi:10.1007/s003390051522.
- ↑ 37,0 37,1 37,2 Heimann, Robert Bertram; Evsyukov, Sergey E. and Kavan, Ladislav (28 February 1999). Carbyne and carbynoid structures. Springer. pp. 1–. ISBN 978-0-7923-5323-2. Retrieved 2011-06-06.
- ↑ Δηλαδή με τουλάχιστον μία κοινή πλευρά.
- ↑ Jenkins, Edgar (1973). The polymorphism of elements and compounds. Taylor & Francis. p. 30. ISBN 0-423-87500-0. Retrieved 2011-05-01.
- ↑ Ebbesen, T. W., ed. (1997). Carbon nanotubes—preparation and properties. Boca Raton, Florida: CRC Press. ISBN 0-8493-9602-6.
- ↑ Schewe, Phil and Stein, Ben (March 26, 2004). "Carbon Nanofoam is the World's First Pure Carbon Magnet". Physics News Update 678 (1).
- ↑ Itzhaki, Lior; Altus, Eli; Basch, Harold; Hoz, Shmaryahu (2005). "Harder than Diamond: Determining the Cross-Sectional Area and Young's Modulus of Molecular Rods". Angew. Chem. Int. Ed. 44 (45): 7432–5. doi:10.1002/anie.200502448. PMID 16240306.
- ↑ «Researchers Find New Phase of Carbon, Make Diamond at Room Temperature». news.ncsu.edu. Ανακτήθηκε στις 6 Απριλίου 2016.
- ↑ Mark, Kathleen (1987). Meteorite Craters. University of Arizona Press. ISBN 0-8165-0902-6.
- ↑ «Online Database Tracks Organic Nano-Particles Across the Universe». Sci Tech Daily. February 24, 2014. http://scitechdaily.com/online-database-tracks-organic-nano-particles-across-universe/. Ανακτήθηκε στις 2015-03-10.
- ↑ Hoover, Rachel (21 Φεβρουαρίου 2014). «Need to Track Organic Nano-Particles Across the Universe? NASA's Got an App for That». NASA. Αρχειοθετήθηκε από το πρωτότυπο στις 10 Μαΐου 2020. Ανακτήθηκε στις 22 Φεβρουαρίου 2014.
- ↑ William F McDonough The composition of the Earth in Earthquake Thermodynamics and Phase Transformation in the Earth's Interior. 2000. ISBN 978-0126851854.
- ↑ "Wonderfuel: Welcome to the age of unconventional gas" by Helen Knight, New Scientist, 12 June 2010, pp. 44–7.
- ↑ Ocean methane stocks 'overstated', BBC, 17 Feb. 2004.
- ↑ "Ice on fire: The next fossil fuel" by Fred Pearce, New Scientist, 27 June 2009, pp. 30-33.
- ↑ Calculated from file global.1751_2008.csv in [1] from the Carbon Dioxide Information Analysis Center.
- ↑ Rachel Gross (Sept. 21, 2013). "Deep, and dank mysterious". New Scientist: 40–43.
- ↑ Kasting, James (1998). "The Carbon Cycle, Climate, and the Long-Term Effects of Fossil Fuel Burning". Consequences: the Nature and Implication of Environmental Change 4 (1).
- ↑ Stefanenko, R. (1983). Coal Mining Technology: Theory and Practice. Society for Mining Metallurgy. ISBN 0-89520-404-5.
- ↑ Carbon-14 formation.
- ↑ "Official SI Unit definitions". Retrieved 2007-12-21.
- ↑ Gannes, Leonard Z.; Del Rio, Carlos Martı́nez; Koch, Paul (1998). "Natural Abundance Variations in Stable Isotopes and their Potential Uses in Animal Physiological Ecology". Comparative Biochemistry and Physiology – Part A: Molecular & Integrative Physiology 119 (3): 725–737. doi:10.1016/S1095-6433(98)01016-2.
- ↑ Brown, Tom (March 1, 2006). "Carbon Goes Full Circle in the Amazon". Lawrence Livermore National Laboratory. Retrieved 2007-11-25.
- ↑ Bowman, S. (1990). Interpreting the past: Radiocarbon dating. British Museum Press. ISBN 0-7141-2047-2.
- ↑ Libby, W. F. (1952). Radiocarbon dating. Chicago University Press and references therein.
- ↑ Westgren, A. (1960). "The Nobel Prize in Chemistry 1960". Nobel Foundation. Retrieved 2007-11-25.
- ↑ Use query for carbon-8". barwinski.net. Retrieved 2007-12-21.
- ↑ Watson, A. (1999). "Beaming Into the Dark Corners of the Nuclear Kitchen". Science 286 (5437): 28–31. doi:10.1126/science.286.5437.28.
- ↑ Audi, G; Bersillon, O.; Blachot, J.; Wapstra, A.H. (1997). "The Nubase evaluation of nuclear and decay properties". Nuclear Physics A 624: 1. Bibcode:1997NuPhA.624....1A. doi:10.1016/S0375-9474(97)00482-X.
- ↑ Ostlie, D.A. and Carroll, B.W. (2007). An Introduction to Modern Stellar Astrophysics. Addison Wesley, San Francisco. ISBN 0-8053-0348-0.
- ↑ Whittet, D. C. B. (2003). Dust in the Galactic Environment. CRC Press. pp. 45–46. ISBN 0-7503-0624-6.
- ↑ Pikelʹner, Solomon Borisovich (1977). Star formation. Springer. pp. 38–. ISBN 978-90-277-0796-3. Retrieved 2011-06-06.
- ↑ Falkowski, P; Scholes, RJ; Boyle, E; Canadell, J; Canfield, D; Elser, J; Gruber, N; Hibbard, K et al. (2000). "The Global Carbon Cycle: A Test of Our Knowledge of Earth as a System". Science 290 (5490): 291–296. Bibcode:2000Sci...290..291F. doi:10.1126/science.290.5490.291. PMID 11030643.
- ↑ Smith, T. M.; Cramer, W. P.; Dixon, R. K.; Leemans, R.; Neilson, R. P.; Solomon, A. M. (1993). "The global terrestrial carbon cycle". Water, Air, & Soil Pollution 70: 19–37. doi:10.1007/BF01104986.
- ↑ Levine, Joel S.; Augustsson, Tommy R.; Natarajan, Murali (1982). "The prebiological paleoatmosphere: stability and composition". Origins of Life and Evolution of Biospheres 12 (3): 245–259. Bibcode:1982OrLi...12..245L. doi:10.1007/BF00926894.
- ↑ Loerting, T. et al. (2001). "On the Surprising Kinetic Stability of Carbonic Acid". Angew. Chem. Int. Ed. 39 (5): 891–895. doi:10.1002/(SICI)1521-3773(20000303)39:5<891::AID-ANIE891>3.0.CO;2-E. PMID 10760883.
- ↑ Haldane J. (1895). "The action of carbonic oxide on man". Journal of Physiology 18 (5–6): 430–462. PMC 1514663. PMID 16992272.
- ↑ 73,0 73,1 Gorman, D.; Drewry, A.; Huang, Y. L.; Sames, C. (2003). "The clinical toxicology of carbon monoxide". Toxicology 187 (1): 25–38. doi:10.1016/S0300-483X(03)00005-2. PMID 12679050.
- ↑ Bayes, K. (1961). "Photolysis of Carbon Suboxide". Journal of the American Chemical Society 83 (17): 3712–3713. doi:10.1021/ja01478a033.
- ↑ Anderson D. J.; Rosenfeld, R. N. (1991). "Photodissociation of Carbon Suboxide". Journal of Chemical Physics 94 (12): 7852–7867. Bibcode:1991JChPh..94.7857A. doi:10.1063/1.460121.
- ↑ Sabin, J. R.; Kim, H. (1971). "A theoretical study of the structure and properties of carbon trioxide". Chemical Physics Letters 11 (5): 593–597. Bibcode:1971CPL....11..593S. doi:10.1016/0009-2614(71)87010-0.
- ↑ Moll N. G., Clutter D. R., Thompson W. E. (1966). "Carbon Trioxide: Its Production, Infrared Spectrum, and Structure Studied in a Matrix of Solid CO2". Journal of Chemical Physics 45 (12): 4469–4481. Bibcode:1966JChPh..45.4469M. doi:10.1063/1.1727526.
- ↑ 78,0 78,1 Fatiadi, Alexander J.; Isbell, Horace S.; Sager, William F. (1963). "Cyclic Polyhydroxy Ketones. I. Oxidation Products of Hexahydroxybenzene (Benzenehexol)". Journal of Research of the National Bureau of Standards A: Physics and Chemistry 67A (2): 153–162. doi:10.6028/jres.067A.015.
- ↑ Pauling, L. (1960). The Nature of the Chemical Bond (3rd ed.). Ithaca, NY: Cornell University Press. p. 93. ISBN 0-8014-0333-2.
- ↑ Scherbaum, Franz et al. (1988). ""Aurophilicity" as a consequence of Relativistic Effects: The Hexakis(triphenylphosphaneaurio)methane Dication [(Ph3PAu)6C]2+". Angew. Chem. Int. Ed. Engl. 27 (11): 1544–1546. doi:10.1002/anie.198815441.
- ↑ Shorter Oxford English Dictionary, Oxford University Press.
- ↑ Chinese made first use of diamond". BBC News. 17 May 2005. Retrieved 2007-03-21.
- ↑ van der Krogt, Peter. "Carbonium/Carbon at Elementymology & Elements Multidict". Retrieved 2010-01-06.
- ↑ Ferchault de Réaumur, R-A (1722). L'art de convertir le fer forgé en acier, et l'art d'adoucir le fer fondu, ou de faire des ouvrages de fer fondu aussi finis que le fer forgé (English translation from 1956). Paris, Chicago.
- ↑ "Carbon". Canada Connects. Retrieved 2010-12-07.
- ↑ Senese, Fred. "Who discovered carbon?". Frostburg State University. Retrieved 2007-11-24.
- ↑ Giolitti, Federico (1914). The Cementation of Iron and Steel. McGraw-Hill Book Company, inc.
- ↑ Senese, Fred (200-09-09). "Who discovered carbon?". Frostburg State University. Retrieved 2007-11-24.
- ↑ Kroto, H. W.; Heath, J. R.; O'Brien, S. C.; Curl, R. F.; Smalley, R. E. (1985). "C60: Buckminsterfullerene". Nature 318 (6042): 162–163. Bibcode:1985Natur.318..162K. doi:10.1038/318162a0.
- ↑ "The Nobel Prize in Chemistry 1996 "for their discovery of fullerenes"". Retrieved 2007-12-21.
- ↑ 91,0 91,1 91,2 USGS Minerals Yearbook: Graphite, 2009 and Graphite: Mineral Commodity Summaries 2011
- ↑ Harlow, G. E. (1998). The nature of diamonds. Cambridge University Press. p. 223. ISBN 0-521-62935-7.
- ↑ Catelle, W.R. (1911). The Diamond. John Lane Company. Page 159 discussion on Alluvial diamonds in India and elsewhere as well as earliest finds
- ↑ Ball, V. (1881). Diamonds, Gold and Coal of India. London, Truebner & Co. Ball was a Geologist in British service. Chapter I, Page 1
- ↑ Hershey, J. W. (1940). The Book Of Diamonds: Their Curious Lore, Properties, Tests And Synthetic Manufacture. Kessinger Pub Co. p. 28. ISBN 1-4179-7715-9.
- ↑ 96,0 96,1 Janse, A. J. A. (2007). "Global Rough Diamond Production Since 1870". Gems and Gemology (GIA). XLIII (Summer 2007): 98–119. doi:10.5741/GEMS.43.2.98.
- ↑ 97,0 97,1 Lorenz, V. (2007). "Argyle in Western Australia: The world's richest diamantiferous pipe; its past and future". Gemmologie, Zeitschrift der Deutschen Gemmologischen Gesellschaft (DGemG) 56 (1/2): 35–40.
- ↑ "Microscopic diamond found in Montana". The Montana Standard. 2004-10-17. Retrieved 2008-10-10.
- ↑ Cooke, Sarah (2004-10-19). "Microscopic Diamond Found in Montana". Livescience.com. Archived from the original on 2008-07-05. Retrieved 2008-09-12.
- ↑ Delta News / Press Releases / Publications". Deltamine.com. Archived from the original on 2008-05-26. Retrieved 2008-09-12.
- ↑ Marshall, Stephen; Shore, Josh (2004-10-22). "The Diamond Life". Guerrilla News Network. Archived from the original on 2008-06-09. Retrieved 2008-10-10.
- ↑ Cantwell, W. J.; Morton, J. (1991). "The impact resistance of composite materials – a review". Composites 22 (5): 347–62. doi:10.1016/0010-4361(91)90549-V.
- ↑ Holtzapffel, Ch. (1856). Turning And Mechanical Manipulation. Charles Holtzapffel. Internet Archive
- ↑ "Industrial Diamonds Statistics and Information". United States Geological Survey. Retrieved 2009-05-05.
- ↑ Coelho, R. T.; Yamada, S.; Aspinwall, D.K.; Wise, M.L.H. (1995). "The application of polycrystalline diamond (PCD) tool materials when drilling and reaming aluminum-based alloys including MMC". International journal of machine tools & manufacture 35 (5): 761. doi:10.1016/0890-6955(95)93044-7.
- ↑ Harris, D. C. (1999). Materials for infrared windows and domes: properties and performance. SPIE Press. pp. 303–334. ISBN 0-8194-3482-5.
- ↑ Nusinovich, G. S. (2004). Introduction to the physics of gyrotrons. JHU Press. p. 229. ISBN 0-8018-7921-3.
- ↑ Sakamoto, M.; Endriz, J. G.; Scifres, D. R. (1992). "120 W CW output power from monolithic AlGaAs (800 nm) laser diode array mounted on diamond heatsink". Electronics Letters 28 (2): 197–199. doi:10.1049/el:19920123.
- ↑ Dorfer, Leopold; Moser, M; Spindler, K; Bahr, F; Egarter-Vigl, E; Dohr, G (1998). "5200-year old acupuncture in Central Europe?". Science 282 (5387): 242–243. Bibcode:1998Sci...282..239D. doi:10.1126/science.282.5387.239f. PMID 9841386.
- ↑ Donaldson, K; Stone, V; Clouter, A; Renwick, L; MacNee, W (2001). "Ultrafine particles". Occupational and Environmental Medicine 58 (3): 211–216. doi:10.1136/oem.58.3.211. PMC 1740105. PMID 11171936.
- ↑ Carbon Nanoparticles Toxic To Adult Fruit Flies But Benign To Young ScienceDaily (Aug. 17, 2009)
Πηγές πληροφόρησης
[Επεξεργασία | επεξεργασία κώδικα]- Sargent-Welch Scientific Company.
- http://el.science.wikia.com/wiki/Γραφένιο
Εξωτερικοί σύνδεσμοι
[Επεξεργασία | επεξεργασία κώδικα] Λεξιλογικός ορισμός του άνθρακας στο Βικιλεξικό
Λεξιλογικός ορισμός του άνθρακας στο Βικιλεξικό Πολυμέσα σχετικά με το θέμα Carbon στο Wikimedia Commons
Πολυμέσα σχετικά με το θέμα Carbon στο Wikimedia Commons
| Περιοδικός πίνακας | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | H | He | ||||||||||||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||||||||
| ||||||||||||||||||||||||||||||||||||||||||






