Διαλυτότητα
| Το λήμμα δεν περιέχει πηγές ή αυτές που περιέχει δεν επαρκούν. |
Διαλυτότητα είναι η ικανότητα μιας χημικής ουσίας να διαλυθεί μέσα σε άλλη. Αυτή η ικανότητα προσδιορίζεται από τη μεγίστη ποσότητά της που μπορεί να διαλυθεί, σε καθορισμένη πάντα ποσότητα διαλύτη και σε ορισμένη θερμοκρασία.
Με κριτήριο αυτή την ικανότητα οι ουσίες διακρίνονται σε διαλυτές ουσίες ή σε αδιάλυτες και, ειδικά για τα αέρια, σε αναμίξιμα ή μη αναμίξιμα.
Διαλυτή ουσία ονομάζεται κάθε χημική ουσία που μπορεί να διαλυθεί μέσα σε άλλη και να σχηματίσει διάλυμα. Χημική ουσία που δεν μπορεί να διαλυθεί μέσα σε άλλη καλείται η ίδια αδιάλυτη ουσία. Για παράδειγμα το αλάτι είναι διαλυτό στο νερό, είναι όμως αδιάλυτο στο μαγειρικό λάδι.
Η διαλυτότητα μιας ουσίας αναφέρεται συνήθως ως το βάρος της ουσίας που, υπό κανονικές συνθήκες, είναι δυνατόν να διαλυθεί σε ορισμένη ποσότητα διαλύτη. Έτσι, η διαλυτότητα του αλατιού στο νερό, σε θερμοκρασία δωματίου, είναι 36 gr ανά 100 ml νερού.
- Το διάλυμα που περιέχει αυτή τη μεγαλύτερη δυνατή ποσότητα διαλυτής ουσίας καλείται κορεσμένο διάλυμα. Σε αντίθετη περίπτωση το διάλυμα ονομάζεται ακόρεστο.
- Υπάρχουν και διαλύματα, στα οποία επιτυγχάνεται διάλυση μιας ουσίας στον διαλύτη σε μεγαλύτερη ποσότητα από αυτήν που θα υποδείκνυε η υπό κανονικές συνθήκες διαλυτότητά της. Στην περίπτωση αυτή - που απαιτεί ιδιαίτερες συνθήκες - το διάλυμα ονομάζεται υπέρκορο.
Παράγοντες που επηρεάζουν την διαλυτότητα[Επεξεργασία | επεξεργασία κώδικα]
Θερμοκρασία[Επεξεργασία | επεξεργασία κώδικα]
Η διαλυτότητα μιας δεδομένης διαλυμένης ουσίας σε έναν δεδομένο διαλυτή τυπικά εξαρτάται από την θερμοκρασία. Για πολλές στερεές διαλυμένες ουσίες σε υγρό νερό, η διαλυτότητα αυξάνεται καθώς αυξάνεται η θερμοκρασία, μέχρι τους 100 °C.[1] Σε υγρό νερό σε υψηλές θερμοκρασίες (π.χ., προσεγγίζοντας την κρίσιμη θερμοκρασία), η διαλυτότητα ιοντικών διαλυμένων ουσιών τείνει να μειώνεται λόγω της αλλαγής των ιδιοτήτων και της δομής του υγρού νερού· η μικρότερη τιμή της διηλεκτρικής σταθεράς έχει ως αποτέλεσμα έναν λιγότερο πολικό διαλύτη.
Οι αέριες διαλυμένες ουσίες εμφανίζουν πιο περίπλοκη συμπεριφορά σε σχέση με την θερμοκρασία. Καθώς η θερμοκρασία αυξάνεται, τα αέρια συνήθως γίνονται λιγότερο διαλυτά σε νερό (μέχρι ένα ελάχιστο όριο, το οποίο είναι μικρότερο από 120 °C για τα περισσότερα μόνιμα αέρια[2]), αλλά περισσότερο διαλυτά σε οργανικούς διαλύτες.[1]
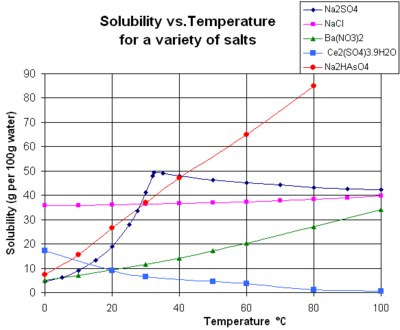
Το γράφημα δείχνει τις καμπύλες διαλυτότητας για μερικά τυπικά στερεά ανόργανα άλατα (η θερμοκρασία είναι σε βαθμούς Κελσίου).[3] Πολλά άλατα συμπεριφέρονται όπως το νιτρικό βάριο (Ba(NO3)2) και το όξινο αρσενικικό νάτριο (HAsNa2O4), και εμφανίζουν μια μεγάλη αύξηση στην διαλυτότητα με την θερμοκρασία. Κάποιές διαλυμένες ουσίες (π.χ. το χλωριούχο νάτριο (NaCl) σε νερό) εμφανίζουν διαλυτότητα η οποία είναι αρκετά ανεξάρτητη της θερμοκρασίας. Μερικές, όπως το θειϊκό δημήτριο(III) (Ce2(SO4)3), γίνονται λιγότερο διαλυτές σε νερό καθώς η θερμοκρασία αυξάνεται. Αυτή η εξάρτηση από την θερμοκρασία μερικές φορές αναφέρεται ως «ανάδρομη» ή «αντίστροφη» διαλυτότητα. Σε μερικές περιπτώσεις παρατηρείται ένα πιο περίπλοκο μοτίβο, όπως με το θειϊκό νάτριο (Na2SO4), όπου ο λιγότερο διαλυτός δεκαένυδρος κρύσταλλος χάνει κρυσταλλικό νερό στους 32 °C και σχηματίζει μια πιο διαλυτή άνυδρη φάση.[εκκρεμεί παραπομπή]
Η διαλυτότητα των οργανικών ενώσεων σχεδόν πάντα αυξάνεται με την θερμοκρασία. Η τεχνική της ανακρυστάλλωσης, η οποία χρησιμοποιείται για τον εξαγνισμό στερεών, εξαρτάται από τις διαφορετικές διαλυτότητες ενός διαλυτού σε θερμό και ψυχρό διαλυτή. Υπάρχουν μερικές εξαιρέσεις, όπως ορισμένες κυκλοδεξτρίνες.[4]
Διαλυτότητα αερίων[Επεξεργασία | επεξεργασία κώδικα]
Η διαλυτότητα των αερίων συστατικών του αέρα μέσα στο νερό υπό κανονική ατμοσφαιρική πίεση χαρακτηρίζεται πολύ μικρή, καθίσταται όμως υπολογίσιμη σε μεγαλύτερες πιέσεις έτσι ώστε να θεωρείται κατά προσέγγιση ότι είναι ανάλογη προς την ασκούμενη πίεση. Στο γεγονός αυτό οφείλεται και η γνωστή «νόσος των δυτών». Ενώ ο δύτης αναπνέει αέρα κατά την κατάδυση, η αύξηση της πίεσης προκαλεί διάλυση περισσότερου αέρα στο αίμα του. Όταν, κατά την ανάδυση, η πίεση επανέρχεται στα φυσιολογικά επίπεδα, ο διαλυμένος αέρας στο αίμα αποβάλλεται υπό μορφή φυσαλίδων, που συγκεντρώνονται στα αιμοφόρα αγγεία, αρχικά με επώδυνους πόνους, μπορεί, όμως, να επιφέρουν και παράλυση μέχρι και θάνατο. Για επαγγελματικές καταδύσεις σε μεγάλα βάθη και χρόνο, οι δύτες χρησιμοποιούν συσκευές παροχής μίγματος οξυγόνου και ηλίου: Το στοιχείο ήλιο παρουσιάζει πολύ μικρότερη διαλυτότητα στο αίμα σε σχέση με το άζωτο του αέρα.
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 John W. Hill, Ralph H. Petrucci, General Chemistry, 2nd edition, Prentice Hall, 1999.
- ↑ P. Cohen, επιμ. (1989). The ASME handbook on Water Technology for Thermal Power Systems. The American Society of Mechanical Engineers. σελ. 442.
- ↑ Handbook of Chemistry and Physics (27th έκδοση). Cleveland, Ohio: Chemical Rubber Publishing Co. 1943.
- ↑ Salvatore Filippone, Frank Heimanna and André Rassat (2002). «A highly water-soluble 2+1 b-cyclodextrin–fullerene conjugate». Chem. Commun. 2002 (14): 1508–1509. doi:.
