Αντίδραση Φρίντελ-Κραφτς
Με τον όρο αντίδραση Φρίντελ-Κραφτς περιγράφεται μια αντίδραση της οργανικής χημείας που αναπτύχθηκε από τους Τσαρλς Φρίντελ και Τζέιμς Κραφτς το 1877[1][2] και με την οποία επιτυγχάνεται η αντικατάσταση ενός υδρογόνου αρωματικού δακτυλίου από μια αλκυλομάδα -R (αλκυλίωση) ή από μια ακυλομάδα -COR (ακυλίωση). Και οι δύο μορφές ανήκουν στην κατηγορία αντιδράσεων ηλεκτρονιόφιλης αρωματικής υποκατάστασης.
Αλκυλίωση Φρίντελ-Κραφτς
[Επεξεργασία | επεξεργασία κώδικα]Πρόκειται για την αλκυλίωση ενός αρωματικού δακτυλίου με ένα αλκυλαλογονίδιο χρησιμοποιώντας ένα ισχυρό οξύ κατά Λιούις ως καταλύτη.
Ο γενικός μηχανισμός της αντίδρασης περιλαμβάνει την αρχική απόσπαση αλογόνου από το αλκυλαλογονίδιο για να σχηματιστεί το κατιόν αλκυλίου, και την συνακόλουθη πυρηνόφιλη προσβολή του αρενίου στο καρβοκατιόν.
Το βασικό μειονέκτημα της αντίδρασης είναι ότι το προϊόν είναι ισχυρότερο πυρηνόφιλο απ' ό,τι το αντιδρόν, εξαιτίας του θετικού επαγωγικού φαινομένου του αλκυλίου. Αυτό έχει σαν αποτέλεσμα να μην μπορεί να σταματήσει η αντίδραση στην μία υποκατάσταση, αλλά να συνεχίζεται εφόσον υπάρχουν διαθέσιμα υδρογόνα στον δακτύλιο. Συνέπεια του γεγονότος αυτού είναι να λαμβάνονται πολλαπλά αλκυλιωμένες ενώσεις. Για τον περιορισμό του αριθμού των αλκυλιώσεων μπορεί να χρησιμοποιηθεί η τεχνική της στερεοχημικής παρεμπόδισης, όπου το μέγεθος μιας οργανικής ομάδας εμποδίζει την εισαγωγή επιπλέον αλκυλίου στον δακτύλιο:
Ακυλίωση Φρίντελ-Κραφτς
[Επεξεργασία | επεξεργασία κώδικα]Πρόκειται για την ακυλίωση ενός αρωματικού δακτυλίου με ένα ακυλοχλωρίδιο χρησιμοποιώντας ένα ισχυρό οξύ κατά Λιούις ως καταλύτη, σε συνθήκες όμοιες με αυτές της αλκυλίωσης. Η αντίδραση είναι επίσης εφικτή με οξικούς ανυδρίτες. Η ακυλίωση Φρίντελ-Κραφτς εμφανίζει σημαντικά πλεονεκτήματα έναντι της αλκυλίωσης, διότι λόγω του αρνητικού επαγωγικού φαινομένου του καρβονυλίου το προϊόν της αντίδρασης (η κετόνη) είναι πάντοτε λιγότερο δραστικό από το αρχικό αντιδρόν, με αποτέλεσμα να μην παρατηρούνται πολλαπλές ακυλιώσεις της αρχικής ένωσης.
Η αποτελεσματικότητα της ακυλίωσης Φρίντελ-Κραφτς εξαρτάται από την σταθερότητα του ακυλοχλωριδίου που χρησιμοποιείται ως αντιδραστήριο. Για παράδειγμα, το φορμυλοχλωρίδιο είναι πολύ ασταθής ένωση, με συνέπεια η κατά Φρίντελ-Κραφτς σύνθεση της βενζαλδεΰδης να απαιτεί την «επί τόπου» (in situ) σύνθεση του φορμυλοχλωριδίου μέσω της αντίδρασης Γκάτερμαν-Κοχ.
Το πρώτο βήμα της αντίδρασης είναι η απόσπαση ενός ατόμου χλωρίου προς σχηματισμό του κατιόντος ακυλίου:
Ακολουθεί η πυρηνόφιλη προσβολή του αρενίου στο ακύλιο:
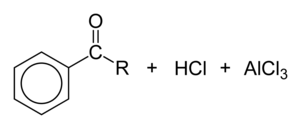
Τέλος, ένα άτομο χλωρίου αντιδρά προς σχηματισμό HCl και αναγέννηση του καταλύτη AlCl3:
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Friedel, C.; Crafts, J. M. Compt. Rend. 1877, 84, 1392 & 1450,
- ↑ Groves, J. K. (1972). «The Friedel–Crafts acylation of alkenes». Chem. Soc. Rev. 1: 73. doi:. https://archive.org/details/sim_chemical-society-great-britain-chemical-society-reviews_1972_1_1/page/73.
Πηγές
[Επεξεργασία | επεξεργασία κώδικα]- Α. Βάρβογλη (1991): Χημεία Οργανικών Ενώσεων. Παρατηρητής.
- Τζ. ΜακΜάρρυ (2005): Οργανική Χημεία. Πανεπιστημιακές Εκδόσεις Κρήτης.