Προπίνιο
| Προπίνιο | |||
|---|---|---|---|
| |||
| Γενικά | |||
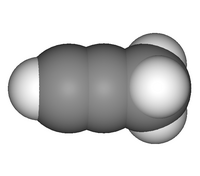
| Όνομα IUPAC | Προπίνιο | ||
| Άλλες ονομασίες | Μεθυλακετυλένιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C3H4 | ||
| Μοριακή μάζα | 40,0639 amu | ||
| Σύντομος συντακτικός τύπος |
CH3C≡CH | ||
| Συντομογραφίες | MeC≡CH | ||
| Αριθμός CAS | 74-99-7 | ||
| SMILES | C#CC | ||
| Δομή | |||
| Μήκος δεσμού | C-H: 106 pm C≡C: 120,6 pm | ||
| Είδος δεσμού | C-H: σ (2sp-1s) C≡C: σ (2sp-2sp) π (2py-2py) π (2pz-2pz) | ||
| Πόλωση δεσμού | C--H+: 3% | ||
| Μοριακή γεωμετρία | Ευθύγραμμη | ||
| Ισομέρεια | |||
| Ισομερή θέσης | 2 προπαδιένιο κυκλοπροπένιο | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -102,7 °C | ||
| Σημείο βρασμού | -23,2 °C | ||
| Πυκνότητα | 530 kg/m3 (υγρό) | ||
| Εμφάνιση | Άχρωμο αέριο | ||
| Χημικές ιδιότητες | |||
| Θερμότητα πλήρους καύσης |
1.724 kJ | ||
| Επικινδυνότητα | |||
| Εξαιρετικά εύφλεκτο (F+) | |||
| Κίνδυνοι κατά NFPA 704 |
|||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Το προπίνιο ή μεθυλακετυλένιο (αγγλικά: propyne) είναι οργανική χημική ένωση με μοριακό τύπο C3H4 και ημισυντακτικό τύπο CH3C≡CH. Είναι το 2ο μέλος της ομόλογης σειράς των αλκινίων, αμέσως μετά από το αιθίνιο, που είναι το απλούστερο αλκίνιο
Το χημικά καθαρό προπίνιο, στις «κανονικές συνθήκες περιβάλλοντος», δηλαδή σε θερμοκρασία 25 °C και υπό πίεση 1 atm, είναι άχρωμο αέριο, που χρησιμοποιείται ευρύτατα ως καύσιμο και ως πρόδρομη ένωση σύνθεσης άλλων οργανικών ενώσεων. Ήταν ένα συστατικό του αερίου MAPP, μαζί με το ισομερές του προπαδιένιο, που χρησιμοποιήθηκε συχνά στην οξυγονοκόλληση, γιατί αντίθετα από το αιθίνιο, το προπίνιο μπορεί να συμπιεστεί με ασφάλεια[1].
Ισομέρεια[Επεξεργασία | επεξεργασία κώδικα]
Με βάση τον παραπάνω αναφερόμενο μοριακό τύπο (C3H4), έχει τα ακόλουθα δύο (2) ισομερή θέσης:
- Το προπαδιένιο: Ένα αλκαδιένιο.
- Το κυκλοπροπένιο: Ένα κυκλοαλκένιο.
Ονοματολογία[Επεξεργασία | επεξεργασία κώδικα]
Η ονομασία «προπίνιο» προέρχεται από την ονοματολογία κατά IUPAC. Συγκεκριμένα, το πρόθεμα «προπ-» δηλώνει την παρουσία τριών (3) ατόμων άνθρακα ανά μόριο της ένωσης, το ενδιάμεσο «-ιν-» δείχνει την παρουσία ενός (1) τριπλού δεσμού μεταξύ ατόμων άνθρακα στο μόριο και η κατάληξη «-ιο» φανερώνει ότι δεν περιέχει χαρακτηριστικές ομάδες, δηλαδή ότι είναι υδρογονάνθρακας.
Δομή[Επεξεργασία | επεξεργασία κώδικα]
Δυο (2) από τα άτομα άνθρακα που περιέχει βρίσκονται σε υβριδισμό sp και συνδέονται με τριπλό δεσμό, δηλαδή ένα (1) σ και δύο (2) π. Το άλλο βρίσκεται σε sp3 υβριδισμό. Οι π-δεσμοί στο μόριο του προπινίου είναι υπεύθυνοι για τη χρήσιμη δραστικότητά του. Η περιοχή του τριπλού δεσμού χαρακτηρίζεται από (σχετικά) υψηλή ηλεκτρονιακή πυκνότητα, που επομένως είναι ευάλωτη σε επιδράσεις ηλεκτρονιόφιλων. Πολλές αντιδράσεις του προπινίου καταλύνται από διάφορα μέταλλα μετάπτωσης, που σχηματίζουν προσωρινά σύμπλοκα με τα π και π* τροχιακά του προπινίου[2].
| Δεσμοί[3] | ||||
| Δεσμός | τύπος δεσμού | ηλεκτρονική δομή | Μήκος δεσμού | Ιονισμός |
|---|---|---|---|---|
| C-H | σ | 2sp-1s | 106 pm | 3% C- H+ |
| C#1≡C#2 | σ | 2sp-2sp | 120,6 pm | |
| C#1≡C#2 | π | 2py-2py | 120,6 pm | |
| C#1≡C#2 | π | 2pz-2pz | 120,6 pm | |
| C#2-#3 | σ | 2sp-2sp3 | 147 pm | |
| Κατανομή φορτίων σε ουδέτερο μόριο | ||||
| C#3 | -0,09 | |||
| C#1 | -0,03 | |||
| C#2 | 0,00 | |||
| H | +0,03 | |||
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
Μείγμα προπίνιου - προπαδιενίου (MAPD) παράγεται ως παραπροϊόν, συχνά ανεπιθύμητο, με πυρόλυση προπανίου, από την οποία το κύριο προϊόν είναι το προπένιο, που είναι μια σημαντική πρόδρομη ένωση της χημικής βιομηχανίας[1]. Στη συνέχεια, το MAPD, αν δεν απομακρυνθεί, παίρνει μέρος στον καταλυτικό πολυμερισμό του προπενίου, σχηματίζοντας (συνήθως ανεπιθύμητα) συμπολυμερή.
Εργαστηριακές μέθοδοι[Επεξεργασία | επεξεργασία κώδικα]
Το προπίνιο μπορεί να συνθεθεί, σε εργαστηριακή κλίμακα, με αναγωγή 1-προπανόλης[4], 2-προπεν-1-όλης ή προπανόνης[5], με διέλευση ατμών τους πάνω από μαγνήσιο.
Εναλλακτικές μέθοδοι[Επεξεργασία | επεξεργασία κώδικα]
Με απόσπαση υδραλογόνων[Επεξεργασία | επεξεργασία κώδικα]
Με απόσπαση δύο ισοδυνάμων υδραλογόνου από 1,1-διαλοπροπάνιο, με χρήση υδροξειδίου του νατρίου (NaOH), παράγεται προπίνιο[6]:
- Το 1,2-διαλοπροπάνιο δίνει και μια σχετικά μικρή ποσότητα προπαδιένιου.
Με απόσπαση αλογόνων[Επεξεργασία | επεξεργασία κώδικα]
Με απόσπαση δύο μορίων αλογόνου από 1,1,2,2-τετραλοπροπάνιο, με χρήση ψευδαργύρου (Zn), παράγεται προπίνιο[7]:
Με μεθυλίωση αιθινίου[Επεξεργασία | επεξεργασία κώδικα]
Το αιθινικό νάτριο μπορεί να μεθυλιωθεί με μεθυλαλογονίδιο[8]:
Χημικές ιδιότητες και παράγωγα[Επεξεργασία | επεξεργασία κώδικα]
Το προπίνιο είναι μια ένωση που είναι βολική στο να προσθέτει ομάδα τριών ατόμων άνθρακα σε οργανικές συνθέσεις. Με επίδραση αλκυλολιθιακών ενώσεων, όπως το βουτυλολίθιο (BuLi), δίνει 1-προπινυλολίθιο (CH3C≡CLi). Το τελευταίο είναι ένα πυρηνόφιλο αντιδραστήριο, που μπορεί να δώσει αντίδραση προσθήκης σε καρβονυλικές ομάδες, παράγοντας έτσι αλκοόλες και εστέρες[9]. Αν και το ίδιο το χημικά καθαρό προπίνιο είναι ακριβό, το αέριο MAPP μπορεί να χρησιμοποιηθεί στη θέση του και παράγεται (σχετικά) φθηνά σε μεγάλες ποσότητες[10].
Το προπίνιο, μαζί με το 2-βουτίνιο, μπορεί επίσης να χρησιμοποιηθεί για τη σύνθεση αλκυλιωμένων υδροκινονών, γεγονός που έχει εφαρμογή στη σύνθεση βιταμίνης Ε[11].
Ισομερείωση[Επεξεργασία | επεξεργασία κώδικα]
Βρίσκεται σε χημική ισορροπία με το ισομερές του προπαδιένιο. Το μείγμα συμβολίζεται συντομογραφικά MAPD (MethylAcetylPropylDiene):
Η σταθερά ισορροπίας της αντίδρασης είναι 0,22 στους 270 °C και 0,1 στους 5 °C. Βιομηχανικά το MAPD παράγεται ως παραπροϊόν της πυρόλυσης του προπανίου, που παράγει κυρίως προπένιο. Το MAPD επεμβαίνει στον κατιονικό πολυμερισμό του προπενίου (αλλάζοντας το προϊόν πολυμερισμού με προϊόν συμπολιμερισμού)[1].
Καύση[Επεξεργασία | επεξεργασία κώδικα]
Με το οξυγόνο του αέρα καίγεται παρέχοντας κυανή φλόγα υψηλότατης θερμοκρασίας:
Ενυδάτωση[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση θειικού οξέος και στη συνέχεια νερού (ενυδάτωση) σε προπίνιο, παρουσία ιόντων υδραργύρου (Hg), παράγεται προπανόνη (CH3COCH3)[12]:
- Ενδιάμεσα παράγεται προπεν-2-όλη (ασταθής ενόλη) που ισομερειώνεται σε προπανόνη.
Προσθήκη υπαλογονώδους οξέος[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση (προσθήκη) υποαλογονώδους οξέος (HOX) προπίνιο παράγεται αλοπροπανόνη[13]:
- Ενδιάμεσα παράγεται 1-αλοπροπεν-2-όλη (ασταθής ενόλη) που ισομερειώνεται σε αλοπροπανόνη.
Καταλυτική υδρογόνωση[Επεξεργασία | επεξεργασία κώδικα]
Με καταλυτική υδρογόνωση προπινίου σχηματίζεται αρχικά προπένιο και στη συνέχεια (με περίσσεια υδρογόνου) προπάνιο.[14]:
Αλογόνωση[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση αλογόνου (X2) (αλογόνωση) σε προπίνιο έχουμε προσθήκη στον τριπλό δεσμό. Παράγεται αρχικά 1,2-διαλοπροπένιο και στη συνέχεια (με περίσσεια αλογόνου) 1,1,2,2-τετραλοπροπάνιο.[15]:
Υδραλογόνωση[Επεξεργασία | επεξεργασία κώδικα]
Με προσθήκη υδραλογόνων (HX) (υδραλογόνωση) σε προπίνιο παράγεται αρχικά 2-αλοπροπένιο και στη συνέχεια (με περίσσεια υδραλογόνου) 2,2-διαλοπροπάνιο.[16]:
Υδροκυάνωση[Επεξεργασία | επεξεργασία κώδικα]
Με προσθήκη υδροκυανίου (HCN) (υδροκυάνωση) σε προπίνιο παράγεται μεθυλαιθενονιτρίλιο:
Προσθήκη μονοξειδίου του άνθρακα[Επεξεργασία | επεξεργασία κώδικα]
1. Με προσθήκη μονοξειδίου του άνθρακα (CO) και νερού (H2O), παράγεται μεθυλο-2-προπενικό οξύ:
2. Με προσθήκη μονοξειδίου του άνθρακα (CO) και αλκοόλης (ROH), παράγεται μεθυλο-2-προπενικός αλκυλεστέρας:
Διυδροξυλίωση[Επεξεργασία | επεξεργασία κώδικα]
Η διυδροξυλίωση προπινίου, αντιστοιχεί σε προσθήκη H2O2 και παράγει υδροξυπροπανόνη[17]:
1. Επίδραση αραιού διαλύματος υπερμαγγανικού καλίου (KMnO4). Π.χ.:
2. Επίδραση καρβονικού οξέος και υπεροξείδιου του υδρογόνου:
- Ενδιάμεσα παράγεται 1,2-προπενοδιόλη (ασταθής ενόλη) που ισομερειώνεται σε υδροξυαιθανάλη.
Επίδραση πυκνού υπερμαγγανικού καλίου[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση πυκνού διαλύματος υπερμαγγανικού καλίου (KMnO4) παράγεται πυροσταφυλικό οξύ[18]:
Προσθήκη αλκοολών[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση αλκοόλης (ROH) σε προπίνιο παράγεται 2-αλκοξυπροπένιο[19]:
Προσθήκη καρβονικών οξέων[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση καρβονικών οξέων (RCOOH) σε προπίνιο παράγεται καρβονικός μεθυλοβινυλεστέρας[20]:
Οζονόλυση[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση όζοντος (οζονόλυση) σε προπίνιο, παράγεται αρχικά ασταθές οζονίδιο που τελικά διασπάται σε οξοπροπανάλη[21]:
Όξινη συμπεριφορά[Επεξεργασία | επεξεργασία κώδικα]
1. Αντιδρά με το νατραμίδιο, σε υγρή αμμωνία, σχηματίζοντας προπινικό νάτριο[22]:
2. Αντιδρά με το βουτυλολίθιο, σε ψυχρό τετραϋδροφουράνιο, σχηματίζοντας προπινικό λίθιο[22]:
3. Με επίδραση μεταλλικού νατρίου παράγεται προπινικό νάτριο[8]:
- Το προπανικό νάτριο αποτελεί πρώτη ύλη για την παραγωγή άλλων παραγώγων με τριπλό δεσμό, γιατί αντιδρά με αλκυλαλογονίδια (RX):
4. Με επίδραση ιόντων αργύρου (Ag+) και παρουσία αμμωνίας (NH3) παράγεται ένα λευκό στερεό, ο προπινικός άργυρος[23]:
5. Με επίδραση ιόντων μονοσθενούς χαλκού (Cu+) και παρουσία αμμωνίας (NH3) παράγεται ένα κεραμιδί στερεό, ο προπινικός χαλκός[24]:
- Οι αντιδράσεις #4 και #5 χρησιμοποιούνται για την ανίχνευση της ομάδας -C ≡ CH.
Χημεία Reppe[Επεξεργασία | επεξεργασία κώδικα]
Ο Γουώλτερ Ρέππε (Walter Reppe) ανακάλυψε ότι, παρουσία διαφόρων καταλυτών, το προπίνιο μπορεί να αντιδράσει με διάφορα αντιδραστήρια παράγοντας μια ευρεία ποικιλία βιομηχανικά σημαντικών χημικών[25][26].
1. Με αλκοόλες (ROH), με το υδροκυάνιο (HCN), με το υδροχλώριο (HCl) και με καρβοξυλικά οξέα (RCOOH), το αιθίνιο παράγει 2-προπενυλενώσεις (δηλαδή ενώσεις γενικού τύπου AC(CH3)=CH2)[1][27][28]:
2. Με αλδεΰδες (RCHO) δίνει προπινυλόλες[1], σύμφωνα με την αντίδραση Φαβόρσκιυ (Favorskii reaction):
3. Με αντίδραση προπινίου με μονοξείδιο του άνθρακα και νερό ή αλκοόλη παράγεται μεθυλοπροπενικό οξύ ή μεθυλοπροπενικός εστέρας, αντιστοίχως, που χρησιμοποιούνται, με τη σειρά τους, για την παραγωγή μεθακρυλικού γυαλιού και άλλων μεθακρυλικών προϊόντων[29]:
4. Με κυκλοποίηση (μαζί με ολιμερισμό) προπινίου παράγεται το μεσιτυλένιο, το 1,3,5,7-τετραμεθυλοκυκλοοκτατετραένιο[1] και η 2,5-διμεθυλουδροκινόνη[26][30][31]:
Προσθήκη καρβενίων[Επεξεργασία | επεξεργασία κώδικα]
Κατά την προσθήκη μεθυλενίου σε προπίνιο σχηματίζονται 1-βουτίνιο, 2-βουτίνιο και κυκλοπροπένιο[32]:
- Η αντίδραση είναι ελάχιστα εκλεκτική και αυτό σημαίνει ότι κατά προσέγγιση έχουμε:
- 1. Παρεμβολή στους τρεις (3) δεσμούς C#3-H: Προκύπτει 1-βουτίνιο, που είναι ένα αλκίνιο.
- 2. Παρεμβολή στον έναν (1) δεσμό C#1-H: Προκύπτει 2-βουτίνιο, που είναι ένα αλκίνιο.
- 3. Προσθήκη στον έναν (1) τριπλό δεσμό: Προκύπτει 1-μεθυλοκυκλοπροπένιο, που είναι ένα κυκλοαλκένιο.
- Προκύπτει επομένως μίγμα 1-βουτινίου ~60%, 2-βουτινίου ~20% και 1-μεθυλοκυκλοπροπενίου ~20%.
- Με τη χρήση διιωδομεθάνιου (CH2I2) και ψευδαργύρου (Zn) επικρατεί η προσθήκη, οπότε είναι:
Χρήση ως καυσίμου πυραύλων[Επεξεργασία | επεξεργασία κώδικα]
Ευρωπαϊκές εταιρίες παραγωγής διαστημικών οχημάτων ερευνούν τη χρήση ελαφρών υδρογονανθράκων σε συνδυασμό με υγρό οξυγόνο, ως υψηλής απόδοσης προωθητικό πυραύλων, που είναι επίσης λιγότερο τοξικό από το συνηθισμένο χρησιμοποιούμενο μίγμα MMH/NTO, που είναι μίγμα μονομεθυλυδραζίνης και τετροξειδίου του αζώτου. Η έρευνά τους έδειξε ότι το προπίνιο θα μπορούσε να δώσει ένα καύσιμο με πολλά πλεονεκτήματα για σκάφη που προορίζονται για επιχειρήσεις χαμηλής τροχιάς πάνω από τη Γη. Έφθασαν σε αυτό το συμπέρασμα βασιζόμενοι στην ειδική προώθηση του προπινίου που αναμένεται να φθάνει, με χρήση οξυγόνου ως οξειδωτικού, τα 370 s, με υψηλή πυκνότητα και πυκνότητα ισχύος, αλλά μέτρια θερμοκρασία βρασμού, γεγονός που κάνει ευκολότερη την αποθήκευσή του, σε σύγκριση με άλλα καύσιμα που απαιτούν πολύ χαμηλές, κρυογονικές θερμοκρασίες.
Παρατηρήσεις, υποσημειώσεις και αναφορές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 Peter Pässler, Werner Hefner, Klaus Buckl, Helmut Meinass, Andreas Meiswinkel, Hans-Jũrgen Wernicke, Günter Ebersberg, Richard Müller, Jürgen Bässler, Hartmut Behringer, Dieter Mayer, "Acetylene" in Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, Weinheim 2007 (doi:10.1002/14356007.a01 097.pub2).
- ↑ Organic Chemistry 7th ed. by J. McMurry, Thomson 2008
- ↑ Τα δεδομένα προέρχονται εν μέρει από το «Table of periodic properties of thw Ellements», Sagrent-Welch Scientidic Company και Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, Σελ. 34.
- ↑ Keiser, Edward; & Breed, Mary (1895). "The Action of Magnesium Upon the Vapors of the Alcohols and a New Method of Preparing Allylene". The Journal of the Franklin Institute. CXXXIX: 304–309. Retrieved 20 February 2014.
- ↑ Reiser, Edward II. (1896). "The preparation of Allylene, and the Action of Magnesium upon Organic Compounds". The Chemical News and Journal of Industrial Science. LXXIV: 78–80. Retrieved 20 February 2014.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.153, §6.4.3.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.153, §6.3.1β.
- ↑ 8,0 8,1 Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 159, §6.9.10α.
- ↑ Michael J. Taschner, Terry Rosen, and Clayton H. Heathcock (1990), "Ethyl Isocrotonate", Org. Synth.; Coll. Vol. 7: 226
- ↑ US patent 5744071, Philip Franklin Sims, Anne Pautard-Cooper, "Processes for preparing alkynyl ketones and precursors thereof", issued 1996-11-19
- ↑ Reppe, Walter; Kutepow, N; and Magin, A (1969). "Cyclization of Acetylenic Compounds". Angewandte Chemie International Edition in English 8 (10): 727–733. doi:10.1002/anie.196907271. Retrieved 26 December 2013.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 158, §6.9.3.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 156, §6.8.4.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 158, §6.9.4α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 158, §6.9.2.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 158, §6.9.1.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 157, §6.8.9.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 158, §6.9.8.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 158, §6.9.5.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 158, §6.9.6.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 158, §6.9.7α.
- ↑ 22,0 22,1 Midland, M. M.; McLoughlin, J. I.; Werley, Ralph T. (Jr.) (1990), "Preparation and Use of Lithium Acetylide: 1-Methyl-2-ethynyl-endo-3,3-dimethyl-2-norbornanol", Org. Synth. 68: 14; Coll. Vol. 8: 391.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 159, §6.9.10β.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 159, §6.9.10γ.
- ↑ Peter Pässler, Werner Hefner, Klaus Buckl, Helmut Meinass, Andreas Meiswinkel, Hans-Jürgen Wernicke, Günter Ebersberg, Richard Müller, Jürgen Bässler, Hartmut Behringer and Dieter Mayer (2007). "Acetylene". Ullmann's Encyclopedia of Industrial Chemistry: pg. 44. doi:10.1002/14356007.a01_097.pub2. Retrieved 26 December 2013.
- ↑ 26,0 26,1 Reppe, Walter; Kutepow, N; and Magin, A (1969). "Cyclization of Acetylenic Compounds". Angewandte Chemie International Edition in English 8 (10): 727–733. doi:10.1002/anie.196907271. Retrieved 26 December 2013.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 158, §6.9.5.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 158, §6.9.6.
- ↑ Takashi Ohara, Takahisa Sato, Noboru Shimizu, Günter Prescher, Helmut Schwind, Otto Weiberg, Klaus Marten and Helmut Greim (2003). "Acrylic Acid and Derivatives". Ullmann's Encyclopedia of Industrial Chemistry: pg. 7. doi:10.1002/14356007.a01_161.pub2. Retrieved 26 December 2013.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 159, §6.9.11γ.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 159, §6.9.11δ.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 157, §6.8.7., σελ. 155, §6.7.3, R = CH2=CH
Πηγές[Επεξεργασία | επεξεργασία κώδικα]
- Speight J. G., “Chemical and Process Design Handbook”, McGraw-Hill, 2002.
- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
- University College of Cork









![{\displaystyle \mathrm {CH_{3}C\equiv CH+H_{2}{\xrightarrow {Ni\;{\acute {\eta }}\;Pd\;{\acute {\eta }}\;Pt}}CH_{3}CH=CH_{2}{\xrightarrow[{+H_{2}}]{Ni\;{\acute {\eta }}\;Pd\;{\acute {\eta }}\;Pt}}CH_{3}CH_{2}CH_{3}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/5824de5e61f5970670ce1082302ebb89276b50ae)
![{\displaystyle \mathrm {CH_{3}C\equiv CH+X_{2}{\xrightarrow {CCl_{4}}}CH_{3}CX=CHX{\xrightarrow[{+X_{2}}]{CCl_{4}}}CH_{3}CX_{2}CHX_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/7db948524c1fea8e97bea3222e699831db1034ce)











![{\displaystyle \mathrm {CH_{3}C\equiv CH+BuLi{\xrightarrow[{-78^{o}C}]{THF}}CH_{3}C\equiv CLi+BuH} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/80c4f8510efcb31d588d7ec0c16915602d38df03)













![{\displaystyle \mathrm {4CH_{3}C\equiv CH{\xrightarrow[{60^{o}C,\;15\;bar}]{Ni(CN)_{2},\;CaC_{2},\;THF}}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/5ddb96f8462836bb53f1f65cacf3dc5cdcb95fca)
![{\displaystyle \mathrm {Fe(CO)_{5}+4CH_{3}C\equiv CH+2H_{2}O{\xrightarrow[{\beta \alpha \sigma \iota \kappa {\acute {\epsilon }}\varsigma \;\sigma \upsilon \nu \theta {\acute {\eta }}\kappa \epsilon \varsigma }]{50-80^{o}C,\;20-25\;atm}}FeCO_{3}+2} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/94b0f9f9c39149748c9bfddcd3e959fa0558652c)


