Αιθέρες
Οι αιθέρες είναι τάξη οργανικών ενώσεων που περιέχουν μία (τουλάχιστον) αιθερική ομάδα (R-O-R΄), δηλαδή ένα (1) άτομο οξυγόνου συνδεμένο με δυο υδροκαρβύλια, συνήθως αλκύλια ή και αρύλια, ως κύρια χαρακτηριστική ομάδα.[1] Οι αιθέρες ταξινομούνται σε δυο μεγάλες ομάδες:
- Τους συμμετρικούς αιθέρες, στους οποίους R = R΄
- Τους ασύμμετρους αιθέρες, στους οποίους R ≠ R΄.
Οι αιθέρες είναι συνηθισμένοι στην οργανική χημεία, ενώ αιθερικές ομάδες παρατηρούνται επίσης σε βιοχημικές ενώσεις, όπως οι υδατάνθρακες και η λιγνίνη.

Ταξινόμηση[Επεξεργασία | επεξεργασία κώδικα]
Οι αιθέρες διακρίνονται σε άκυκλους όπως οι από (Ι) έως (V), κυκλικούς όπως οι (VI), (VII) κορεσμένους όπως οι (Ι), (V), (VΙ), (VII) και ακόρεστους όπως (II), (III), (IV) ).
Παραδείγματα :

Ειδικά οι κορεσμένοι άκυκλοι αιθέρες θεωρητικά προκύπτουν από αλκοόλες με αντικατάσταση του αλκοολικού υδρογόνου από οργανική ρίζα ή από το νερό με αντικατάσταση των δύο ατόμων Η από οργανικές ρίζες ή από τα αλκάνια (RH) με αντικατάσταση ενός ατόμου Η από την αλκοξυομάδα : RO- (CH3O-, CH3CH2O- κλπ.). Έχουν γενικό μοριακό τύπο CnH2n+2Ο (n ≥ 2) και είναι ισομερείς με τις κορεσμένες μονοσθενείς αλκοόλες.
Οι αιθέρες του γενικού τύπου R-O-R ή Ph-O-Ph ονομάζονται απλοί (συμμετρικοί) ενώ οι αιθέρες του τύπου R-O-R' ή Ph-O-R ή Ph-O-R λέγονται μικτοί (ασύμμετροι).
Οι όροι "πρωτοταγής", "δευτεροταγής" και "τριτοταγής αιθέρας" αναφέρονται στους απλούς αιθέρες και έχουν σχέση με το άτομο άνθρακα που είναι ενωμένο με το οξυγόνο. Στους πρωτοταγείς αιθέρες, ο άνθρακας αυτός ενώνεται με ένα άλλο άτομο άνθρακα (π.χ. ο διαιθυλ-αιθέρας CH3-CH2-O-CH2-CH3), στους δευτεροταγείς με δύο άτομα άνθρακα όπως ο διισοπροπυλ-αιθέρας (CH3)2CH-O-CH(CH3)2 και στους τριτοταγείς με τρία όπως ο δι-τριτ.βουτυλ-αιθέρας (CH3)3C-O-C(CH3)3.
Ονοματολογία[Επεξεργασία | επεξεργασία κώδικα]
Οι αιθέρες ονομάζονται με δύο τρόπους :
- Προτάσσεται το όνομα της απλούστερης ομάδα RO- (π.χ. μεθόξυ-, αιθόξυ-, κλπ.) και ακολουθεί το όνομα του υδρογονάνθρακα που αντιστοιχεί στην άλλη ομάδα (την πολυπλοκότερη) R'-.
- Προτάσσονται αλφαβητικά τα ονόματα των ριζών και ακολουθεί η λέξη "αιθέρας".
Παραδείγματα :

Με το πρόθεμα "εποξυ-" δηλώνεται ένα άτομο οξυγόνου ενωμένο με δύο άτομα άνθρακα κάποιου δακτυλίου ή με δύο γειτονικά άτομα άνθρακα μιας C-αλυσίδας [ένωση (Ι)]. Σ'έναν αιθέρα μπορεί να υπάρχουν και άτομα αλογόνου [ένωση (ΙΙ)] ή υδροξύλια [ένωση (ΙΙΙ)].
Μονοκυκλικές ενώσεις που περιέχουν ένα ή περισσότερα οξυγόνα ως ετεροάτομα σε δακτύλιο με τρία μέχρι δέκα μέλη ονομάζονται με το πρόθεμα "οξα-" και κατάληξη "-ιρανιο" (για κορεσμένο δακτύλιο με 3 μέλη), "-ετανιο" (για κορεσμένο δακτύλιο με 4 μέλη), "-ολανιο" (για κορεσμένο δακτύλιο με 5 μέλη), "-ανιο" (για κορεσμένο δακτύλιο με 6 μέλη) κλπ. [ενώσεις (IV), (V)]. Αν οι δακτύλιοι είναι ακόρεστοι τότε οι καταλήξεις γίνονται αντίστοιχα "-ιρενιο", "-ετιο", "-ολιο", "-ινιο" κλπ.

Παρακάτω φαίνονται επίσης και κάποιες ενώσεις που ανήκουν στους αιθέρες και είναι γνωστές με τα εμπειρικά τους ονόματα [ενώσεις (VI), (VII), (VIII)]
 Φαινετόλη (VI),
Φαινετόλη (VI),  Ευγενόλη (VII),
Ευγενόλη (VII),
 Ανισόλη (VIII)
Ανισόλη (VIII)
Παρασκευές[Επεξεργασία | επεξεργασία κώδικα]
Οι αιθέρες παρασκευάζονται με διάφορους τρόπους :
Αφυδάτωση αλκοολών
Οι συμμετρικοί αιθέρες που περιέχουν τις μικρότερες αλκυλομάδες παρασκευάζονται στη βιομηχανία σε μεγάλη κλίμακα με αφυδάτωση αλκοολών που καταλύεται από οξέα. Ο πιο σημαντικός απ' αυτούς είναι ο διαιθυλαιθέρας. Άλλοι είναι ο διισοπροπυλ-αιθέρας και ο δι-n-βουτυλ-αιθέρας. Η αντίδραση πραγματοποιείται σε αρκετά ήπιες συνθήκες, ώστε να επικρατήσει η επιθυμητή διαμοριακή αφυδάτωση (SN2) και όχι η ενδομοριακή απόσπαση (Ε) που οδηγεί στο σχηματισμό αλκενίων. Τα οξέα που χρησιμοποιούνται στους 140°C είναι διαλύματα ανόργανων οξέων όπως το πυκνό H2SO4 ή τα οξέα κατά Lewis BF3, AlCl3, ZnCl2. Χρησιμοποιούνται ακόμα και όξινα άλατα όπως το NaHSO4. Αν η αφυδάτωση γίνει στην υγρή φάση, η απόδοση μεγαλώνει όταν ο σχηματιζόμενος αιθέρας απομακρύνεται με απόσταξη. Αν η αφυδάτωση γίνει στην αέρια φάση, τότε οι ατμοί της αλκοόλης περνούν, στους 240°C - 260°C, πάνω από θερμαινόμενο στερεό καταλύτη όπως το Al2O3 ή το TiO2. Συνολικά η αντίδραση μπορεί να γραφεί :
Παράδειγμα :
- 2CH3CH2OH → CH3CH2-O-CH2CH3 + H2O
Το σύστημα αλκοόλη-θειικό οξύ μπορεί να δώσει επίσης όξινους και ουδέτερους θειικούς εστέρες, λόγω όμως της σχετικά ψηλής θερμοκρασίας δεν παρατηρείται σχηματισμός τους σε υπολογίσιμες ποσότητες, γιατί υδρολύονται στα συστατικά τους. Ένας απλός μηχανισμός της αφυδάτωσης, θα μπορούσε να είναι ο εξής :

Αρχικά πρωτονιώνεται η αλκοόλη και έτσι γίνεται ευκολότερη η προσβολή της από το πυρηνόφιλο ROH από την οποία σχηματίζεται ο πρωτονιωμένος αιθέρας. Με απόσπαση στη συνέχεια του Η+ από τη βάση -ΟSO3Η (ή γενικότερα τη συζυγή βάση του χρησιμοποιούμενου οξέος) παράγεται ο αιθέρας και ελευθερώνεται το οξύ.
Από την αφυδάτωση των άκυκλων αλκοολών μπορεί να προκύψει μίγμα αιθέρων που δύσκολα διαχωρίζεται :
- 3R-OH + 3R'-OH → R-O-R + R'-O-R + R'-O-R' + 3H2Ο
Αν όμως η μια αλκοόλη είναι τριτοταγής, παράγεται μικτός αιθέρας με μεγάλη απόδοση :
- CH3CH2OH + (CH3)3COH → CH3CH2-O-C(CH3)3 (απόδοση 95 %)
Σύνθεση Williamson
Πρόκειται για αλκυλίωση αλκυλαλογονιδίων. Σύμφωνα με τη μέθοδο αυτή ένα πρωτοταγές και μερικές φορές δευτεροταγές αλκυλαλογονίδιο, θερμαίνεται με αλκοξείδιο του νατρίου το οποίο έχει παρασκευάσθείι απευθείας με προσθήκη μεταλλικού νατρίου σε περίσσεια άνυδρης αλκοόλης : ROH + Na → RONa + 1/2H2 μέσα σε διάλυμα αλκοόλης. Με τη μέθοδο αυτή μπορούμε να πάρουμε απλούς και μικτούς αιθέρες καθώς και παράγωγα αιθέρων :
Μια τυπική αντίδραση Williamson διεξάγεται σε 50-100°C και έχει ολοκληρωθεί σε 1-8 ώρες. Συχνά, η πλήρης αντίδραση της πρώτης ύλης, είναι δύσκολο να επιτευχθεί, καθώς οι ανεπιθύμητες αντιδράσεις είναι συχνές.
Παραδείγματα :
- CH3(CH2)5CH2ONa + CH3CH2I → CH3(CH2)5CH2-O-CH2CH3 + NaI (απόδοση 91 %)
- CH3OCH2CH2ONa + CH3Cl → CH3-O-CH2CH2-O-CH3 + NaCl (απόδοση 78 %)
- CH3ONa + Br-(CH2)6-Br → Br-(CH2)6-O-CH3 + NaBr (απόδοση 80 %)
 + NaOCH3 →
+ NaOCH3 →  + NaCl
+ NaCl [2] + RX →
[2] + RX →  + NaX
+ NaX
Η αντίδραση είναι τυπική πυρηνόφιλη υποκατάσταση μηχανισμού SN2 αλλά δύσκολα αποφεύγεται και η παράλληλη αντίδραση απόσπασης προς αλκένια ιδίως όταν το αλκυλαλογονίδιο είναι τριτοταγές. Ο γενικός μηχανισμός της αντίδρασης είναι :

Για να παρασκευάσουμε λοιπόν τριτ.βουτυλο-μεθυλ-αιθέρα, CH3-O-(CH3)3, θα χρησιμοποιήσουμε τριτ.βουτοξείδιο του νατρίου, (CH3)3ONa, με μεθυλο-αλογονίδιο, CH3X, και όχι μεθοξείδιο του νατρίου, CH3ONa, με τριτ.βουτυλο-αλογονίδιο, (CH3)3X :
- (CH3)3ONa + CH3X → CH3-O-(CH3)3 + NaX
- CH3ONa + (CH3)3X → ΟΧΙ
Οι καταλύτες δεν είναι απαραίτητοι στις εργαστηριακές αντιδράσεις. Εντούτοις αν χρησιμοποιηθεί κάποιο μη δραστικό αλκυλαλογονίδιο (π.χ. αλκυλο-χλωρίδιο), η ταχύτητα της αντίδρασης μπορεί να επιταχυνθεί αν χρησιμοποιηθεί ως καταλύτης κάποιο ευδιάλυτο ιωδιούχο άλας το οποίο θα αλλάξει το αλογόνο του αλκυλαλογονιδίου[3] κάνοντας το πιο δραστικό. Σε ακραίες περιπτώσεις μπορεί να χρησιμοποιηθεί ως καταλύτης Ag2O.
Αλκοξυ-υδραργύρωση - αφυδραργύρωση Είναι εργαστηριακή μέθοδος παρασκευής αιθέρων η οποία πλεονεκτεί έναντι της μεθόδου Williamson διότι δεν συμβαίνει ανταγωνιστική αντίδραση απόσπασης. Έτσι μπορεί να χρησιμοποιηθεί για την παρασκευή σχεδόν κάθε είδους αλκυλαιθέρα εκτός των δι-τριτ.αλκυλαιθέρων, για στερεοχημικούς λόγους. Η αντίδραση πραγματοποιείται σε δύο στάδια :
- Αρχικά το αλκένιο (που έχει διαλυθεί σε τετραϋδροφουράνιο, THF) αντιδρά με τριφθοροξικό υδράργυρο, (CF3COO)2Hg, που έχει διαλυθεί σε αλκοόλη. Ο τριφθοροξικός υδράργυρος προτιμάται από τον οξικό υδράργυρο, (CH3COO)2Hg για καλύτερες αποδόσεις κυρίως όταν χρησιμοποιούνται ογκώδεις αλκοόλες. Η ηλεκτρονιόφιλη αυτή προσθήκη (που λέγεται αλκοξυδραργύρωση) γίνεται σύμφωνα με τον κανόνα του Markovnikov και η αλκοξυ-ομάδα, RO-, της αλκοόλης πηγαίνει στον περισσότερο υποκατεστημένο άνθρακα του διπλού δεσμού του αλκενίου, ενώ η ομάδα CF3COOHg- του τριφθοροξικού υδραργύρου, πηγαίνει στον άλλο άνθρακα. Έτσι σχηματίζεται μια αλκοξυ-υδραργυρωμένη ένωση :
Ο μηχανισμός περιλαμβάνει τον ενδιάμεσο σχηματισμό ασταθούς τριμελούς δακτυλίου που είναι ένα κλειστό ιόν υδραργυρωνίου :

- Στη συνέχεια η οργανοϋδραργυρική αυτή ένωση, χωρίς να απομονωθεί, με αναγωγή με αλκαλικό διάλυμα (NaOH) υδριδίου βορίου-νατρίου, NaBH4, δίνει αιθέρα. Γίνεται δηλαδή αντικατάσταση (αφυδραργύρωση) της υδραργυρικής ομάδας από Η του αναγωγικού NaBH4 :
Παραδείγματα :
- CH3-(CH2)3-C(CH3)=CH2 + (CH3)2CH-OH → → CH3-(CH2)3-CH(CH3)-O-CH(CH3)2 (απόδοση 98 %)
- (CH3)3C-CH=CH2 + (CH3)2CH-OH → → (CH3)3-CH(CH3)-O-CH(CH3)2
Φυσικές ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Τα μόρια των αιθέρων παρουσιάζουν πολικότητα (η συνισταμένη διπολική ροπή είναι το πράσινο βέλος της εικόνας στις χημικές ιδιότητες) π.χ. για τον διαιθυλαιθέρα είναι 1,18 D. Αυτή η μικρή πολικότητα δεν επηρεάζει πολύ τα σημεία βρασμού των αιθέρων, τα οποία είναι περίπου ίδια με εκείνα των αλκανίων με ανάλογες σχετικές μοριακές μάζες : το n-επτάνιο (Mr = 72) έχει σ.β 98°C ενώ το μεθοξυ-πεντάνιο (Mr = 102) έχει 100°C.
Η απουσία της ομάδας ΟΗ- από το μόριο των αιθέρων αποκλείει την ύπαρξη δεσμών υδρογόνου μεταξύ των αιθερικών μορίων και συνεπώς οι αιθέρες έχουν χαμηλότερα σημεία βρασμού από τις ισομερείς αλκοόλες : η 1-εξανόλη (ισομερής με το μεθοξυ-πεντάνιο) έχει σ.β. 157°C.
Οι διαλυτότητες των αιθέρων στο νερό είναι συγκρίσιμες μ' εκείνες των ισομερών τους αλκοολών διότι στους αιθέρες μπορούν να δημιουργηθούν δεσμοί υδρογόνου μεταξύ του Ο του αιθέρα και των Η του νερού : ο διαιθυλαιθέρας (CH3CH2-O-CH2CH3) έχει την ίδια διαλυτότητα με την ισομερή του 1-βουτανόλη (CH3CH2CH2CH2-OH), περίπου 9.1 mL/100 mL H2Ο στους 25 °C. Το τετραϋδροφουράνιο και το 1,4-διοξάνιο είναι πολύ διαλυτά στο νερό.
| Φυσικές ιδιότητες ορισμένων αιθέρων | |||||
|---|---|---|---|---|---|
| Αιθέρας | Δομή | Σημείο τήξης (°C) | Σημείο βρασμού(°C) | Διαλυτότητα σε 1 L νερού | Διπολική ροπή (D) |
| Διμεθυλαιθέρας | CH3-O-CH3 | -138.5 | -23.0 | 70 g | 1,30 |
| Διαιθυλαιθέρας | CH3CH2-O-CH2CH3 | -116.3 | 34.4 | 69 g | 1.18 |
| Τετραϋδροφουράνιο | O(CH2)4 | -108.4 | 66.0 | Διαλυτό | 1.74 |
| Διοξάνιο | O(C2H4)2O | 11.8 | 101.3 | Διαλυτό | 0.45 |

Οι αιθέρες διαλύονται πολύ στους οργανικούς διαλύτες, ενώ αποτελούν και οι ίδιοι άριστα διαλυτικά. Χαρακτηρίζονται ως απρωτικοί διαλύτες επειδή δεν ανταλλάσσουν πρωτόνια με τη διαλυμένη ουσία. Ο διαιθυλαιθέρας και το τετραϋδροφουράνιο είναι, για παράδειγμα, οι διαλύτες στους οποίους συνήθως παρασκευάζονται και χρησιμοποιούνται τα αντιδραστήρια Grignard. Οι αιθέρες διαλύουν όχι μόνο οργανικές αλλά και ανόργανες ενώσεις και χρησιμοποιούνται πολύ σαν διαλύτες σε διάφορες αντιδράσεις λόγω της χημικής αδράνειας που εμφανίζουν. Η ικανότητά τους να διαλύουν οργανικές ενώσεις οφείλεται στο ότι τα μόριά τους είναι ελαφρώς πολωμένα και μπορούν και συγκρατούνται με δυνάμεις van der Waals με τα οργανικά μόρια που διαλύουν.
Από τα κατώτερα μέλη των κορεσμένων αλειφατικών αιθέρων αέρια είναι ο διαιθυλαιθέρας και ο αιθυλ-μεθυλ-αιθέρας. Τα υπόλοιπα κατώτερα μέλη, όπως και τα μεσαία, είναι υγρά ενώ τα ανώτερα είναι στερεά. Οι αιθέρες είναι εύφλεκτα υλικά.
Δομή και χημικές ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]


Ο εξαμελής ετεροκυκλικός αιθέρας, το τετραϋδροπυράνιο, αλλά και τα παράγωγά του έχουν δομή "ανάκλιντρου" και όχι δομή "λουτήρα" που είναι ασταθέστερη, επειδή στερούνται τάσης κατά Μπάϋερ (Bayer) η οποία οφείλεται στην αλλοίωση των γωνιών των δεσμών. Στο ανάκλιντρο οι υποκαταστάτες είναι διαβαθμισμένοι και γι' αυτό είναι πιο σταθερό, ενώ στο λουτήρα εμφανίζονται και τάσεις στρέψης γιατί υπάρχουν και άτομα σε εκλειπτική διαμόρφωση.
Το μόριο ενός αλειφατικού αιθέρα (R-O-R') μοιάζει με το μόριο του νερού μόνο που στη θέση των δύο ατόμων υδρογόνου υπάρχουν δύο αλκύλια. Η γωνία του δεσμού C-O-C είναι περίπου 110°C (π.χ. στον διμεθυλαιθέρα είναι 111,5°C).
Το φάσμα υπερύθρου ενός αιθέρα παρουσιάζει ισχυρή ταινία που οφείλεται στην τάση C-Ο στην περιοχή των 1060 – 1150 cm−1 για τους αλκυλ-αιθέρες και στους 1200 – 1275 cm−1 για τους αρυλ-αιθέρες και βινυλ-αιθέρες (με μια ασθενεστερη στους 1020 – 1075 cm−1).
Οι αιθέρες έχουν ασθενείς βασικές ιδιότητες και είναι αρκετά σταθερές ενώσεις. Με κοινά οξειδωτικά δεν αντιδρούν.
Καύση
Καίγονται πλήρως καθαρό ή ατμοσφαιρικό O2 και εφόσον αποτελούνται μόνο από C, H, O, δίνουν CO2 και Η2Ο. Η γενική αντίδραση καύσης των κορεσμένων μονο-αιθέρων είναι :
Παράδειγμα :
- CH3OCH3 + 3O2 → 2CO2 + 3H2O
Αντικατάσταση υδρογόνων από χλώριο
Παρουσία ακτινοβολίας ορατής ή υπεριώδους, αντικαθίστανται τα α-υδρογόνα[4] από χλώριο με μηχανισμό ελευθέρων ριζών :
Τα α-υδρογόνα των δευτεροταγών ανθράκων αντικαθίστανται ευκολότερα από τα αντίστοιχα των πρωτοταγών.
Παράδειγμα :
- (CH3)2CH-O-CH2CH3 + Cl2 → (CH3)2C(Cl)-O-CH2CH3 + HCl
Διάλυση σε οξέα
Είναι διαλυτοί σε πυκνά οξέα (H2SO4) όπου σχηματίζονται μη απομονώσιμα οξωνικά άλατα :
R2Ο + H2SO4 → R2O+Η HSO4-
Τα οξωνιακά άλατα R2O+Η HSO4- δεν υδρολύονται επειδή το ανιόν HSO4- δεν έχει έντονο πυρηνόφιλο χαρακτήρα.
Η βασικότητα των αιθέρων είναι μεγαλύτερη από των αλκοολών λόγω του αρνητικού επαγωγικού φαινομένου (-Ι) σύμφωνα με το οποίο το ηλεκτρονιακό νέφος μετατοπίζεται διαμέσου των σ-δεσμών από τα ηλεκτροθετικότερα άτομα προς τα ηλεκτραρνητικότερα των αλκυλίων, αυξάνοντας έτσι την ηλεκτρονική πυκνότητα του οξυγόνου. Με οξέα κατά Lewis, όπως το BF3, οι αιθέρες δίνουν σταθερά εσωτερικά οξωνιακά άλατα :
ROR + BF3 → R2O+BF3-
Φωτοξείδωση και σχηματισμός υπεροξειδίων
Οι αιθέρες υφίστανται φωτοξείδωση κατά την έκθεσή τους στο φως (hν) και τον ατμοσφαιρικό αέρα. Η αντίδραση αυτή οδηγεί στο σχηματισμό υπεροξειδίων των αιθέρων, RCH(OOH)OR, που είναι δηλητηριώδη, στερεά και εκρηκτικά σώματα. Ένας αιθέρας μπορεί να περιέχει υπεροξείδια, των οποίων η συγκέντρωση αυξάνεται καθώς ο αιθέρας αποστάζει, οπότε μπορεί να εκραγούν. Οι διεργασίες καθαρισμού γίνονται κυρίως με FeSO4 που ανάγει τα υπεροξείδια σε μη εκρηκτικές αλκοόλες.
Ο μηχανισμός της φωτοξείδωσης είναι ελευθέρων ριζών και τα α-υδρογόνα των δευτεροταγών ατόμων άνθρακα σχηματίζουν υπεροξείδια ευκολότερα από τα αντίστοιχα των πρωτοταγών διότι η σταθερότητα των ελεύθερων ριζών ελαττώνεται κατά τη σειρά R3C. > R2CH. > RCH2. > CH3..

Διάσπαση από υδραλογόνα
Οι αιθέρες αντιδρούν με τα πυκνά υδραλογόνα ΗΧ (Χ = I, Br, Cl) ευκολότερα με ΗΙ, λιγότερο εύκολα με ΗΒr και μόνο όσοι έχουν τριτοταγές αλκύλιο με HCl.
Παράδειγμα :
- CH3-O-CH2CH3 + 2HI → CH3-I + CH3CH2-I
- Όταν η διάσπαση γίνει με περίσσεια ΗΙ ή ΗBr σε υψηλή θερμοκρασία, τότε προκύπτουν τα αντίστοιχα αλκυλαλογονίδια :
- Όταν η διάσπαση γίνει με στοιχειομετρικές ποσότητες ΗΙ ή HBr και σε θερμοκρασίες 0°C - 70°C, προκύπτει μείγμα αλκοόλης και αλκυλαλογονιδίου. Το αλκυλαλογονίδιο σχηματίζεται με το αλκύλιο μικρότερης σχετικής μοριακής μάζας :
Παράδειγμα :
- CH3CH2CH2-O-CH3 + HI → CH3CH2CH2-OH + CH3-I
Το πρώτο στάδιο είναι η πρωτονίωση της αλκοόλης από το οξύ :

Μετά η αντίδραση χωρεί με μηχανισμούς SN1 ή SN2 ανάλογα με τις συνθήκες : Αν το ΗΙ είναι άνυδρο και ο διαλύτης είναι ελάχιστα ή καθόλου πολικός, λειτουργεί ο SN2. Πραγματοποιείται δηλ. πυρηνόφιλη προσβολή από το Χ στον C της απλούστερης αλκυλομάδας αφού αυτός παρουσιάζει τη μικρότερη στερεοχημική παρεμπόδιση από τον C (που ενώνεται με το Ο) του άλλου αλκυλίου που είναι πιο ογκώδες :

Όταν οι αντιδράσεις γίνονται μέσα σε πολικούς διαλύτες (π.χ. υδατικά διαλύματα), τότε χωρούν μέσω σχηματισμού καρβονιόντων και μηχανισμού SN1 :

Πρέπει να τονισθεί το γεγονός ότι οι αλκυλο-αρυλο-αιθέρες δίνουν αλκυλο-ϊωδίδιο και φαινόλη ακόμη και όταν θερμανθούν με περίσσεια ΗΙ :
Επίδραση αλκυλο-λιθίου - Μετάθεση Wittig
Όταν σε έναν αιθέρα με α-υδρογόνα επιδράσει αλκυλο-λίθιο, πραγματοποιείται 1,2-μετάθεση και αλλάζουν θέση μεταξύ τους το α-υδρογόνο με ένα αλκύλιο του αιθέρα με τελικό αποτέλεσμα τη δημιουργία αλκοόλης. Τα αλκύλια που συμμετέχουν στην 1,2-μετάθεση είναι κατά σειρά θερμοδυναμικής σταθερότητας : -C(CH3)3 > -CH(CH3)2 > -CH2CH3 > -CH3.
Ο μηχανισμός είναι :

Όταν ο αιθέρας περιέχει και πολική ομάδα όπως το κυάνιο, -CN, τότε τελικά σχηματίζεται κετόνη :
Ετεροκυκλικοί αιθέρες[Επεξεργασία | επεξεργασία κώδικα]
Οι ετεροκυκλικοί αιθέρες μοιάζουν με τους άκυκλους στη χημική συμπεριφορά, με εξαίρεση το οξιράνιο, το πρώτο μέλος της τάξης των εποξειδίων. Ορισμένες ενδιαφέρουσες αντιδράσεις του :
- Αντιδρά με πυρηνόφιλα αντιδραστήρια οπότε ανοίγει ο τριμελής του δακτύλιος και σχηματίζονται παράγωγα της αιθανόλης. Αντιδρά με ΝΗ3 σχηματίζοντας αιθανολαμίνες :
- Αντιδρά με γλυκόλη (1,2-αιθανοδιόλη, HOCH2CH2OH) παρουσία αραιών ανόργανων οξέων δίνοντας τελικά διοξάνιο που χρησιμοποιείται ως διαλύτης :
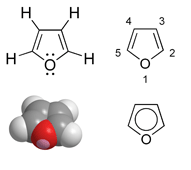
Το φουράνιο μπορεί εύκολα να παρασκευαστεί από ενώσεις που απομονώνονται από το φλοιό της βρώμης και τους σπόρους του καλαμποκιού. Οι σημαντικότερες χρήσεις του είναι ότι μετατρέπεται σε τετραϋδροφουράνιο και σε 1,4-διχλωρο-βενζόλιο. Το 2,3-διϋδρο-4Η-πυράνιο (DHP) αντιδρά με αλκοόλες παρουσία οξέος προς σχηματισμό αλκυλο-τετραϋδροπυρανυλο-αιθέρων (RO-THP). Ένας τέτοιος αιθέρας περιέχει την ομάδα ΤΗΡ που είναι όλο το υπόλοιπο μόριο εκτός του τμήματος RO-. Η ΤΗΡ ομάδα είναι πολύ καλή προστατευτική ομάδα : εύκολα προσκολλάται και εύκολα απομακρύνεται σε μια αντίδραση και μάλιστα κάτω από συνθήκες που δεν επηρεάζουν τις άλλες δραστικές ομάδες στο μόριο :
Πολυμερείς αιθέρες[Επεξεργασία | επεξεργασία κώδικα]
Ορισμένοι ετεροκυκλικοί αιθέρες σε κατάλληλες συνθήκες πολυμερίζονται :
Οι πολυαιθέρες είναι πολυμερή που περιέχουν στην αλυσίδα τους την αιθερομάδα. Μπορούν να παρασκευαστούν με αλυσιδωτό πολυμερισμό π.χ. αλδεϋδών ή κυκλικών αιθέρων, ή με σταδιακό πολυμερισμό π.χ. αυτοσυμπύκνωση διολών :
- n HOCH2CH2CH2OH → —(OCH2CH2CH2)—n + nH2Ο
Ιδιαίτερο ενδιαφέρον παρουσιάζει μια ειδική τάξη πολυαιθέρων, οι εποξειδικές ρητίνες που έχουν μεγάλο εμπορικό ενδιαφέρον γιατί χρησιμοποιούνται ως κόλλες :

Από τους πολυαιθέρες ενδιαφέρον έχουν επίσης και οι πλήρως αρωματικοί που ανήκουν στην τάξη των θερμοσταθερών πολυμερών. Για την παρασκευή τους χρησιμοποιούνται διάφορες μέθοδοι, από τις οποίες μεγαλύτερη σπουδαιότητα παρουσίαζει η οξειδωτική σύζευξη 2,6-δις-υποκατεστημένων φαινολών (π.χ. της 2,6-ξυλενόλης), που έχει αναπτυχθεί και σε βιομηχανική κλίμακα. Με τη μέθοδο αυτή παράγεται το πολυ(φαινυλενοξείδιο), πολυμερές με πολύ καλή θερμική και υδρολυτική σταθερότητα και εξαιρετικές μηχανικές ιδιότητες. Η πολυσυμπύκνωση γίνεται σε θερμοκρασία περιβάλλοντος με τη διοχέτευση ρεύματος οξυγόνου μέσα στο διάλυμα της φαινόλης :
Αιθέρες στέμματα[Επεξεργασία | επεξεργασία κώδικα]


Στη φύση έχουν βρεθεί διάφορα παράγωγα με πολυμελείς οξυγονούχους δακτυλίους, τα μακρολίδια.Ένα τέτοιο μακρολίδιο είναι και η νονακτίνη που έχει 32-μελή δακτύλιο με 8 αιθερικά οξυγόνα. Ανάλογοι πολυαιθέρες έχουν παρασκευαστεί συνθετικά και έχουν την πολύ σημαντική ιδιότητα να σχηματίζουν σταθερά σύμπλοκα με αλκαλιμέταλλα (Na, K). Οι συνθετικοί πολυαιθέρες ονομάζονται αιθέρες-στέμματα και βρίσκουν πολλές εφαρμογές στην Αναλυτική Χημεία και σε διάφορες αντιδράσεις. Περιέχουν αρκετά - τέσσερα, πέντε, έξι ή περισσότερα - άτομα οξυγόνου. Τα ονόματά τους είναι της μορφής Α-στέμμα-Β όπου Α = αριθμός συνολικών ατόμων που αποτελούν το δακτύλιο και Β = τα άτομα Ο στο δακτύλιο. Ο πρώτος που παρασκευάστηκε ήταν ο 16-στέμμα-4 από τον Πέντερσεν (Charles Pedersen)[5] το 1967.
Γενικά οι αιθέρες στέμματα χρησιμοποιούνται ως καταλύτες μεταφοράς φάσης δηλ. χρησιμοποιούνται στη μεταφορά ιοντικών ενώσεων σε μια οργανική φάση είτε από μια υδατική φάση είτε συνήθως από στερεό κρύσταλλο.
Ενδιαφέρον παρουσιάζει ο αιθέρας 18-στέμμα-6 που αποτελείται από 18 άτομα από τα οποία τα 6 είναι οξυγόνα. Έχει τη μεγαλύτερη πυκνότητα (1.237 g/mL) από όλους τους αιθέρες και είναι από τους πιο αποτελεσματικούς και χρησιμοποιούμενους καταλύτες. Όπως φαίνεται και στην εικόνα, προς το εσωτερικό βρίσκονται τα 6 οξυγόνα δημιουργώντας ένα υδρόφιλο περιβάλλον και προς τα έξω οι 12 ομάδες CH2- δημιουργώντας ένα λιπόφιλο περιβάλλον. Στο εσωτερικό χωράει, προσαρμόζεται και προστατεύεται ακριβώς ένα ιόν Κ+ σχηματίζοντας έτσι ένα νέο κατιόν που είναι διαλυτό σε οργανικούς διαλύτες λόγω των εξωτερικών ομάδων CH2-. Το σύμπλεγμα αυτό συνοδεύεται από ένα ανιόν το οποίο προστατεύεται από το θετικό φορτίο του Κ λόγω της ύπαρξης του ογκώδους αιθέρα, σχηματίζοντας έτσι μόνο χαλαρά ιοντικά ζεύγη, με συνέπεια να είναι αρκετά δραστικό.
Τάξεις οργανικών ενώσεων με παραπλήσιες δομές[Επεξεργασία | επεξεργασία κώδικα]

Οι αιθέρες, δεν πρέπει να συγχέονται με τις ακόλουθες τάξεις ενώσεων με την ίδια γενική δομή :
- Αρωματικές ενώσεις όπως το φουράνιο όπου το οξυγόνο είναι μέρος του αρωματικού συστήματος αρωματικών
- Ενώσεις, όπου ένα από τα άτομα άνθρακα δίπλα στο οξυγόνο είναι συνδεδεμένο με το οξυγόνο, άζωτο, ή θείο:
- Εστέρες
- Ημιακετάλες ή α-υδροξυ-αιθέρες
- Ακετάλες ή α-αλκοξυ-αιθέρες
- α-αμινο-αιθέρες
- Ανυδρίτες
Χρήσεις των αιθέρων[Επεξεργασία | επεξεργασία κώδικα]
Οι αιθέρες χρησιμοποιούνται κυρίως ως διαλύτες λιπών, ελαίων, ρητινών κλπ. Επίσης, λόγω της σχετικής τους χημικής αδράνειας, χρησιμοποιούνται ως διαλύτες οργανικών κυρίως ενώσεων οι οποίες είτε δε διαλύονται στο νερό είτε αντιδρούν μ' αυτό δίνοντας ανεπιθύμητα παραπροϊόντα. Χρησιμοποιούνται επίσης για την επίτευξη χαμηλών θερμοκρασιών γιατί με την ταχεία εξάτμισή τους παράγεται ψύχος.
Ο διαιθυλαιθέρας χρησιμοποιείται στην ιατρική ως αναισθητικό.
Το οξιράνιο χρησιμοποιείται ως αποστειρωτικό.
Πολυμερείς αιθέρες, (π.χ. η πολυ-αιθυλενογλυκόλη), χρησιμοποιούνται στην παραγωγή καλλυντικών και φαρμάκων. Άλλοι αιθέρες όπως η ανισόλη χρησιμοποιούνται ως αιθέρια έλαια.
Ο μεθυλο-τριτοταγής-βουτυλ-αιθέρας χρησιμοποιείται ως πρόσθετο βενζίνης.
Ο διμεθυλαιθέρας ως προωθητικό αέριο σε σπρέι.
Η ανηθόλη χρησιμοποιείται ως προσθετικό γεύσης στις τσίχλες και στα αλκοολούχα ποτά με γεύση γλυκάνισου. Επίσης, στη ζαχαροπλαστική γλυκόριζας και στο μέλι, το καρύδι, τη σαρσαπαρίλλα και τις διάφορες γεύσεις καρυκευμάτων. Χρησιμοποιείται επιπλέον για να γλυκάνει τα αρώματα των σαπουνιών και των απορρυπαντικών, στα οικιακά προϊόντα και στα βιομηχανικά αποσμητικά. Συνδυάζεται καλά με αρώματα λουλουδιών και ξύλου.
Η ευγενόλη προσθέτεται σε καλλυντικά, φαρμακευτικά σκευάσματα και οδοντόκρεμες για να δώσει γεύση. Μια παρενέργεια της ευγενόλης είναι ότι λειτουργεί ως παυσίπονο. Έτσι, τα γαρύφαλλα χρησιμοποιούνταν για μεγάλο χρονικό διάστημα ως παυσίπονα για τον πονόδοντο.
Σημειώσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Ορισμένοι συγγραφείς κατατάσσουν στους αιθέρες και ενώσεις που περιέχουν απλά μία τουλάχιστον αιθερική ομάδα, άσχετα με το αν αυτή είναι η κύρια χαρακτηριτική ομάδα της ένωσης ή όχι.
- ↑ Το φαινολικό νάτριο παρασκευάζεται με την αντίδραση : Ph-OH + NaOH Ph-ONa + H2O
- ↑ Παράδειγμα : CH3CH2Cl + NaI → CH3CH2I + NaCl
- ↑ α-υδρογόνα είναι αυτά που ανήκουν σε α-άνθρακα δηλ. σε άνθρακα που ενώνεται απευθείας με το οξυγόνο
- ↑ Ο C. Pedersen (1904-1989) ήταν Αμερικανός οργανικός χημικός που πήρε το βραβείο Nobel Χημείας το 1987 για τις μελέτες του στους αιθέρες στέμματα.
Πηγές[Επεξεργασία | επεξεργασία κώδικα]
- Βάρβογλης Α. "Χημεία Οργανικών Ενώσεων", Θεσσαλονίκη 1986.
- Μανωλκίδης Κ., Μπέζας Κ. "Στοιχεία οργανικής χημείας", Έκδοση 13η, Αθήνα 1985.
- Αλεξάνδρου Ν. Ε. "Γενική Οργανική Χημεία, Δομή-Φάσματα-Μηχανισμοί", Τόμοι 1ος και 2ος, Θεσσαλονίκη 1985.
- Τσακιστράκης Α. "Οργανική Χημεία", Αθήνα 1993
- Morrison R. T., Boyd R. N. "Οργανική Χημεία" Τόμοι 1ος,2ος,3ος, Μετάφραση:Σακαρέλλος-Πηλίδης-Γεροθανάσης, Ιωάννινα 1991.
- Meislich H., Nechamkin H., Sharefkin J. "Οργανική Χημεία", Μετάφραση:Βάρβογλης Α., Αθήνα 1983.
- Ιακώβου Π. "Οργανική Χημεία. Σύγχρονη Θεωρία και Ασκήσεις", Θεσσαλονίκη 1995.
- Τοσσίδης Ι. "Χημεία Ενώσεων Συναρμογής", Θεσσαλονίκη 1986.
- Βασιλικιώτης Γ. Σ. "Χημεία Περιβάλλοντος", Θεσσαλονίκη 1986.
- Μπαζάκης Ι. Α. "Γενική Χημεία", Αθήνα.
Δείτε επίσης[Επεξεργασία | επεξεργασία κώδικα]
Εξωτερικοί σύνδεσμοι[Επεξεργασία | επεξεργασία κώδικα]
- Η ασυνήθιστη ιστορία του διαιθυλαιθέρα
- Ονοματολογία IUPAC των αιθέρων
- Σημεία τήξης αιθέρων
- Σημεία βρασμού αιθέρων
- Πυκνότητες αιθέρων
| |||||||||||||||||||||||














![{\displaystyle {\xrightarrow[{O_{2}}]{CuCl-\pi \upsilon \rho \iota \delta {\acute {\iota }}\nu \eta }}\;}](https://wikimedia.org/api/rest_v1/media/math/render/svg/864ff380cc7535a564f071cd16c847a29f037e14)
