Κυκλοπροπάνιο
| Κυκλοπροπάνιο | |||
|---|---|---|---|
| |||

| |||
| |||

| |||
| Γενικά | |||
| Όνομα IUPAC | Κυκλοπροπάνιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C3H6 | ||
| Μοριακή μάζα | 42,08 amu | ||
| Σύντομος συντακτικός τύπος |
|||
| Αριθμός CAS | 75-19-4 | ||
| SMILES | C1CC1 | ||
| InChI | 1/C3H6/c1-2-3-1/h1-3H2 | ||
| PubChem CID | 6351 | ||
| ChemSpider ID | 6111 | ||
| Δομή | |||
| Είδος δεσμού | C-H: σ(2sp2-1s) | ||
| Πόλωση δεσμού | C--H+: 3% | ||
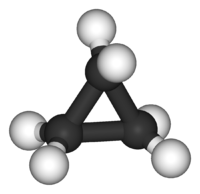
| Μοριακή γεωμετρία | Τα ανθρακοάτομα σε επίπεδη τριγωνική θέση. | ||
| Ισομέρεια | |||
| Ισομερή θέσης | 1 Προπένιο | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -128 °C | ||
| Σημείο βρασμού | -33 °C | ||
| Πυκνότητα | 1,879 kg/m3 (1 atm, 0°C) | ||
| Εμφάνιση | Άχρωμο αέριο | ||
| Χημικές ιδιότητες | |||
| Θερμότητα πλήρους καύσης |
2.088 kJ/mole | ||
| Επικινδυνότητα | |||

| |||
| Εξαιρετικά εύφλεκτο (F+) | |||
| Κίνδυνοι κατά NFPA 704 |
|||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
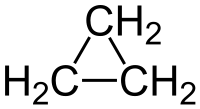
Το κυκλοπροπάνιο (αγγλικά cyclopropane) είναι οργανική χημική ένωση με μοριακό τύπο C3H6, αλλά συνήθως παριστάνεται με το γραμμικό του τύπο, που μοιάζει με ένα ισόπλευρο τρίγωνο (![]() ). Είναι το απλούστερο κυκλοαλκάνιο, δηλαδή κορεσμένος υδρογονάνθρακας με ένα δακτύλιο ανά μόριο. Το μόριό του περιέχει τρία (3) άτομα άνθρακα που σχηματίζουν τριμελή δακτύλιο, καταλήγοντας σε μοριακή συμμετρία D3h. Καθένα από αυτά τα άτομα άνθρακα είναι ενωμένο με δύο (2) άτομα υδρογόνου. Το κυκλοπροπάνιο έχει μόνο ένα (1) (σταθερό) ισομερές θέσης, το προπένιο, αλλά είναι ισομερές και με δύο (2) καρβένια, το 1-προπυλιδένιο (CH3CH2CH:) και το 2-προπυλιδένιο [(CH3)2C:].
). Είναι το απλούστερο κυκλοαλκάνιο, δηλαδή κορεσμένος υδρογονάνθρακας με ένα δακτύλιο ανά μόριο. Το μόριό του περιέχει τρία (3) άτομα άνθρακα που σχηματίζουν τριμελή δακτύλιο, καταλήγοντας σε μοριακή συμμετρία D3h. Καθένα από αυτά τα άτομα άνθρακα είναι ενωμένο με δύο (2) άτομα υδρογόνου. Το κυκλοπροπάνιο έχει μόνο ένα (1) (σταθερό) ισομερές θέσης, το προπένιο, αλλά είναι ισομερές και με δύο (2) καρβένια, το 1-προπυλιδένιο (CH3CH2CH:) και το 2-προπυλιδένιο [(CH3)2C:].
Το κυκλοπροπάνιο έχει ιδιότητες αναισθητικού, όταν εισπνέεται, αλλά στη σύγχρονη αναισθητική πρακτική έχει ξεπεραστεί από άλλα αναισθητικά μέσα, ενώ αποφεύγεται η χρήση του για το σκοπό αυτό, γιατί η εξαιρετική του χημική δραστικότητα το καθιστά επικίνδυνο. Άλλωστε, όταν το αέριο αυτό αναμειγνύεται με οξυγόνο, υπάρχει και ένας σημαντικός κίνδυνος έκρηξης.
Ονοματολογία[Επεξεργασία | επεξεργασία κώδικα]
Η ονομασία «κυκλοπροπάνιο» προέρχεται από την ονοματολογία κατά IUPAC. Συγκεκριμένα, το πρόθεμα της κύριας ονομασίας «προπ-» δηλώνει την παρουσία τριών (3) ατόμων άνθρακα ανά μόριο της ένωσης, το ενδιάμεσο «-αν-» δείχνει την παρουσία μόνο απλών δεσμών μεταξύ ατόμων άνθρακα στο μόριο και η κατάληξη «-ιο» φανερώνει ότι δεν περιέχει χαρακτηριστικές ομάδες, δηλαδή ότι είναι υδρογονάνθρακας. Το αρχικό πρόθεμα «κυκλο-» δηλώνει την παρουσία ενός (1) ισοκυκλικού δακτυλίου στο μόριο της ένωσης.
Ιστορία[Επεξεργασία | επεξεργασία κώδικα]
Το κυκλοπροπανιο ανακαλύφθηκε το 1881, από τον Αυγκούστ Φρέουντ (August Freund), που πρότεινε τη σωστή δομή για τη νέα (τότε) ένωση στις πρώτες κιόλας αναφορές του. Ο Αυγκούστ Φρέουντ επέδρασε νάτριο σε 1,3-διβρωμοπροπάνιο. Η χημική αντίδραση που ακολούθησε είναι μια ενδομοριακή αντίδραση Βουρτζ (Wurtz reaction), που οδηγεί απευθείας σε κυκλοπροπάνιο[1][2]. Η απόδοση της αντίδρασης μπορεί να βελτιωθεί με τη χρήση ψευδαργύρου αντί νατρίου[3]. Το κυκλοπροπάνιο δεν είχε εμπορική εφαρμογή μέχρι που οι Χέντερσον (Henderson) και Λούκας (Lucas) ανακάλυψαν τις αναισθητικές του ιδιότητες το 1929[4]. Η βιομηχανική του παραγωγή άρχισε από το 1936[5].
Δομή[Επεξεργασία | επεξεργασία κώδικα]


Η ισόπλευρη τριγωνική δομή του κυκλοπροπανίου απαιτεί οι δεσμικές γωνίες C-C-C να είναι 60°. Η γωνία αυτή είναι πολύ μικρότερη από την πλέον σταθερή, θερμοδυναμικά, δεσμική γωνία των περίπου 109.5°, των δεσμών σ μεταξύ υβριδικών τροχιακών sp³-sp³. Αυτό οδηγεί στην ύπαρξη σημαντικής παραμόρφωσης δακτυλίου. Το μόριο έχει επίσης και παραμόρφωση στρέψης, εξαιτίας της εκλειπτικής διαμόρφωσης των ατόμων υδρογόνου του. Για τους παραπάνω λόγους, οι χημικοί δεσμοί μεταξύ των ατόμων άνθρακα του κυκλοπροπανίου είναι σχετικά ασθενέστεροι από τους τυπικούς δεσμούς C-C ενός τυπικού αλκανίου, οδηγώντας σε πολύ μεγαλύτερη χημική δραστικότητα (σε σύγκριση με τα αλκάνια).
Η δεσμολογία μεταξύ των ατόμων άνθρακα γενικά περιγράφεται με τους όρους των δεσμών με κάμψη (bent bonds)[6]. Σύμφωνα με αυτό το μοντέλο, οι δεσμοί άνθρακα - άνθρακα στο κυκλοπροπάνιο κάμπτονται έτσι ώστε να σχηματίζεται μια ενδοτροχιακή γωνία των 104°. Αυτό ελαττώνει το επίπεδο της παραμόρφωσης δακτυλίου στρεβλώνοντας τον sp3 υβριδισμό των ατόμων άνθρακα έτσι ώστε να έχουν μεγαλύτερο π χαρακτήρα από το κανονικό[7], ενώ από την άλλη οι δεσμοί άνθρακα - υδρογόνου αποκτούν μεγαλύτερο σ χαρακτήρα, από το κανονικό. Μια ασυνήθιστη συνέπεια της δεσμολογίας με κάμψη είναι ότι ενώ οι δεσμοί C-C, είναι ασθενέστεροι από το κανονικό, τα άτομα άνθρακα βρίσκονται κοντύτερα το ένα με το άλλο, σε σύγκριση με έναν κανονικό απλό δεσμό αλκανίων: Πιο συγκεκριμένα, βρίσκονται σε απόσταση 151 pm αντί για το κανονικό που είναι 153 pm. Λάβετε υπόψη, ακόμη, ότι ο μέσος όρος για τα αλκένια είναι 146 pm[8].
Ένα εναλλακτικό μοντέλο περιγραφής της δεσμολογίας του κυκλοπροπανίου περιλαμβάνει διαγράμματα Γουάλς (Walsh diagrams) και στοχεύει να κάνει καλύτερη δουλειά ώστε να ταιριάζει η θεωρία μοριακών τροχιακών, υπό το φως των φασματοσκοπικών ενδείξεων και των επιχειρημάτων της συμμετρίας ομάδας. Σε αυτό το μοντέλο, το μόριο του κυκλοπροπάνιο περιγράφεται με τη χρήση δεσμικού τροχιακού συνδυασμού τριών κέντρων τριών (3) καρβενίων μεθυλενίου.
Ο κυκλικός απεντοπισμός των έξι (6) ηλεκτρονίων των τριών (3) C-C σ δεσμών δόθηκε από τον Μάικλ Ντιούαρ (Michael J. S. Dewar) ως μια εξήγηση της σχετικά μικρή ενέργεια παραμόρφωσης, σε σύγκριση με την αντίστοιχη του κυκλοβουτανίου (μόνο 27,6 έναντι 26,2 kcal/mol), με το κυκλοεξάνιο ως ένωση αναφοράς με Estr = 0 kcal/mol[9]. Αυτή η (σχετική) σταθεροποίηση αναφέρεται ως «αρωματικότητα σ»[10][11]. Η παραδοχή ενός διαμαγνητικού δακτυλικού ρεύματος στο κυκλοπροπάνιο ευθυγραμμίζεται με την «προστασία» των πρωτονίων στη φασματοσκοπία πυρηνικού μαγνητικού συντονισμού και στις ασυνήθιστες μαγνητικές ιδιότητες του κυκλοπροπανίου, που περιλαμβάνουν υψηλή διαμαγνητική ευαισθησία και υψηλή ανισοτροπία της διαμαγνητικής ευαισθησίας. Πιο πρόσφατες έρευνες που ενισχύουν την υπόθεση ότι το κυκλοπροπάνιο σταθεροποιείται από μια αρωματικότητα αποδίδουν μια σταθεροποίηση της τάξης των 11,3 kcal/mol από αυτό το φαινόμενο[12].
Ύστερα από ενεργειακή ανάλυση των πιθανών δομών - μοριακών μοντέλων με κβαντομηχανικές μεθόδους προέκυψε ως πιθανότερη η εκδοχή του sp2 υβριδισμού και της δημιουργίας δύο μοριακών τροχιακών τριών κέντρων (των τριών ατόμων C), σ (2sp2-2sp2-2sp2) και π (2p-2p-2p), με 3 ηλεκτρόνια ανά μοριακό τροχιακό, ώστε να χρησιμοποιηθούν τα 6 διαθέσιμα ηλεκτρόνια των 3 ατόμων C (τα άλλα 6 χρησιμοποιούνται για τους 6 σ δεσμούς με τα 6 άτομα υδρογόνου ή και με τα αλκύλια). Αντί δηλαδή των κλασσικών 3 ομοιοπολικών δεσμών δύο κέντρων μεταξύ των ατόμων C, υπάρχουν 2 ομοιοπολικοί δεσμοί τριών κέντρων[13].
Εξαιτίας αυτού του γεγονότος προκύπτει η λεγόμενη «ενέργεια τάσης δεσμών» που συνυπολογίζει την ενέργεια παραμόρφωσης δεσμικής γωνίας (κατά Baeyer), που οφείλεται στη διαφορά γωνίας από την κανονική, και την ενέργεια στρέψης (κατά Piltzer), που οφείλεται στην αδυναμία του συστήματος να στρέψει τους δεσμούς του και να πάρει διαμόρφωση αποφυγής των απώσεων τύπου Van der Waals, που αναπτύσσονται από την προσέγγιση αλληλαπωθούμενων ατόμων και ομάδων αυτών. Ενώ λοιπόν το ισομερές προπένιο έχει θερμότητα ολικής καύσης 1.971 kcal/mole το κυκλοπροπάνιο έχει 2.088 kcal/mole. Το ΔQ = 117 kJ/mole αντιστοιχεί ακριβώς στην επιπλέον ενέργεια που παγιδεύει η ιδιάζουσα δομή του τριμελή δακτυλίου[14].
Αποτέλεσμα των παραπάνω είναι τα κυκλοπροπάνια να δίνουν αντιδράσεις 1,3-κυκλοπροσθήκης.
| Δεσμοί[15] | ||||
| Δεσμός | τύπος δεσμού | ηλεκτρονική δομή | Μήκος δεσμού | Ιονισμός |
|---|---|---|---|---|
| C-H | σ | 2sp²-1s | 108,7 pm | 3% C- H+ |
| C-C-C | σ τριών ηλεκτρονίων και τριών κέντρων | 2sp²-2sp²-2sp² | 151 pm (C-C) | |
| C-C-C | π τριών ηλεκτρονίων και τριών κέντρων | 2p-2p-2p | 151 pm (C-C) | |
| Κατανομή φορτίων σε ουδέτερο μόριο | ||||
| C | -0,06 | |||
| H | +0,03 | |||
Κυκλοπροπάνια[Επεξεργασία | επεξεργασία κώδικα]
Τα «Κυκλοπροπάνια» είναι κατηγορία οργανικών ενώσεων. Η κατηγορία περιλαμβάνει το «μητρικό» κυκλοπροπάνιο καθώς αλλά και όλες τις «θυγατρικές» ενώσεις που περιέχουν έναν τουλάχιστον τριμελή δακτύλιο κυκλοπροπανίου. Οι πλευρικές αλυσίδες, όταν υπάρχουν, διαμορφώνονται όπως στα αλκάνια. Η δομή του κυκλοπροπανικού δακτυλίου περιγράφεται παραπάνω. Η απλούστερη πολυκυκλική ένωση που περιέχει πολλαπλούς συμπυκνωμένους δακτυλίους πολυπροπανίου είναι το τετραεδράνιο, που το μόριό του αποτελείται από τέσσερις (4) κυκλοπροπανικούς δακτυλίους που σχηματίζουν τις έδρες ενός τετραέδρου. Ακόμη, το [1.1.1]-προπελάνιο περιέχει τρεις (3) κυκλοπροπανικούς δακτυλίους που μοιράζονται ένα κοινό κεντρικό ζεύγος ατόμων άνθρακα και το δεσμό τους.
-
[1.1.1]-προπελάνιο
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
Ενδομοριακή αντίδραση Würz[Επεξεργασία | επεξεργασία κώδικα]
Ιστορικά πρωτοπαρασκευάστηκε από τον August Freund το 1881 με τη χρήση ενδομοριακής αντίδρασης Würtz, από 1,3-διβρωμοπροπάνιο[16][17]
- Όμως η απόδοση αυτής της αντίδρασης είναι σχετικά μικρή, αφού ταυτόχρονα διεξάγεται αναπόφευκτα και διαμοριακή[18]:
- Σήμερα χρησιμοποιείται περισσότερο η τροποποιημένη αντίδραση Freund με Zn, που δίνει μεγαλύτερη απόδοση στην ενδομοριακή αντίδραση. Σ' αυτήν την περίπτωση η στοιχειομετρική εξίσωση της αντίδρασης γίνεται[19][20]:
Αιθένιο και μεθυλένιο[Επεξεργασία | επεξεργασία κώδικα]
Λόγω της τάσης χρήσης του αιθενίου ως κεντρική πρώτη ύλη της οργανικής χημείας, επικράτησε περισσότερο η προσθήκη του κατάλληλου καρβενίου σ' αυτό, δηλαδή του μεθυλενίου, που παράγεται επί τόπου από CH3Cl και KOH. Η στοιχειομετρική εξίσωση της αντίδρασης είναι[21]:
- Επειδή η αντίδραση αυτή δίνει και προϊόν παρεμβολής (~80%) προπένιο, χρησιμοποιείται η ακόλουθη που δίνει (σχεδόν) αποκλειστικά κυκλοπροπάνιο[22]:
Χημικές ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
- Τα κυκλοαλκάνια με τριμελή δακτύλιο (δηλαδή τα «κυκλοπροπάνια») έχουν αρκετή ενέργεια τάσης δεσμών για να δώσουν 1,3-κυκλοπροσθήκη, αλλά κάτω από πιο έντονες συνθήκες και με μικρότερη ταχύτητα αντίδρασης σε σχέση με τα αλκένια. Κατά τα άλλα συμπεριφέρονται χημικά όπως τα αλκάνια[23]:
- Ο όρος «κυκλοπροσθήκη» σημαίνει διάσπαση δακτυλίου και προσθήκη στα άκρα της αλυσίδας που προκύπτει.
Οξείδωση[Επεξεργασία | επεξεργασία κώδικα]
1. Όπως όλα τα κυκλοαλκάνια, το κυκλοπροπάνιο με περίσσεια οξυγόνου καίγεται προς διοξείδιο του άνθρακα και νερό[24][25]:
2. Παραγωγή υδραερίου:
3. Καταλυτική οξείδωση:
- 1. Χωρίς κυκλοπροσθήκη προς κυκλοπροπανόνη:
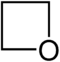
- 2. Με πιο έντονες συνθήκες δίνει 1,3-κυκλοπροσθήκη, σχηματίζοντας οξετάνιο:
Αλογόνωση[Επεξεργασία | επεξεργασία κώδικα]
1. Φωτοχημική αλογόνωση υποκατάστασης υδρογόνου: Το κυκλοπροπάνιο έχει 6 ισότιμα, άτομα υδρογόνου, που μπορούν να χρησιμοποιηθούν για φωτοχημική αντικατάσταση από αλογόνα, οπότε προκύπτει ένα μόνο κυκλοπροπυλαλογονίδιο[29]:
- Δραστικότητα των X2: F2 > Cl2 > Br2 > Ι2.
Ανάλυση του μηχανισμού της χλωρίωσης του κυκλοπροπανίου:
- 1. Έναρξη: Παράγονται ελεύθερες ρίζες:
- Η απαιτούμενη ενέργεια προέρχεται από το υπεριώδες φως (UV) ή θερμότητα (Δ).
- 2. Διάδοση: Καταναλώνονται οι παλιές ελεύθερες ρίζες, σχηματίζοντας νέες.
- 3. Τερματισμός: Καταναλώνονται μεταξύ τους οι ελεύθερες ρίζες, κατά τη στατιστικά σπάνια περίπτωση της συνάντησής τους.
- Είναι όμως πρακτικά δύσκολο να σταματήσει η αντίδραση στην παραγωγή μονοαλογονοπαραγώγων.
- Αν χρησιμοποιηθούν ισομοριακές ποσότητες
 και Χ2 θα παραχθεί μίγμα όλων των X-παραγώγων του
και Χ2 θα παραχθεί μίγμα όλων των X-παραγώγων του 
- Αν όμως χρησιμοποιηθει περίσσεια
 , τότε η απόδοση τωμ μονοπαραγώγων αυξάνεται πολύ, λόγω της αύξησης της στατιστική πιθανότητας συνάντισης
, τότε η απόδοση τωμ μονοπαραγώγων αυξάνεται πολύ, λόγω της αύξησης της στατιστική πιθανότητας συνάντισης  με X. σε σχέση με την πιθανότητα συνάντισης μονοπαραγώγου και X., που μπορεί να οδηγήσει στην παραγωγή των υπόλοιπων X-παραγώγων.
με X. σε σχέση με την πιθανότητα συνάντισης μονοπαραγώγου και X., που μπορεί να οδηγήσει στην παραγωγή των υπόλοιπων X-παραγώγων.
- Αν χρησιμοποιηθούν ισομοριακές ποσότητες
2. Με 1,3-κυκλοπροσθήκη παράγεται 1,3-διαλοπροπάνιο:
Επίδραση καρβενίων[Επεξεργασία | επεξεργασία κώδικα]
- Το κυκλοπροπάνιο έχει 6 ισότιμα, για παρεμβολή καρβενίων, άτομα υδρογόνου, οπότε προκύπτει ένα μόνο προϊόν. Π.χ. με επίδρση μεθυλενίου παράγεται μεθυλοκυκλοπροπάνιο[31]:
Νίτρωση[Επεξεργασία | επεξεργασία κώδικα]
Καταλυτική 1,3-υδρογόνωση[Επεξεργασία | επεξεργασία κώδικα]
Με καταλυτική υδρογόνωση - Παράγεται προπάνιο[33]:
1,3-υδραλογόνωση[Επεξεργασία | επεξεργασία κώδικα]
Με υδραλογόνο (ΗΧ) - Παράγεται προπυλοαλογονίδιο:
1,3-Υδροξυαλογόνωση[Επεξεργασία | επεξεργασία κώδικα]
Με υπαλογονώδες οξύ (HOX) - Παράγεται 3-αλο-1-προπανόλη:
1,3-ενυδάτωση[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση θειικού οξέως σε κυκλοπροπάνιo παράγεται ο μονοπροπυλεστέρας του θειικού οξέος, που υδρολύεται σχηματίζοντας 1-προπανόλη:
1,3-διυδροξυλίωση[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση υπεροξείδιο του υδρογόνου σε κυκλοπροπάνιo, παρουσία καρβονικών οξέων παράγεται 1,3-προπανoδιόλη:
Εφαρμογή ως αναισθητικό[Επεξεργασία | επεξεργασία κώδικα]
Το κυκλοπροπάνιο χρησιμοποιήθηκε για πρώτη φορά σε κλινική χρήση από τον Αμερικανό αναισθησιολόγο Ραλφ Γουάτερς (Ralph Waters), που χρησιμοποίησε ένα κλειστό σύστημα με απορρόφηση διοξειδίου του άνθρακα για να τη φύλαξη αυτού του ακριβού (τότε) μέσου. Το κυκλοπροπάνιο είναι ένα σχετικά ισχυρό, μη ερεθιστικό και με γλυκιά οσμή αέριο (υπό συνηθισμένες συνθήκες) με ελάχιστη κυψελιδική συγκέντρωση 17,5%[34] και συντελεστή κατανομής αερίων αίματος 0,55. Αυτό σημαίνει ότι η αναισθησία με εισπνοή κυκλοπροπανίου και οξυγόνου είναι γρήγορη και όχι δυσάρεστη. Ωστόσο το συμπέρασμα από την παρατεταμένη αναισθησία ασθενών, που υποβλήθηκαν σε αναισθησία από κυκλοπρπάνιο, ήταν ότι μπορεί να υπέφεραν από ξαφνική μείωση της πίεσης αίματος, που μπορούσε να οδηγήσει σε καρδιακή δυσρυθμία, μια αντίδραση που έγινε γνωστή ως «σοκ κυκλοπροπανίου» (cyclopropane shock)[35]. Για το λόγο αυτό, αλλά και εξαιτίας του υψηλού του οικονομικού κόστους και της εκρηκτικής του φύσης[36], πρόσφατα χρησιμοποιούνταν μόνο για την επαγωγή της αναισθησίας, πριν σταματήσει τελείως η χρήση του ως αναισθητικό. Οι κύλινδροι και μετρητές ροής είχαν ένα ενδεικτικό πορτοκαλί χρώμα.
Φαρμακολογία[Επεξεργασία | επεξεργασία κώδικα]
Το κυκλοπροπάνιο είναι ανενερό για τους υποδοχείς GABAA και γλυκίνης, αλλά δρα σε έναν ανταγωνιστικό υποδοχέα NMDA[37][38]. Επίσης, εμποδίζει τον υποδοχέα AMPA και τους υποδοχείς νικοτινικής ακετυλοχολίνης, και ενεργοποιεί αρκετά κανάλια K2P[39][37][38]
Ασφάλεια[Επεξεργασία | επεξεργασία κώδικα]
Το κυκλοπροπάνιο είναι πολύ εύφλεκτο. Ωστόσο, παρά την ενέργεια παραμόρφωσής του, δεν είναι πιο εκρηκτικό σε σύγκριση με τα αλκάνια.
Πηγές[Επεξεργασία | επεξεργασία κώδικα]
- Ν. Αλεξάνδρου, Γενική Οργανική Χημεία, ΘΕΣΣΑΛΟΝΙΚΗ 1985
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
Αναφορές και παρατηρήσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ August Freund (1881). "Über Trimethylen". Journal für Praktische Chemie 26 (1): 625–635. doi:10.1002/prac.18820260125
- ↑ August Freund (1882). "Über Trimethylen". Monatshefte für Chemie 3 (1): 625–635. doi:10.1007/BF01516828.
- ↑ G. Gustavson (1887). "Ueber eine neue Darstellungsmethode des Trimethylens". J. Prakt. Chem. 36: 300–305. doi:10.1002/prac.18870360127.
- ↑ G. H. W. Lucas and V. E. Henderson (1 August 1929). "A New Anesthetic: Cyclopropane : A Preliminary Report". Can Med Assoc J. 21 (2): 173–5. PMC 1710967. PMID 20317448.
- ↑ H. B. Hass, E. T. McBee, and G. E. Hinds (1936). "Synthesis of Cyclopropane". Industrial & Engineering Chemistry 28 (10): 1178–81. doi:10.1021/ie50322a013.
- ↑ Eric V. Anslyn and Dennis A. Dougherty. Modern Physical Organic Chemistry. 2006. pages 850-852
- ↑ Knipe, edited by A.C. (2007). March's advanced organic chemistry reactions, mechanisms, and structure. (6th ed. ed.). Hoboken, N.J.: Wiley-Interscience. p. 219. ISBN 0470084944.
- ↑ Allen, Frank H.; Kennard, Olga; Watson, David G.; Brammer, Lee; Orpen, A. Guy; Taylor, Robin (1987). "Tables of bond lengths determined by X-ray and neutron diffraction. Part 1. Bond lengths in organic compounds". Journal of the Chemical Society, Perkin Transactions 2 (12): S1–S19. doi:10.1039/P298700000S1.
- ↑ S. W. Benson, Themochemical Kinetics, S. 273, J. Wiley & Sons, New York, London, Sydney, Toronto 1976
- ↑ M. J. Dewar. Chemical Implicatons of σ Conjugation. In: J. Am. Chem. Soc., 1984, 106, p. 669-682.
- ↑ D. Cremer.Pros and Cons of σ-Aromaticity. In: Tetrahedron, 1988, 44 (2), p. 7427-7454.
- ↑ Kai Exner and Paul von Ragué Schleyer. Theoretical Bond Energies: A Critical Evaluation. In: J. Phys. Chem. A, 2001, 105 (13), Seiten 3407–3416. doi:10.1021/jp004193o.
- ↑ Ν. Αλεξάνδρου, Γενική Οργανική Χημεία, ΘΕΣΣΑΛΟΝΙΚΗ 1985: Σελ.127-128, §6.2.
- ↑ Ν. Αλεξάνδρου, Γενική Οργανική Χημεία, ΘΕΣΣΑΛΟΝΙΚΗ 1985, Σελ. 125-126, §6.1.
- ↑ Τα δεδομένα προέρχονται εν μέρει από το «Table of periodic properties of thw Ellements», Sagrent-Welch Scientidic Company και Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, Σελ. 34.. Ο πίνακας αντιστοιχεί στην τελευταία προτινόμενη δομή.
- ↑ August Freund (1881). "Über Trimethylen". Journal für Praktische Chemie 26 (1): 625–635. doi:10.1002/prac.18820260125.
- ↑ August Freund (1882). "Über Trimethylen". Monatshefte für Chemie 3 (1): 625–635. doi:10.1007/BF01516828.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 152, §6.2.2.
- ↑ G. Gustavson (1887). "Ueber eine neue Darstellungsmethode des Trimethylens". J. Prakt. Chem. 36: 300–305. doi:10.1002/prac.18870360127. http://gallica.bnf.fr/ark:/12148/bpt6k90799n/f308.table.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 154, §6.5.Β1.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 154, §6.5.Β2 και 157, §6.8.7.
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, σελ. 138, §9.2Β5β.
- ↑ Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991, σελ.24, §1.2.
- ↑ Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991, σελ.21, §1.1.
- ↑ Ν. Αλεξάνδρου, Γενική Οργανική Χημεία, ΘΕΣΣΑΛΟΝΙΚΗ 1985: Σελ.126, 6.1.
- ↑ ΔHC-C= +347 kJ/mol
- ↑ ΔHC-H = +415 kJ/mol
- ↑ ΔHO-O=+146 kJ/mol
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, σελ. 43-46 §4.4.3.
- ↑ καθοριστικό ταχύτητας
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, σελ. 46 §4.4.4.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ. 244, §10.3.2.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 160, §6.11.
- ↑ Eger, Edmond I.; Brandstater, Bernard; Saidman, Lawrence J.; Regan, Michael J.; Severinghaus, John W.; Munson, Edwin S. (1965). "Equipotent Alveolar Concentrations of Methoxyflurane, Halothane, Diethyl Ether, Fluroxene, Cyclopropane, Xenon and Nitrous Oxide in the Dog". Anesthesiology 26 (6): 771–777. doi:10.1097/00000542-196511000-00012.
- ↑ JOHNSTONE, M; Alberts, JR (July 1950). "Cyclopropane anesthesia and ventricular arrhythmias.". British heart journal 12 (3): 239–44. doi:10.1136/hrt.12.3.239. PMID 15426685.
- ↑ MacDonald, AG (June 1994). "A short history of fires and explosions caused by anaesthetic agents.". British journal of anaesthesia 72 (6): 710–22. doi:10.1093/bja/72.6.710. PMID 8024925.
- ↑ 37,0 37,1 Hugh C. Hemmings; Philip M. Hopkins (2006). Foundations of Anesthesia: Basic Sciences for Clinical Practice. Elsevier Health Sciences. pp. 292–. ISBN 0-323-03707-0.
- ↑ 38,0 38,1 Hemmings, Hugh C. (2009). "Molecular Targets of General Anesthetics in the Nervous System". pp. 11–31. doi:10.1007/978-1-60761-462-3_2.
- ↑ Hara K, Eger EI, Laster MJ, Harris RA (December 2002). "Nonhalogenated alkanes cyclopropane and butane affect neurotransmitter-gated ion channel and G-protein-coupled receptors: differential actions on GABAA and glycine receptors". Anesthesiology 97 (6): 1512–20. PMID 12459679.



![[1.1.1]-προπελάνιο](http://upload.wikimedia.org/wikipedia/commons/thumb/7/79/1.1.1-propellane.svg/102px-1.1.1-propellane.svg.png)






![{\displaystyle \mathrm {+3H_{2}O{\xrightarrow[{700-1100^{o}C}]{Ni}}3CO+6H_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/4092ba3a99c06c6660e229ed6517eb6aa67c6ac2)
![{\displaystyle \mathrm {+O_{2}{\xrightarrow[{\triangle }]{Cu}}H_{2}O+} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/5ad0e766c90ff9dd6d78efd9e1c5ab564423ca9e)
![{\displaystyle \mathrm {+{\frac {1}{2}}O_{2}{\xrightarrow[{1-2MPa,\;280^{o}C}]{Ag}}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/d7c6afaa463770e8f338d24528e88bab69cf21d9)
![{\displaystyle \mathrm {+X_{2}{\xrightarrow[{\triangle }]{UV}}HX+} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/32d971c77e4c7bf3933a6b8058fff314dd3f149a)
![{\displaystyle \mathrm {Cl_{2}{\xrightarrow[{\triangle }]{UV}}2Cl^{\bullet }-239kJ} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/73fe9c8e7397e9e50d5b5a7ea91a25e26bed2f96)















![{\displaystyle \mathrm {+H_{2}SO_{4}{\xrightarrow {}}CH_{3}CH_{2}CH_{2}OSO_{3}H{\xrightarrow[{-H_{2}SO_{4}}]{+H_{2}O}}CH_{3}CH_{2}CH_{2}OH} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/c7eb661ef73415051303afa182b8fab34848af08)
