Καρβοξυλικά οξέα
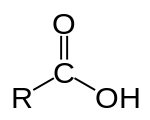



Τα καρβοξυλικά οξέα ή καρβονικά οξέα είναι οργανικά οξέα που χαρακτηρίζονται από την παρουσία μιας τουλάχιστον χαρακτηριστικής ομάδας καρβοξυλίου ή καρβοξυλομάδας, που συμβολίζεται: -CO2H, -COOH ή -C(=O)OH[1]. Ο γενικός τύπος τους είναι RCOOH, όπου R υδρογόνο ή κάποια άλλη μονοσθενής ρίζα. Η χαρακτηριστική καρβοξυλομάδα είναι μια σύνθετη ομάδα που αποτελείται από την παρουσία ενός καρβονυλίου (>C=O) και μιας υδροξυλομάδας (-ΟΗ) ενωμένης στο άτομο άνθρακα του καρβονυλίου[2].
Τα καρβοξυλικά οξέα είναι οξέα κατά Brønsted-Lowry, δηλαδή δότες πρωτονίων. Είναι ο πιο συνηθισμένος τύπος οργανικών οξέων. Τα απλούστερα από αυτά είναι το μεθανικό οξύ (HCOOH) και το αιθανικό οξύ (CH3COOH). Υπάρχουν καρβοξυλικά οξέα με δύο (2) καρβοξυλομάδες (δικαρβοξυλικά οξέα, από τα οποία το απλούστερο είναι το οξαλικό οξύ (HOOCCOOH), με τρεις καρβοξυλομάδες (τρικαρβοξυλικά οξέα, από τα οποία το απλούστερο είναι το καρβοξυπροπανοδιικό οξύ (CH(COOH)3), κ.τ.λ.. Το μηλιτικό οξύ (C6(COOH)6) είναι ένα παράδειγμα εξακαρβοξυλικού οξέος. Άλλα σημαντικά παραδείγματα φυσικών καρβοξυλικών οξέων είναι το κιτρικό οξύ (HOOCCH2C(OH)(COOH)CH2COOH) (το χαρακτηριστικό οξύ των λεμονιών) και το τρυγικό οξύ (ΗΟΟOCCH(OH)CH(OH)COOH) (που βρίσκεται στους ταμάρινδους).
Τα άλατα και οι εστέρες των καρβοξυλικών οξέων ονομάζονται καρβοξυλικά άλατα και καρβοξυλικοί εστέρες, αντίστοιχα. Όταν ένα καρβοξυλικό οξύ αποπρωτονιώνεται σχηματίζεται μια «συζυγής βάση», το καρβοξυλικό ανιόν. Τα ανιόντα αυτά σταθεροποιούνται σημαντικά, και ακριβώς αυτή η αυξημένη σταθερότητα, κάνει τα καρβοξυλικά οξέα πιο ισχυρά οξέα από τις αντίστοιχες αλκοόλες. Τα καρβοξυλικά οξέα μπορούν να θεωρηθούν αναγμένες ή αλκυλιωμένες μορφές του ανθρακικού οξέος, που είναι η ένυδρη μορφή του διοξείδιο του άνθρακα (CO2) και πράγματι, κάτω από ορισμένες συνθήκες, δίνουν αντιδράσεις αποκαρβοξυλίωσης, από τις οποίες εκλύεται διοξείδιο του άνθρακα.
Ταξινόμηση[Επεξεργασία | επεξεργασία κώδικα]
Μερικές από τις ταξινομήσεις τους είναι οι ακόλουθες:
1. Ως προς τον αριθμό των ομάδων COOH που διαθέτουν:
- Μονοκαρβοξυλικά οξέα: Διαθέτουν μία (1) ομάδα -CΟΟΗ. Π.χ. οξικό οξύ (CH3COOH).
- Δικαρβοξυλικά οξέα: Διαθέτουν δύο (2) ομάδες -COOH. Π.χ. οξαλικό οξύ (HCOOCOOH).
- Πολυκαρβοξυλικά οξέα: Διαθέτουν τρεις (3) ή περισσότερες ομάδες -CΟΟΗ. Π.χ. κιτρικό οξύ [HOOCCH2C(OH)(COOH)CH2COOH].
2. Ως προς την παρουσία κατώτερων χαρακτηριστικών ομάδων. Π.χ.:
- Σουλφοξυοξέα: Διαθέτουν μία (1) τουλάχιστον σουλφοξυομάδα. Π.χ. σουλφοξυαιθανικό οξύ (HSO3CH2COOH).
- Κυανοξέα: Διαθέτουν μία (1) τουλάχιστον κυανομάδα. Π.χ. κυανοαιθανικό οξύ (NCCH2COOH).
- Φορμυλοξέα: Διαθέτουν μία (1) τουλάχιστον φορμυλομάδα. Π.χ. φορμυλοαιθανικό οξύ (HCOCH2COOH).
- Οξοξέα: Διαθέτουν μία (1) τουλάχιστον οξομάδα. Π.χ. πυροσταφυλικό οξύ (CH3COCOOH).
- Υδροξυοξέα: Διαθέτουν μία (1) τουλάχιστον υδροξυομάδα. Π.χ. γαλακτικό οξύ [CH3CΗ(OH)COOH].
- Υδροθειοξέα: Διαθέτουν μία (1) τουλάχιστον υδροθειομάδα. Π.χ. θειογαλακτικό οξύ [CH3CΗ(SH)COOH].
- Αμινοξέα: Διαθέτουν μία (1) τουλάχιστον αμινομάδα. Π.χ. αλανίνη [CH3CH(NH2COOH).
- Ιμινοξέα: Διαθέτουν μία (1) τουλάχιστον ιμινομάδα. ιμιναιθανικό οξύ [HN=CHCOOH).
- Αλκοξυοξέα: Διαθέτουν μία (1) τουλάχιστον αλκοξυομάδα. μεθοξυαιθανικό οξύ [CH3OCH2COOH).
- Αλκοθειόξέα: Διαθέτουν μία (1) τουλάχιστον αλκοθειομάδα. μεθυλοθειαιθανικό οξύ [CH3SCH2COOH).
3. Ως προς το είδος της ανθρακικής αλυσίδας τους:
- Αλειφατικά καρβοξυλικά οξέα: Η ένωση δεν περιέχει κανένα δακτύλιο. Π.χ. οξικό οξύ (CH3COOH).
- Ισοκυκλικά καρβοξυλικά οξέα: Η ένωση περιέχει έναν τουλάχιστον δακτύλιο χωρίς ετεροάτομα. Π.χ. κυκλοεξυλκαρβονικό οξύ (
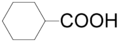 )
) - Αρωματικά καρβοξυλικά οξέα: Η ένωση περιέχει έναν τουλάχιστον δακτύλιο με αρωματικό χαρακτήρα. Π.χ. βενζοϊκό οξύ (PhCOOH)
- Αντιαρωματικά καρβοξυλικά οξέα Η ένωση περιέχει έναν τουλάχιστον δακτύλιο με αντιαρωματικό χαρακτήρα. Π.χ. κυκλοβουταδιενυλομεθανικό οξύ.
- Ετεροκυκλικά καρβοξυλικά οξέα: Η ένωση περιέχει έναν τουλάχιστον δακτύλιο με ετεροάτομα. Π.χ καρβοξυλιράνιο (
 ).
).
Ονοματολογία[Επεξεργασία | επεξεργασία κώδικα]
Η κατά IUPAC ονοματολογία των μονοκαρβονικών οξέων γίνεται όπως στους υδρογονάνθρακες με την προσθήκη της ατάληξης «-ικό οξύ» ή «-οϊκό οξύ» αντί του «-ιο» [π.χ. προπανικό οξύ (CH3CH2COOH) αντί προπάνιο (CH3CH2CH3)]. Στα δικαρβονικά οξέα η κατάληξη γίνεται «-διικό οξύ» [π.χ. προπανοδιικό οξύ) (HOOCCH2COOH). Στα πολυκαρβονικά οξέα τα επιπλέον καρβοξύλια μπαίνουν ως υποκαταστάτες {π.χ. καρβοξυπροπανοδιικό οξύ) [HOOCCH(COOH)COOH]}.
- Τα μέχρι δύο (2) ακραία καρβοξύλια μετράνε στην αρίθμηση των ατόμων άνθρακα της κύριας ανθρακικής αλυσίδας.
- Οι υποκαταστάτες, όταν είναι μόνο ένας μεριούνται συχνά με το σύστημα α-, β-, γ-,... αντί 2-, 3-, 4-,...
- Σε πολύπλοκες ενώσεις είναι δυνατό και όλα τα καρβοξύλια να προτάσσονται ως υποκαταστάτες.
Τα παρακάτω καρβονικά οξέα είναι περισσότερο γνωστά με τις εμπειρικές τους ονομασίες, καθώς η χρήση τους είναι διαδεδομένη σε μεγάλο βαθμό:
- Μυρμηγκικό οξύ (HCOOH, συστηματική ονομασία μεθανικό οξύ).
- Οξικό οξύ (CH3COOH, συστηματική ονομασία αιθανικό οξύ).
- Προπιονικό οξύ (CH3CH2COOH, συστηματική ονομασία προπανικό οξύ).
- Βουτυρικό οξύ (CH3(CH2)2COOH, συστηματική ονομασία βουτανικό οξύ).
- Βαλερικό οξύ (CH3(CH2)3COOH, συστηματική ονομασία πεντανικό οξύ).
- Καπροϊκό οξύ (CH3(CH2)4COOH, συστηματική ονομασία εξανικό οξύ).
- Ενανθικό οξύ (CH3(CH2)5COOH, συστηματική ονομασία επτανικό οξύ).
- Καπρυλικό οξύ (CH3(CH2)6COOH, συστηματική ονομασία οκτανικό οξύ).
- Πελαργονικό οξύ (CH3(CH2)7COOH, συστηματική ονομασία εννεανικό οξύ).
- Καπρικό οξύ (CH3(CH2)8COOH, συστηματική ονομασία δεκανικό οξύ).
- Ενδεκυλικό οξύ (CH3(CH2)9COOH, συστηματική ονομασία ενδεκανικό οξύ).
- Λαυρικό οξύ (CH3(CH2)10COOH, συστηματική ονομασία δωδεκανικό οξύ).
- Τριδεκυλικό οξύ (CH3(CH2)11COOH, συστηματική ονομασία δεκατριανικό οξύ).
- Μυριστικό οξύ (CH3(CH2)12COOH, συστηματική ονομασία δεκατεσσερανικό οξύ).
- Πενταδεκυλικό οξύ (CH3(CH2)13COOH, συστηματική ονομασία δεκαπεντανικό οξύ).
- Παλμιτικό οξύ (CH3(CH2)14COOH, συστηματική ονομασία δεκαξανικό οξύ).
- Μαργαρικό οξύ (CH3(CH2)15COOH, συστηματική ονομασία δεκαπτανικό οξύ).
- Στεατικό οξύ (CH3(CH2)16COOH, συστηματική ονομασία δεκοκτανικό οξύ).
- Νοναδεκυλικό οξύ (CH3(CH2)18COOH, συστηματική ονομασία δεκοεννεανικό οξύ).
- Αραχιδικό οξύ (CH3(CH2)18COOH, συστηματική ονομασία εικοσανικό οξύ).
- Ενεικοσυλικό οξύ (CH3(CH2)19COOH, συστηματική ονομασία εικοσιενανικό οξύ).
- Βαχενικό οξύ (CH3(CH2)20COOH, συστηματική ονομασία εικοσιδυανικό οξύ).
- Τριεικοσυλικό οξύ (CH3(CH2)21COOH, συστηματική ονομασία εικοσιδυανικό οξύ).
- Λιγνοκερικό οξύ (CH3(CH2)22COOH, συστηματική ονομασία εικοσιτεσσερανικό οξύ).
- Ακρυλικό οξύ (CH2=CHCOOH, συστηματική ονομασία προπενικό οξύ).
- Προπιολικό οξύ (HC≡CCOOH, συστηματική ονομασία προπινικό οξύ).
- Οξαλικό οξύ (HOOCCOOH, συστηματική ονομασία αιθανοδιικό οξύ).
- Μηλονικό οξύ (HOOCCH2COOH, συστηματική ονομασία προπανοδιικό οξύ).
- Ηλεκτρικό οξύ [HOOC(CH2)2COOH, συστηματική ονομασία βουταανοδιικό οξύ].
- Γλουταρικό οξύ [HOOC(CH2)3COOH, συστηματική ονομασία πενταανοδιικό οξύ].
- Αδιπικό οξύ [HOOC(CH2)4COOH, συστηματική ονομασία εξανοδιικό οξύ].
- Μηλεϊνικό οξύ (cis-HOOCH=CHCOOH, συστηματική ονομασία cis-βουτενοδιικό οξύ).
- Φουμαρικό οξύ (trans-HOOCH=CHCOOH, συστηματική ονομασία trans-βουτενοδιικό οξύ).
- Γλυκολικό οξύ (HOCH2COOH συστηματική ονομασία υδροξυαιθανικό οξύ).
- Γαλακτικό οξύ [CH3CH(OH)COOH συστηματική ονομασία α-υδροξυπροπανικό οξύ ή 2-υδροξυπροπανικό οξύ].
- Τρυγικό οξύ [HOOCCH(OH)CH(OH)COOH συστηματική ονομασία 2,3-διυδροξυβουτανοδιικό οξύ].
- Κιτρικό οξύ [CH3CH2C(OH)(COOH)CH2COOH συστηματική ονομασία 3-καρβοξυ-3-υδροξυπενταανοδιικό οξύ].
- Πυροσταφυλικό οξύ (CH3COCOOH συστηματική ονομασία οξοπροπανικό οξύ ή 2-κετοπροπανικό οξύ).
- Ακετοξικό οξύ (CH3COCH2COOH συστηματική ονομασία α-οξοπροπανικό οξύ ή 3-κετοπροπανικό οξύ).
- Βενζοϊκό οξύ (PhCOOH συστηματική ονομασία βενζοκαρβονικό οξύ ή φαινυλομεθανικό οξύ ή καρβοξυβενζόλιο).
- Κιναμωμικιό οξύ (PhCH=CHCOOH συστηματική ονομασία β-φαινυλοπροπενικό οξύ ή 3--φαινυλοπροπενικό οξύ).
- Βενζιλικό οξύ [Ph2C(OH)COOH συστηματική ονομασία διφαινυλυδροξυαιθανικό οξύ].
- Φθαλικό οξύ (
συστηματική ονομασία π-καρβοξυβενζοϊκό οξύ ή π-δικαρβοξυβενζόλιο).
- Ισαφθαλικό οξύ (
συστηματική ονομασία μ-καρβοξυβενζοϊκό οξύ ή μ-δικαρβοξυβενζόλιο).
- Τερεφθαλικό οξύ (
συστηματική ονομασία π-καρβοξυβενζοϊκό οξύ ή π-δικαρβοξυβενζόλιο).
- Ανθρανιλικό οξύ (
 συστηματική ονομασία ο-αμινοβενζοϊκό οξύ ή α-καρβοξυλανιλίνη).
συστηματική ονομασία ο-αμινοβενζοϊκό οξύ ή α-καρβοξυλανιλίνη). - Σαλικυλικό οξύ (
 συστηματική ονομασία ο-υδροξυβενζοϊκό οξύ).
συστηματική ονομασία ο-υδροξυβενζοϊκό οξύ). - Ασπιρίνη ή ακετυλοσαλικυλικό οξύ(
 συστηματική ονομασία ο-καρβομεθοξυβενζοϊκό οξύ).
συστηματική ονομασία ο-καρβομεθοξυβενζοϊκό οξύ). - π-αμινοσαλικυλικό οξύ (PAS) (
 συστηματική ονομασία 4-αμινο-2-υδροξυβενζοϊκό οξύ).
συστηματική ονομασία 4-αμινο-2-υδροξυβενζοϊκό οξύ). - Γαλλικό οξύ (
 συστηματική ονομασία 3,4,5-τριυδροξυβενζοϊκό οξύ).
συστηματική ονομασία 3,4,5-τριυδροξυβενζοϊκό οξύ). - μ-Διγαλλικό οξύ [
 συστηματική ονομασία 3,4-διυδροξυ-5-καρβο(3',4',5'-τριυδροξυφαινυλο)βενζοϊκό οξύ)].
συστηματική ονομασία 3,4-διυδροξυ-5-καρβο(3',4',5'-τριυδροξυφαινυλο)βενζοϊκό οξύ)]. - Γλυκίνη (H2NCH2COOH συστηματική ονομασία αμινοαιθανικό οξύ).
- Αλανίνη [CH3CH(NH2)COOH συστηματική ονομασία α-αμινοπροπανικό οξύ].
- Βαλίνη [(CH3)2CHCH(NH2)COOH συστηματική ονομασία 2-αμινο-3-μεθυλοβουτανικό οξύ].
- Λευκίνη [(CH3)2CHCH2CH(NH2)COOH συστηματική ονομασία 2-αμινο-4-μεθυλοπεντανικό οξύ].
- Ισολευκίνη [CH3CH2CH(CH3)CH(NH2)COOH συστηματική ονομασία 2-αμινο-3-μεθυλοπεντανικό οξύ].
- Φαινυλαλανίνη [PhCH2CH(NH2)COOH συστηματική ονομασία 2-αμινο-3-φαινυλοπροπανικό οξύ].
- Σερίνη [HOCH2CH(NH2)COOH συστηματική ονομασία 2-αμινο-3-υδροξυπροπανικό οξύ].
- Θρεονίνη [CH3CH(OH)CH(NH2)COOH συστηματική ονομασία 2-αμινο-3-υδροξυβουτανικό οξύ].
- Τυροσίνη [
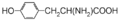 συστηματική ονομασία 2-αμινο-3-(π-υδροξυφαινυλο)προπανικό οξύ].
συστηματική ονομασία 2-αμινο-3-(π-υδροξυφαινυλο)προπανικό οξύ]. - Κυστεΐνη [HSCH2CH(NH2)COOH συστηματική ονομασία 2-αμινο-3-σουλφυδρυλοπροπανικό οξύ].
- Μεθειονίνη [CH3SCH2CH(NH2)COOH συστηματική ονομασία 2-αμινο-3-μεθυλοθειοπροπανικό οξύ].
- Αργινίνη [Η2ΝC(=NH)NH(CH2)3CH(NH2)COOH συστηματική ονομασία 2-αμινο-5-(αμινοϊμινομεθυλαμινο)πεντανικό οξύ].
- Λυσίνη [Η2N(CH2)4CH(NH2)COOH συστηματική ονομασία 2,6-διαμινοεξανικό οξύ].
- Αλλυσίνη [ HCO(CH2)3CH(NH2)COOH συστηματική ονομασία 2-αμινο-5-φορμυλοπεντανικό οξύ].
- Ασπαργανίνη [Η2NCOCH(NH2)COOH συστηματική ονομασία 2-αμινο-2-καρβαμιδοαιθανικό οξύ].
- Ασπαργανικό οξύ [HOOCCH(NH2)COOH συστηματική ονομασία αμινοπροπανοδιικό οξύ].
- Γλουταμίνη [Η2NCOCH2CH(NH2)COOH συστηματική ονομασία 2-αμινο-3-καρβαμιδοπροπανικό οξύ].
- Γλουταμινικό οξύ [HOOCCCH2CH(NH2)COOH συστηματική ονομασία αμινοβουτανοδιικό οξύ].
- Προλίνη (
 συστηματική ονομασία 2-καρβοξυ-αζολιδίνη).
συστηματική ονομασία 2-καρβοξυ-αζολιδίνη). - Ιστιδίνη [
 συστηματική ονομασία 4-(2΄-αμινο-2΄-καρβοξυαιθυλο)-1,3-διαζολίνη].
συστηματική ονομασία 4-(2΄-αμινο-2΄-καρβοξυαιθυλο)-1,3-διαζολίνη]. - Θρυπτοφάνη ή τρυπτοφάνη
 συστηματική ονομασία [2,3]-βενζο-4-(2΄-αμινο-2΄-καρβοξυαιθυλο)αζολίνη.
συστηματική ονομασία [2,3]-βενζο-4-(2΄-αμινο-2΄-καρβοξυαιθυλο)αζολίνη.
Φυσική παρουσία[Επεξεργασία | επεξεργασία κώδικα]
Πολλά καρβονικά οξέα ονομάζονται λιπαρά οξέα και είναι προϊόντα υδρόλυσης λιπών, επομένως με τον αντίστοιχο βιολογικό ρόλο ως συστατικά των λιπιδίων. Επίσης είναι γνωστός ο βιολογικός ρόλος ορισμένων αμινοξέων. Πολλά από τα καρβονικά οξέα παράγονται βιομηχανικά σε μεγάλη κλίμακα, τόσο συνθετικά, όσο και από βιολογικής προέλευσης πρώτες ύλες.
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
- Όπου R παρακάτω με την ευρεία έννοια κάθε ανθρακούχας ομάδας ή και υδρογόνου.
- Όπου Χ παρακάτω αλογόνο (φθόριο, χλώριο, βρώμιο, ιώδιο).
- Μέθοδοι που αφορούν την παραγωγή ενός συγκεκριμένου ή μικρής ομάδας καρβονικών οξέων παραλήφθηκαν για να εκτεθούν στα άρθρα των σχετικών ενώσεων.
Βιομηχανική παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
Οι βιομηχανικές μέθοδοι παραγωγής καρβοξυλικών οξέων γενικά διαφέρουν από τις εργαστηρακές, που προορίζονται για παραγωγή πολύ μικρότερης κλίμακας, επειδή οι πρώτες απαιτούν εξειδικευμένο εξοπλισμό, που είναι οικονομικά ασύμφορος για τις δεύτερες. Μερικές μέθοδοι πάντως έχουν διπλό ρόλο, με παραλλαγές. Οι κυριότερες βιομηχανικές μέθοδοι παραγωγής καρβονικών οξέων είναι οι ακόλουθες:
1. Η οξείδωση αλδεϋδών με αέρα [περιέχει οξυγόνο (Ο)], χρησιμοποιώντας ως καταλύτες κοβάλτιο (Co) ή και μαγγάνιο (Mn). Οι απαιτούμενες αλδεΰδες προέρχονται συνήθως από αντίστοιχα αλκένια με προσθήκη μεθανάλης (HCHO). Τα αλκένια είναι παράγωγα συστατικών του πετρελαίου ή και του φυσικού αερίου.
2. Η οξείδωση υδρογονανθράκων με αέρα. Από απλά αλκάνια, η μέθοδος δεν είναι καθόλου εκλεκτική (δηλαδή συμπαράγονται πολλά παραπροϊόντα), αλλά οικονομική και χρήσιμη. Αλλυλικά και βενζυλικά παράγωγα δίνουν πιο εκλεκτικές οξςιδώσεις. Τα αλκύλια σε βενζολικούς δακτυλίους οξειδώνονται προς αντίστοιχα καρβονικά οξέα, ανεξάρτητα από το μήκος τους. Με αυτόν τον τρόπο παράγεται βενζοϊκό οξύ από τολουόλιο, τερεφθαλικό οξύ από π-ξυλένιο και φθαλικό οξύ από ο-ξυλένιο. Το ακρυλικό οξύ παράγεται ομοίως από το προπένιο[3].
3. Μερικά καρβονυλικά οξέα παράγονται και με υδρόλυση τριγλυκεριδίων που προέρχονται από φυτικά και ζωικά λίπη και έλαια. Αυτή η μέθδος σχετίζεται και με τη σαπωνοποίηαη.
4. Μερικά καρβονυλικά οξέα παράγονται με βιοχημικές μεθόδους, συνήθως με ζύμωση. Για παράδειγμα, η ζύμωση αιθανόλης χρησιμοποιείται για την παραγωγή ξυδιού.
Εργαστηριακή παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση CO2 σε οργανομαγνησιακές ενώσεις[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση διοξειδίου του άνθρακα (CO2) σε οργανοαλομαγνησιακές ενώσεις (RMgX)[4]:
Με υδρόλυση νιτριλίων[Επεξεργασία | επεξεργασία κώδικα]
Με υδρόλυση νιτριλίων (RCN) σε όξινο περιβάλλον[5]:
Με οξείδωση[Επεξεργασία | επεξεργασία κώδικα]
1. Με οξείδωση αλκενίων (τύπου RCH=CHR[6])[7]:
2. Με οξείδωση πρωτοταγών αλκοολών (RCH2OH)[8]:
3. Με οξείδωση αλδεϋδών (RCHO)[8]:
Με μονοαποκαρβοξυλίωση παραγώγων του μηλονικού οξέος[Επεξεργασία | επεξεργασία κώδικα]
Με μονοαποκαρβοξυλίωση παραγώγων του μηλονικού οξέος [ΗΟΟCCH(R)COOH][9]:
Με αλκαλική διάσπαση παραγώγων του ακετοξικού αιθυλεστέρα[Επεξεργασία | επεξεργασία κώδικα]
Με αλκαλική διάσπαση παραγώγων του ακετοξικού αιθυλεστέρα (AcOEt)[10]:
Φυσικές ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Σύζευξη[Επεξεργασία | επεξεργασία κώδικα]
Τα μόρια των μονοκαρβονικών οξέων διμερίζονται σχηματίζοντας δεσμούς υδρογόνου[11]:

Γενικά τα καρβονικά οξέα είναι πολικά, γιατί διαθέτουν και δέκτες (καρβονύλιο) και δότες (υδροξύλιο) δεσμών υδρογόνου. Διαθέτουν όμως και την υδρόφοβη (αν δεν περιέχει πολικές χαρακτηριστικές ομάδες). Αποτέλεσμα των παραπάνω είναι τα μονοκαρβονικά οξέα με ένα (1) ως πέντε (5) άτομα άνθρακα να είναι ευδιάλυτα στο νερό, ενώ τα βαρύτερα λιγότερο διαλυτά, καθώς αυξάνεται το υδρόφοβο τμήμα του μορίου τους. Αυτά τα ανώτερα οξέα είναι πιο ευδιάλυτα σε λιγότερο πολικούς διαλύτες, όπως οι αιθέρες και οι αλκοόλες[12]. Επίσης αποστάζουν με υδρατμούς[11].
Σημεία βρασμού[Επεξεργασία | επεξεργασία κώδικα]
Τα καρβονικά οξέα έχουν υψηλότερα σημεία βρασμού από το νερό, κυρίως επειδή σχηματίζουν σταθερά διμερή, που δεν διασπώνται πάντα με το βρασμό. Στην περίπτωση που δισσπούνται η ενθαλπία διάσπασης προστίθεται σ' αυτύην της εξαέρωσης, ενώ στη δεύτερη και πάλι είναι αυξημένη, αφού εξαερώνται διπλάσιο σε μάζα μόριο.
Οσμή[Επεξεργασία | επεξεργασία κώδικα]
Τα καρβονικά οξέα έχουν συχνά ισχυρές οσμές και ιδιαίτερα τα πτητικά τους παράγωγα. Πιο γνωστές από αυτές είναι του οξικού οξέος, (ως ξύδι) και του βουτυρικού οξέος (ως ταγγισμένο βούτυρο). Οι εστέρες τους έχουν συνήθως ευχάριστες οσμές και πολλοί από αυτούς χρησιμοποιούνται ως αρώματα ή αιθέρια έλαια.
Χημικές ιδιότητες και παράγωγα[Επεξεργασία | επεξεργασία κώδικα]
- Όπου R παρακάτω με την ευρεία έννοια κάθε ανθρακούχας ομάδας ή και υδρογόνου.
- Όπου Χ παρακάτω αλογόνο (φθόριο, χλώριο, βρώμιο, ιώδιο).
΄Οξινος χαρακτήρας και καρβονικά άλατα[Επεξεργασία | επεξεργασία κώδικα]
Τα καρβονικά οξέα έχουν όξινη συμπεριφορά και γι' αυτό δίνουν άλατα με βάσεις όπως το υδροξείδιο του νατρίου (NaΟΗ)[13]:
Τα καρβονικά οξέα είναι τυπικά ασθενή έως μετρίως ισχυρά οξέα, με την έννοια ότι η διάστασή τους περιορίζεται σε ένα μικρό ποσοστό των μορίων τους. Η παρουσία ηλεκτρονιόφιλων υποκαταστατών συξάνει σημαντικά την οξύτητά τους.
| Καρβονικά οξέα | pKa |
|---|---|
| Μεθανικό οξύ (HCOOH) | 3,77 |
| Αιθανικό οξύ (CH3COOH) | 4,76 |
| Χλωραιθανικό οξύ (ClCH2COOH) | 2,86 |
| Διχλωραιθανικό οξύ (CHCl2COOH) | 1,29 |
| Τριχλωραιθανικό οξύ (CCl3COOH) | 0,65 |
| Τριφθοραιθανικό οξύ (CF3COOH) | 0,5 |
| Οξαλικό οξύ (HOOCCOOH) | 1,27 (pKa1) |
| Βενζοϊκό οξύ (PhCOOH) | 4,2 |
Ωστόσο, ο ιονισμός του καρβοξυλίου (-COOH) δίνει καρβοξυλανιόν (-COO-), που σταθεροποιείται επιπλέον από την ανταλλαγή του επιπλέον ηλεκτρονίου και του φορτίου του μεταξύ των δυο ατόμων οξυγγόνου (O) του, σχηματίζοντας ταυτόχρονα και δυο διπλούς δεσμούς του ενός ηλεκτρονίου με το καρβοξυλικό άτομο άνθρακα (C).
Αποκαρβοξυλίωση[Επεξεργασία | επεξεργασία κώδικα]
- 1. Με θέρμανση καρβονικών οξέων ή καλύτερα αλάτων τους με μονοσθενή μέταλλα παράγονται συμμετρικοί υδρογονάνθρακες, αν το R τους δεν περιέχει χαρακτηριστική ομάδα (αν περιέχει παράγονται άλλες κατηγορίες συμμετρικών οργανικών ενώσεων. Π.χ. από υδροξυαιθανικό οξύ παράγεται αιθανόλη)[14]:
- 2. Με ηλεκτρόλυση αλάτων καρβονικών οξέων (μέθοδος Kolbe), παράγονται συμμετρικοί υδρογονάνθρακες, εφάσον αν το R τους δεν περιέχει χαρακτηριστική ομάδα[15]:

- 3. Με θέρμανση μονοκαρβονικών αλάτων του ασβεστίου παράγονται κετόνες (ή φορμαλδεΰδη από το μυρμηκικό οξύ) [16]:
- 4. Με θέρμανση δικαρβονικών αλάτων με 6-9 άτομα άνθρακα του ασβεστίου ή του βαρίου παράγονται κυκλοκετόνες[17]. Π.χ. με το εξανοδιικό ασβέστιο παίρνουμε κυκλοπεντανόνη
- Πρόκειται για μέθοδο παραγωγής δακτυλίου 5-8 ατόμων άνθρακα.
Αναγωγή[Επεξεργασία | επεξεργασία κώδικα]
Τα καρβονικά οξέα ανάγονται με LiAlH4 ή NaBH4 στις αντίστοιχες πρωτοταγείς αλκοόλες[19]:
Οξείδωση[Επεξεργασία | επεξεργασία κώδικα]
Τα καρβονικά οξέα οξειδώνονται σε καρβονικά υπεροξέα από το υπεροξείδιο του υδρογόνου (H2O2), σε όξινο περιβάλλον[20]:
Αλογόνωση[Επεξεργασία | επεξεργασία κώδικα]
1. Αλογόνωση σε α-θέση - Αντίδραση Hell-Volhard-Zelinsky[21]:
- Συμπαράγεται και μια ποσότητα RCH2COX[22]:
- Απευθείας επίδραση με διφθόριο αποφεύγεται, ως επικίνδυνη. Προτιμάται η παραγωγή άλλου αλοκαρβονικού οξέος και μετά υποκατάσταση με χρήση υποφθοριούχου υδραργύρου:
2. Παραγωγή ακυλαλογονιδίων με θειονυλοχλωρίδιο (SOCl2)[23]:
3. Παραγωγή ακυλαλογονιδίων με πενταχλωριούχο φωσφόρο (PCl5)[24]:
Εστεροποίηση[Επεξεργασία | επεξεργασία κώδικα]
- Όπου, τα δύο R όχι απαραίτητα ίδια.
Εφαρμογές[Επεξεργασία | επεξεργασία κώδικα]
Τα καρβονικά οξέα χρησιμοποιούνται στην παραγωγή πολυμερών, φαρμάκων, καλυντικών, διαλυτών και προσθέτων τροφίμων. Τα σημαντικότερα για τη βιομηχανία είναι το οξικό οξύ (ως ξύδι, διαλύτης και πρόσθετο τροφίμων), το ακρυλικό οξύ (πολυμερή, κόλλες), το μεθακρυλικό οξύ (πολυμερή, κόλλες), το αδιπικό οξύ (πολυμερή), το κιτρικό οξύ (πρόσθετο τροφίμων και κυρίως αναψυκτικών), το αιθενοδιαμινοτετραοξικό οξύ (EDTA) (καθαριστικό αλάτων, αποσκληρυντικό), τα λιπαρά οξέα (πρόσθετα τροφίμων), το μαλεϊκό οξύ (πολυμερή), το προπιονικό οξύ (πρόσθετο τροφίμων), το τρυγικό οξύ (πρόσθετο τροφίμων), το τερεφθαλικό οξύ (πολυμερή) και το βενζοϊκό οξύ (συντηριτικό).
Αναφορές και σημειώσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Compendium of Chemical Terminology, carboxylic acids, accessed 15 Jan 2007.
- ↑ March, Jerry (1992), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (4th ed.), New York: Wiley, ISBN 0-471-60180-2
- ↑ Wilhelm Riemenschneider “Carboxylic Acids, Aliphatic” in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. doi: 10.1002/14356007.a05_235.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.283, §12.2.1.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.283, §12.2.2.
- ↑ Αν χρησιμοποιηθούν μη συμμετρικά προκύπτουν μίγματα καρβονικών οξέων. Π.χ. με RCH=CH2 παράγονται RCOOH και HCOOH
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.283, §12.2.3α.
- ↑ 8,0 8,1 Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.283, §12.2.3β.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.283, §12.2.4.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.283, §12.2.5.
- ↑ 11,0 11,1 Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.285, §12.4.1.
- ↑ R.T. Morrison, R.N. Boyd. Organic Chemistry, 6th Ed. (1992) ISBN 0-13-643669-2.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.285, §12.4.2.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.285, §12.4.3α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.285, §12.4.3β.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.285, §12.4.3γ.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.154, §6.5Α1..
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.285, §12.4.3δ.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.285, §12.4.4.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.285, §12.4.5α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.286, §12.4.7.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.286, §12.4.8β.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.286, §12.4.8α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.286, §12.4.8γ.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ.285, §12.4.8α.
Πηγές[Επεξεργασία | επεξεργασία κώδικα]
- Ν. Αλεξάνδρου, Γενική Οργανική Χημεία, ΘΕΣΣΑΛΟΝΙΚΗ 1985
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
- Πολυχρόνη Σ. Καραγκιοζίδη: Ονοματολογία οργανικών ενώσεων, Θεσσαλονίκη 1991, Έκδοση Β΄.
- Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροκυκλικών Ενώσεων, Θεσσαλονίκη 1985, Έκδοση Β΄.
- Δ. Νικολαΐδη: Ειδικά κεφάλαια Οργανικής Χημεία, Θεσσαλονίκη 1983.
| |||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
|
















![{\displaystyle \mathrm {CH_{3}COCH(R)COOCH_{2}CH_{3}+H_{2}O{\xrightarrow[{-CH_{3}COOH}]{\pi .KOH}}RCH_{2}COOCH_{2}CH_{3}{\xrightarrow[{-CH_{3}CH_{2}OH}]{+KOH}}RCH_{2}COOK{\xrightarrow {+HCl}}RCH_{2}COOH+KCl} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/fabb4ad4e074d5a7c6977d04d2a4dbafc1304df5)

















