Διοξείδιο του άνθρακα
| Διοξείδιο του άνθρακα | |||
|---|---|---|---|

| |||
| |||
| Γενικά | |||
| Όνομα IUPAC | Διοξείδιο του άνθρακα | ||
| Άλλες ονομασίες | ανθρακικός ανυδρίτης, ξηρός πάγος (ως στερεό) | ||
| Χημικά αναγνωριστικά | |||
| Μοριακή μάζα | 44.010 g/mol, αέριο | ||
| Αριθμός CAS | 124-38-9 | ||
| SMILES | C(=O)=O | ||
| InChI | 1/CO2/c2-1-3 | ||
| Αριθμός EINECS | 204-696-9 | ||
| Αριθμός RTECS | FF6400000 | ||
| PubChem CID | 280 | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | −78 °C (195K) (-109 °F ) εξαχνώνεται | ||
| Σημείο βρασμού | −57 °C (216K) (-70 °F) υπό πίεση | ||
| Πυκνότητα | 1,562 g/mL (στερεό 1 Αtm, −78,5 °C) 0,770 g/mL (υγρό 56 Αtm, 20 °C) 1.977 g/L (αέριο 1 Αtm, 0 °C) 849,6 g/L (υπερκρίσιμο υγρό 150 Αtm, 30 °C) | ||
| Διαλυτότητα στο νερό |
1,45 g/L | ||
| Ιξώδες | 0.07 cP στους −78 °C | ||
| Δείκτης διάθλασης , nD |
1,1120 | ||
| Χημικές ιδιότητες | |||
| pKa | 6,35, 10,33 | ||
| Ελάχιστη θερμοκρασία ανάφλεξης |
Μη αναφλέξιμο | ||
| Επικινδυνότητα | |||
| Φράσεις ασφαλείας | S9, S23, S26, S36 | ||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
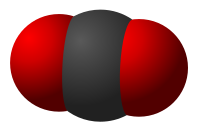
Το διοξείδιο του άνθρακα (χημικός τύπος CO2) είναι χημική ένωση που αποτελείται από δύο άτομα οξυγόνου ενωμένα με ομοιοπολικό δεσμό με ένα άτομο άνθρακα. Είναι γραμμικό μόριο χωρίς διπολική ροπή. Περιέχει 27,3 % w/w άνθρακα και 72,7 % w/w οξυγόνο. Μπορεί να αποδοθεί με το συντακτικό τύπο : O=C=O. Είναι αέριο συστατικό της γήινης ατμόσφαιρας, άχρωμο, άοσμο και άγευστο σε κανονικές συνθήκες πίεσης και θερμοκρασίας και επίσης είναι ένα από τα αέρια του θερμοκηπίου.
Προέλευση
[Επεξεργασία | επεξεργασία κώδικα]Αποτελεί υποπροϊόν όλων των καύσεων ορυκτών καυσίμων (κάρβουνου, πετρελαίου, βενζίνης, φυσικού αερίου κλπ.), αλλά και του ξύλου, πλαστικών κ.ά. οργανικών ενώσεων. Παράγεται ακόμα από την αποσύνθεση οργανικών ουσιών. Μεγάλες ποσότητες διοξειδίου του άνθρακα εκπέμπονται επίσης από τα ηφαίστεια* και από τις θερμές πηγές αλλά και από τη διάλυση των ανθρακικών πετρωμάτων. Ενωμένο, με τη μορφή ανθρακικών αλάτων, βρίσκεται σε μεγάλες ποσότητες στο στερεό φλοιό της γης. Τα κυριότερα ανθρακικά ορυκτά είναι οι διάφορες ποικιλίες του CaCO3 (ασβεστόλιθοι, ασβεστίτης, μάρμαρο κ.ά.), ο μαγνησίτης MgCO3, ο σιδηρίτης FeCO3, ο δολομίτης CaCO3.MgCO3 κ.ά. Παράγεται επίσης κατά την αναπνοή όλων των φυτών και των ζώων και από τους μύκητες και μικροοργανισμούς που εξαρτώνται άμεσα ή έμμεσα από τα φυτά για την τροφή τους.
- (*) Σύμφωνα με εκτιμήσεις του Γεωλογικού Ινστιτούτου των ΗΠΑ τα ηφαίστεια παράγουν σε παγκόσμιο επίπεδο 200 εκατομ. τόνους διοξειδίου του άνθρακα ετησίως.
Ιστορικά στοιχεία
[Επεξεργασία | επεξεργασία κώδικα]Το διοξείδιο του άνθρακα ήταν ένα από τα πρώτα αέρια που μελετήθηκε ως συστατικό του αέρα. Τον 17ο αιώνα ο Φλαμανδός χημικός Γιάν Μπατίστ φαν Χέλμοντ (Jan Baptist van Helmont) παρατήρησε ότι όταν καίγεται ο άνθρακας σε κλειστό δοχείο, η μάζα της στάχτης που προκύπτει ήταν πολύ μικρότερη από εκείνη του αρχικού άνθρακα. Η ερμηνεία που έδωσε ήταν ότι ο άνθρακας που έλειπε είχε μεταλλαχθεί σε μια αόρατη ουσία, που την ονόμασε «αέριο» ή «άγριο πνεύμα».
Οι ιδιότητες του διοξειδίου του άνθρακα μελετήθηκαν πιο διεξοδικά στη δεκαετία 1750-1760 από το Σκωτσέζο φυσιολόγο Τζόζεφ Μπλακ (Joseph Black). Αυτός πρόσεξε ότι ο ασβεστόλιθος (ανθρακικό ασβέστιο) όταν θερμαίνεται ή υφίσταται κατεργασία με οξέα παράγει ένα αέριο που το ονόμασε «σταθερό αέρα». Παρατήρησε επίσης ότι ο "σταθερός αέρας" ήταν πυκνότερος από τον αέρα και δε συντηρούσε ούτε την καύση ούτε τις ζωικές λειτουργίες. Ο Μπλακ παρατήρησε ακόμα ότι όταν διοχετεύονταν φυσαλίδες του αερίου σε υδατικό διάλυμα ασβέστη (υδροξείδιο του ασβεστίου), παραγόταν ίζημα ανθρακικού ασβεστίου. Χρησιμοποίησε μάλιστα αυτή τη διαπίστωσή του για να αποδείξει ότι το διοξείδιο του άνθρακα παράγεται από την αναπνοή των ζώων και τη μικροβιακή ζύμωση.
Το 1772, ο Άγγλος χημικός Τζόζεφ Πρίστλεϋ (Joseph Priestley) δημοσίευσε μια εργασία με τίτλο "Εμπλουτισμός του νερού με Σταθερό Αέρα" στην οποία περιέγραφε μια διαδικασία κατά την οποία όταν έπεφταν σταγόνες θειικού οξέος (ή βιτριόλι όπως το ήξερε ο Πρίστλεϋ) στην κιμωλία, για να παράγουν διοξείδιο του άνθρακα, το αέριο στη συνέχεια όταν διοχετευόταν σε μπολ με νερό, διαλυόταν.
Το διοξείδιο του άνθρακα υγροποιήθηκε για πρώτη φορά (σε υψηλές πιέσεις) το 1823 από τον Χάμφρι Ντέιβι (Humphry Davy) και το μαθητή του Μάικλ Φάραντεϊ (Michael Faraday).
Η παλιότερη περιγραφή του στερεού διοξειδίου του άνθρακα δόθηκε από τον Σαρλ Τιλοριέ (Charles Thilorier), ο οποίος το 1834 άνοιξε ένα δοχείο υπό πίεση με υγρό διοξείδιο του άνθρακα, και διαπίστωσε την ταχεία εξάτμιση του υγρού που μετατράπηκε σε ένα "χιόνι" στερεού CO2.
Πώς παρασκευάζεται
[Επεξεργασία | επεξεργασία κώδικα]Το διοξείδιο του άνθρακα μπορεί να παραληφθεί από την απόσταξη του αέρα. Η μέθοδος αυτή όμως χρησιμοποιείται για την παραγωγή μικρών ποσοτήτων.
Εργαστηριακές μέθοδοι
[Επεξεργασία | επεξεργασία κώδικα]1. Με αντίδραση των ανθρακικών ή όξινων ανθρακικών αλάτων με οξέα:
- CaCO3 + 2HCl→ CaCl2 + CO2 + H2O
- NaHCO3 + H2SO4 → NaHSO4 + CO2 + H2Ο
2. Με τη θερμική διάσπαση των ίδιων αλάτων:
- CaCO3 → CaO + CO2 (στους 850 °C)
- 2KHCO3 → K2CO3 + CO2 + H2Ο
Βιομηχανικές παρασκευές
[Επεξεργασία | επεξεργασία κώδικα]1. Με την αναγωγή οξειδίων του σιδήρου από άνθρακα σε υψικαμίνους:
- 2Fe2O3 + 3C → 4Fe + 3CO2
2. Με πύρωση του ασβεστόλιθου στα ασβεστοκάμινα για την παραγωγή ασβέστη (CaO):
- CaCO3 → CaO + CO2
3. Με καύση του άνθρακα σε περίσσεια οξυγόνου ή αέρα. Έτσι προκύπτει μίγμα με άλλα αέρια (Ν2, CO) από το οποίο το CO2 απομονώνεται με διάφορες μεθόδους.
4. Με την αλκοολική ζύμωση των σακχάρων κατά τη διαδικασία παραγωγής αλκοολούχων ποτών, από την οποία προκύπτει πολύ καθαρό διοξείδιο του άνθρακα:
- C6H12O6 → 2CO2 + 2C2H5OH
5. Με την καύση όλων των καυσίμων που περιέχουν άνθρακα όπως είναι το μεθάνιο (ως συστατικό του φυσικού αερίου), τα διάφορα κλάσματα του πετρελαίου (βενζίνη, diesel, κηροζίνη κλπ.) αλλά και το κάρβουνο και το ξύλο.
- CH4 + 2O2 → CO2 + 2H2Ο
6. Ως υποπροϊόν των μονάδων παραγωγής υδρογόνου, όπου το μεθάνιο μετατρέπεται σε CO2
Φυσικές ιδιότητες
[Επεξεργασία | επεξεργασία κώδικα]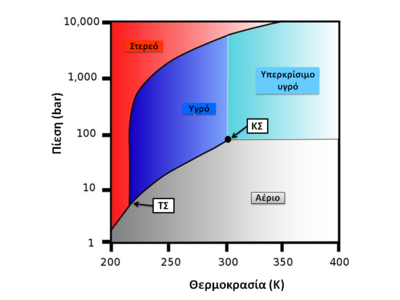
Είναι αέριο άχρωμο και σε μικρές συγκεντρώσεις είναι και άοσμο. Σε κανονικές συνθήκες πίεσης και θερμοκρασίας η πυκνότητα του είναι 1,98 kg/m3, είναι δηλ. 1,5 φορά πυκνότερο του αέρα.
Σε 1 Atm (δηλ. σε πίεση στο επίπεδο της θάλασσας), μετατρέπεται απευθείας σε στερεό, σε θερμοκρασίες κάτω από -78,51 °C και, αν είναι σε στερεή μορφή, εξαχνώνεται πάνω από τους -78,51 °C.
Στη στερεή του κατάσταση, το διοξείδιο του άνθρακα, είναι γνωστό ως «ξηρός πάγος».
Η κρίσιμη θερμοκρασία του είναι 31,1 °C και επομένως υγροποιείται εύκολα στη συνηθισμένη θερμοκρασία αλλά μόνο με συμπίεση (7,38 MPa). Είναι λίγο διαλυτό στο νερό, η διαλυτότητά του όμως αυξάνεται, όπως όλων των αερίων, με την πίεση. Νερό κορεσμένο από CO2 με πίεση λέγεται "νερό του Seltz".
Το τριπλό σημείο του διοξειδίου του άνθρακα είναι περίπου 518 kPa στους -56.6 °C.
Υπάρχει και μια εναλλακτική μορφή άμορφου κρυσταλλικού στερεού διοξειδίου του άνθρακα, όχι όμως σε ατμοσφαιρική πίεση. Αυτή η μορφή γυαλιού, που ονομάζεται "καρμπόνια" παράχθηκε με υπέρψυξη θερμαινόμενου CO2 σε ακραίες συνθήκες πίεσης (περίπου 400000 Atm). Η ανακάλυψη αυτή επιβεβαίωσε τη θεωρία ότι το διοξείδιο του άνθρακα θα μπορούσε να υπάρχει σε μια κατάσταση παρόμοια με τις κρυσταλλικές μορφές των άλλων στοιχείων της ομάδας του άνθρακα στον περιοδικό πίνακα όπως το πυρίτιο και το γερμάνιο. Σε αντίθεση όμως με τα διοξείδια του πυριτίου και του γερμανίου, η "καρμπόνια" δεν είναι σταθερή σε κανονική πίεση.
Χημικές ιδιότητες
[Επεξεργασία | επεξεργασία κώδικα]Μοριακή δομή
[Επεξεργασία | επεξεργασία κώδικα]
Το μόριο του διοξειδίου του άνθρακα (O=C=O) περιέχει δύο διπλούς δεσμούς, και έχει γραμμική μορφή. Η ενέργεια κάθε δεσμού[1] C=Ο είναι 799 KJ/mol.
Αποδεικνύεται κβαντομηχανικά ότι η δομή του CO2 περιέχει διάχυτους (μη εντοπισμένους) διπλούς δεσμούς C=Ο (δηλ. τα 4 ηλεκτρόνια των π-δεσμών είναι ελεύθερα να κινούνται σε όλο το μήκος του πυρηνικού σκελετού) και όχι εντοπισμένους επειδή η ολική ενέργεια της βασικής κατάστασης στην πρώτη περίπτωση είναι μικρότερη και επομένως το μόριο είναι σταθερότερο.
Το CO2 όπως είναι φανερό δεν έχει διπολική ροπή, είναι δηλ. μόριο μη-πολικό.
Χημικές αντιδράσεις
[Επεξεργασία | επεξεργασία κώδικα]Εφόσον στο CO2 ο C έχει αριθμό οξείδωσης +4, είναι όξινο κανονικό οξείδιο και ανυδρίτης του διπρωτικού ανθρακικού οξέος (H2CO3) το οποίο είναι ασταθές οξύ και υπάρχει μόνο με μορφή αλάτων (π.χ. Na2CO3) ή σε υδατικό διάλυμα στα αεριούχα ποτά όπου αποκαθίσταται η ισορροπία : CO2 + H2Ο ⇄ H2CO3.
Το CO2 είναι γενικά σταθερή ένωση και σε κατάλληλες συνθήκες ανάγεται από διάφορα αναγωγικά προς άνθρακα (C) ή προς μονοξείδιο του άνθρακα (CO), δηλαδή συμπεριφέρεται σαν οξειδωτικό.
Αντιδρά με βάσεις και ανυδρίτες βάσεων και σχηματίζει ανάλογα με την υπάρχουσα αναλογία mol των αντιδρώντων, δύο σειρές αλάτων, τα όξινα και τα ουδέτερα :
- CO2 + CaO → CaCO3
- CO2 + NaOH → NaHCO3
- CO2 + 2ΚΟΗ → Κ2CO3 + H2Ο
Όταν το CO2 διαβιβάζεται σε διάλυμα ή σε αιώρημα ουδέτερου ανθρακικού άλατος, τότε το μετατρέπει σε όξινο :
- Na2CO3 + CO2 + H2Ο → 2NaHCO3
- CaCO3 + CO2 + H2O → Ca(HCO3)2
Σε κατάλληλες συνθήκες ανάγεται από τον C προς CO και από ορισμένα μέταλλα (K, Na, Mg) προς C :
- C + CO2 → 2CO
- 2Mg + CO2 → 2MgO + C
Ανίχνευση - ποσοτικός προσδιορισμός
[Επεξεργασία | επεξεργασία κώδικα]Το CO2 ανιχνεύεται από την ιδιότητά του να σβήνει τη φλόγα και από το ότι σχηματίζει θόλωμα ή ίζημα δυσδιάλυτου ανθρακικού άλατος, όταν διαβιβάζεται σε ασβεστόνερο :
- Ca(OH)2 + CO2 → CaCO3↘ + H2O
Η αντίδραση με ΚΟΗ (CO2 + 2ΚΟΗ → Κ2CO3 + H2O) χρησιμοποιείται για τον ποσοτικό προσδιορισμό του CO2 σε μίγμα αερίων (δείγμα) : Σε κατάλληλο σκεύος υπάρχει διάλυμα 36 % w/v ΚΟΗ ή 32 % w/v NaOH. Και τα δύο διαλύματα απορροφούν 30/πλάσιο όγκο CO2. Προτιμάται όμως το ΚΟΗ γιατί το σχηματιζόμενο K2CO3 είναι διαλυτό σε διάλυμα ΚΟΗ ενώ το αντίστοιχο Na2CO3 δεν είναι σε διάλυμα NaOH και σχηματίζεται επίπαγος. Στο διάλυμα διοχετεύεται το μίγμα των αερίων που περιέχει το CO2 και από τη μείωση του όγκου προσδιορίζεται τελικά το διοξείδιο του άνθρακα, με την προϋπόθεση βέβαια ότι τα άλλα αέρια του μίγματος δεν αντιδρούν με το ΚΟΗ. Αν οι συγκεντρώσεις του CO2 στο δείγμα είναι μικρές, τότε χρησιμοποιείται διάλυμα Ba(OH)2 και μετά τη διέλευση του δείγματος, ογκομετρείται η περίσσεια του Ba(OH)2.
Διαλυτότητα στο νερό
[Επεξεργασία | επεξεργασία κώδικα]
Η διαλυτότητα του CO2 στο νερό εξαρτάται από πολλούς παράγοντες όπως η πίεση του CO2 σε ισορροπία με το διάλυμα (η διαλυτότητα αυξάνεται με αύξηση της πίεσης), η θερμοκρασία (η διαλυτότητα ελαττώνεται με αύξηση της θερμοκρασίας), το pH (η διαλυτότητα του CO2 αυξάνεται με την αύξηση του pH), η παρουσία άλλων ουσιών (η διαλυτότητα μειώνεται με την παρουσία ενώσεων όπως το χλωριούχο νάτριο, αλλά μπορεί και να αυξηθεί ή να μειωθεί με την αύξηση της συγκέντρωσης των οργανικών ενώσεων).
Σε θερμοκρασία δωματίου (25 °C), η διαλυτότητα του CO2 είναι περίπου 90 mL ανά 100 mL νερού. Σε υδατικό διάλυμα, το διοξείδιο του άνθρακα βρίσκεται με διάφορες μορφές :
CO2(aq) + H2Ο ⇄ H2CO3 ⇄ HCO3- + H+ ⇄ CO32- + 2H+
Τα ανιόντα του παραπάνω σχήματος αντιδρούν με κατιόντα που πιθανόν υπάρχουν στο νερό, παράγοντας αδιάλυτα άλατα. Έτσι, αν π.χ. υπάρχουν ιόντα Ca2+ ή/και Mg2+ τότε σχηματίζονται αδιάλυτα CaCO3 και MgCO3 τα οποία, δεσμεύοντας τα CO32-, μετατοπίζουν την ισορροπία προς τα δεξιά αυξάνοντας την οξύτητα του νερού.
Είναι σημαντικό να σημειωθεί ακόμη ότι το καρβονικό οξύ που παράγεται κατά την διάλυση του CO2 στο νερό είναι ακόμη ένας λόγος που η αύξηση του CO2 από ανθρωπογενείς παράγοντες απειλεί την ισορροπία του οικοσυστήματος, αφού η αυξημένη οξύτητα του νερού προκαλεί προβλήματα στους θαλάσσιους οργανισμούς
Χρήσεις
[Επεξεργασία | επεξεργασία κώδικα]Το διοξείδιο του άνθρακα χρησιμοποιείται από τη βιομηχανία τροφίμων, τη βιομηχανία πετρελαίου, και τη χημική βιομηχανία. Βρίσκει εφαρμογές σε πολλά καταναλωτικά προϊόντα που απαιτούν πεπιεσμένο αέριο γιατί είναι φθηνό και άφλεκτο, και λόγω του ότι μεταβαίνει από την αέρια φάση στην υγρή σε θερμοκρασία δωματίου και σε χαμηλή, σχετικά, πίεση. Τα σωσίβια γιλέκα συχνά περιέχουν CO2 υπό πίεση. Πωλούνται επίσης μικρές κάψουλες από αλουμίνιο με συμπιεσμένο CO2 για αεροβόλα όπλα, για φούσκωμα των ελαστικών των ποδηλάτων και για την παρασκευή αναβραζόντων δισκίων φαρμάκων. Η ταχεία εξάτμιση του υγρού διοξειδίου του άνθρακα χρησιμοποιείται για ανατινάξεις σε ορυχεία άνθρακα. Οι υψηλές συγκεντρώσεις διοξειδίου του άνθρακα μπορούν επίσης να χρησιμοποιηθούν για την εξολόθρευση επιβλαβών εντόμων, όπως ο σκόρος των ρούχων.
Ποτά
[Επεξεργασία | επεξεργασία κώδικα]Το διοξείδιο του άνθρακα χρησιμοποιείται για την παραγωγή αεριούχων ποτών και σόδας. Η περιεκτικότητα των ανθρακούχων ποτών σε CO2 οφείλεται σε φυσικούς λόγους (ζύμωση), μπορεί όμως να διοχετευθεί ανθρακικό και με τεχνητούς τρόπους. Σύμφωνα με έρευνες του 2009 από το Πανεπιστημίου της Καλιφόρνια στο Σαν Ντιέγκο και ερευνητών των αμερικανικών Εθνικών Ινστιτούτων Υγείας, τα μόρια διοξειδίου του άνθρακα ενεργοποιούν ένα ένζυμο που υπάρχει στους υποδοχείς της γλώσσας για την γεύση του ξινού, της καρβονική ανυδράση 4, παράγοντας την αίσθηση της αντίστοιχης γεύσης. Επίσης τα μόρια του ενεργοποιούν τους υποδοχείς αφής στο στόμα, αφήνοντας μια χαρακτηριστική αίσθηση.[2]
Τρόφιμα
[Επεξεργασία | επεξεργασία κώδικα]Μια καραμέλα που ονομάζεται Pop Rocks συμπιέζεται με διοξείδιο του άνθρακα περίπου στα 40 bar. Όταν η καραμέλα μπαίνει στο στόμα, διαλύεται και απελευθερώνει φυσαλίδες αερίου. Η μαγιά της αρτοποιίας παράγει διοξείδιο του άνθρακα από τη ζύμωση των σακχάρων στο εσωτερικό της ζύμης, ενώ άλλα προϊόντα, όπως το baking powder και η μαγειρική σόδα, απελευθερώνουν διοξείδιο του άνθρακα όταν θερμαίνονται ή όταν εκτεθούν σε οξέα.
Πυροπροστασία
[Επεξεργασία | επεξεργασία κώδικα]Το διοξείδιο του άνθρακα επειδή είναι άφλεκτο χρησιμοποιείται υπό πίεση σε ορισμένους πυροσβεστήρες που είναι σχεδιασμένοι για κατάσβεση πυρκαγιών που οφείλονται σε ηλεκτρικά βραχυκυκλώματα. Επίσης ειδικοί πυροσβεστήρες με CO2 χρησιμοποιούνται και για την πυροπροστασία πλοίων και μηχανοστασίων. Όμως τα συστήματα πυρασφάλειας που βασίζονται στο διοξείδιο του άνθρακα έχουν συνδεθεί και με πολλούς θανάτους.
Υδραυλικά συστήματα
[Επεξεργασία | επεξεργασία κώδικα]Το CO2 είναι ένα από τα πιο συνηθισμένα αέρια που χρησιμοποιούνται κυρίως σε φορητά υδροπνευματικά συστήματα αλλά και σε ρομποτικά συστήματα που χρησιμοποιούν υδραυλικά συστήματα.
Συγκολλήσεις
[Επεξεργασία | επεξεργασία κώδικα]Το διοξείδιο του άνθρακα μπορεί να χρησιμοποιηθεί για τη δημιουργία αδρανούς ατμόσφαιρας μέσα στην οποία γίνονται συγκολλήσεις, αν και στις υψηλές θερμοκρασίες που αναπτύσσονται οξειδώνει τα περισσότερα μέταλλα. Η χρήση του στην αυτοκινητοβιομηχανία είναι πολύ συνηθισμένη επειδή είναι πιο φθηνό από το αέριο αργό ή το ήλιο. Πάντως, οι συγκολλήσεις που γίνονται μέσα σε ατμόσφαιρα CO2 είναι πιο εύθραυστες από αυτές που πραγματοποιούνται σε πιο αδρανή ατμόσφαιρα, και με το πέρασμα του χρόνου εξασθενούν λόγω σχηματισμού ανθρακικού οξέος.
Απομάκρυνση καφεΐνης
[Επεξεργασία | επεξεργασία κώδικα]Το υγρό διοξείδιο του άνθρακα είναι καλός διαλύτης για πολλές λιπόφιλες οργανικές ενώσεις, και χρησιμοποιείται για την αφαίρεση καφεΐνης από τον καφέ : Αρχικά οι πράσινοι κόκκοι καφέ εμποτίζονται με νερό και τοποθετούνται στην κορυφή στήλης ύψους 21 m. Στη συνέχεια, υπερκρίσιμο διοξείδιο του άνθρακα σε υγρή μορφή (περίπου 93 °C) διοχετεύεται από το κάτω μέρος της στήλης με αποτέλεσμα η καφεΐνη να διαχέεται από τους κόκκους μέσα στο διοξείδιο του άνθρακα.
Φαρμακευτικές και άλλες χημικές διεργασίες
[Επεξεργασία | επεξεργασία κώδικα]Το διοξείδιο του άνθρακα έχει αρχίσει να χρησιμοποιείται στις φαρμακοβιομηχανίες ως λιγότερο τοξική εναλλακτική λύση στη θέση παραδοσιακών διαλυτών όπως είναι το χλωροφόρμιο (CΗCl3) ή άλλες οργανοχλωριωμένες ενώσεις. Επίσης, για τους ίδιους λόγους, χρησιμοποιείται στο ξηρό καθάρισμα των ρούχων στα στεγνοκαθαριστήρια. Στη χημική βιομηχανία, το CO2 χρησιμοποιείται για την παραγωγή ουρίας, ανθρακικών και όξινων ανθρακικών αλάτων και σαλικυλικού νατρίου.
Γεωργικές, βιολογικές και ιατρικές εφαρμογές
[Επεξεργασία | επεξεργασία κώδικα]Τα φυτά χρειάζονται το CO2 για τη φωτοσύνθεση. Λόγω της μικρής ατμοσφαιρικής του συγκέντρωσης, το CO2 είναι πρακτικά ο περιοριστικός παράγοντας της ζωής στη Γη, σε σύγκριση με άλλα δύο εξίσου σημαντικά συστατικά - το νερό και το ηλιακό φως.
Ενώ τα μη καλλιεργήσιμα ("άγρια") φυτά είναι προσαρμοσμένα στο γεγονός αυτό, μεγάλες εγκαταστάσεις - θερμοκήπια μπορούν να εμπλουτίζουν την ατμόσφαιρα με περίσσεια CO2 για τη διατήρηση της καλλιεργήσιμης χλωρίδας. Ο εμπλουτισμός με CO2 δεν πρέπει όμως να είναι υπερβολικός για να μην δηλητηριαστούν τα φυτά. Σε πολύ υψηλές συγκεντρώσεις, το διοξείδιο του άνθρακα μπορεί να είναι τοξικό για τα ζώα. Έτσι η αύξηση της συγκέντρωσης κατά 1% και άνω για αρκετές ώρες, μπορεί να εξαλείψει βλαβερά ζωύφια, αράχνες και ακάρεα στο θερμοκήπιο.
Μελετάται επίσης η διοχέτευση του διοξειδίου του άνθρακα, που προέρχεται από την ηλεκτροπαραγωγή, σε ταμιευτήρες για την ανάπτυξη φυκιών που θα μπορούσαν στη συνέχεια να μετατραπούν σε καύσιμο βιοντίζελ. Ήδη το διοξείδιο του άνθρακα χρησιμοποιείται ως η κύρια πηγή άνθρακα για τα φύκια σπιρουλίνα.
Στην ιατρική, το CO2 προστίθεται στο καθαρό οξυγόνο μέχρι ποσοστού 5% για την τόνωση της αναπνοής μετά από επεισόδια άπνοιας για να σταθεροποιηθεί η ισορροπία O2/CO2 στο αίμα.
Εφαρμογές στα λέιζερ
[Επεξεργασία | επεξεργασία κώδικα]Ο συνηθέστερος τύπος βιομηχανικού αερίου Λέϊζερ είναι το CO2.
Πολυμερή και πλαστικά
[Επεξεργασία | επεξεργασία κώδικα]Το CO2 μπορεί να συνδυαστεί με το λεμονένιο της φλούδας των πορτοκαλιών ή με άλλα εποξείδια για τη δημιουργία πολυμερών και πλαστικών.
Εξόρυξη πετρελαίου
[Επεξεργασία | επεξεργασία κώδικα]Το διοξείδιο του άνθρακα χρησιμοποιείται στην άντληση του πετρελαίου συνήθως υπό συνθήκες υπερκρίσιμες. Λειτουργεί ταυτόχρονα ως προωθητικό υπό πίεση αλλά και για να μειώσει σημαντικά το ιξώδες του πετρελαίου επιτρέποντας έτσι την καλύτερη και γρηγορότερη ροή του προς την επιφάνεια της γεώτρησης.
Χρήσεις ως ψυκτικού
[Επεξεργασία | επεξεργασία κώδικα]
Το υγρό και το στερεό διοξείδιο του άνθρακα είναι σημαντικά ψυκτικά μέσα, κυρίως στη βιομηχανία τροφίμων, όπου χρησιμοποιούνται για τη μεταφορά και αποθήκευση παγωτών και άλλων κατεψυγμένων προϊόντων. Το στερεό διοξείδιο του άνθρακα ονομάζεται "ξηρός πάγος" και χρησιμοποιείται για μικρές μεταφορές στις οποίες δεν είναι πρακτικά τα ογκώδη ψυγεία. Το υγρό διοξείδιο του άνθρακα (που ονομάζεται στη βιομηχανία R744 ή R-744) χρησιμοποιήθηκε ως ψυκτικό μέσο, πριν από την ανακάλυψη του R-12[3]. Οι φυσικές ιδιότητές του είναι ιδιαίτερα κατάλληλες για κατάψυξη ή και απλή ψύξη. Λόγω της λειτουργίας τους σε πιέσεις μέχρι 130 bar, τα ψυκτικά συστήματα που χρησιμοποιούν CO2 απαιτούν ιδιαίτερα ανθεκτικά εξαρτήματα. Στους κλιματισμούς των αυτοκινήτων, σε πάνω από το 90% του συνόλου των συνθηκών οδήγησης, το R744 λειτουργεί πιο αποτελεσματικά από τα συστήματα που χρησιμοποιούν R-134a[4]. Τα περιβαλλοντικά πλεονεκτήματα του CO2 (μη τοξικό, μη εύφλεκτο, φθηνό) θα μπορούσαν στο μέλλον να αποτελέσουν έναν καλό λόγο για την αντικατάσταση των σημερινών HFCs[5] των ψυκτικών συστημάτων των αυτοκινήτων, των σούπερ-μάρκετ κλπ.
Παραγωγή κρασιού
[Επεξεργασία | επεξεργασία κώδικα]Το διοξείδιο του άνθρακα με τη μορφή του ξηρού πάγου χρησιμοποιείται συχνά στα οινοποιεία για τη γρήγορη ψύξη των σταφυλιών με σκοπό την αποτροπή της πρόωρης ζύμωσης. Το κύριο πλεονέκτημα της χρήσης του ξηρού πάγου σε σχέση με το παγωμένο νερό είναι ότι ψύχει τα σταφύλια χωρίς προσθήκη νερού το οποίο θα μπορούσε να αραιώσει τα σάκχαρα στο γλεύκος των σταφυλιών και, κατά συνέπεια, να μειώσει τη συγκέντρωση αιθανόλης στο τελικό προϊόν. Το αέριο CO2 που προκύπτει από την εξάχνωση του ξηρού πάγου, επειδή είναι βαρύτερο από τον αέρα, συσσωρεύεται στον πυθμένα των δεξαμενών, δημιουργώντας έτσι ένα περιβάλλον που βοηθά στην καταπολέμηση των βακτηρίων, που προέρχονται από τα σταφύλια μέχρι τη στιγμή κατά την οποία θα αρχίσει η ελεγχόμενη ζύμωση.
Το διοξείδιο του άνθρακα τοποθετείται μερικές φορές στην κορυφή μπουκαλιών κρασιού ή άλλων δοχείων αποθήκευσης όπως βαρέλια για αποφυγή της οξείδωσης. Επειδή όμως υπάρχει κίνδυνος να διαλυθεί μέσα στο κρασί, αντικαθίσταται συνήθως από άλλα αέρια, όπως άζωτο ή αργό.
Έλεγχος του pH
[Επεξεργασία | επεξεργασία κώδικα]Το διοξείδιο του άνθρακα χρησιμοποιείται ως μέσο ελέγχου του pH των κολυμβητηρίων. Με τη συνεχή προσθήκη CO2 στο νερό, διατηρείται το pH σε χαμηλά επίπεδα. Ανάμεσα στα πλεονεκτήματα αυτής της πρακτικής είναι και η αποφυγή χρήσης πιο επικίνδυνων οξέων.
Το CO2 στην ατμόσφαιρα
[Επεξεργασία | επεξεργασία κώδικα]
Από το ανθρωπογενές CO2 που εκπέμπεται από τα ορυκτά καύσιμα: 50% διαλύεται στους ωκεανούς και απορροφάται από τα επίγεια οικοσυστήματα και το 50% διοχετεύεται στην ατμόσφαιρα.
Το διοξείδιο του άνθρακα στη γήινη ατμόσφαιρα θεωρείται ιχνοστοιχείο με μέση συγκέντρωση περίπου 385 ppm. Η συνολική μάζα των ατμοσφαιρικών εκπομπών διοξειδίου του άνθρακα είναι περίπου 3×1015 kg (3000 γιγατόνοι). Η συγκέντρωση κυμαίνεται εποχικά (βλέπε διάγραμμα) αλλά και σε περιφερειακή βάση. Η διακύμανση αυτή οφείλεται κατά κύριο λόγο στην εποχική ανάπτυξη των φυτών στο Βόρειο Ημισφαίριο. Οι συγκεντρώσεις του διοξειδίου του άνθρακα στο βορρά μειώνονται κατά τη διάρκεια της άνοιξης και του καλοκαιριού καθώς το καταναλώνουν τα φυτά και αυξάνονται το φθινόπωρο και το χειμώνα όταν τα φυτά πεθαίνουν και αποσυνθέτονται. Στις αστικές περιοχές οι συγκεντρώσεις είναι γενικά υψηλότερες.
Πεντακόσια εκατομμύρια χρόνια πριν, το διοξείδιο του άνθρακα ήταν 20 φορές περισσότερο από ό,τι σήμερα. Κατά τη διάρκεια της Ιουράσιας Περιόδου, μειώθηκε κατά 4 έως 5 φορές, στη συνέχεια παρατηρήθηκε αργή μείωση και μετά πριν 49 εκατομμύρια χρόνια περίπου, ταχεία μείωση.
Οι ανθρώπινες δραστηριότητες, όπως η καύση ορυκτών καυσίμων και η αποψίλωση των δασών έχουν προκαλέσει αύξηση της ατμοσφαιρικής συγκέντρωσης του διοξειδίου του άνθρακα κατά περίπου 35% από την αρχή της εποχής της εκβιομηχάνισης.
Έως και το 40% των αερίων που εκπέμπονται από ορισμένες ηφαιστειακές δραστηριότητες είναι διοξείδιο του άνθρακα. Εκτιμάται ότι τα ηφαίστεια απελευθερώνουν περίπου 130-230 εκατομμύρια τόνους CO2 στην ατμόσφαιρα κάθε χρόνο. Το διοξείδιο του άνθρακα παράγεται επίσης από θερμές πηγές όπως αυτές στο Bossoleto κοντά στην Τοσκάνη της Ιταλίας. Στην κυκλική αυτή τοποθεσία με διάμετρο περίπου 100 μέτρα, οι τοπικές συγκεντρώσεις του CO2 αυξάνονται σε ποσοστό πάνω από 75% μέσα σε μια νύχτα και είναι αρκετές για να σκοτώσουν τα έντομα και τα μικρά ζώα της περιοχής.
Οι εκπομπές του CO2 από τις ανθρώπινες δραστηριότητες ανέρχονται σήμερα περίπου σε 27 δισεκατομμύρια τόνους ετησίως και είναι πολύ μεγαλύτερες από τις ποσότητες που εκλύονται από τα ηφαίστεια.
Το CO2 θεωρείται αέριο θερμοκηπίου, αφού διαπερνάται από το ορατό φως αλλά απορροφά έντονα στην υπέρυθρη και εγγύς υπέρυθρη περιοχή του φάσματος.
Η ορυκτολογική δέσμευση του διοξειδίου του άνθρακα είναι φυσική μέθοδος δέσμευσης του CO2 σε στερεά ορυκτά, όπως μαγνησίτη (MgCO3), ασβεστίτη (CaCO3) και δολομίτη (CaMg(CO3)2). Τα τελευταία παραμένουν σταθερά για χιλιάδες έως εκατομμύρια χρόνια, εξασφαλίζοντας τη μη διαρροή του CO2 πίσω στην ατμόσφαιρα της Γης. Για το λόγο αυτό, η συγκεκριμένη μέθοδος θεωρείται από πολλούς επιστήμονες ως η ασφαλέστερη μέθοδος αποθήκευσης CO2 με σκοπό την εξισορρόπηση της παγκόσμιας κλιματικής αλλαγής. Η διαδικασία αυτή λαμβάνει χώρα στη φύση με πολύ αργούς ρυθμούς, επομένως τα τελευταία χρόνια σκοπός πολλών επιστημονικών ερευνών είναι να μιμηθούν και να επιταχύνουν αυτό που κάνει η φύση από μόνη της, στα πλαίσια της εξισορρόπησης της υπερθέρμανσης του πλανήτη.
Το CO2 στους ωκεανούς
[Επεξεργασία | επεξεργασία κώδικα]Η διάλυση του άνθρακα στους ωκεανούς με τη μορφή CO2, H2CO3 και ιόντων HCO3- και CO32- είναι περίπου 50 φορές μεγαλύτερη από ότι στην ατμόσφαιρα. Οι ωκεανοί ενεργούν ως μία τεράστια δεξαμενή άνθρακα, και δέχονται περίπου το ένα τρίτο των εκπομπών CO2 από τις ανθρώπινες δραστηριότητες. Η διαλυτότητα του CO2 μειώνεται καθώς η θερμοκρασία του νερού αυξάνεται.
Ένα μέρος του διαλυμένου CO2 στους ωκεανούς καταναλώνεται για τη φωτοσύνθεση από οργανισμούς στο νερό, και ένα μικρό ποσοστό συντηρεί τον κύκλο του άνθρακα. Η αύξηση του CO2 στην ατμόσφαιρα έχει οδηγήσει σε αύξηση της οξύτητας του θαλασσινού νερού και υπάρχει ανησυχία ότι αυτό μπορεί να επηρεάσει αρνητικά οργανισμούς με κελύφη που ζουν στο νερό, αφού είναι γνωστό ότι τα οξέα διαλυτοποιούν το ανθρακικό ασβέστιο από το οποίο είναι φτιαγμένο το κέλυφος.
Βιολογικός ρόλος του CO2
[Επεξεργασία | επεξεργασία κώδικα]Το διοξείδιο του άνθρακα είναι τελικό προϊόν του μεταβολισμού των οργανισμών που παίρνουν την ενέργειά τους από τη διάσπαση με οξυγόνο των σακχάρων, των λιπών και των αμινοξέων με μια διαδικασία που είναι γνωστή ως κυτταρική αναπνοή. Στους οργανισμούς αυτούς περιλαμβάνονται όλα τα φυτά και τα ζώα, πολλοί μύκητες και ορισμένα βακτήρια. Στους ανώτερους οργανισμούς, το διοξείδιο του άνθρακα μεταφέρεται με το αίμα από τους ιστούς του σώματος στους πνεύμονες, από όπου και εκπνέεται.
Ο ρόλος του CO2 στη φωτοσύνθεση και στις φυτικές λειτουργίες
[Επεξεργασία | επεξεργασία κώδικα]
CO2 + H2Ο → Γλυκόζη + Ο2
Φωτοσύνθεση είναι η διαδικασία κατά την οποία τα φυτά που περιέχουν χλωροφύλλη, με τη βοήθεια του φωτός και με αρχικά αντιδρώντα το νερό και το CO2, μετατρέπουν ανόργανες ουσίες σε τροφή. Πρόκειται για μια φυσιολογική λειτουργία με την οποία τα πράσινα φυτά προμηθεύονται τον άνθρακα και το οξυγόνο, που είναι απαραίτητα για τη θρέψη τους. Η φωτοσύνθεση είναι μια εξώθερμη διαδικασία, η συνολική χημική αντίδραση της οποίας είναι : 6CO2 + 6H2Ο → C6H12O6 + 6O2 + 2817 KJ.
Ο μηχανισμός της φωτοσύνθεσης σε γενικές γραμμές είναι ο ακόλουθος: το νερό διαλύει και μεταφέρει το διοξείδιο του άνθρακα μέχρι τα κύτταρα και τους χλωροπλάστες των φύλλων. Εκεί με την ενέργεια του φωτός που απορροφά η χλωροφύλλη, διασπάται το νερό στα στοιχεία του. Το οξυγόνο απελευθερώνεται, ενώ το ατομικό υδρογόνο δεσμεύεται από διάφορα ένζυμα. Έπειτα το υδρογόνο συμμετέχει στις αντιδράσεις με το διοξείδιο του άνθρακα: CΟ2 + |Η| → (CΗ2Ο)x. Στο δεύτερο στάδιο αντιδράσεων δε χρειάζεται ηλιακή ενέργεια, γι' αυτό οι αντιδράσεις αυτές ονομάζονται "σκοτεινές". Με λίγα λόγια, οι χλωροπλάστες, με την βοήθεια του φωτός και του CO2, παράγουν οξυγόνο και ενέργεια απορροφώντας CO2 κατά την φωτοπερίοδο η οποία δεν θα πρέπει να ξεπερνά τις 12 ώρες ημερησίως. Τις υπόλοιπες ώρες απορροφούν οξυγόνο και παράγουν CO2.
Έχει αποδειχθεί ότι τα φυτά μπορούν να αναπτυχθούν μέχρι και 50% ταχύτερα σε συγκεντρώσεις 1000 ppm CO2. Ορισμένοι επιστήμονες πιστεύουν ότι αν αυξηθεί η συγκέντρωση CO2 στην ατμόσφαιρα, αυτό θα οδηγήσει σε ταχύτερη ανάπτυξη των φυτών και, επομένως, σε αύξηση της παραγωγής τροφίμων. Μελέτες όμως έχουν δείξει ότι η αύξηση των εκπομπών CO2 οδηγεί σε μείωση της χρήσης του νερού από τα φυτά και σε ελάττωση της συγκέντρωσης των ιχνοστοιχείων σ' αυτά. Αυτό μπορεί να έχει αλυσιδωτές συνέπειες σε άλλους οργανισμούς των οικοσυστημάτων, όπως τα φυτοφάγα ζώα τα οποία θα πρέπει να τρώνε περισσότερο για να αποκτήσουν την ίδια ποσότητα πρωτεϊνών.
Τα φυτά εκπέμπουν CO2 κατά τη διαδικασία της αναπνοής. Αν και τα δάση θα μπορούσαν να απορροφήσουν πολλούς τόνους CO2 κάθε χρόνο, μελέτες αναφέρουν ότι ένα ώριμο δάσος παράγει τόσο πολύ CO2 κατά την αναπνοή και την αποσύνθεση των νεκρών δένδρων, όσο χρησιμοποιείται στην βιοσύνθεση και στην καλλιέργεια των φυτών.
Τοξικότητα του CO2 - Επιδράσεις στο νευρικό σύστημα
[Επεξεργασία | επεξεργασία κώδικα]Η περιεκτικότητα του καθαρού αέρα σε CO2 (κατά μέσο όρο μεταξύ της στάθμης της θάλασσας και μέχρι ύψους περίπου 30 χλμ.) κυμαίνεται από 0,036 % (360 ppm) έως και 0,039% (390 ppm), ανάλογα με την τοποθεσία.
Η παρατεταμένη έκθεση σε μέτριες συγκεντρώσεις μπορεί να προκαλέσει οξέωση και να έχει αρνητικές συνέπειες για το μεταβολισμό του ασβεστίου και του φωσφόρου. Το διοξείδιο του άνθρακα είναι τοξικό για την καρδιά και προκαλεί αρρυθμίες.
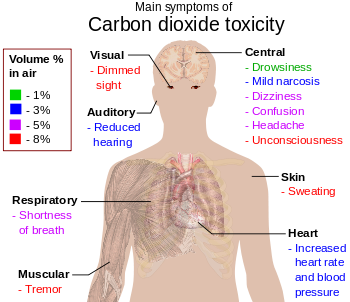
Η τοξικότητα και οι επιπτώσεις της αυξάνονται με την αύξηση της περιεκτικότητας του αέρα σε CO2 :
- Σε περιεκτικότητα 1% v/v[6] (γεμάτη αίθουσα με κακό εξαερισμό), το CO2 μπορεί σε παρατεταμένη έκθεση να προκαλέσει υπνηλία.
- Σε περιεκτικότητα 2% v/v το CO2 συμπεριφέρεται ως ήπιο ναρκωτικό. Προκαλεί αυξημένη αρτηριακή πίεση και καρδιακό ρυθμό, και μειώνει την ακοή.
- Σε περιεκτικότητα περίπου 5% v/v προκαλεί διέγερση του αναπνευστικού κέντρου, ζάλη, σύγχυση και δυσκολία στην αναπνοή συνοδευόμενη από κεφαλαλγία και δύσπνοια.
- Σε περιεκτικότητα 8% v/v προκαλεί κεφαλαλγία, εφίδρωση, παραισθήσεις, τρέμουλο και απώλεια συνείδησης μετά την έκθεση για πέντε έως δέκα λεπτά.
Το 1984 στη λίμνη Monoun του Καμερούν αναφέρθηκαν 37 θάνατοι που οφείλονταν σε τοπικά πολύ υψηλές συγκεντρώσεις CO2, το οποίο παράχθηκε από την διατάραξη της λίμνης που ήταν κορεσμένη σε CO2. Το 1986 στη λίμνη Nyos πάλι στο Καμερούν αναφέρθηκαν 1700 θάνατοι από τα ίδια αίτια.
Λόγω των κινδύνων για την υγεία που συνδέονται με την έκθεση σε CO2, ο Οργανισμός Επαγγελματικής Ασφάλειας και Υγείας των Η.Π.Α., αναφέρει ότι η μέση έκθεση για υγιείς ενήλικες κατά την οκτάωρη εργασίας δεν πρέπει να υπερβαίνει τα 5000 ppm (0,5%). Το μέγιστο επίπεδο ασφάλειας για βρέφη, παιδιά, ηλικιωμένους και άτομα με προβλήματα υγείας είναι σημαντικά μικρότερη. Για βραχυπρόθεσμες (κάτω των δέκα λεπτών) εκθέσεις, το όριο είναι 30000 ppm (3 %). Αν οι συγκεντρώσεις CO2 υπερβαίνουν το 4% είναι άμεσα επικίνδυνες για την υγεία.
Η προσαρμογή σε αυξημένα ποσοστά CO2 μεταβάλλεται από άνθρωπο σε άνθρωπο. Η συνεχής παραμονή σε ατμόσφαιρα με CO2 μπορεί γίνει ανεκτή σε περιεκτικότητες 3 % τουλάχιστον για ένα μήνα και 4 % για πάνω από μια εβδομάδα. Υποστηρίχθηκε ότι συγκεντρώσεις 2 % θα μπορούσαν να γίνουν ανεκτές σε κλειστούς χώρους (π.χ. υποβρύχια), δεδομένου ότι η προσαρμογή είναι φυσιολογική και αναστρέψιμη. Μάλιστα δεν θα παρατηρηθεί μείωση της απόδοσης στην εργασία ή σε κανονική σωματική δραστηριότητα.
Συγκεντρώσεις CO2 μεταξύ 300 ppm και 2500 ppm, χρησιμοποιούνται ως δείκτες ποιότητας αέρα σε εσωτερικούς χώρους. Σε κλειστούς χώρους με πολλούς ανθρώπους, συγκεντρώσεις μεγαλύτερες από 1000 ppm θα προκαλέσουν δυσφορία σε ποσοστό πάνω από το 20 % των ανθρώπων. Σε 2000 ppm, η πλειοψηφία των ανθρώπων, θα αισθανθεί σε σημαντικό βαθμό ενόχληση, και πολλοί θα υποφέρουν από ναυτία και πονοκεφάλους.
Παλιότερα, η ύπαρξη CO2 σε χώρους όπου ζυμωνόταν το κρασί ή σε ορυχεία, γινόταν αντιληπτή από την τοξικότητά του : Οι εργάτες τοποθετούσαν στο πάτωμα του χώρου ένα κλουβί με καναρίνι που είναι πιο ευαίσθητο από τον άνθρωπο. Το CO2 επειδή είναι βαρύτερο από τον αέρα, συσσωρεύονταν στα χαμηλά σημεία και αν το καναρίνι δηλητηριαζόταν, ο χώρος περιείχε αυξημένα ποσοστά CO2.
Από τις αρχές του 20ού αιώνα νευρολόγοι και ψυχίατροι είχαν διαπιστώσει ότι το διοξείδιο του άνθρακα επιδρά αρνητικά στο νευρικό σύστημα, προκαλώντας έντονη αγωνία και φόβο, έως και κρίσεις πανικού. Μέχρι το 2009 όμως δεν είχαν καταφέρει να βρουν μια ικανοποιητική νευροβιολογική εξήγηση του φαινομένου. Πρόσφατα μια ομάδα επιστημόνων από το Πανεπιστήμιο της Αϊόβα, στις ΗΠΑ, ανακάλυψε ότι ρόλο-κλειδί σε αυτήν τη διαδικασία κατέχει μια πρωτεΐνη, η λεγόμενη ASIC1a. Η πρωτεΐνη αυτή υπάρχει σε αφθονία στην αμυγδαλή, μια περιοχή του εγκεφάλου η οποία, μαζί με άλλες εγκεφαλικές δομές, συναποτελεί το μεταιχμιακό σύστημα του εγκεφάλου, έναν από τους βασικούς ρυθμιστές ανώτερων ψυχικών λειτουργιών όπως τα συναισθήματα και η συμπεριφορά. Κάνοντας πειράματα με ποντικούς, οι ερευνητές διαπίστωσαν ότι όταν το εγκεφαλικό περιβάλλον γινόταν πιο όξινο η παραγωγή της πρωτεΐνης ASIC1a αυξανόταν στην αμυγδαλή, προκαλώντας συμπεριφορές με τυπικά φοβικά χαρακτηριστικά. Αντίθετα, όταν εξουδετερωνόταν η δράση της συγκεκριμένης πρωτεΐνης, οι συμπεριφορές αυτές δεν εκδηλώνονταν.
Δεδομένου ότι μία από τις βασικές συνέπειες της εισπνοής διοξειδίου του άνθρακα είναι η αύξηση της οξίνισης του εγκεφαλικού περιβάλλοντος, και συνεπώς η άμεση παραγωγή της πρωτεΐνης ASIC1a, οι ερευνητές συμπέραναν ότι για τις κρίσεις πανικού που συνοδεύουν την εισπνοή μεγάλης ποσότητας διοξειδίου του άνθρακα θα πρέπει να ευθύνεται η υψηλή συγκέντρωση της συγκεκριμένης πρωτεΐνης. Πιστεύουν, μάλιστα, ότι ανακαλύπτοντας την ακριβή δράση αυτής της πρωτεΐνης θα μπορέσουν να ερμηνεύσουν και ένα άλλο σχετικό φαινόμενο, την αγχολυτική και άκρως χαλαρωτική επίδραση των αναπνευστικών ασκήσεων.
To CO2 στην ανθρώπινη φυσιολογία
[Επεξεργασία | επεξεργασία κώδικα]To CO2 μεταφέρεται στο αίμα με τρεις διαφορετικούς τρόπους. (Τα ακριβή ποσοστά διαφέρουν ανάλογα με το αν το αίμα είναι φλεβικό ή αρτηριακό) :
- Το μεγαλύτερο μέρος του CO2 (περίπου 70% - 80%), μετατρέπεται σε όξινα ανθρακικά ιόντα (HCO3-) στα ερυθρά αιμοσφαίρια με την αντίδραση : CO2 + H2Ο ⇄ H2CO3 ⇄ H+ + HCO3-.
- Ποσοστό 5% - 10% διαλύεται στο πλάσμα.
- Ποσοστό 5% - 10% είναι συνδεδεμένο με την αιμοσφαιρίνη.
Η αιμοσφαιρίνη, το κύριο μόριο-μεταφορέας οξυγόνου στα ερυθρά αιμοσφαίρια, μεταφέρει και Ο2 και CO2. Ωστόσο, το CO2 δεσμεύεται στο μόριο της αιμοσφαιρίνης σε διαφορετικό μέρος από το Ο2. Όταν η δέσμευση του Ο2 είναι αυξημένη, ελαττώνεται η ποσότητα του CO2 που δεσμεύεται στην αιμοσφαιρίνη και αντιστρόφως εξαιτίας του αλλοστερικού φαινομένου. Το CO2 απομακρύνεται από το ανθρώπινο σώμα με τον εξής μηχανισμό : Η γλυκόζη οξειδώνεται στα κύτταρα σύμφωνα με το σχήμα : C6H12O6 + 6O2 ⇄ 6CO2 + 6H2Ο + Ενέργεια. Το παραγόμενο CO2 διαλύεται στο νερό και δίνει ανθρακικό οξύ : CO2 + H2Ο ⇄ H2CO3. Το οξύ σύντομα διαχέεται έξω από τα τριχοειδή αγγεία και όταν φθάσει στο αίμα εξουδετερώνεται εν μέρει από το ανθρακικό νάτριο, που υπάρχει εκεί : Na2CO3 + H2CO3 ⇄ 2NaHCO3 (Ι).
Στους πνεύμονες η αντίδραση γίνεται αντίστροφα. Το H2CO3 διαχέεται στις κυψελίδες και διασπάται σε νερό και CO2, το οποίο εμπνέεται. Η απομάκρυνση όμως μιας ποσότητας H2CO3, μετατοπίζει την ισορροπία (Ι) προς τα αριστερά με συνέπεια να διασπάται νέα ποσότητα NaHCO3 προς Na2CO3 και H2CO3 και η διαδικασία συνεχίζεται.
Συνήθως ο αέρας της εκπνοής περιέχει 4 % έως 5 % περισσότερο CO2 και 4 % έως 5 % λιγότερο Ο2 από τον αέρα της εισπνοής. Η αναπνοή ενός ανθρώπου παράγει περίπου 1 Kg CO2 κάθε μέρα.
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Είναι η ενέργεια που απαιτείται για να διασπαστεί ο δεσμός. Αποτελεί μέτρο της ισχύος ενός χημικού δεσμού.
- ↑ Πώς το διοξείδιο του άνθρακα δίνει γεύση στα αναψυκτικά Αρχειοθετήθηκε 2009-10-19 στο Wayback Machine., in.gr
- ↑ Διφθορο-διχλωρο-μεθάνιο, CF2Cl2 πιο γνωστό ως FREON-12, Χρησιμοποιήθηκε στους κλιματισμούς των αυτοκινήτων πριν το 1995.
- ↑ 1,1,1,2-τετραφθορο-αιθάνιο, F3C-CFH2, Genetron 134a, Suva 134a ή και HFC-134a. Ψυκτικό που αντικατέστησε τη δεκαετία του 1990 το R-12.
- ↑ Φθοριωμένοι υδρογονάνθρακες. Αντικατέστησαν στα συστήματα ψύξης τους CFCs που περιείχαν και χλώριο.
- ↑ % v/v ή % κ.ό. (% όγκο κατ' όγκο). Έκφραση περιεκτικότητας που χρησιμοποιείται κυρίως στα αέρια μίγματα και δηλώνει τα mL ενός αερίου σε 100 mL αερίου μίγματος.
Πηγές
[Επεξεργασία | επεξεργασία κώδικα]- Βασιλικιώτης Γ.Σ.: Χημεία Περιβάλλοντος, Θεσσαλονίκη 1986
- Μανωλκίδης Κ., Μπέζας Κ.: Χημικές Αντιδράσεις, Αθήνα 1976
- Γιαννακουδάκης Δ.Α.: Φυσική Χημεία Καταστάσεων της Ύλης και Θερμοδυναμική, Θεσσαλονίκη 1986
- Αλεξάνδρου Ν.Ε.: Γενική Οργανική Χημεία, Δομή-Φάσματα-Μηχανισμοί, Τόμοι 1ος και 2ος, Θεσσαλονίκη 1985
- Morrison R.T., Boyd R.N.: Οργανική Χημεία, Τόμοι 1ος,2ος,3ος, μετάφραση Σακαρέλλος-Πηλίδης-Γεροθανάσης, Ιωάννινα 1991
- Meislich H., Nechamkin H., Sharefkin J.: Οργανική Χημεία, μετάφρ. Α. Βάρβογλης, Αθήνα 1983
- Murell J.N., Kettle S.F.A., Tedder J.N.: Ο Χημικός Δεσμός, μετάφρ.Σ. Φαράντος, Ηράκλειο 1992
- Γεωργάτσος Ι.Ε.: Βιοχημεία, Τόμος Β', Ενδιάμεση Ανταλλαγή της Ύλης-Μοριακή Πληροφορική, Θεσσαλονίκη 1985
- Τσίπης Κ.Α.: Εισαγωγή στην Κβαντική Χημεία, Τόμος Ι, Στοιχειώδης Μεθοδολογία και Ατομική Δομή, Θεσσαλονίκη 1984
- Μπόσκου Δ.: Χημεία τροφίμων με Στοιχεία Τεχνολογίας Τροφίμων, Θεσσαλονίκη 1986
- Βασιλικιώτης Γ.Σ.: Ποσοτική Ανάλυση, Θεσσαλονίκη 1980
- Μπαζάκης Ι.Α.: Γενική Χημεία, Αθήνα
- Pople J.A., Beveridge D.L.: Approximate Molecular Orbital Theory, Νέα Υόρκη 1970
- Szabo A., Ostlund N.: Modern Quantum Chemistry, Νέα Υόρκη 1982
- Μανουσάκης Γ.Ε.: Γενική και Ανόργανη Χημεία, Τόμοι 1ος και 2ος, Θεσσαλονίκη 1981
- Μανωλκίδης Κ., Μπέζας Κ.: Στοιχεία Ανόργανης Χημείας, Έκδοση 14η, Αθήνα 1984
Εξωτερικοί σύνδεσμοι
[Επεξεργασία | επεξεργασία κώδικα]- 3-D δονήσεις του CO2
- Πρόσθετο Ε290 - Το CO2 στα τρόφιμα
- Φυσικοχημικά δεδομένα για το CO2
- Θερμοδυναμικά κ.ά. στοιχεία για το CO2
- Πληροφορίες για τον ξηρό πάγο
- Φαινόμενο του θερμοκηπίου
- Παγκόσμια θέρμανση

