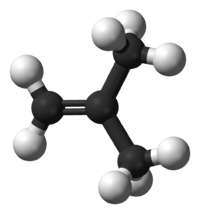
Μεθυλοπροπένιο
| Μεθυλοπροπένιο | |||
|---|---|---|---|

| |||

| |||
| |||
| Γενικά | |||
| Όνομα IUPAC | Μεθυλοπροπένιο | ||
| Άλλες ονομασίες | ισοβουτυλένιο γ-βουυλένιο 1,1-διμεθυλαιθυλένιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C4H8 | ||
| Μοριακή μάζα | 56,11 amu | ||
| Σύντομος συντακτικός τύπος |
(CH3)2C=CH2 | ||
| Συντομογραφίες | Me2C=CH2 | ||
| Αριθμός CAS | 115-11-7 | ||
| SMILES | CC(=C)C | ||
| InChI | 1/C4H8/c1-4(2)3/h1H2,2-3H3 | ||
| Αριθμός EINECS | 204-066-3 | ||
| Αριθμός RTECS | UD0890000 | ||
| Αριθμός UN | 1055 (υγρό 1075) | ||
| PubChem CID | 8255 | ||
| ChemSpider ID | 7957 | ||
| Δομή | |||
| Είδος δεσμού | CNo1,1'-H: σ(2sp3-1s) CNo2,No3-H: σ(2sp2-1s) C=C: σ(2sp2-2sp2) π(2p-2p) C-C: σ(2sp2-2sp3) | ||
| Πόλωση δεσμού | C--H+: 3% | ||
| Μοριακή γεωμετρία | Επίπεδη εκτός μεθυλίων | ||
| Ισομέρεια | |||
| Ισομερή θέσης | 4 Βουτένιο-1 (CH3CH=CHCH3) Ε,Ζ-Βουτένιο-2 (CH3CH=CHCH3 Κυκλοβουτάνιο ( Μεθυλοκυκλοπροπάνιο ( | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | −140,3 °C | ||
| Σημείο βρασμού | -6,9 °C | ||
| Εμφάνιση | Άχρωμο αέριο | ||
| Χημικές ιδιότητες | |||
| Θερμότητα πλήρους καύσης |
2.628 kJ | ||
| Βαθμός οκτανίου | 106,3[1] | ||
| Επικινδυνότητα | |||

| |||
| Εξαιρετικά εύφλεκτο (F+) | |||
| Κίνδυνοι κατά NFPA 704 |
|||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Το μεθυλοπροπένιο[2] ή ισοβουτυλένιο ή γ-βουτυλένιο είναι ένα αλκένιο με σημαντική βιομηχανική σπουδαιότητα. Είναι ένα από τα τέσσερα (4) ισομερή βουτένια. Με βάση το χημκικό του τύπο (C4H8) είναι ισομερές θέσης με τις ακόλουθες τέσσερεις (4) ενώσεις:
- Βουτένιο-1
- Ε,Ζ-βουτένιο-2 (με 2 γεωμερικά ισομερή) και
- Κυκλοβουτάνιο
- Μεθυλοκυκλοπροπάνιο
Ονοματολογία
[Επεξεργασία | επεξεργασία κώδικα]Η ονομασία «μεθυλοπροπένιο» από την ονοματολογία κατά IUPAC. Συγκεκριμένα, το αρχικό πρόθεμα «μεθυλο-»[3] δηλώνει την παρουσία διακλάδωσης ενός (1) ατόμου άνθρακα, το τμήμα «προπ-» δηλώνει την παρουσία τριών (3) ατόμων άνθρακα στην κύρια ανθρακική αλυσίδα της ένωσης, το ενδιάμεσο «-εν-» δείχνει την παρουσία ενός (1) διπλού δεσμού μεταξύ ατόμων άνθρακα στο μόριο και η κατάληξη «-ιο» φανερώνει ότι δεν περιέχει χαρακτηριστικές ομάδες, δηλαδή ότι είναι υδρογονάνθρακας.
Δομή
[Επεξεργασία | επεξεργασία κώδικα]Αυτός ο υδρογονάνθρακας έχει μόριο που αποτελείται από δύο (2) άτομα υδρογόνου και δύο (2) μεθύλια ενωμένα με ένα ζεύγος ατόμων άνθρακα που συνδέονται μεταξύ τους με ένα διπλό δεσμό. Όλα αυτά τα έξι (6) συνολικά άτομα [2 υδρογόνου + 4 άνθρακα (τα 2 με το διπλό δεσμό + 2 από τα 3 μεθύλια)] είναι ομοεπίπεδα. Η γωνία είναι 119°, δηλαδή πολύ κοντά στις 120° που προβλέπονται για τον sp2 υβριδισμό των ατόμων άνθρακα, που συνδέονται με διπλό δεσμό. Η περιστροφή του δεσμού C=C απαιτεί (σχετικά) υψηλή ποσότητα ενέργειας, γιατί απαιτεί την (προσωρινή) διάσπαση του π-δεσμού.
Ο π-δεσμός στο μόριο του προπενίου είναι υπεύθυνος για τη χρήσιμη δραστικότητά του. Ή περιοχή του διπλού δεσμού χαρακτηρίζεται από (σχετικά) υψηλή ηλεκτρονιακή πυκνότητα, που επομένως είναι ευάλωτη σε επιδράσεις ηλεκτρονιόφιλων. Πολλές αντιδράσεις του προπενίου καταλύνται από διάφορα μέταλλα μετάπτωσης, που σχηματίζουν προσωρινά σύμπλοκα με τα π και π* τροχιακά του προπενίου.
| Δεσμοί[4] | ||||
| Δεσμός | τύπος δεσμού | ηλεκτρονική δομή | Μήκος δεσμού | Ιονισμός |
|---|---|---|---|---|
| C#3,#1΄-H | σ | 2sp3-1s | 109 pm | 3% C- H+ |
| C#1,#2-H | σ | 2sp2-1s | 108,7 pm | 3% C- H+ |
| C#3-C#2 | σ | 2sp3-2sp2 | 151 pm | |
| C#3-C#1΄ | σ | 2sp3-2sp2 | 151 pm | |
| C=C | σ | 2sp2-2sp2 | 133,9 pm | |
| C=C | π | 2p-2p | 133,9 pm | |
| Κατανομή φορτίων σε ουδέτερο μόριο | ||||
| C#3,#1΄ | -0,09 | |||
| C#1 | -0,06 | |||
| C#2 | 0,00 | |||
| H | +0,03 | |||
Παραγωγή
[Επεξεργασία | επεξεργασία κώδικα]Με αφυδάτωση αλκανολών
[Επεξεργασία | επεξεργασία κώδικα]Με ενδομοριακή αφυδάτωση μεθυλοπροπανόλης-1 ή μεθυλοπροπανόλης-1 παράγεται μεθυλοπροπένιο. Η αντίδραση ευνοείται σε σχετικά υψηηλές θερμοκρασίες, >150 °C[5]:
1.
2.
Με απόσπαση υδραλογόνου
[Επεξεργασία | επεξεργασία κώδικα]Με απόσπαση υδραλογόνου (HX) από ισοβουτυλοαλογονίδιο ή τ.βουτυλοαλογονίδιο παράγεται μεθυλοπροπένιο[6]:
1.
2.
Με απόσπαση αλογόνου
[Επεξεργασία | επεξεργασία κώδικα]Με απόσπαση αλογόνου (X2) από 1,2-διαλομεθυλοπροπάνιο παράγεται μεθυλοπροπένιο[7]:
Με καταλυτική αφυδρογόνωση αλκανίων
[Επεξεργασία | επεξεργασία κώδικα]Με καταλυτική αφυδρογόνωση ισοβουτανίου, παράγεται μεθυλοπροπένιο:
- Όπου .
Με θέρμανση τεταρτοταγών αμμωνιακών αλάτων
[Επεξεργασία | επεξεργασία κώδικα]Με θέρμανση τεταρτοταγών αμμωνιακών αλάτων (μέθοδος Hoffmann) παράγεται και μεθυλοπροπένιο. Π.χ[5].
Με επίδραση φωσφοροϋλιδίων σε καρβονυλικές ενώσεις
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση φωσφοροϋλιδίου σε μεθανάλη (μέθοδος Wittig) παράγεται μεθυλοπροπένιο:. Π.χ.[8]:
Παράγωγα
[Επεξεργασία | επεξεργασία κώδικα]Τέλεια καύση
[Επεξεργασία | επεξεργασία κώδικα]
Ενυδάτωση
[Επεξεργασία | επεξεργασία κώδικα]1. Επίδραση θειικού οξέος και στη συνέχεια νερού (ενυδάτωση). Παράγεται μεθυλοπροπανόλη-2[9]:
2. Υδροβορίωση και στη συνέχεια επίδραση με υπεροξείδιο του υδρογόνου. Παράγεται ισοβουτυλοβοράνιο και στη συνέχεια μεθυλοπροπανόλη-1[10]:
- Προσθήκη διβορανίου έχει το ίδιο αποτέλεσμα.
3. Αντίδραση με οξικό υδράργυρο και έπειτα αναγωγή. Παράγεται μεθυλοπροπανόλη-2:
4. Υπάρχει ακόμη η δυνατότητα αλλυλικής υδροξυλίωσης κατά Prins με επίδραση αλδευδών ή κετονών σε μεθυλοπροπένιο απουσία νερού. Π.χ. με μεθανάλη προκύπτει 3-μεθυλοβουτεν-2-όλη-1:
Προσθήκη υποαλογονώδους οξέως
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση (προσθήκη) υποαλογονώδους οξέος (HOX) σε μεθυλοπροπένιο παράγεται 1-αλο-μεθυλοπροπανόλη-2[11]:
- Το HOX παράγεται συνήθως επιτόπου με την αντίδραση:
Καταλυτική υδρογόνωση
[Επεξεργασία | επεξεργασία κώδικα]Με καταλυτική υδρογόνωση μεθυλοπροπένιο σχηματίζεται ισοβουτάνιο. Π.χ.[12]:
Αλογόνωση
[Επεξεργασία | επεξεργασία κώδικα]1. Με προσθήκη αλογόνου (X2) (αλογόνωση) σε μεθυλοπροπένιο έχουμε προσθήκη στο διπλό δεσμό. Παράγεται 1,2-διαλομεθυλοπροπάνιο. Π.χ.[13]::
2. Υποκατάσταση σε αλλυλική θέση, δηλαδή σε α θέση ως προς το διπλό δεσμό. Παράγεται 1-αλο-μεθυλοπροπένιο: Π.χ.:
- Η αλλυλική υποκατάσταση ευνοείται με ορισμένα ειδικά αντιδραστήρια αλογόνωσης ή σε υψηλές θερμοκρασίες.
Υδραλογόνωση
[Επεξεργασία | επεξεργασία κώδικα]Με προσθήκη υδραλογόνων (HX) (υδραλογόνωση) σε μεθυλοπροπένιο[14]:
1. Με τον πολικό μηχανισμό. Παράγεται τ.βουτυλαλογονίδιο:
2. Με το μηχανισμό ελευθέρων ριζών. Παράγεται ισοβουτυλαλογονίδιο:
Καταλυτική αμμωνίωση
[Επεξεργασία | επεξεργασία κώδικα]1. Προσθήκη αμμωνίας (NH3). Παράγεται τ. βουτυλαμίνη. Π.χ.:
- Τα παραπάνω μέταλλα που αναφέρονται στη θέση του καταλύτη χρησιμοποιούνται με τη μορφή συμπλόκων τους και όχι σε μεταλλική μορφή.
2. Προσθήκη πρωτοταγούς αμίνης. Παράγεται δευτεροταγής δ. βουτυλαμίνη. Π.χ. με μεθυλαμίνη παράγεται τ. βουτυλομεθυλαμίνη:
3. Προσθήκη δευτεροταγούς αμίνης. Παράγεται τριτοταγής δ. βουτυλαμίνη. Π.χ. με διμεθυλαμίνη παράγεται τ. βουτυλοδιμεθυλαμίνη:
Καταλυτική φορμυλίωση
[Επεξεργασία | επεξεργασία κώδικα]Με προσθήκη μεθανάλης (CO + H2) σε μεθυλοπροπένιο παράγεται διμεθυλοπροπανάλη ή μεθυλοβουτανάλη. Π.χ.:
- Τα παραπάνω μέταλλα που αναφέρονται στη θέση του καταλύτη χρησιμοποιούνται με τη μορφή συμπλόκων τους και όχι σε μεταλλική μορφή.
- Όπου . Εξαρτάται από την επιλογή του καταλύτη. Οι σχετικά ογκώδεις καταλύτες ευνοούν το δεύτερο παραγωγο.
Προσθήκη αλδεΰδών ή κετονών κατά Prins
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση περίσσειας αλδευδών ή κετονών σε προπένιο απουσία νερού, σε χαμηλή θερμοκρασία παράγεται παράγωγο διοξανίου. Π.χ. με μεθανάλη παράγεται 4,4-διμεθυλο-1,3-διοξάνιο και 5,5-διμεθυλο-1,3-διοξάνιο:
Διυδροξυλίωση
[Επεξεργασία | επεξεργασία κώδικα]Η διυδροξυλίωση μεθυλοπροπένιου, αντιστοιχεί σε προσθήκη H2O2[15]:
1. Επίδραση αραιού διαλύματος υπερμαγγανικού καλίου. Παράγει μεθυλοπροανοδιόλη-1,2:
2. Επίδραση καρβονικού οξέος και υπεροξείδιου του υδρογόνου. Παράγει μεθυλοπροανοδιόλη-1,2:
3. Μέθοδος Sharpless. Παράγει μεθυλοπροανοδιόλη-1,2:
4. Μέθοδος Woodward. Παράγει μεθυλοπροανοδιόλη-1,2:
5. Υπάρχει ακόμη δυνατότητα για 1,3-διυδροξυλίωση με επίδραση αλδευδών ή κετονών σε μεθυλοπροπένιο, παρουσία νερού. Αντίδραση Prins. Π.χ. με μεθανάλη παράγεται 3-μεθυλοβουτανοδιόλη-1,3:
Οζονόλυση
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση όζοντος (οζονόλυση) σε μεθυλοπροπένιο, παράγεται ασταθές οζονίδιο που τελικά διασπάται σε μεθανάλη και προπανόνη[16]:
Αλλυλική οξείδωση
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση διοξειδίου του σεληνίου σε μεθυλοπροπένιο παράγεται μεθυλοπροπεν-2-όλη-1:
- Η μέθοδος αυτή ονομάζεται αλλυλική οξείδωση.
Αντίδραση Diels–Adler
[Επεξεργασία | επεξεργασία κώδικα]Κατά την επίδραση αλκαδιενίου (διένιου) σε μεθυλοπροπένιο (διενόφιλο) έχουμε την ονομαζόμενη (αντίδραση Diels–Adler) που στην περίπτωση αυτή οδηγεί σε παραγωγή παραγώγου κυκλοεξενίου. Π.χ. με βουταδιένιο-1,3 παίρνουμε 4,4-διμεθυλοκυκλοεξένιο[17]:
Αντίδραση Pauson-Khand
[Επεξεργασία | επεξεργασία κώδικα]Κατά την επίδραση αλκίνια και μονοξειδίου του άνθρακα σε μεθυλοπροπένιο έχουμε την ονομαζόμενη αντίδραση Pauson-Khand που στην περίπτωση αυτή οδηγεί σε παραγωγή παραγώγων κυκλοπεντόνης. Π.χ. με αιθίνιο παράγεται 4,4-διμεθυλοκυκλοπεντεν-2-όνη και 5,5-διμεθυλοκυκλοπεντεν-2-όνη:
Προσθήκη καρβενίων
[Επεξεργασία | επεξεργασία κώδικα]Κατά την προσθήκη μεθυλενίου σε μεθυλοκυκλοπροπένιο σχηματίζεται 1,1-διμεθυλοκυκλοπροπάνιο. Ταυτόχρονα όμως γίνονται και αντιδράσεις παρεμβολής στους δεσμούς C-C και C-H, οπότε παράγονται και πεντένια[18]::
- Η αντίδραση είναι ελάχιστα εκλεκτική και αυτό σημαίνει ότι κατά προσέγγιση έχουμε:
- 1. Παρεμβολή στους έξι (6) δεσμούς CH2-H: 6.
- 2. Παρεμβολή στους δύο (2) δεσμούς CH-H: 2.
- 3. Προσθήκη στον (ένα διπλό) δεσμό: 1.
Προκύπτει επομένως μίγμα 2-μεθυλοβουτένιου-1 ~67%, μεθυλοβουτένιου-2 ~22% και [1,1-διμεθυλοκυκλοπροπάνιου ~11%.
Καταλυτική προσθήκη οξυγόνου
[Επεξεργασία | επεξεργασία κώδικα]Κατά την καταλυτική προσθήκη οξυγόνου σε μεθυλοκυκλοπροπένιο σχηματίζεται 2,2-διμεθυλοξιράνιο. Π.χ.:
Πολυμερισμός
[Επεξεργασία | επεξεργασία κώδικα]Διακρίνονται τα ακόλουθα είδη πολυμερισμού μεθυλοκυκλοπροπένιο που όλα παράγουν πολυϊσοβουτυλένιο[19]:
1. Κατιονικός. Π.χ.:
2.. Ελευθέρων ριζών. Π.χ.:
- Όπου v ο βαθμός πολυμερισμού.
Φωτοχημικός διμερισμός
[Επεξεργασία | επεξεργασία κώδικα]Κατά το φωτοχημικό διμερισμό μεθυλοκυκλοπροπένιο σχηματίζεται 1,1,3,3-τετραμεθυλοκυκλοβουτάνιο. Π.χ.[20]:
Φωτοχημική προσθήκη αλδεϋδών ή κετονών
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση αλδευδών ή κετονών σε μεθυλοκυκλοπροπένιο απουσία νερού σχηματίζονται και φωτοχημικά παράγωγα οξετανίου (Αντίδραση Paterno–Büchi). Π.χ. με μεθανάλη παράγεται 3,3-διμεθυλοξετάνιο:
Αναφορές και σημειώσεις
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Διαδικτυακός τόπος researchgate.net
- ↑ Τυπικά, το πλήρες συστηματικό του όνομα θα ήταν 2-μεθυλοπροπένιο-1, αλλά οι αριθμοί θέσης παραλήπονται επειδή εννοούνται, αφού δεν υπάρχει άλλο μεθυλοπροπένιο.
- ↑ Ο αριθμός θέσης (2-) της διακλάδωσης παραλείπεται, επειδή δεν υπάρχει άλλο μεθυλοπροπένιο.
- ↑ Τα δεδομένα προέρχονται εν μέρει από το «Table of periodic properties of thw Ellements», Sagrent-Welch Scientidic Company και Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, Σελ. 34.
- ↑ 5,0 5,1 Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.153, §6.3.3.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.153, §6.3.1α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.153, §6.3.1β.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.153, §6.3.4.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 156, §6.8.3.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 156, §6.8.5.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 156, §6.8.4.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 156, §6.8.6.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 156, §6.8.2.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 156, §6.8.1.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 157, §6.8.9.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 157, §6.8.10.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 160, §6.10.2.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 157, §6.8.7., σελ. 155, §6.7.3, R = (CH3)2C=CH ή CH3C(CH2)=CH2
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 157, §6.8.11.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 157, §6.8.12.
Πηγές
[Επεξεργασία | επεξεργασία κώδικα]- Speight J. G., “Chemical and Process Design Handbook”, McGraw-Hill, 2002.
- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982



![{\displaystyle \mathrm {(CH_{3})_{2}CHCH_{2}OH{\xrightarrow[{>150^{o}C}]{\pi .H_{2}SO_{4}}}(CH_{3})_{2}C=CH_{2}+H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/0ed2004e240ddc9725e1096c1b5292f68777ff40)
![{\displaystyle \mathrm {(CH_{3})_{3}COH{\xrightarrow[{>150^{o}C}]{\pi .H_{2}SO_{4}}}(CH_{3})_{2}C=CH_{2}+H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/d6373e3fd3e5e9a3c560b7061b1d142d219c66b0)
![{\displaystyle \mathrm {(CH_{3})_{2}CHCH_{2}X+NaOH{\xrightarrow[{\triangle }]{ROH}}(CH_{3})_{2}C=CH_{2}+NaX+H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/17c20b51b88c5fe5d6799b8c2f53a3e133d4f021)
![{\displaystyle \mathrm {(CH_{3})_{3}CX+NaOH{\xrightarrow[{\triangle }]{ROH}}(CH_{3})_{2}C=CH_{2}+NaX+H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/32fe7ca2721e23dd5e5abd6dbe9f445fad95c9e6)

![{\displaystyle \mathrm {(CH_{3})_{3}CH{\xrightarrow[{\triangle }]{Pt}}(CH_{3})_{2}C=CH_{2}+H_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/c33cc4730deeb64e0bfce4e9f828d80ac18b2289)
![{\displaystyle \mathrm {x\in [0,1]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/0071b94225d029fe1a86257743a800e11207d6eb)
![{\displaystyle \mathrm {[RCH_{2}CH_{2}N^{+}(CH_{3})_{2}(CH_{2}CH(CH_{3})_{2})]OH^{-}{\xrightarrow {\triangle }}CH_{3}CH_{2}CH=CH_{2}+RCH_{2}CH_{2}N(CH_{3})_{2}+H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/5bb3216a6f4a8d9fc1cc61a2dd9b1b27072dffbf)




![{\displaystyle \mathrm {(CH_{3})_{2}C=CH_{2}+(CH_{3}COO)_{2}Hg+H_{2}O{\xrightarrow[{-CH_{3}COOH}]{Et_{2}O}}(CH_{3})_{2}C(OH)CH_{2}HgOOCCH_{3}{\xrightarrow {+NaBH_{4}+NaOH}}(CH_{3})_{3}COH+Hg+CH_{3}COONa+Na[BH_{3}OH]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/382755034789ca9e0d6048496d2ccd872f5d3bc1)











![{\displaystyle \mathrm {(CH_{3})_{2}C=CH_{2}+CO+H_{2}{\xrightarrow[{10-100\;atm,40^{o}C-100^{o}C}]{Co\;{\acute {\eta }}\;Rh}}x(CH_{3})_{3}CCHO+(1-x)(CH_{3})_{2}CHCHO} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/3c0be555407a5ca955c9e6e128273a1579f6a9d0)
![{\displaystyle \mathrm {(CH_{3})_{2}C=CH_{2}+2HCHO{\xrightarrow[{\chi \alpha \mu \eta \lambda {\acute {\eta }}\;\theta \epsilon \rho \mu o\kappa \rho \alpha \sigma {\acute {\iota }}\alpha }]{H_{2}SO_{4}}}{\frac {1}{2}}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/ed1eecb34824d9c7c8e971f64be760c9c3396009)




![{\displaystyle \mathrm {(CH_{3})_{2}C=CH_{2}+OsO_{4}+2H_{2}O+2KOH{\xrightarrow {}}(CH_{3})_{2}C(OH)CH_{2}OH+K_{2}[OsO_{2}(OH)_{4}]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/c79c11ddc4d93c6796554553e2889c91129442b7)


![{\displaystyle \mathrm {(CH_{3})_{2}C=CH_{2}+{\frac {2}{3}}O_{3}{\xrightarrow[{Zn}]{H_{2}O}}HCHO+CH_{3}COCH_{3}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/9129b0c1d2e229597dcf09a75089cef1a5d3b84b)








![{\displaystyle \mathrm {(CH_{3})_{2}C=CH_{2}+{\frac {1}{2}}O_{2}{\xrightarrow[{1-2MPa,\;280^{o}C}]{Ag}}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/bd4707b3a28b2ace6b707984f3bf3045899476be)

![{\displaystyle \mathrm {v(CH_{3})_{2}C=CH_{2}{\xrightarrow {H^{+}}}[-C(CH_{3})_{2}CH_{2}-]_{v}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/3495b195b0b780034ae39ced6167768aff3045cc)
![{\displaystyle \mathrm {v(CH_{3})_{2}C=CH_{2}{\xrightarrow {ROOR}}[-C(CH_{3})_{2}CH_{2}-]_{v}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/9af78d62c9fbe34acfd41fd5db2618ee02387551)