Αμίνες
| πρωτοταγής αμίνη | δευτεροταγής αμίνη | τριτοταγής αμίνη |
|---|---|---|
 |
 |
 |
- Να μην συγχέονται με τις ανόργανες αμίνες, τις ιμίνες ή τα αμίδια.
Οι αμίνες είναι οι αζωτούχες οργανικές ενώσεις με μία τουλάχιστον αμινομάδα, δηλαδή -NR2, όπου τα όχι απαραίτητα ίδια R μπορεί να είναι υδρογόνο, αλογόνα, υποκατεστημένα ή μη υδροκαρβύλια και ορισμένες άλλες μονοσθενείς ομάδες, ως κύρια χαρακτηριστική ομάδα. Η αμινομάδα μπορεί να θεωρηθεί ότι προέρχεται από την αντικατάσταση ενός τουλάχιστον ατόμου υδρογόνου αμμωνίας από ένα τουλάχιστον υδροκαρβύλιο (ή υποκατεστημένο παράγωγο αυτών με χαρακτηριστικές ομάδες «κατώτερες» από την αμινομάδα). Ανάλογα με τον αριθμό των υδρογόνων της αμμωνίας που έχουν αντικατασταθεί από υδροκαρβύλια οι αμίνες διακρίνονται σε πρωτοταγείς, δευτεροταγείς και τριτοταγείς. Αντίθετα όμως από άλλες οργανικές ενώσεις (όπως π.χ. αλκοόλες, ο τελευταίος χαρακτηρισμός (πρωτοταγής κ.τ.λ.), αναφέρεται στη συνδεσμολογία του ατόμου του αζώτου, και όχι του άνθρακα.[1][2]. Τα αμινοξέα που περιέχουν μία τουλάχιστον αμινομάδα και έχουν ορισμένες ιδιότητες των αμινών, αλλά δεν ανήκουν (επίσημα) σ' αυτές, αλλά στα καρβοξυλικά οξέα, γιατί η καρβοξυλομάδα που περιέχουν θεωρείται «ανώτερη» χαρακτηριστική ομάδα από την αμινομάδα. Υπάρχουν ακόμη ανόργανα παράγωγα της αμμωνίας, ή ανόργανες αμίνες, που επίσης ονομάζονται «αμίνες», όπως π.χ. η χλωραμίνη NH2Cl, αλλά δεν περιλαμβάνονται στις οργανικές αμίνες, στις οποίες αναφέρεται αυτό το λήμμα. Οι ιμίνες διαφέρουν από τις αμίνες στο ότι σ' αυτές (τις ιμίνες) το άζωτο ενώνεται με ένα άτομο άνθρακα με διπλό δεσμό. Τα αμίδια πάλι, διαφέρουν στο ότι η αμινομάδα τους ενώνεται άμεσα με καρβονύλιο, γεγονός που μεταβάλλει τις ιδιότητες αρκετά ώστε να αποτελούν διαφορετική κατηγορία ενώσεων. Δυο ομάδες -NH2 δεν μπορούν να είναι ενωμένες με το ίδιο άτομο άνθρακα (τουλάχιστον όχι σε σταθερή ένωση), αλλά δυο ομάδες R2N- ή και RHN- (όπου τα R παριστάνουν εδώ υδροκαρβύλια, όχι απαραίτητα ίδια), δίνουν τις σχετικά σταθερές «gem-διαμίνες». Οι πρωτοταγείς και οι δευτεροταγείς αμίνες με α- διπλό δεσμό ισομερειώνονται στις ταυτομερείς τους ιμίνες, αλλά οι τριτοταγείς σμίνες με α- διπλό δεσμό, οι «εναμίνες», είναι σταθερές όπως και οι ενολαιθέρες[1].
Ταξινόμηση των αμινών[Επεξεργασία | επεξεργασία κώδικα]
Μια πρώτη διάκριση αμινών γίνεται ανάλογα τον αριθμό των αμινομάδων τους:
- Οι μονοαμίνες περιέχουν μόνο μία (1) αμινομάδα.
- Οι διαμίνες περιέχουν δυο (2) αμινομάδες.
- Οι τριαμίνες περιέχουν τρεις (3) αμινομάδες.
- Οι πολυαμίνες περιέχουν περισσότερες από τρεις (3) αμινομάδες.
Μια διάκριση αμινών γίνεται ανάλογα με το αν το άζωτο της αμινομάδας της ενώνεται απευθείας με ένα (τουλάχιστον) αρωματικό σύστημα, αντιαρωματικό σύστημα ή μόνο με μη αρωματικά[3].
- Οι αλειφατικές αμίνες δεν έχουν αρωματικό σύστημα άμεσα ενωμένο με το άτομο αζώτου της αμινομάδας τους[4].
- Οι αρωματικές αμίνες έχουν αρωματικό σύστημα άμεσα ενωμένο με το άτομο αζώτου της αμινομάδας τους. Οι αρωματικές αμίνες συχνά ονομάζονται ανιλίνες, από το όνομα της απλούστερης αυτών[5].
- Οι αντιαρωματικές αμίνες έχουν αντιαρωματικό σύστημα άμεσα ενωμένο με το άτομο αζώτου της αμινομάδας τους[6].
Η άμεση επαφή με ένα αρωματικό σύστημα περιορίζει δραστικά την αλκαλικότητα των αρωματικών αμινών, ανάλογα και με την παρουσία ή μη και άλλων υποκαταστατών. Επίσης, η παρουσία άμεσα συνδεμένης αμινομάδας επιρεάζει άμεσα και τη δραστικότητα του αρωματικού συστήματος, την οποία αυξάνει μερικώς, γιατί το άζωτο αφενώς περιέχει ένα μονήρες ζεύγος ηλεκτρονίων, οπότε λειτουργεί ως «δότης ηλεκτρονίων» στο αρωματικό σύστημα, δηλαδή υπρρχει θετικό συζυγιακό φαινόμενο (+R), αλλά είναι ηλεκτραρνητικότερο από τον άνθρακα και επομένως συνυπάρχει αρνητικό επαγωγικό αφαινόμενο (-I). Σε περίπτωαη αντίδρασης αρωματικής ηλεκτρονιόφιλης υποκατάστασης παράγονται ορθο- και παρα- αρωματικά διπαράγωγα.
Μια διάκριση αμινών γίνεται σνάλογα με τον αριθμό των ατόμων υδρογόνου της αμμωνίας που έχουν αντικατασταθεί από ανθρακούχες ομάδες:
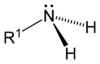
- Στις πρωτοταγείς αμίνες ένα (1) μόνο άτομο υδρογόνου της αμμωνίας έχει αντικατασταθεί από μία (1) ανθρακούχα ομάδα.
- Στις δευτεροταγείς αμίνες δύο (2) άτομα υδρογόνου της αμμωνίας έχουν αντικατασταθεί από δύο (2) ανθρακούχες ομάδες:
- Στις τριτοταγείς αμίνες τρία (3) άτομα υδρογόνου της αμμωνίας έχουν αντικατασταθεί από τρεις (3) ανθρακούχες ομάδες:
Ονοματολογία αμινών[Επεξεργασία | επεξεργασία κώδικα]

Οι αμίνες ονομάζονται στο σύστημα IUPAC ως αμινοαλκάλια. Για παράδειγμα αν μία αμίνη συνδέεται με μία ανθρακική αλυσίδα αλκανίου έξι ανθράκων και είναι συνδεδεμένη στον δεύτερο άνθρακα της αλυσίδας η ένωση ονομάζεται 2-άμινο-εξάνιο. Αν η ανθρακική αλυσίδα έχει διακλαδώσεις τότε η ονοματολογία ακολουθεί τους κανόνες της ονοματολογίας των υδρογονανθράκων με την συνοδεία του προθέματος άμινο-. Η ονοματολογία των δευτεροταγών και τριτοταγών αμινών είναι πιο πολύπλοκη. Οι μικρότερες αλκυλομάδες των αμινών αυτών χρησιμοποιούνται ως πρόθεμα ενώ η μεγαλύτερη αλκυλομάδα αποτελεί την κατάληψη συνοδευόμενη από το πρόθεμα άμινο. Παραδείγματα ονοματολογίας αμινών φαίνονται στο διπλανό σχήμα. Επειδή η ονοματολογία των αμινών κατά IUPAC οδηγεί σε πολύπλοκα ονόματα χρησιμοποιούνται και εμπειρικά ονόματα για τις απλούστερες αμίνες στα οποία η λέξη αμίνη τοποθετειται ως κατάληξη. Η απλούστερη αμίνη π.χ. η οποία αποτελείται από μία μόνο μεθυλομάδα έχει εμπειρική ονομασία μεθυλαμίνη ενώ κατά IUPAC αμινομεθάνιο.
Φυσικές ιδιότητες αμινών[Επεξεργασία | επεξεργασία κώδικα]
Οι αμίνες με μικρές ανθρακικές αλυσίδες είναι υγρά σε κανονικές συνθήκες θερμοκρασίας και πίεσης. Με ανθρακικές αλυσίδες που υπερβαίνουν τους 10 άνθρακες οι αμίνες είναι στερεά. Οι αμίνες επίσης με μικρή ανθρακική αλυσίδα είναι διαλυτές στο νερό ενώ οι αμίνες με μεγαλύτερη ανθρακική αλυσίδα είναι αδιάλυτες στο νερό.
Χημικές ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Μέθοδοι παρασκευής[Επεξεργασία | επεξεργασία κώδικα]
Οι αμίνες παράγονται με τις παρακάτω μεθόδους:
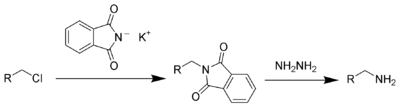
- Από αλκυλαλογονίδια που αντιδρούν με περίσσεια αμμωνίας ή με C8H4KNO2. Το αποτέλεσμα της αντίδρασης οδηγεί σε σύνθεση πρωτοταγών αμινών. Η αντίδραση αυτή ονομάζεται σύνθεση Gabriel.
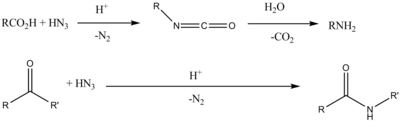
- Δευτεροταγείς αμίνες παράγονται από καρβονυλικές ενώσεις όπως κετόνες ή από καρβονικά οξέα ή εστέρες, όπως φαίνεται παρακάτω στο παρακάτω σχήμα. Η αντίδραση αυτή λέγεται αντίδραση Schmidt και οδηγεί σε μίγμα πρωτοταγών,δευτεροταγών και τριτοταγών
Χημικές αντιδράσεις[Επεξεργασία | επεξεργασία κώδικα]
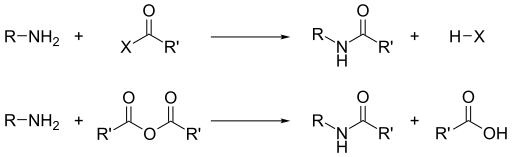
- Οι αμίνες αντιδρούν με ανυδρίτες οξέων ή ακυλοχλωρίδια και παράγονται αμίδια και αλκυλαλογονίδια όπως φαίνεται στο παρακάτω σχήμα:
- Επίσης μπορούν να οδηγήσουν σε παρασκευή αλκοολών με την επίδραση ισχυρού διαλύματος υδροχλωρικού οξέος και νιτρώδους νατρίου, όπως φαίνεται στο παρακάτω σχήμα.

Χρήσεις των αμινών[Επεξεργασία | επεξεργασία κώδικα]
Οι αμίνες συναντώνται σε πολλές βιολογικές λειτουργίες. Μία μεγάλη κατηγορία νευροδιαβιβαστών είναι αμίνες και είναι γνωστές ως κατεχολαμίνες. Χαρακτηριστική ένωση αυτής της κατηγορίας είναι η αδρεναλίνη. Πολλές αμίνες έχουν εθιστική δράση στους οργανισμούς και μία μεγάλη κατηγορία τέτοιων ενώσεων αποτελούν ναρκωτικές ουσίες, όπως η αμφεταμίνη. Λόγω της έντονης δράσης τους στον οργανισμό κάποιες χρησιμοποιούνται ως φαρμακευτικές ουσίες, ως ηρεμιστικά ή αντιαλλεργιογόνα.
Σημειώσεις και παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 Αναστάσιου Βάρβογλη, «Χημεία Οργανικών Ενώσεων», Παρατηρητής, Θεσσαλονίκη 1991, σελ. 115, §8.2.
- ↑ McMurry, John E. (1992), Organic Chemistry (3rd ed.), Belmont: Wadsworth, ISBN 0-534-16218-5.
- ↑ «Αρχειοθετημένο αντίγραφο». Αρχειοθετήθηκε από το πρωτότυπο στις 20 Οκτωβρίου 2015. Ανακτήθηκε στις 7 Ιανουαρίου 2013.
- ↑ Σύμφωνα με έναν άλλο τρόπο κατάταξης δεν περιέχουν καθόλου αρωματικό ή αντιαρωματικό σύστημα.
- ↑ Σύμφωνα με έναν άλλο τρόπο κατάταξης περιέχουν ένα τουλάχιστον αρωματικό σύστημα. Οι ανιλίνες, που έχουν αρωματικό σύστημα άμεσα ενωμένο με το άτομο αζώτου της αμινομάδας τους θεωρούνται υποκατηγορία των αρωματικών αμινών.
- ↑ Σύμφωνα με έναν άλλο τρόπο κατάταξης περιέχουν ένα τουλάχιστον αντιαρωματικό σύστημα. Οι αμίνες, που έχουν αντιαρωματικό σύστημα άμεσα ενωμένο με το άτομο αζώτου της αμινομάδας τους θεωρούνται υποκατηγορία των αρωματικών αμινών.
Πηγές[Επεξεργασία | επεξεργασία κώδικα]
- SCHAUM'S OUTLINE SERIES, «ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ», Μτφ. Α. Βάρβογλη, 1999
- «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982
- Αναστάσιου Βάρβογλη, «Χημεία Οργανικών Ενώσεων», Παρατηρητής, Θεσσαλονίκη 1991
- Καραγκιοζίδη Σ. Πολυχρόνη, «Ονοματολογία Οργανικών Ενώσεων στα Ελληνικά & Αγγλικά» Β΄ ΈκδοσηΘεσσαλονίκη 1991
- Νικολάου Ε. Αλεξάνδρου, «Γενική Οργανική Χημεία», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985
- Δημητρίου Ν. Νικολαΐδη, «Ειδικά Μαθήματα Οργανικής Χημείας», ΑΠΘ, θεσσαλονίκη 1983
- Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Φαίδωνα Χατζημηχαλάκη, «Εργαστηριακός Οδηγός», Εκδόσεις Ζήτη, Θεσσαλονίκη 1986
- Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Δημητρίου Ν. Νικολαΐδη: «Χημεία Ετεροκυκλικών Ενώσεων», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985
- Οργανική χημεία, John Mc Murry, Τόμος ΙΙ, Πανεπιστημιακές εκδόσεις Κρήτης
- Γενική χημεία, Eding Gammon, εκδόσεις Τραυλός
| |||||||||||||||||||||||
| |||||||||||
| |||||||||||||||||||||||||||||||||||
|