Οξετάνιο
| Οξετάνιο | |||
|---|---|---|---|

| |||
| |||

| |||
| Γενικά | |||
| Όνομα IUPAC | Οξετάνιο | ||
| Άλλες ονομασίες | 1,3-εποξυπροπάνιο 1,3-προπυλενοξείδιο Οξακυκλοβουτάνιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C3H6O | ||
| Μοριακή μάζα | 58,08 amu | ||
| Σύντομος συντακτικός τύπος |
|||
| Αριθμός CAS | 503-30-0 | ||
| SMILES | O1CCC1 | ||
| Αριθμός UN | I279Q16FU6 | ||
| Δομή | |||
| Μοριακή γεωμετρία | Επίπεδη ρομβική ως προς C-C-C-O. | ||
| Ισομέρεια | |||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -97 °C | ||
| Σημείο βρασμού | 49-50 °C | ||
| Πυκνότητα | 893 kg/m3 | ||
| Διαλυτότητα στο νερό |
Διαλυτό | ||
| Τάση ατμών | 35 kPa (20 °C) | ||
| Εμφάνιση | Υγρό | ||
| Χημικές ιδιότητες | |||
| Ελάχιστη θερμοκρασία ανάφλεξης |
-28 °C | ||
| Επικινδυνότητα | |||
 
| |||
| Εύφλεκτο (F) Βλαβερό (Xn) | |||
| Φράσεις κινδύνου | 11-20/21/22 | ||
| Φράσεις ασφαλείας | (2)-9-16-26-29 | ||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
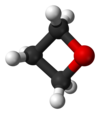
Το οξετάνιο[1] (αγγλικά oxetane) είναι οργανική χημική ένωση, που περιέχει άνθρακα, υδρογόνο και οξυγόνο, με μοριακό τύπο C3H6O, αν και συνήθως παριστάνεται με το γραμμικό τύπο του, ![]() . Είναι ένας ετεροκυκλικός αιθέρας. Το χημικά καθαρό οξετάνιο στις κανονικές συνθήκες περιβάλλοντος, δηλαδή σε θερμοκρασία 25°C και υπό πίεση 1 atm, είναι υγρό. Το μόριό του αποτελείται από έναν τετραμελή δακτύλιο, με ένα (1) άτομο οξυγόνου και τρία (3) άτομα άνθρακα.
. Είναι ένας ετεροκυκλικός αιθέρας. Το χημικά καθαρό οξετάνιο στις κανονικές συνθήκες περιβάλλοντος, δηλαδή σε θερμοκρασία 25°C και υπό πίεση 1 atm, είναι υγρό. Το μόριό του αποτελείται από έναν τετραμελή δακτύλιο, με ένα (1) άτομο οξυγόνου και τρία (3) άτομα άνθρακα.
Ισομέρεια[Επεξεργασία | επεξεργασία κώδικα]
Με βάση χημικό τύπο του (C3H6O) έχει τα ακόλουθα οκτώ (8) ισομερή θέσης:
- Προπανάλη, με μοριακό τύπο CH3CH2CHO.
- Προπανόνη, με μοριακό τύπο CH3COCH3.
- 1-προπεν-1-όλη, με μοριακό τύπο CH3CH=CHOH, σε δύο (2) γεωμετρικά ισομερή. Αποτελεί έλασον ταυτομερές της προπανάλης.
- 2-προπεν-1-όλη ή αλλυλική αλκοόλη, με μοριακό τύπο CH2=CHCH2OH.
- (1-)-προπεν-2-όλη, με μοριακό τύπο CH3C(OH)=CH2. Αποτελεί έλασον ταυτομερές της προπανόνης.
- Βινυλομεθυλαιθέρας, με μοριακό τύπο CH2=CHOCH3.
- Κυκλοπροπανόλη, με γραμμικό τύπο
![76x76εσ[νεκρός σύνδεσμος]](//upload.wikimedia.org/wikipedia/commons/thumb/4/46/Cyclopropanol.svg/33px-Cyclopropanol.svg.png) .
. - Μεθυλοξιράνιο, με γραμμικό τύπο
![80x80εσ[νεκρός σύνδεσμος]](//upload.wikimedia.org/wikipedia/commons/thumb/3/30/Methyloxirane.png/50px-Methyloxirane.png) .
.
«Μητρικό» και «θυγατρικά» οξετάνια[Επεξεργασία | επεξεργασία κώδικα]
Το οξετάνιο είναι η «μητρική ένωση» για μια σειρά «θυγατρικών» του παραγώγων , που μαζί με τη «μητρική ένωση», ονομάζονται συλλήβδην «οξετάνια».
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
1. Μια τυπική και καλά μελετημένη μέθοδος παραγωγής οξετανίου είναι η επίδραση υδροξειδίου του καλίου σε αιθανικό 3-χλωροπροπυλεστέρα, στους 150 °C[2][3]:
2. Εναλλακτικά, μπορεί να παραχθεί και με φωτοχημική 2+2 αντίδραση Πατέρνο-Μπούχι (Paternò-Büchi-Reaktion), μεταξύ αιθενίου και μεθανάλης[3][4][5]:
Δομή και φασματοσκοπικές ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Το μόριο του οξετανίου είναι επίπεδο (και περίπου) ρομβικό, ως προς C-C-C-O. Οι πλευρές του μετρήθηκαν C-O: 145 pm και C-C: 155 pm. Οι γωνίες του μετρήθηκαν COC = 92°, CCO = 84°, CCC = 100°. Η επιπεδότητα του οξετανίου, σε αντίθεση με το πτυχωμένο κυκλοβουτάνιο, αποδίδεται στο σχετικά μειωμένο απωθητικό αποτέλεσμα της αλληλεπίδρασης των ατόμων υδρογόνων των μεθυλενικών του ομάδων (εξαιτίας της έλξης τους από το άτομο του οξυγόνου). Στη φάσματα φασματοσκοπία πυρηνικού μαγνητικού συντονισμού (NMR spectroscopy) τα α-μεθυλενικά άτομα υδρογόνου συντονίζονται σε 4,7 δ, ενώ τα β-μεθυλενικά σε 2,7 δ[6].
Χημική συμπεριφορά[Επεξεργασία | επεξεργασία κώδικα]
Το οξετάνιο έχει ανάλογη συμπεριφορά με το οξιράνιο, αλλά οι αντιδράσεις του πρώτου με πυρηνόφιλα αντιδραστήρια απαιτούν πιο έντονες συνθήκες. Αντίθετα, με ηλεκτρονιόφιλα αντιδραστήρια η κυκλοπροσθήκη γίνεται ευκολότερα. Το οξετάνιο χρησιμοποιείται σε αντιδράσεις ανοικοδόμησης του ανθρακικού σκελετού κατά τρία (3) άτομα άνθρακα. Παραδείγματα[7]
Αντίδραση με θειόλες[Επεξεργασία | επεξεργασία κώδικα]
Το οξετάνιο αντιδρά με θειόλες (RSH), παράγοντας 3-αλκυλοθειο-1-προπανόλη:
Αντίδραση με αρένια[Επεξεργασία | επεξεργασία κώδικα]
Το οξετάνιο αντιδρά με αρένια (ArH), παρουσία τριχλωριούχου αργιλίου, παράγοντας 3-αρυλο-1-προπανόλη:
Πακλιταξέλιο[Επεξεργασία | επεξεργασία κώδικα]

Το πακλιταξέλιο (Taxol) είναι ένα παράδειγμα φυσικού προϊόντος που περιέχει έναν οξετανικό δακτύλιο. Το παλιτοξέλιο έχει γίνει μεγάλο επίκεντρο έρευνας ανάμεσα στους ερευνητές, εξαιτίας της ασυνήθιστης δομής του και της επιτυχούς εμπλοκής του στη θεραπεία του καρκίνου[8]. Ο οξετανικός δακτύλιος, που περιέχει, αποτελεί μια σημαντική ομάδα της ένωσης, που χρησιμοποιείται για τη σύνδεση των μικροσωληνίσκων στη δομική συγγένεια, αλλά ωστόσο ελάχιστα είναι γνωστά για τον τρόπο με τον οποίο η αντίδραση καταλύεται στη φύση, γεγονός που δημιουργεί μια πρόκληση για τους επιστήμονες που προσπαθούν να συνθέσουν αυτό το προϊόν[8].
Πηγές πληροφόησης[Επεξεργασία | επεξεργασία κώδικα]
- Παπαγεωργίου, Β.Π., Εφαρμοσμένη Οργανική Χημεία, Εκδόσεις Παρατηρητής, Θεσσαλονίκη 2005, ISBN 960-260-342-7
- SCHAUM'S OUTLINE SERIES, «ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ», Μτφ. Α. Βάρβογλη, 1999
- «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982
- Αναστάσιου Βάρβογλη, «Χημεία Οργανικών Ενώσεων», Παρατηρητής, Θεσσαλονίκη 1991
- Καραγκιοζίδη Σ. Πολυχρόνη, «Ονοματολογία Οργανικών Ενώσεων στα Ελληνικά & Αγγλικά» Β΄ Έκδοση Θεσσαλονίκη 1991
- Νικολάου Ε. Αλεξάνδρου, «Γενική Οργανική Χημεία», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985
- Δημητρίου Ν. Νικολαΐδη, «Ειδικά Μαθήματα Οργανικής Χημείας», ΑΠΘ, θεσσαλονίκη 1983
- Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Φαίδωνα Χατζημηχαλάκη, «Εργαστηριακός Οδηγός», Εκδόσεις Ζήτη, Θεσσαλονίκη 1986
- Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Δημητρίου Ν. Νικολαΐδη: «Χημεία Ετεροκυκλικών Ενώσεων», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985
- Διαδικτυακοί τόποι που αναφέρονται στις «Αναφορές και παρατηρήσεις».
Παραπομπές και παρατηρήσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Για εναλλακτικές ονομασίες δείτε τον πίνακα πληροφοριών.
- ↑ C. R. Noller (1955), "Trimethylene Oxide", Org. Synth. 29: 92; Coll. Vol. 3: 835
- ↑ 3,0 3,1 Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985, §3.1., σελ. 31.
- ↑ E. Paterno, G. Chieffi (1909). «.». Gazz. Chim. Ital. 39: 341.
- ↑ G. Büchi, Charles G. Inman, and E. S. Lipinsky (1954). «Light-catalyzed Organic Reactions. I. The Reaction of Carbonyl Compounds with 2-Methyl-2-butene in the Presence of Ultraviolet Light». Journal of the American Chemical Society 76 (17): 4327–4331. doi:10.1021/ja01646a024.
- ↑ Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985, §3.1., σελ. 32.
- ↑ Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985, §3.1., σελ. 32-34.
- ↑ 8,0 8,1 Willenbring, Dan, and Dean J. Tantillo.. "Mechanistic possibilities for oxetane formation in the biosynthesis of Taxol’s D ring." Russian Journal of General Chemistry 78.4 (Apr. 2008): 7237–31. Advanced Placement Source. EBSCO. [Library name], [City], [State abbreviation]. 22 Apr. 2009 <http://search.ebscohost.com/login.aspx?direct=true&db=aqh&AN=32154883&site=ehost-live>
| ||||||||||||||||||||




