Φαινυλοξιράνιο
| Φαινυλοξιράνιο | |||
|---|---|---|---|

| |||
| Γενικά | |||
| Όνομα IUPAC | Φαινυλοξιράνιο | ||
| Άλλες ονομασίες | Οξείδιο του στυρενίου Εποξυστυρένιο Οξείδιο του Φαινυλαιθυλενίου Στυρολοξείδιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C8H8O | ||
| Μοριακή μάζα | 120,14852 amu | ||
| Σύντομος συντακτικός τύπος |
Ph[CHOCH2] | ||
| Αριθμός CAS | 96-09-3 | ||
| SMILES | c1ccccc1C2CO2 | ||
| InChI | 1S/C8H8O/c1-2-4-7(5-3-1)8-6-9-8/h1-5,8H,6H2 | ||
| Αριθμός EINECS | 100-002-252 | ||
| PubChem CID | 7276 | ||
| ChemSpider ID | 7005 | ||
| Δομή | |||
| Ισομέρεια | |||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | −37°C | ||
| Σημείο βρασμού | 194°C | ||
| Πυκνότητα | 1.052 kg/m³ | ||
| Δείκτης διάθλασης , nD |
1,5342 (20 °C) | ||
| Τάση ατμών | 40 Pa (20 °C) | ||
| Εμφάνιση | Άχρωμο προς κιτρινωπό υγρό | ||
| Χημικές ιδιότητες | |||
| Επικινδυνότητα | |||
 
| |||
| Βλαβερό (Xn) και διαβρωτικό (C) | |||
| Φράσεις κινδύνου | 20, 22, 34, 36, 37, 38 | ||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Το φαινυλοξιράνιο[1] (αγγλικά styrene oxide) είναι ετεροαρωματική (δηλαδή ετεροκυκλική και αρωματική) οργανική χημική ένωση, που περιέχει άνθρακα, υδρογόνο και οξυγόνο, με μοριακό τύπο C8H8O, Πιο συγκεκριμένα, αποτελεί ένα «θυγατρικό» οξιράνιο, που προέρχεται από το στυρόλιο (PhVi). Εφόσον το φαινυλοξιράνιο έχει ένα χειρόμορφο κέντρο, στο βενζυλικό άτομο άνθρακα, το φαινυλοξιράνιο υπάρχει σε δύο (2) οπτικά ισομερή, R- και S-.
Παραγωγή
[Επεξεργασία | επεξεργασία κώδικα]Το φαινυλοξιράνιο μπορεί να παραχθεί με προσθήκη υποχλωριώδους οξέος (HClO) σε στυρένιο, ακολουθούμενη από αντίδραση εσωτερική απόσπασης υδροχλωρίου (HCl), από την παρουσία διαλύματος υδροξειδίου αλκαλιμέταλλου:[2]
Μια άλλη δυνατότητα σύνθεσης φαινυλοξιρανίου είναι η άμεση επίδραση σε στυρένιο αιθανικού υπεροξέος (CH3CO3H) ή υπεροξειδίου του υδρογόνου (Η2Ο2), σε μια αντίδραση εποξείδωσης[2]:

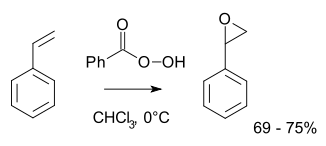
Η εποξείδωση στυρενίου μπορεί να γίνει και με βενζοϊκό υπεροξύ (PhCO3H) , σύμφωνα με την αντίδραση Πρίζαεφ (Prilezhaev reaction):[3]
Τα καθαρά διακριτά εναντιομερή μπορούν να συνθεθούν με την ασύμμετρη εποξείδωση Τζάκομπσεν (Jacobsen-Epoxidierung) ή την επίσης ασύμμετρη εποξείδωση Σι (Shi-Epoxidierung).[2] Οι αντιδράσεις αυτές είναι επίσης προσβάσιμες μέσω χρήσης κατάλληλου ενζύμου ή χημικής κινητικής ανάλυσης.[2]
Χαρακτηριστικά και ιδιότητες
[Επεξεργασία | επεξεργασία κώδικα]Το χημικά καθαρό φαινυλοξιράνιο, στις κανονικές συνθήκες περιβάλλοντος, δηλαδή σε θερμοκρασία 25°C και υπό πίεση 1 atm, είναι άχρωμο προς κιτρινωπό υγρό. Το φαινυλοξιράνιο είναι ελαφρώς υδατοδιαλυτό. Όμως, ακόμη και ίχνη οξέος στο νερό προκαλούν υδρόλυση του φαινυλοξιρανίου, σχηματίζοντας ρακεμική φαινυλ-1.2-αιθανοδιόλη [PhCH(OH)CH2OH], μέσω φαινυλοκατιόντων (Ph+). Αν η ποσότητα του νερού δεν είναι αρκετή για την πλήρη υδρόλυση όλης της ποσότητας φαινυλοξιρανίου, η τυχόν περίσσια οξέος καταλύει αντίδραση ισομερείωσης του φαινυλοξιρανίου που απέμεινε σε φαινυλαιθανάλη (PhCH2CHO).[4][5] Η ισομερείωση αυτή, αν είναι ανεπιθύμητη, μπορεί να αποτροπή με την προσθήκη διαλύματος όξινου ανθρακικού νατρίου (NaHCO3). In vivo η ισομερείωση καταλύεται από το ένζυμο ισομεράση του στυρολοξειδίου (StyrolOxide Isomerase, SOI).
Το φαινυλοξιράνιο υδρολύεται in vivo σε φαινυλ-1,2-αιθανοδιόλη, με το ένζυμο υδρολάση εποξειδίου.[6]
Σχηματίζει αζεοτροπικό μίγμα με το νερό στους 99,2 °C, που περιέχει 77,6% φαινυλοξιράνιο.[7]
Αντιδρά βίβαια με πυρηνόφιλα αντιδραστήρια, όπως είναι για παράδειγμα οι αμίνες (RNH2), αλλά αντιδρά και με ηλεκτρονιόφιλα. Σε αυτήν την περίπτωση, η υψηλή χημική ενέργεια παραμόρφωσης που εμπεριέχει ο τριμελής οξιρανικός δακτύλιος της ένωσης απελευθερώνεται.
Εφαρμογές
[Επεξεργασία | επεξεργασία κώδικα]Με υδρογόνωση φαινυλοξιρανίου παράγεται η ένωση 2-φαινυλαιθανόλη (PhCH2CH2OH), που χρησιμοποιείται ως οσμοθέτης. Το φαινυλοξιράνιο χρησιμεύει, επίσης, ως πρόδρομη ύλη για τη σύνθεση φενιπεντόλης, που είναι ένα χολορυθμιστικό φάρμακο. Επίσης, το φαινυλοξιράνιο χρησιμεύει ως πρόδρομη ένωση για την παραγωγή διαφόρων καταλυτών και αναστολέων πολυμερισμού. Επιπλέον, χρησιμοποιείται ως υπόστρωμα για τη δοκιμή της δραστικότητας διαφόρων υδρολασών και για να δοκιμαστεί η αποτελεσματικότητα των χρωματογραφικών μεθόδων για τον διαχωρισμό εναντιομερών.[2]
Τοξικολογία
[Επεξεργασία | επεξεργασία κώδικα]Οι ατμοί του φαινυλοξιρανίου είναι ερεθιστικοί για τα μάτια και για την αναπνευστική οδό. Η άμεση επαφή φαινυλοξιρανίου με το (ανθρώπινο) δέρμα προκαλεί μέτριο ερεθισμό του. Σε περίπτωση μαζικής αναπνευστικής έκθεσης στην ένωση προκαλείται ερεθισμός της αναπνευστικής οδού, σχηματισμός τοξικού πνευμονικού οιδήματος, με συμπτώματα ναυτίας και κατάθλιψης του κεντρικού νευρικού συστήματος.[2]
Το φαινυλοξιράνιο είναι ο κύριος μεταβολίτης του στυρενίου, για ανθρώπους και ζώα, καθώς προκύπτει από την οξείδωση του στυρενίου στο κυτόχρωμα P540. Το φαινυλοοξιράνιο, θιεωρείται πιθανό καρκινογόνο, όταν βιοσυσσωρεύεται σε σημαντικές ποσότητες σε ποντίκια και αρουραίους.[8] Μετά από πειράματα σε ζώα το φαινυλοξιράνιο βρέθηκε ότι είναι καρκινογόνο, εξαιτίας του υψηλού δυναμικού αλκυλίωσης που η ένωση έχει. Γι' αυτό θεωρείται τοξική ένωση. Το φαινυλοξιράνιο μεταβολίζεται από το ανθρώπινο σώμα σε μανδελικό οξύ, σε φαινυλογλυοξυλικό οξύ, σε βενζοϊκό οξύ (PhCOOH) και σε ιππουρικό οξύ.
Το φαινυλοξιράνιο ένα χειρόμορφο κέντρο και, συνεπώς, δύο εναντιομερή. Έχει αναφερθεί ότι τα δύο εναντιομερή έχουν διαφορετική τοξικοκινητική και τελικά τοξικότητα. Έχει αναφερθεί ότι το R-φαινυλοξιράνιο σχηματίζεται κατά προτίμηση στους πνεύμονες των ποντικιών, ενώ το S-φαινυλοξιράνιο σχηματίζεται κατά προτίμηση στους αρουραίους. Σύμφωνα με πειράματα που έγιναν σε εθελοντές, η αθροιστική απέκκριση της S-φαινυλ-1,2-αιθανοδιόλης και του μανδελικού οξέος ήταν μεγαλύτερη σε σύγκριση με την αντίστοιχη της S-φαινυλ-1,2-αιθανοδιόλης. Διαπιστώθηκε, επίσης, ότι το S-φαινυλοξιράνιο υδρολύεται κατά προτίμηση από τα ανθρώπινα ηπατικά μικροσώματα, σε σύγκριση με το R-φαινυλοξιράνιο. Μελέτες σε ζώα έχουν δείξει ότι το R-φαινυλοξιράνιο είναι πιο τοξικό από το S-φαινυλοξιράνιο, για τα ποντίκια.
Ασφάλεια
[Επεξεργασία | επεξεργασία κώδικα]Το φαινυλοξιράνιο σχηματίζει εκρηκτικά μείγματα ατμών του και αέρα, σε αυξημένη θερμοκρασία. Η ένωση έχει ελάχιστη θερμοκρασία ανάφλεξης κάτω από 74°C. Το εκρηκτικό εύρος της ένωσης είναι 1,1%-22% κατ' όγκο. Η θερμοκρασία αυτανάφλεξης της ένωσης είναι 498°C. Το υλικό εμπίπτει στην κατηγορία θερμοκρασίας Τ1.[9]
Πηγές
[Επεξεργασία | επεξεργασία κώδικα]- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
- Δημήτριου Ν. Νικολαΐδη: Ειδικά μαθήματα Οργανικής Χημείας, Θεσσαλονίκη 1983.
Αναφορές και σημειώσεις
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Δείτε τις εναλλακτικές ονομασίες στον παρακείμενο πίνακα πληροφοριών χημικής ένωσης.
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 Styroloxid. 17 Δεκεμβρίου 2014.
- ↑ Harold Hibbert and Pauline Burt (1941), «Styrene Oxide», Org. Synth., http://www.orgsyn.org/orgsyn/orgsyn/prepContent.asp?prep=cv1p0494; Coll. Vol. 1: 494
- ↑ «Verfahren zur Herstellung von Phenylacetaldehyden, BASF-Patent DE3546372A1 vom 2». Αρχειοθετήθηκε από το πρωτότυπο στις 5 Δεκεμβρίου 2017. Ανακτήθηκε στις 10 Ιουλίου 2017.
- ↑ «Verfahren zur Herstellung von Phenylacetaldehyden, BASF-Patent DE3546372A1 vom 2. Juli 1987». Αρχειοθετήθηκε από το πρωτότυπο στις 5 Δεκεμβρίου 2017. Ανακτήθηκε στις 10 Ιουλίου 2017.
- ↑ Kenneth C. Liebman (1975). «Metabolism and toxicity of styrene». Environmental Health Perspectives 11: 115–119. doi:. http://ehis.niehs.nih.gov/members/1975/011/11018.PDF.[νεκρός σύνδεσμος]
- ↑ L.H. Horsley: Azeotropic Data II, Advances in Chemistry Series 35, American Chemical Society, Washington D.C., 1962.
- ↑ EPA Styrene Oxide evaluation
- ↑ Eintrag zu (Epoxyethyl)benzol[νεκρός σύνδεσμος] in der GESTIS-Stoffdatenbank des IFA, abgerufen am 22. Februar 2017.


