Υδροχλώριο
- "HCl" ανακατευθύνει εδώ. Για το οξύ : Υδροχλωρικό οξύ
| Υδροχλώριο | |||
|---|---|---|---|

| |||

| |||

| |||

| |||
| Γενικά | |||
| Όνομα IUPAC | Υδροχλωρίδιο | ||
| Άλλες ονομασίες | Υδροχλώριο Χλωράνιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | HCl | ||
| Μοριακή μάζα | 36.46 amu | ||
| Αριθμός CAS | 7647-01-0 | ||
| SMILES | Cl | ||
| InChI | 1S/ClH/h1H | ||
| Αριθμός EINECS | 231-595-7 | ||
| Αριθμός RTECS | MW4025000 | ||
| PubChem CID | 313 | ||
| ChemSpider ID | 307 | ||
| Δομή | |||
| Διπολική ροπή | 1,05 D | ||
| Είδος δεσμού | πολωμένος ομοιοπολικός | ||
| Πόλωση δεσμού | 21% (H+-Cl-) | ||
| Γωνία δεσμού | 0° | ||
| Μοριακή γεωμετρία | γραμμική | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -114,22 °C | ||
| Σημείο βρασμού | -85,05 °C | ||
| Πυκνότητα | 1,49 kg/m3 | ||
| Διαλυτότητα στο νερό |
720 kg/m3 (20 °C) | ||
| Δείκτης διάθλασης , nD |
1,0004456 | ||
| Τάση ατμών | 4.352 kPa (21.1 °C) | ||
| Χημικές ιδιότητες | |||
| pKa | -7,0 | ||
| Επικινδυνότητα | |||
 
| |||
| Φράσεις κινδύνου | R23, R35 | ||
| Φράσεις ασφαλείας | S1/2, S9, S26, S36/37/39, S45 | ||
| LD50 | 238 mg/kg | ||
| Κίνδυνοι κατά NFPA 704 |
|||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Το υδροχλώριο[1] (αγγλικά hydrogen chloride) είναι ανόργανη διατομική ομοιοπολική χημική ένωση, που περιέχει υδρογόνο και χλώριο, με μοριακό τύπο HCl. Ανήκει στην κατηγορία των υδραλογόνων. Το χημικά καθαρό υδροχλώριο, σε κανονικές συνθήκες περιβάλλοντος, δηλαδή σε θερμοκρασία 25°C και υπό πίεση 1 atm, είναι άχρωμο αέριο, το οποίο, όταν έρχεται σε επαφή με την υγρασία του ατμοσφαιρικού αέρα, σχηματίζει ορατούς λευκούς ατμούς[2]. Το υδατικό διάλυμα υδροχλωρίου ονομάζεται υδροχλωρικό οξύ και συχνά παριστάνεται επίσης με τον τύπο HCl. Τόσο το υδροχλώριο όσο και το υδροχλωρικό οξύ είναι σημαντικές ενώσεις για την τεχνολογία και τη βιομηχανία.
Ιστορία[Επεξεργασία | επεξεργασία κώδικα]
Οι αλχημιστές του Μεσαίωνα αναγνώριζαν ότι το υδροχλωρικό οξύ («acidum salis», όπως το ονόμαζαν τότε στα λατινικά, που αποδίδεται στα ελληνικά ως «σπίρτο του άλατος») παρήγαγε ατμούς υδροχλωρίου, τους οποίους ονόμαζαν «θαλασσινό όξινο αέρα» («marine acid air»). Το 17ο αιώνα, ο Γιόχαν Ρούντολφ Γκλάουμπερ (Johann Rudolf Glauber) χρησιμοποίησε αλάτι (χλωριούχο νάτριο, NaCl) και θειικό οξύ (H2SO4) για την παρασκευή θειικού νατρίου (Na2SO4),, απελευθερώνοντας έτσι (ταυτόχρονα) αέριο υδροχλώριο. Ο Καρλ Βίλελμ Σέελε (Carl Wilhelm Scheele) ανέφερε, επίσης, αυτήν την αντίδραση το 1772, και μερικές φορές πιστώνεται (σε διάφορα έντυπα) την ανακάλυψή της. Την ίδια χρονιά, ο Τζόζεφ Πρίστλεϋ (Joseph Priestley) παρασκεύασε υδροχλώριο, ενώ το 1810 ο Χάμφρυ Ντέυβυ (Humphry Davy) ανακάλυψε ότι αυτό (δηλαδή το υδροχλώριο) αποτελείται από υδρογόνο και χλώριο[3].
Κατά τη διάρκεια της Βιομηχανικής Επανάστασης, η ζήτηση για αλκαλικές ουσίες, όπως το ανθρακικό νάτριο (Na2CO3), αυξήθηκε και το 1791 ο Νικολά Λεμπλάν (Nicolas Leblanc) ανέπτυξε μια νέα βιομηχανική διαδικασία για την παραγωγή του ανθρακικού νατρίου. Κατά τη «μέθοδο Λεμπλάν» (Leblanc process), κοινό αλάτι μετατρέπεται σε ανθρακικό νάτριο, με θειικό οξύ, ασβεστόλιθο (ανθρακικό ασβέστιο, CaCO3) και άνθρακα, δίνοντας επίσης υδροχλώριο, ως παραπροϊόν. Μέχρι το 1863 το υδροχλώριο απελευθερωνόταν στον αέρα, αλλά η «Αλκαλική Δράση» (Alkali Act) του 1863 απαγόρευσε αυτήν την απελευθέρωση, οπότε οι μονάδες παραγωγής ανθρακικού νατρίου διοχέτευαν το αέριο υδροχλώριο σε νερό, παράγοντας έτσι υδροχλωρικό οξύ σε βιομηχανική κλίμακα. Αργότερα, αναπτύχθηκε η «μέθοδος Χάργκρειβς» (Hargreaves process), η οποία είναι παρόμοια με τη μέθοδο Λεμπλάν, εκτός από το ότι χρησιμοποιεί διοξείδιο του θείου (SO2, αντί για θειικό οξύ) και το νερό (αυτό το μείγμα δίνει θειώδες οξύ, H2SO3). Η διαδικασία είναι συνολικά εξώθερμη. Στις αρχές του 20ού αιώνα, η μέθοδος Λεμπλάν αντικαταστάθηκε από τη «μέθοδο Σολβέ» (Solvay process), κατά την οποία δεν συμπαράγεται υδροχλώριο. Ωστόσο, η παραγωγή υδροχλωρίου συνεχίστηκε, επειδή απ' αυτό παραγόταν το υδροχλωρικό οξύ.
Κατά τον 20ό αιώνα, ιστορικές χρήσεις του υδροχλωρίου ήταν η υδροχλωρίωση των αλκινίων για την παραγωγή χλωροπρενίου, βινυλοχλωριδίου και τα παράγωγα αυτών νεοπρένιο και PVC, αντίστοιχα. Στην παραγωγή του βινυλοχλωριδίου, γίνεται προσθήκη υδροχλωρίου στον τριπλό δεσμό του αιθίνιου, μετατρέποντας έτσι τον τριπλό σε διπλό δεσμό, και δίνοντας έτσι βινυλοχλωρίδιο:
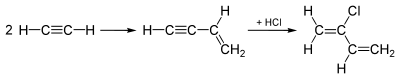
Η λεγόμενη «ακετυλενική μέθοδος», που χρησιμοποιήθηκε μέχρι τη δεκαετία του 1960 (για την παραγωγή χλωροπρενίου), ξεκινούσε με το διμερισμό του ακετυλενίου, που παρήγαγε ενδιάμεσα βουτενίνιο. Στη συνέχεια, με προσθήκη υδροχλωρίου στον τριπλό δεσμό, παράγεται χλωροπρένιο (2-χλωρο-1,3-βουταδιένιο):
Η ακετυλενική μέθοδος αντικαταστάθηκε, μεταγενέστερα, από μια άλλη διαδικασία, κατά την οποία με 1,2-προσθήκη χλωρίου σε 1,3-βουταδιένιο παράγεται ενδιάμεσα 3,4-διχλωρο-1-βουτένιο, από το οποίο αποσπάται ως υδροχλώριο το άτομο χλωρίου που βρίσκεται στο άτομο άνθρακα #4, και τελικά παράγεται έτσι και πάλι χλωροπρένιο:
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
Το μεγαλύτερο μέρος της παραγωγής υδροχλωρίου χρησιμοποιείται για την παρασκευή υδροχλωρικού οξέος.
Βιομηχανικές μέθοδοι[Επεξεργασία | επεξεργασία κώδικα]
Ανόργανες μέθοδοι[Επεξεργασία | επεξεργασία κώδικα]
Σύμφωνα με τη χλωραλκαλική βιομηχανική μέθοδο, ηλεκτρολύεται άλμη (δηλαδή υδατικό διάλυμα χλωριούχου νατρίου), συμπαράγοντας υδρογόνο και χλώριο[4]. Το χημικά καθαρό χλώριο, που παράγεται έτσι, μπορεί να συνδυαστεί με το υδρογόνο, παράγοντας υδροχλώριο, με την παρουσία υπεριώδους ακτινοβολίας (UV):
Επειδή η αντίδραση είναι εξώθερμη, πραγματοποιείται μέσα σε ειδική εγκατάσταση που ονομάζεται «φούρνος υδροχλωρίου» ή «καυστήρας υδροχλωρίου». Το αέριο υδροχλώριο που παράγεται, απορροφάται σε απιονισμένο νερό, με αποτέλεσμα χημικώς καθαρό υδροχλωρικό οξύ. Αυτή η αντίδραση μπορεί να δώσει πολύ καθαρό προϊόν, που μπορεί να χρησιμοποιηθεί ακόμη και από τις βιομηχανίες τροφίμων και φαρμάκων[5].
Οργανικές μέθοδοι[Επεξεργασία | επεξεργασία κώδικα]
Η μεγαλύτερη παραγωγή του υδροχλωρικού οξέος σχετίζεται με το σχηματισμό χλωριούχων οργανικών ενώσεων, όπως το τεφλόν (teflon), τα φρεόν (freon) και άλλοι χλωροφθοράνθρακες (CFCs), καθώς και του χλωροξικού οξέος αλλά και του PVC. Συχνά αυτή η παραγωγή του υδροχλωρικού οξέος συνδυάζεται με την απορρόφησή του επιτόπου (in situ).[6] Στις χημικές αντιδράσεις, τα άτομα υδρογόνου του υδρογονάνθρακα, αντικαθίστανται από άτομα χλωρίου οπότε σχηματίζονται χλωραλκάνια και υδροχλώριο. Η υποκατάσταση του χλωρίου από το δραστικότερο φθόριο του υδροφθορίου είναι μεταγενέστερη αντίδραση[7]:
Το υδροχλώριο που παράγεται είτε χρησιμοποιείται άμεσα είτε απορροφάται στο νερό με αποτέλεσμα την παραγωγή υδροχλωρικού οξέος για βιομηχανική χρήση.
Εργαστηριακές μέθοδοι[Επεξεργασία | επεξεργασία κώδικα]
Μικρές ποσότητες αερίου HCl, για εργαστηριακή χρήση, παράγονται από αφυδάτωση (πυκνού) υδροχλωρικού οξέος, που γίνεται με αφυδατικά μέσα, όπως το θειικό οξύ ή το άνυδρο χλωριούχο ασβέστιο (CaCl2). Εναλλακτικά, το HCl μπορεί να παραχθεί και από την αντίδραση του θειικού οξέος με χλωριούχο νάτριο[8]:
Αυτή η αντίδραση συμβαίνει στη θερμοκρασία δωματίου. Αν το όξινο θειικό νάτριο που απομένει θερμανθεί πάνω από τους 200 °C, η αντίδραση προχωρεί στην παραγωγή θειικού νατρίου:
Το HCl μπορεί επίσης να παρασκευαστεί με υδρόλυση ορισμένων δραστικών χλωριούχων ενώσεων όπως π.χ. οι ακόλουθες:
1. Ο πενταχλωριούχος φωσφόρος (PCl5) στον οποίο αν ενσταλάξουμε κρύο νερό πραγματοποιείται η αντίδραση:
- Η χημική ένωση POCl3 ονομάζεται οξυχλωριούχος φωσφόρος.
- Αν στην παραπάνω αντίδραση χρησιμοποιήσουμε ζεστό νερό, σχηματίζεται φωσφορικό οξύ:
2. Ο τριχλωριούχος φωσφόρος (PCl3):
- Η χημική ένωση H3PO3 ονομάζεται φωσφορώδες οξύ.
3. Το θειονυλοχλωρίδιο (SOCl2):
4.Διάφορα ακυλοχλωρίδια (RCOCl):
Η προσθήκη περίσσειας νερού στα αντιδρώντα των παραπάνω αντιδράσεων απορροφά το αέριο HCl που παράγεται, σχηματίζοντας υδροχλωρικό οξύ.
Δομή και ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]

|

| |
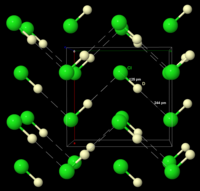
Δομή DCl (δευτεριοχλωρίου), όπως ερμηνεύθηκε από περίθλαση νετρονίων σε σκόνη DCl στους 77 K. Το DCl χρησιμοποιήθηκε αντί του HCl επειδή ο βαρύτερος πυρήνας του δευτερίου ανιχνεύεται ευκολότερα από τον πυρήνα του κοινού πρώτιου υδρογόνου. Μια «άπειρη» αλυσίδα ...DCl... παριστάνεται με διακεκομένες γραμμές.
| ||

Από αριστερά προς τα δεξιά : HF, HCl, HBr, HI
| Θερμοκρασία (°C) | 0 | 20 | 30 | 50 |
|---|---|---|---|---|
| Νερό | 823 | 720 | 673 | 596 |
| Μεθανόλη | 513 | 470 | 430 | |
| Αιθανόλη | 454 | 410 | 381 | |
| Διαιθυλαιθέρας | 356 | 249 | 195 |
Το μόριο του υδροχλωρίου είναι διατομικό και αποτελείται από ένα άτομο υδρογόνου (H) και ένα άτομο χλωρίου (Cl), που συνδέονται με απλό ομοιοπολικό δεσμό. Δεδομένου ότι το άτομο του χλωρίου είναι πολύ πιο ηλεκτροαρνητικό από το άτομο του υδρογόνου, ο δεσμός μεταξύ των δύο ατόμων είναι έντονα πολωμένος. Κατά συνέπεια, το μόριο έχει μεγάλη διπολική ροπή, με το στοιχειώδες αρνητικό φορτίο (δ-) να αποδίδεται στο άτομο χλωρίου και το θετικό (δ+) στο άτομο του υδρογόνου. Λόγω της μεγάλης του πολικότητας, το HCl είναι πολύ διαλυτό στο νερό (αλλά και σε άλλους πολικούς διαλύτες).
Το στερεοποιημένο HCl αλλάζει φάση δομής σε θερμοκρασία κάτω από 98,4 K. Η περίθλαση ακτίνων Χ σε σκόνη στερεού HCl δείχνει ότι αλλάζει από ορθορομβική δομή σε κυβική δομή κατά τη μετάβαση αυτής της της θερμοκρασίας. Και στις δυο δομές τα άτομα χλωρίου βρίσκονται σε προσωποκεντρική διάταξη. Ωστόσο, για τα άτομα υδρογόνου δεν μπορούσε αρχικά να γίνει προσδιορισμός θέσης[10]. Ανάλυση των φασματοσκοπικών και διηλεκτρικών δεδομένων και ο καθορισμός της δομής DCl τελικά έδειξαν ότι το HCl σχηματίζει αλυσίδες ζικ-ζακ στη στερεή κατάσταση, όπως κάνει και το υδροφθόριο[11].
Φάσματα υπερύθρου (IR)[Επεξεργασία | επεξεργασία κώδικα]

Το υπέρυθρο φάσμα του αέριου υδροχλωρίου αποτελείται από μια σειρά έντονων γραμμών απορρόφησης, συγκεντρωμένων γύρω από τα 2886 cm−1 (μήκος κύματος, λ ~ 3,47 μm). Το μόριο του HCl απορροφά φωτόνια και διεγείρεται έτσι η κινητική του ενέργεια, από περιστροφή και δόνηση.
Ένας χημικός δεσμός μπορεί να θεωρηθεί απλοϊκά ως ένα ελατήριο με ορισμένη σταθερά του Χουκ (Hooke). Ωστόσο, σύμφωνα με την κβαντομηχανική, μόνο ορισμένοι τρόποι δόνησης είναι επιτρεπτοί. Η ενέργεια επομένως μπορεί να γραφτεί ως εξής:
Σε θερμοκρασία δωματίου, σχεδόν όλα τα μόρια είναι στη βασική τους κατάσταση και έχουν v = 0. Για να μεταβεί ένα μόριο HCl μόριο στην πρώτη διεγερμένη κατάσταση (v = 1), θα έπρεπε να απορροφά περίπου στα 2880 cm−1. Αυτή η απορρόφηση (σειρά Q), όμως, δεν παρατηρείται, επειδή είναι απαγορευμένη, για λόγους συμμετρίας. Στη θέση της εμφανίζονται οι δύο σειρές των σημάτων (σειρές P και R) που οφείλονται στην περιστροφή των μορίων. Λόγω των κανόνων της κβαντομηχανικής, επιτρέπονται μόνον ορισμένοι τρόποι περιστροφής ενός μορίου. Χαρακτηρίζονται από τον κβαντικό αριθμό περιστροφής J = 0, 1, 2, 3, ... Το ΔJ μπορεί να πάρει μόνο τιμές ±1.
Η τιμή του Β είναι πολύ μικρότερη από το ve, έτσι ώστε να απαιτείται μικρότερη ενέργεια για την περιστροφή του μορίου, σε σύγκριση με αυτήν που απαιτείται για τη δόνηση.

Αυτή η ενέργεια για ένα τυπικό μόριο, βρίσκεται στην περιοχή των μικροκυμάτων. Ωστόσο, λόγω της ενέργειας δόνησης του μορίου, το σύνολο των απορροφήσεων βρίσκεται μέσα στην υπέρυθρη περιοχή. Έτσι η λήψη του φάσματος IR του υδροχλωρίου που δείχνει τους τρόπους δόνησης και περιστροφής του μορίου, δεν παρουσιάζει δυσκολίες και μπορεί να γίνει με ένα απλό φασματοφωτόμετρο υπερύθρων.
Το φυσικό χλώριο αποτελείται από δύο ισότοπα, 35Cl και 37Cl, με λόγο περίπου 3:1. Παρόλο που για τα δύο ισότοπα οι σταθερές δόνησης είναι παρόμοιες, οι ανηγμένες μάζες είναι διαφορετικές, δημιουργώντας διαφορές στην ενέργεια περιστροφής, οπότε οι δύο κορυφές παρατηρούνται δίπλα (δίπλα, δηλαδή πολύ κοντά η μία με την άλλη) στη γραμμή απορρόφησης και τα ύψη τους έχουν λόγο 3:1, λόγω της ύπαρξης των διαφορετικών ισοτόπων.
Όξινη συμπεριφορά[Επεξεργασία | επεξεργασία κώδικα]
Σε υδατικό διάλυμα, το HCl ιοντίζεται πλήρως αποδίδοντας κατιόντα υδροξωνίου (H3O+) και ανιόντα χλωρίου (Cl-) σύμφωνα με την πρωτολυτική μονόδρομη αντίδραση:
Το υδατικό διάλυμα ονομάζεται υδροχλωρικό οξύ και είναι ισχυρό οξύ. Όμως και απουσία νερού, δηλαδή σε άνυδρες συνθήκες, το υδροχλώριο εξακολουθεί να δρα ως οξύ. Για παράδειγμα, μπορεί να διαλυθεί σε άλλους διαλύτες όπως η μεθανόλη:
ή να αντιδράσει στην αέρια φάση με βάσεις όπως η αμμωνία :
Αντιδράσεις με οργανικές ενώσεις[Επεξεργασία | επεξεργασία κώδικα]
Αντιδράσεις προσθήκης[Επεξεργασία | επεξεργασία κώδικα]
1. Η προσθήκη του υδροχλωρίου[12] στο διπλό δεσμό άνθρακα-άνθρακα καθορίζεται από τον κανόνα του Μαρκόβνικοβ (Markovnikov)[13]. Π.χ.[14]:
2. Η αντίδραση του υδροχλωρίου με αλκίνια είναι ηλεκτρονιόφιλη προσθήκη και ακολουθεί τον ίδιο μηχανισμό όπως και στα αλκένια δηλαδή μέσω ενός καρβοκατιόντος. Π.χ.[15]:
3. Η αντίδραση του υδροχλωρίου με συζυγή αλκαδιένια αντιστοιχεί κυρίως σε 1,4-προσθήκη, αν και είναι επίσης δυνατές η 1,2-προσθήκη και η 3,4-προσθήκη, με τη χρήση κατάλληλων συνθηκών. Π.χ[14]:
(1,4-προσθήκη)
(1,2-προσθήκη)
(3,4-προσθήκη)
4. Η αντίδραση του υδροχλωρίου με κυκλοπροπάνιο αντιστοιχεί με 1,3-κυκλοπροσθήκη[16]:
5. Η αντίδραση του υδροχλωρίου με οξιράνιο αντιστοιχεί με 1,3-κυκλοπροσθήκη[17].:
Πυρηνόφιλη υποκατάσταση σε αλκοόλες[Επεξεργασία | επεξεργασία κώδικα]
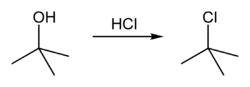
Οι αλκοόλες (ROH) αντιδρούν με υδροχλώριο με αντίδραση πυρηνόφιλης υποκατάστασης και η αντίδραση καταλύεται από θειικό οξύ:
Το HCl είναι το δεύτερο λιγότερο δραστικό για πυρηνόφιλη υποκατάσταση από τα υδραλογόνα (μετά το υδροφθόριο) και γενικά απαιτεί την παρουσία χλωριούχου ψευδαργύρου (ZnCl2) για να αντιδράσει με δευτεροταγείς και πρωτοταγείς αλκοόλες όπως (για παράδειγμα) η 1-προπανόλη:
Από την άλλη πλευρά, η πολύ δραστική μεθυλο-2-προπανόλη (τριτοταγής αλκοόλη), μετατρέπεται σε μεθυλο-2-χλωροπροπάνιο, με απλή ανάδευση της αλκοόλης με πυκνό υδροχλωρικό οξύ, σε θερμοκρασία δωματίου:
Εφαρμογές[Επεξεργασία | επεξεργασία κώδικα]
Το μεγαλύτερο μέρος του υδροχλωρίου χρησιμοποιείται για την παραγωγή του υδροχλωρικού οξέος. Αποτελεί επίσης σημαντικό αντιδραστήριο σε άλλες βιομηχανικές εφαρμογές όπως π.χ. στην υδροχλωρίωση του καουτσούκ και στην παραγωγή του βινυλο- και αλκυλο-χλωριδίων.
Στη βιομηχανία των ημιαγωγών, το αέριο υδροχλώριο χρησιμοποιείται και στον καθαρισμό των κρυστάλλων των ημιαγωγών αλλά και στη μετατροπή του πυριτίου (Si) σε τριχλωροσιλάνιο (SiHCl3)[18]
Όταν πρέπει να χρησιμοποιηθεί άνυδρο υδροχλώριο, σε διεργασίες μικρής κλίμακας, φυλάσσεται σε κυλίνδρους.
Ασφάλεια[Επεξεργασία | επεξεργασία κώδικα]
Εισπνοή αναθυμιάσεων υδροχλωρικού οξέος μπορεί να προκαλέσει βήχα, πνιγμό, φλεγμονή της μύτης, του λαιμού, και του ανώτερου αναπνευστικού συστήματος. Σε σοβαρές περιπτώσεις, δηλαδή αν εισπνευθεί σε αρκετά μεγάλες συγκεντρώσεις, προκαλείται πνευμονικό οίδημα, ανεπάρκεια του κυκλοφορικού συστήματος, και τέλος θάνατος. Επαφή με το δέρμα μπορεί να προκαλέσει ερυθρότητα, πόνο και σοβαρά χημικά εγκαύματα. Το υδροχλώριο μπορεί επίσης να προκαλέσει σοβαρά εγκαύματα στα μάτια ή και μόνιμη τύφλωση.
Το αέριο υδροχλώριο είναι έντονα υδρόφιλο και μπορεί εύκολα να καθαριστεί από τα υπόλοιπα αέρια προϊόντα μιας αντίδρασης που το παράγει με απευθείας διέλευσή τους μέσα από νερό, παράγοντας έτσι χρήσιμο υδροχλωρικό οξύ, ακόμη και ως παραπροϊόν, απαλλάσσοντας συγχρόνως τη γύρω ατμόσφαιρα από την επικίνδυνη παρουσία του.
Κάθε εξοπλισμός που χειρίζεται αέριο υδροχλώριο πρέπει οπωσδήποτε να ελέγχεται σε μια τακτική βάση, ιδιαίτερα τα συστήματα βαλβίδων και οι ρυθμιστές. Ο χειρισμός του αερίου υδροχλωρίου απαιτεί τη χρήση ειδικών υλικών σε όλα τα υγρά τμήματα της οδού ροής του, αφού το υδροχλώριο (ή το υδροχλωρικό οξύ που παράγεται στα υγρά σημεία) αντιδρούν και διαβρώνουν πολλά υλικά. Απαιτείται η χρήση ανοξείδωτων ή πολυμερών υλικών.
Πηγές[Επεξεργασία | επεξεργασία κώδικα]
- Μπαζάκης Ι. Α. "Γενική Χημεία", Αθήνα.
- Βασιλικιώτης Γ. Σ. "Ποιοτική Ανάλυση", Θεσσαλονίκη 1980.
- Βασιλικιώτης Γ. Σ. "Ποσοτική Ανάλυση", Θεσσαλονίκη 1980.
- Μανουσάκης Γ.Ε. "Γενική και Ανόργανη Χημεία", Τόμοι 1ος και 2ος, Θεσσαλονίκη 1981.
- Μανωλκίδης Κ., Μπέζας Κ. "Στοιχεία Ανόργανης Χημείας", Έκδοση 14η, Αθήνα 1984.
- Μανωλκίδης Κ., Μπέζας Κ. "Χημικές Αντιδράσεις", Αθήνα 1976.
- Δημητριάδης Θ. Γ. "Test Οξειδοαναγωγής", Αθήνα 1989.
- Τοσσίδης Ι. "Χημεία Ενώσεων Συναρμογής", Θεσσαλονίκη 1986.
- Βασιλικιώτης Γ. Σ. "Χημεία Περιβάλλοντος", Θεσσαλονίκη 1986.
- Μπόσκου Δ. "Χημεία τροφίμων με Στοιχεία Τεχνολογίας Τροφίμων", Θεσσαλονίκη 1986.
Αναφορές και σημειώσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Για εναλλακτικές ονομασίες δείτε τον πίνακα πληροφοριών.
- ↑ Σχηματίζονται από σταγονίδια πυκνού υδροχλωρικού οξέος
- ↑ Hartley, Harold (1960). "The Wilkins Lecture. Sir Humphry Davy, Bt., P.R.S. 1778–1829". Proceedings of the Royal Society A 255 (1281): 153–180. Bibcode:1960RSPSA.255..153H. doi:10.1098/rspa.1960.0060.
- ↑ Ενδιάμεσα παράγεται νάτριο που όμως αντιδρά με το νερό παράγοντας υδρογόνο και υδροξείδιο του νατρίου.
- ↑ Αυτές οι βιομηχανίες θέτουν προδιαγραφές μεγαλύτερης καθαρότητας των πρώτων υλών τους και των προϊόντων τους, για ευνόητους λόγους.
- ↑ Επιτόπου, στη θέση παραγωγής
- ↑ Η δεύτερη αντίδραση σε τριτοταγή αλκυλοχλωρίδια με τον SN1 μηχανισμό είναι εφικτή, αν και δημιουργείται χημική ισορροπία, που μπορεί να ευνοήσει την παραγωγή αέριου υδροχλωρίου σε θερμοκρασίες αρκετά χαμηλές ώστε το υδροχλώριο να απομακρύνεται ως αέριο, ενώ το υδροφθόριο να παραμένει στο χώρο της αντίδρασης ως υγρό. Φυσικά αυτή η περίπτωση δεν ισχύει αν τα αλκυλοφθορίδια και τα υδροχλωρίδια είναι επίσης αέρια. Στα υπόλοιπα, με τον SN2 μηχανισμό που επικρατεί, ευνοείται η αντίστροφη αντίδραση, δηλαδή η παραγωγή αλκυλοχλωριδίου και υδροφθορίου, γιατί τα ανιόντα Cl- αποτελούν αρκετά ισχυρότερο πυρηνόφιλο αντιδραστήριο από τα ανιόντα F-.
- ↑ Francisco J. Arnsliz (1995). "A Convenient Way To Generate Hydrogen Chloride in the Freshman Lab". J. Chem. Ed. 72 (12): 1139. Bibcode:1995JChEd..72.1139A. doi:10.1021/ed072p1139.
- ↑ Hydrochloric Acid - Compound Summary. Pubchem
- ↑ Natta, G. (1933). «Struttura e polimorfismo degli acidi alogenidrici» (στα Italian). Gazzetta Chimica Italiana 63: 425–439.
- ↑ Sándor, E.; Farrow, R. F. C. (1967). «Crystal Structure of Solid Hydrogen Chloride and Deuterium Chloride». Nature 213 (5072): 171–172. doi:. Bibcode: 1967Natur.213..171S.
- ↑ Αποφεύγεται η χρήση υδροχλωρικού οξέος για να μην γίνει ταυτόχρονα προσθήκη νερού στο αλκένιο.
- ↑ Το Cl προστίθεται στον άνθρακα του διπλού δεσμού με τα λιγότερα υδρογόνα
- ↑ 14,0 14,1 Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 156, §6.8.1.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 158, §6.9.1.
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, §6.3., σελ. 79, εφαρμογή για κυκλοαλκάνια και για Ε = Η και Nu = Cl σε συνδυασμό με Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985, §1.2., σελ. 22-25
- ↑ Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985, §2.1., σελ. 16-17. Εφαρμογή γενικού τύπου για A = Cl και B = H.
- ↑ Si + 3HCl → SiHCl3 + H2. Το τριχλωροσιλάνιο χρησιμοποιείται για την παρασκευή πολυμερών του πυριτίου
Δείτε επίσης[Επεξεργασία | επεξεργασία κώδικα]
Εξωτερικοί σύνδεσμοι[Επεξεργασία | επεξεργασία κώδικα]
| |||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
|






![{\displaystyle \mathrm {RH+Cl_{2}{\xrightarrow[{\triangle }]{hv}}RCl+HCl} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/c08ce7a157173a9b031ca9d479319ca7f7218ae9)