Ομοιοπολικός δεσμός

Ομοιοπολικός δεσμός ονομάζεται ο χημικός δεσμός που αναπτύσσεται μεταξύ εκείνων των ατόμων που «μοιράζονται» κάποια ηλεκτρόνια, συνήθως κατά ζεύγη. Πιο αναλυτικά, η σταθερή ισορροπία των ελκτικών και των απωστικών δυνάμεων που αναπτύσσονται μεταξύ των ατόμων που «μοιράζονται» ηλεκτρόνια είναι γνωστή ως «ομοιοπολικός δεσμός»[1]. Για πολλά μόρια, η συνεισφορά ηλεκτρονίων επιτρέπει κάθε άτομο να αποκτά το ισοδύναμο της εξωτερικής στιβάδας ενός ευγενούς αερίου, που αντιπροσωπεύει μια σταθερή ηλεκτρονιακή διαμόρφωση.
Οι ομοιοπολικοί δεσμοί συμπεριλαμβάνουν πολλά υποείδη αλληλεπιδράσεων. Πιο συγκεκριμένα, τα πιο συνηθισμένα είναι τα ακόλουθα[2][3]:
- Δεσμοί σ.
- Δεσμοί π.
- Διαμεταλλικοί δεσμοί.
- Γωνιακοί δεσμοί.
- Δεσμοί τριών κέντρων και δύο ηλεκτρονίων.
Η χρήση του όρου «ομοιοπολικός δεσμός» χρονολογείται από το 1939[4]. Προέρχεται από την απόδοση στα ελληνικά του αγγλικού όρου covalent[5], το πρόθεμα co- του οποίου σημαίνει «μαζί», δηλαδή συνεργασία σε μια δράση, συνεταιρισμός σε μικρότερο βαθμό κ.τ.λ. Έτσι ένας co-valent bond σημαίνει επομένως ότι τα άτομα μοιράζονται σθένος, γιατί η λέξη valent προέρχεται από τον όρο valence, όπως αυτό συζητήθηκε στη θεωρία σθένους - δεσμού (valence bond theory). Στο μόριο του (δι)υδρογόνου (H2) (το απλουστερο δυνατό ουδέτερο μόριο) τα άτομα υδρογόνου μοιράζονται τα δυο (συνολικά) ηλεκτρόνιά τους μέσω ενός ομοιοπολικού δεσμού[6]. Η «συνεργασία σθένους» είναι μέγιστη μεταξύ των ατόμων που έχουν παρόμοιες ηλεκτραρνητικότητες. Έτσι, οι ομοιοπολικοί δεσμοί δεν γίνονται αναγκαστικά μεταξύ δυο ατόμων του ίδιου χημικού στοιχείου, αλλά απλά μεταξύ ατόμων χημικών στοιχείων με συγκρίσιμη ηλεκτραρνητικότητα. Όταν σχηματίζεται ομοιοπολικός δεσμός με συνεισφορά ηλεκτρονίων που προέρχονται από περισσότερα από δυο άτομα, τότε λέγεται ότι ένας τέτοιος δεσμός είναι «απεντοπισμένος».
Όταν σ΄ ένα ομοιοπολικό δεσμό και τα δύο ηλεκτρόνια προσφέρονται από το ίδιο άτομο τότε ο δεσμός λέγεται ημιπολικός δεσμός ή δοτικός ομοιοπολικός δεσμός ή δεσμός σύνταξης ή δεσμός συναρμογής ή διπολικός δεσμός.
Επίσης διπλός δεσμός καλείται το ζεύγος ομοιοπολικών δεσμών μεταξύ δύο ατόμων όπου κάθε άτομο προσφέρει από 2 ηλεκτρόνια, ενώ τριπλός δεσμός καλείται η τριάδα ομοιοπολικών δεσμών μεταξύ δύο ατόμων όπου κάθε άτομο προσφέρει από 3 ηλεκτρόνια.
Ιστορικό[Επεξεργασία | επεξεργασία κώδικα]
Ο όρος «ομοιοπολικός», όσον αφορά τη δεσμολογία, χρησιμοποιήθηκε για πρώτη φορά το 1919 από τον Ίρβιγκ Λάγκμουιρ (Irving Langmuir) σε ένα άρθρο στο Περιοδικό της Αμερικανικής Χημικής Κοινωνίας (Journal of the American Chemical Society article) που είχε τίτλο «Η διευθέτηση των ηλεκτρονίων σε άτομα και μόρια» (The Arrangement of Electrons in Atoms and Molecules). Ο Λάγκμουιρ έγραψε ότι «...θα συμβολίζουμε με τον όρο ομοιοπολικότητα τον αριθμό των ζευγών των ηλεκτρονίων που ένα δεδομένο άτομο μοιράζεται με τα γειτονικά του...» ("...we shall denote by the term covalence the number of pairs of electrons that a given atom shares with its neighbors...")[7]
Η ιδέα του ομοιοπολικού δεσμού μπορεί να ιχνηλατηθεί αρκετά χρόνια νωρίτερα από το 1919, στον Γκίλμπερτ Λιούις (Gilbert N. Lewis), ο οποίος το 1916 περιέγραψε το μοίρασμα των ηλεκτρονιακών ζευγών μεταξύ των ατόμων[8]. Εισήγαγε τη σημειογραφία κατά Λιούις ή «ηλεκτρονιακή σημειογραφία με σημεία» ή «ηλεκτρονιακή σημειογραφία Λιούις με σημεία», στην οποία τα ηλεκτρόνια σθένους, δηλαδή τα ηλεκτρόνια της εξωτερικής στιβάδας, αναπαριστάνονται με σημεία (βούλες) γύρω από τα χημικά σύμβολα των χημικών στοιχείων. Τα ζεύγη των ηλεκτρονίων που τοποθετούνται ανάμεσα στα χημικά σύμβολα αντιπροσωπεύουν τους ομοιοπολικούς δεσμούς. Πολλαπλά ζεύγη ηλεκτρονίων αντιπροσωπεύουν πολλαπλούς δεσμούς, όπως διπλούς δεσμούς και τριπλούς δεσμούς. Σε μια άλλη μορφή αναπαράστασης, που δεν δείχνεται εδώ, τα ηλεκτρονιακά ζεύγη που σχηματίζουν χημικούς δεσμούς αντιπροσωπεύονται με συνεχόμενες γραμμές.
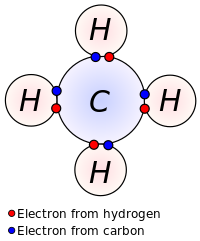
Ο Λιούις πρότεινε ότι ένα άτομο σχηματίζει αρκετούς ομοιοπολικούς δεσμούς για να σχηματίσει μια πλήρη εξωτερική ηλεκτρονιακή στιβάδα. Στο διάγραμμα του μεθανίου που δείχνεται εδώ, ο άνθρακας έχει σθένος 4, και γι' αυτό περιβάλλεται από 8 ηλεκτρόνια («κανόνας οκτάδας»), από τα οποία τα 4 προέρχονται από το ίδιο το άτομο του άνθρακα και τα άλλα 4 από τα 4 άτομα υδρογόνου που συνδέονται με το άτομο του άνθρακα (στο μόριο του μεθανίου πάντα). Κάθε άτομο υδρογόνου έχει σθένος 1 και περιβάλλεται από 2 ηλεκτρόνια («κανόνας δυάδας»), δηλαδή το μοναδικό δικό του συν ένα από το άτομο του άνθρακα. Ο αριθμός των ηλεκτρονίων που αντιστοιχεί σε πλήρη στιβάδα σύμφωνα με την κβαντική θεωρία του ατόμου λέει για το άτομο του άνθρακα, με εξώτατη στιβάδα που έχει n = 2, ότι μπορεί να κρατήσει μέχρι και 8 ηλεκτρόνια, ενώ για το άτομο του υδρογόνου, με εξώτατη στιβάδα που έχει n = 1, ότι μπορεί να κρατήσει μέχρι και 2 μόνο ηλεκτρόνια.
Ενώ η ιδέα των μοιραζόμενων ηλεκτρονιακών ζευγών προσφέρει μια αποτελεσματική ποιοτική εικόνα της ομοιοπολικής δεσμολογίας, η κβαντομηχανική χρειάστηκε να κατανοήσει τη φύση αυτών των δεσμών και να προβλέψει τις δομές και τις ιδιότητες των απλών μορίων. Οι Bάλτερ Χάιτλερ (Walter Heitler) και Φριτζ Λόντον (Fritz Londo) πιστώθηκαν με την πρώτη επιτυχημένη κβαντομηχανική εξήγηση ενός χημικού δεσμού, και πιο συγκεκριμένα του δεσμού του μοριακού υδρογόνου, το 1927[9]. Η εργασία τους βασίστηκε στο μοντέλο του δεσμού σθένους, που υποθέτει ότι ένας χημικός δεσμός σχηματίζεται όταν υπάρχει μια καλή επικάλυψη μεταξύ των ατομικών τροχιακών των ατόμων που συμμετέχουν στον χημικό δεσμό. Αυτά τα ατομικά τροχιακά είναι γνωστό ότι έχουν ειδικές γωνιακές σχέσεις μεταξύ τους, και έτσι το μοντέλο του δεσμού σθένους μπορεί να προβλέψει επιτυχημένα τις δεσμικές γωνίες που παρατηρούνται σε απλά μόρια.
Φυσικές ιδιότητες των ομοιοπολικών ενώσεων (πολικών και μη πολικών)[Επεξεργασία | επεξεργασία κώδικα]
| Φυσικές ιδιότητες | Ομοιοπολικές ενώσεις |
|---|---|
| Κατάσταση της ύλης (σε συνθήκες δωματίου, 20 °C, 1 atm) | Στερεές, υγρές ή αέριες |
| Ηλεκτρική αγωγιμότητα | Συνήθως καθόλου |
| Θερμοκρασίες τήξης και βρασμού | Ποικίλλουν, αλλά συνήθως χαμηλότερες από τις ιονικές ενώσεις |
| Διαλυτότητα στο νερό | Ποικίλλει, αλλά συνήθως χαμηλότερη από τις ιονικές ενώσεις |
| Θερμική αγωγιμότητα | Συνήθως χαμηλή |
Πολικότητα των ομοιοπολικών δεσμών[Επεξεργασία | επεξεργασία κώδικα]
Οι ομοιπολικοί δεσμοί επηρεάζονται από τη διαφορά ηλεκτραρνητικότητας των συνδεμένων ατόμων. Δύο άτομα με ίση ηλεκτραρνητικότητα δίνουν μη πολικούς ομοιοπολικούς δεσμούς, όπως ο δεσμός Η - H. Μια άνιση σχέση δημιουργεί έναν πολωμένο ομοιοπολικό δεσμό, όπως ο δεσμός Η - Cl. Καθε πολωμενος ομοιοπολικος δεσμός χαρακτηριζεται απο ενα διανυσματικο μέγεθος, τη διπολικη ροπη.
Υποδιαίρεση των ομοιοπολικών δεσμών[Επεξεργασία | επεξεργασία κώδικα]
Υπάρχουν τρεις (3) τύποι ομοιοπολικών ουσιών:
- Ανεξάρτητα μόρια.
- Μοριακές δομές.
- Μακρομοριακές δομές.
Τα ανεξάρτητα μόρια έχουν πολύ ισχυρούς δεσμούς που κρατούν τα άτομα μαζί, αλλά υπάρχουν αμελητέες δυνάμεις έλξης μεταξύ των μορίων. Τέτοιες ομοιοπολικές ουσίες είναι συνήθως αέριες. Παραδείγματα αυτών αποτελούν το HCl, το SO2, το CO2 και το CH4. Στις μοριακές δομές υπάρχουν αδύναμες δυνάμεις διαμοριακής έλξης. τέτοιες ομοιοπολικές ουσίες είναι συνήθως πτητικές υγρές, όπως για παράδειγμα η αιθανόλη, ή χαμηλότηκτα στερεά, όπως για παράδειγμα το ιώδιο και το στερεό διοξείδιο του άνθρακα. Οι μακρομοριακές δομές περιέχουν μεγάλο αριθμό ατόμων συνδεμένων σε οιονεί 1-D σχηματισμούς / αλυσίδες (πχ πολυαιθυλένιο και άλλα οργανικά πολυμερή), φύλλα (πχ γραφίτης) ή και τριδιάστατα πλέγματα (πχ διαμάντι και χαλαζίας). Τα οργανικά πολυμερή εμφανίζουν μέσου επιπέδου σημεία τήξεως (ενδεικτικά: 50-300 °C) ενώ δεν εμφανίζουν σημείο ζέσεως. Κάποιες από τις ουσίες με 2-D ή 3-D πλέγματα έχουν υψηλά σημεία τήξεως και ζέσεως, και τα στερεά τους είναι συχνά εύθραυστα και ηλεκτρικοί μονωτές (όχι όμως ο γραφίτης). Χημικά στοιχεία που έχουν υψηλή ηλεκτραρνητικότητα και την ικανότητα να σχηματίζουν δεσμούς με 3 - 4 ηλεκτρονιακά ζεύγη, συχνά σχηματίζουν τέτοιες μεγάλες μακρομοριακές δομές[10].
Δείτε επίσης[Επεξεργασία | επεξεργασία κώδικα]
- Μεταλλικός δεσμός
- Ομοιοπολικός δεσμός συναρμογής
- Δεσμολογία στερεών
- Γραμμικός συνδυασμός ατομικών τροχιακών
- Υβριδισμός
- Δεσμός υδρογόνου
- Μη ομοιοπολική δεσμολογία
- Δισουλφιδικός δεσμός
- Ετεροπολικός δεσμός
- Ομοιοπολική ακτίνα
- Μεσομέρεια
- Τάξη δεσμού
- Μοιραζόμενο ζεύγος ηλεκτρονίων
Παραπομπές και σημειώσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Campbell, Neil A.; Brad Williamson; Robin J. Heyden (2006). Biology: Exploring Life. Boston, Massachusetts: Pearson Prentice Hall. ISBN 0-13-250882-6. Retrieved 2012-02-05.
- ↑ March, Jerry (1992). Advanced organic chemistry: reactions, mechanisms, and structure. John Wiley & Sons. ISBN 0-471-60180-2.
- ↑ Gary L. Miessler; Donald Arthur Tarr (2004). Inorganic chemistry. Prentice Hall. ISBN 0-13-035471-6.
- ↑ Merriam-Webster – Collegiate Dictionary (2000).
- ↑ Η ακριβολογική μετάφραση του όρου στα ελληνικά θα ήταν μάλλον «δεσμός συνεταιρικού σθένους»
- ↑ Chemical Bonds". Hyperphysics.phy-astr.gsu.edu. Retrieved 2013-06-09.
- ↑ Langmuir, Irving (1919-06-01). "The Arrangement of Electrons in Atoms and Molecules". Journal of the American Chemical Society 41 (6): 868–934. doi:10.1021/ja02227a002.
- ↑ Lewis, Gilbert N. (1916-04-01). "The atom and the molecule". Journal of the American Chemical Society 38 (4): 762–785. doi:10.1021/ja02261a002.
- ↑ W. Heitler and F. London, Zeitschrift für Physik, vol. 44, p. 455 (1927). English translation in Hettema, H. (2000). Quantum chemistry: classic scientific papers. World Scientific. pp. 140–. ISBN 978-981-02-2771-5. Retrieved 2012-02-05.
- ↑ Stranks, D. R.; M. L. Heffernan, K. C. Lee Dow, P. T. McTigue, G. R. A. Withers (1970). Chemistry: A structural view. Carlton, Victoria: Melbourne University Press. p. 184. ISBN 0-522-83988-6.
| ||||||||||||||||||||||||||||||||||||||
| |||||||||||
