Οξύ

Τα οξέα (από τη λατινική λέξη acidus, που σημαίνει «ξινό»[1]) είναι ένα σύνολο χημικών ουσιών που εμφανίζει ένα σύνολο κοινών ιδιοτήτων, γνωστών ως «όξινος χαρακτήρας» ή «όξινη αντίδραση». Οι πιο χαρακτηριστικές από αυτές είναι η όξινη γεύση, η ικανότητα να αλλάζουν το χρώμα οξεοβασικών δεικτών, όπως το βάμμα ηλιοτροπίου, που αλλάζει χρώμα από μπλε σε κόκκινο, παρουσία οξέων. Επίσης, τα οξέα έχουν την ικανότητα να αντιδρούν με βάσεις, ανθρακικά άλατα και ορισμένα μέταλλα, όπως το ασβέστιο, σχηματίζοντας άλατα. Τα υδατικά διαλύματα των οξέων έχουν pH < 7. Ένα χαμηλότερο pH, σημαίνει μια υψηλότερη οξύτητα, και έτσι μια υψηλότερη συγκέντρωση υδρογονοκατιόντων στο διάλυμα. Οι χημικές ουσίες που έχουν «όξινο χαρακτήρα», δηλαδή ιδιότητες οξέων, λέγονται «όξινες».
Συνηθισμένα παραδείγματα οξέων περιλαμβάνουν το υδροχλωρικό οξύ, ένα διάλυμα υδροχλωρίου, το οποίο βρίσκεται στο γαστρικό οξύ, που βρίσκεται στο στομάχι και ενεργοποιεί ορισμένα πεπτικά ένζυμα, το αιθανικό οξύ, με το γνωστό ξίδι να αποτελεί αραιό διάλυμα αυτού του υγρού, το θειικό οξύ, που χρησιμοποιήθηκε σε ηλεκτρικούς συσσωρευτές αυτοκινήτων, και το τρυγικό οξύ, ένα στερεό οξύ που χρησιμοποιείται στην παραγωγή αρτοσκευασμάτων και στη ζαχαροπλαστική. Αυτά τα παραδείγματα δείχνουν ότι τα οξέα μπορούν να είναι διαλύματα ή και καθαρές χημικές ουσίες, που μπορεί να είναι σε αέρια, υγρή ή στερεά κατάσταση. Τα ισχυρά οξέα και κάποια πυκνά ασθενή οξέα είναι διαβρωτικά, αλλά υπάρχουν κάποιες εξαιρέσεις, όπως τα καρβοράνια και το βορικό οξύ.
Υπάρχουν τρεις (3) συνηθισμένοι ορισμοί για τα οξέα:
- Ο ορισμός κατ' Αρρένιους, που ορίζει ως οξέα τα μόρια, που όταν διαλύονται στο νερό, αυξάνουν τη συγκέντρωση των υδρογονοκατιόντων (H+), ή για μεγαλύτερη ακρίβεια, αυξάνουν τη συγκέντρωση των υδροξωνίων (H3O+).
- Ο ορισμός κατά Μπρόνστεντ και Λόρυ, που ορίζει ως οξέα τις χημικές ουσίες που μπορούν να δράσουν ως δότες πρωτονίων. Σύμφωνα με τον ορισμό αυτό κάθε χημική ουσία που μπορεί εύκολα να αποπρωτονιωθεί μπορεί να θεωρείται ως ένα οξύ. Παραδείγματα τέτοιων ουσιών, που δεν περιλαμβάνονται στον ορισμό κατ' Αρρένιους, περιλαμβάνουν τις αλκοόλες και τις αμίνες, που περιέχουν ομάδες O-Η ή N-H. Και οι δυο ομάδες ενώσεων συμπεριφέρονται και ως οξέα και ως βάσεις κατά Μπρόνστεντ και Λόρυ, γιατί ανάλογα με τις συνθήκες μπορούν να δώσουν ή να λάβουν πρωτόνιο.
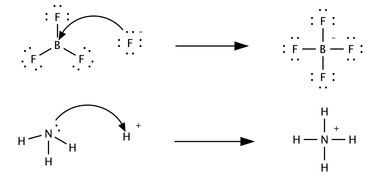
- Ο ορισμός κατά Λιούις, που ορίζει ως οξέα τις χημικές ουσίες που μπορούν να δράσουν ως δέκτες ζεύγους ηλεκτρονίων, για να σχηματίσουν έναν ομοιοπολικό δεσμό. Παραδείγματα τέτοιων ουσιών, που δεν περιλαμβάνονται στους υπόλοιπους δύο (2) ορισμούς οξέων περιλαμβάνουν όλα τα κατιόντα μετάλλων, και μόρια με έλλειμμα ηλεκτρονίων, όπως το τριφθοριούχο βόριο (BF3) και το τριφθοριούχο αργίλιο (AlF3).
Ορισμοί και έννοιες
[Επεξεργασία | επεξεργασία κώδικα]Οι σύγχρονοι ορισμοί για τα οξέα ασχολούνται με τις θεμελιώδεις χημικές αντιδράσεις που είναι κοινές για όλα τα οξέα.
Τα περισσότερα οξέα που συναντώνται στην καθημερινή ζωή είναι υδατικά διαλύματα, ή μπορούν να διαλυθούν στο νερό, για τα οποία οι ορισμοί του Αρρένιους και των Μπρόνστεντ - Λόουρυ είναι πιο σχετικοί. Ιδιαίτερα ο ορισμός των Μπρόνστεντ - Λόουρυ είναι ο ευρύτερα χρησιμοποιούμενος ορισμός, ή αλλιώς, οι οξεοβασικές αντιδράσεις θεωρούνται ότι περιλαμβάνουν τη μεταφορά ενός (τουλάχιστον) πρωτονίου από ένα οξύ σε μια βάση.
Τα ιόντα υδροξωνίου (H3O+) είναι οξέα σύμφωνα και με τους τρεις (3) ορισμούς. Επιπρόσθετα, παρόλο που οι αλκοόλες και οι αμίνες είναι οξέα σύμφωνα με τον ορισμό κατά Μπρόνστεντ - Λόουρυ, μπορούν επίσης να λειτουργήσουν ως βάσεις, με βάση τον ορισμό κατά Λιούις, γιατί τα άτομα οξυγόνου και αζώτου που διαθέτουν, έχουν μονήρη ζεύγη ηλεκτρονίων για να δώσουν.
Οξέα κατ' Αρρένιους
[Επεξεργασία | επεξεργασία κώδικα]
Ο Σουηδός χημικός Σβάντε Αρρένιους (Svante Arrhenius) απέδωσε τις ιδιότητες της οξύτητας στα υδρογονοκατιόντα ή πρωτόνια (H+) το 1884. Ένα οξύ κατ' Αρρένιους είναι μια χημική ουσία, που όταν προστίθεται σε νερό, αυξάνει τη συγκέντρωση των υδρογονοκατιόντων σε αυτό. Σημειώστε ότι οι χημικοί συχνά γράφουν H+(aq) για να αναφερθούν στα υδροονοκατιόντα όταν περιγράφουν οξεοβασικές αντιδράσεις, αλλά ξέρουν ότι στην πραγματικότητα ελεύθερα, δηλαδή γυμνά πρωτόνια, δεν υπάρχουν στο νερό, αλλά σχηματίζουν ιόντα υδροξωνίου (H3O+). Έτσι, ένα οξύ κατ' Αρρένιους μπορεί επίσης να περιγραφεί ως μια χημική ουσία, αυξάνει τη συγκέντρωση των υδροξωνίων, όταν προστίθεται σε νερό. Αυτός ο ορισμός πηγάζει από τη χημική ισορροπία διάστασης του νερού σε ιόντα υδροξωνίου και υδροξυλίου (OH-)[2]:
Στο καθαρό νερό η πλειοψηφία των μορίων του νερού βρίσκονται στη μορφή των ουδέτερων μορίων H2O, αλλά ένα μικρό κλάσμα αυτών, σε αναλογία περίπου 1:107, σταθερά και συνεχόμενα διίστανται, και ταυτόχρονα ένα ζευγάρι ιόντων υδροξωνίου και υδροξυλίου επανενώνονται. Επειδή στο καθαρό νερό οι αριθμοί των ιόντων υδροξωνίου και υδροξυλίου είναι ίσοι, το καθαρό νερό είναι ουδέτερο, δηλαδή ούτε όξινο, ούτε βασικό.
Μια βάση, κατ' Αρρένιου, από την άλλη, είναι μια ουσία που αυξάνει τη συγκέντρωση ιόντων υδροξυλίου, όταν διαλύεται στο νερό, οπότε ταυτόχρονα μειώνεται η συγκέντρωση των ιόντων υδροξωνίου.
Η συνεχής διάσταση και αποδιάσταση των μορίων του νερού σχηματίζει μια χημική ισορροπία στην οποία κάθε αύξηση της συγκέντρωσης ιόντων υδροξωνίου συνοδεύεται από αντίστοιχη μείωση στη συγκέντρωση των ιόντων υδροξυλίου, έτσι ώστε ένα οξύ κατ' Αρρένιους μπορεί να πει κανείς ότι επίσης μειώνει τη συγκέντρωση των ιόντων υδροξυλίου, την οποία αυξάνει μια βάση κατ' Αρρένιους.
Ο λόγος για τον οποίο τα pH των οξέων είναι μικρότερα από 7 είναι ότι έχουν συγκέντρωση ιόντων υδροξωνίου μεγαλύτερη από 10-7 moles/lit, εφόσον το pH ορίζεται ως ο αντίθετος αριθμός από τον δεκαδικό λογάριθμο της συγκέντρωσης των ιόντων υδροξωνίου.
Σημειώστε ότι στο νερό, εκτός από το υδροξώνιο σχηματίζονται και άλλες εφυδατωμένες μορφές του υδρογονοκατιόντος, με τύπους Η5Ο2+, Η7Ο3+, Η9Ο4+, κ.τ.λ..
Παραδείγματα οξέων κατ' Αρρένιους:
1. Το υδροχλωρικό οξύ (HCl):
2. Το νιτρικό οξύ (ΗΝΟ3):
3. Το αιθανικό οξύ (CH3COOH):
4. Το θειικό οξύ (H2SO4):
Σημειώστε ότι σύμφωνα με τον ορισμό κατ' Αρρένιους τα οξέα πρέπει να περιέχουν οπωσδήποτε υδρογόνο, αλλά κάθε υδρογονούχα ένωση δεν είναι απαραίτητα οξύ. Ακόμα, ο όξινος χαρακτήρας τους εκδηλώνεται μόνο σε υδατικό διάλυμα.
Οξέα κατά Μπρόνστεντ και Λόρυ
[Επεξεργασία | επεξεργασία κώδικα]


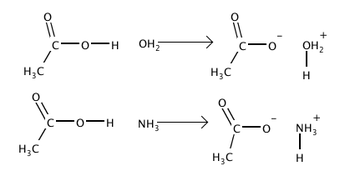
Ενώ ο κατ' Αρρένιους ορισμός είναι χρήσιμος για την περιγραφή πολλών χημικών αντιδράσεων, είναι επίσης σχετικά περιορισμένος στο πεδίο εφαρμογής του. Το 1923 οι χημικοί Γιοχάνες Νίκολαους Μπρόνστεντ (Johannes Nicolaus Brønsted) και Τόμας Μάρτιν Λόρυ (Thomas Martin Lowry) ανεξάρτητα αναγνώρησαν ότι οι οξεοβασικές αντιδράσεις περιλαμβάνουν τη μεταφορά ενός πρωτονίου. Ένα οξύ κατά Μπρόνστεντ - Λόρυ είναι ένα χημικό είδος που δίνει ένα πρωτόνιο (οπότε είναι «πρωτονιοδότης») σε μια βάση κατά Μπρόνστεντ - Λόρυ, που παίρνει το πρωτόνιο (οπότε είναι «πρωτονιοδέκτης»)[2]. Η οξεοβασική θεωρία κατά Μπρόνστεντ - Λόρυ έχει αρκετά πλεονεκτήματα απέναντι στην αντίστοιχη θεωρία κατ' Αρρένιους. Εξετάστε, για παράδειγμα, τις ακόλουθες αντιδράσεις του αιθανικού οξέος, του οργανικού οξέος που δίνει στο ξίδι τη χαρακτηριστική του γεύση:
Και οι δυο θεωρίες εύκολα περιγράφουν την πρώτη αντίδραση. Το αιθανικό οξύ δρα ως ένα οξύ κατ' Αρρένιους, γιατί δρα ως πηγή υδροξωνίου όταν διαλυθεί σε νερό, αλλά και ως οξύ κατά Μπρόνστεντ - Λόρυ, γιατί δίνει ένα πρωτόνιο στο νερό. Στη δεύτερη αντίδραση, όμως, το αιθανικό οξύ και πάλι δίνει ένα πρωτόνιο, αυτήν τη φορά στην αμμωνία (NH3), οπότε είναι οξύ κατά Μπρόνστεντ - Λόρυ, αλλά δεν παράγει υδροξώνιο, οπότε δεν είναι οξύ κατ' Αρρένιους.
Η θεωρία κατά Μπρόνστεντ - Λόρυ μπορεί επίσης να χρησιμοποιείται για να περιγράψει μοριακές χημικές ενώσεις, ενώ τα οξέα κατ' Αρρένιους πρέπει να είναι ιονικές ενώσεις. Το υδροχλώριο (HCl) και η αμμωνία (NH3) μπορούν να συνδυαστούν κάτω από πολλές διαφορετικές συνθήκες και να σχηματίσουν χλωριούχο αμμώνιο (NH4Cl). Το υδατικό διάλυμα υδροχλωρίου, δηλαδή το υδροχλωρικό οξύ, υπάρχει ως ιόντα υδροξωνίου και ανιόντα χλωρίου. Οι ακόλουθες αντιδράσεις απεικονίζουν τους περιορισμούς του ορισμού κατ' Αρρένιους:
Όπως και στην αντίδραση με το αιθανικό οξύ, και οι δυο ορισμοί λειτουργούν στο πρώτο παράδειγμα, όπου το νερό (aq) είναι διαλύτης και το ιόν υδροξωνίου σχηματίζεται από τη διάσταση του υδροχλωρίου. Οι δυο επόμενες αντιδράσεις, όμως, δεν περιλαμβάνουν τον σχηματισμό ιόντων, αλλά και πάλι επιτρέπουν τη μεταφορά πρωτονίου. Στη δεύτερη αντίδραση, το υδροχλώριο και η αμμωνία διαλύονται σε βενζόλιο (PhH) και αντιδρούν παράγοντας στερεό (s) χλωριούχο αμμώνιο. Στην τρίτη αντίδραση, το υδροχλώριο και η αμμωνία αντιδρούν στην αέρια (g) κατάσταση και παράγουν και πάλι στερεό χλωριούχο αμμώνιο.
Τα δυο ζευγάρια χημικών ειδών, αυτό των χημικών ειδών που αντέδρασαν και αυτό των χημικό ειδών που προέκυψε, μιας οξεοβασική αντίδραση κατά Μπρόνστεντ και Λόρυ ονομάζονται «συζυγή οξεοβασικά ζεύγη».
Άλλα παραδείγματα:
1. Στην αντίδραση διάλυσης σε νερό, και μετά διάστασης, έχουμε:
Εδώ το υδροχλώριο δρα σαν οξύ και κατ' Αρρένιους, αφού παράγει υδροξώνιο, και κατά Μπρόνστεντ και Λόρυ, αφού δίνει πρωτόνιο στο νερό. Εδώ τα συζυγή ζεύγη της αντίδρασης είναι το υδροχλώριο και το νερό, που αντέδρασαν, και το υδροξώνιο και ανιόν χλωρίου, που παράχθηκαν.
2. Στην αντίδραση διάλυσης σε νερό και μετά πρώτης διάστασης του θειικού οξέος, έχουμε:
Εδώ το θειικό οξύ δρα σαν οξύ και κατ' Αρρένιους, αφού παράγει υδροξώνιο, και κατά Μπρόνστεντ και Λόρυ, αφού δίνει πρωτόνιο στο νερό. Εδώ τα συζυγή ζεύγη της αντίδρασης είναι το θειικό οξύ και το νερό, που αντέδρασαν, και το υδροξώνιο και το όξινο θειικό ανιόν, που παράχθηκαν.
3. Στην αντίδραση διάστασης του νερού, έχουμε:
Εδώ το νερό δρα σαν οξύ κατ' Αρρένιους, αφού παράγει υδροξώνιο, αλλά ταυτόχρονα ως οξύ και ως βάση κατά Μπρόνστεντ και Λόρυ, αφού δίνει και δέχεται πρωτόνιο. Εδώ τα συζυγή ζεύγη της αντίδρασης είναι το νερό και το νερό, που αντέδρασαν, και το υδροξώνιο και το ανιόν υδροξυλίου, που παράχθηκαν.
4. Στη διάσταση του όξινου ανιόντος θείου, το οποίο μπορεί να προέλθει από το πρώτο στάδιο διάστασης του υδρόθειου ή από τη διάσταση ενός όξινου θειούχου άλατος, όπως το όξινο θειούχο νάτριο (NaHS), έχουμε:
Εδώ το όξινο ανιόν θείου δρα σαν οξύ κατ' Αρρένιους, αφού παράγει υδροξώνιο, αλλά ταυτόχρονα και ως οξύ κατά Μπρόνστεντ και Λόρυ, αφού δίνει πρωτόνιο. Εδώ τα συζυγή ζεύγη της αντίδρασης είναι το όξινο ανιόν θείου και το νερό, που αντέδρασαν, και το υδροξώνιο και το διανιόν θείου, που παράχθηκαν.
Είναι προφανές, από τα παραπάνω, ότι κατά Μπρόνστεντ και Λόρυ, είναι δυνατό το ίδιο χημικό είδος να μπορεί να δρα άλλοτε ως οξύ και άλλοτε ως βάση ανάλογα με ποια ουσία αντιδρά κάθε φορά.
Έτσι, το Η2Ο, στο παράδειγμα #3, δρα και ως οξύ αλλά και ως βάση. Τέτοια χημικά είδη με διπλή δράση λέγονται αμφολύτες ή επαμφοτερίζοντα σώματα.
Οξέα κατά Λιούις
[Επεξεργασία | επεξεργασία κώδικα]
Ένας τρίτος κανόνας προτάθηκε το 1923 από τον Γκίλμπερτ Λιούις (Gilbert N. Lewis), ο οποίος συμπεριλαμβάνει αντιδράσεις με οξεοβασικά χαρακτηριστικά που δεν περιλαμβάνουν μεταφορά ενός πρωτονίου. Ένα οξύ κατά Λιούις είναι ένα χημικό είδος που δέχεται ένα ζευγάρι ηλεκτρονίων από ένα άλλο χημικό είδος. Με άλλα λόγια, ένα οξύ κατά Λιούις είναι ένας «δέκτης ηλεκτρονίων»[2]. Οι οξεοβασικές αντιδράσεις κατά Μπρόνστεντ - Λόρυ είναι αντιδράσεις μεταφοράς ενός πρωτονίου, ενώ οι οξεοβασικές αντιδράσεις κατά Λιούις είναι αντιδράσεις μεταφοράς ενός ζεύγους ηλεκτρονίων. Όλα τα οξέα κατά Μπρόνστεντ - Λόρυ είναι και οξέα κατά Λιούις, αλλά το αντίστροφο δεν ισχύει. Δηλαδή τα οξέα κατά Λιούις δεν είναι πάντα και οξέα κατά Μπρόνστεντ - Λόρυ. Κατ' επέκταση, οι ακόλουθες χημικές αντιδράσεις μπορούν να περιγραφούν με όρους οξεοβασικής χημείας κατά Λιούις:
Στην πρώτη αντίδραση, ένα ανιόν φθορίου (F-, δίνει ένα ζεύγος ηλεκτρονίων στο τριφθοριούχο βόριο, σχηματίζοντας ως προϊόν τετραφθοροβοριούχο ανιόν. Το ανιόν φθορίου «χάνει» ένα ζεύγος ηλεκτρονίων σθένους, γιατί το «μοιράζεται» στον δεσμό B - F, που βρίσκεται στην περιοχή ανάμεσα στους δυο ατομικούς πυρήνες (του φθορίου και του βορίου), και γι' αυτό βρίσκεται μακρύτερα από ότι στον πυρήνα του φθορίου όταν αποτελούσε ένα μονήρες ζεύγος ηλεκτρονίων του ανιόντος φθορίου. Το τριφθοριούχο βόριο είναι ένα οξύ κατά Λιούις γιατί δέχεται το ηλεκτρονικό ζεύγος του ανιόντος φθορίου. Αυτή η αντίδραση δεν μπορεί να περιγραφεί με όρους της θεωρίας κατά Μπρόνστεντ - Λόρυ, γιατί δεν υπάρχει μεταφορά κανενός πρωτονίου. Η δεύτερη αντίδραση μπορεί να περιγραφεί και με τις δυο θεωρίες: Ένα πρωτόνιο μεταφέρεται από ένα αδιευκρίνιστο χημικό είδος στην αμμωνία, μια βάση κατά Μπρόνστεντ - Λόρυ. Εναλλακτικά, η αμμωνία δρα και ως βάση κατά Λιούις, μεταφέροντας το μονήρες ζεύγος αζώτου της στο υδρογονακατιόν του αδιευκρίνιστου χημικού είδους. Το αδιευκρίνιστο χημικό είδος που έλαβε το μονήρες ζεύγος ηλεκτρονίων του αζώτου της αμμωνίας είναι το οξύ κατά Λιούις, σε αυτήν τη χημική αντίδραση. Σύμφωνα με ένα άλλο παράδειγμα, το άτομο οξυγόνου του υδροξωνίου (H3O+) κερδίζει ένα ζεύγος ηλεκτρονίων όταν ένας χημικός δεσμός H-Ο διασπάται και τα ηλεκτρόνια του δεσμού που μοιράζονταν στον χημικό δεσμό τοπικοποιούνται στο άτομο του οξυγόνου, που μετείχε στον πρώην χημικό δεσμό H-O. Εξαρτάται από τα συμφραζόμενα, αλλά ένα οξύ κατά Λιούις μπορεί επίσης να περιγραφεί ως ένα οξειδωτικό ή ως ένα ηλεκτρονιόφιλο.
Παραδείγματα:

- H+ + :NH3 → NH4+. Ως οξύ δρα το Η+ και ως βάση η ΝΗ3.
- CaO: + SO3 → CaΟ:SO3 ως οξύ δρα το SO3 και ως βάση το CaO. Η αντίδραση μπορεί να γραφεί και ως : SO3 + O2- → SO42-.
- PtCl2 + 2 :NH3 ⇆ (H3N)2PtCl2, η ΝΗ3 είναι δότης ασύζευκτου ζεύγους ηλεκτρονίων (:) και είναι βάση κατά Λιούις ενωμένη ημιπολικά με τον PtCl2 που είναι το οξύ κατά Λιούις.
- F3B + :NH3 → F3B:NH3. Το BF3 είναι οξύ κατά Λιούις και η ΝΗ3 η βάση.
- PO4-3 + H2Ο ⇆ HPO4-2 + OH-. Το PO4-3 δρα ως βάση και το Η2Ο είναι το οξύ.
- Ο συμβολισμός «:» δηλώνει μονήρες, δηλαδή ασύζευκτο, ζεύγος ηλεκτρονίων.
Σημειώστε επίσης τα ακόλουθα:
Ο ορισμός αυτός είναι γενικότερος και των δύο άλλων αφού δέχεται ως οξέα όχι μόνο τις ενώσεις του τύπου ΗxA αλλά και τα κανονικά οξείδια των αμετάλλων (όπως είναι τα SO3, N2O5 κ.ά.). Ακόμα, ο ορισμός του Λιούις αναφέρεται και σε αντιδράσεις που πραγματοποιούνται σε διαλύτες διαφορετικούς από το νερό ή και κατά την απόλυτη απουσία διαλύτη.
Ενδιαφέρον παρουσιάζει επίσης και το γεγονός ότι, σε μιά αντίδραση, μιά ουσία θεωρείται οξύ κατά Λιούις αν αντιδρά με άλλη ουσία που είναι ασθενέστερο οξύ από την πρώτη, οπότε η δεύτερη θεωρείται αυτομάτως βάση. Έτσι, η ισχύς οξέων-βάσεων εξαρτάται από τη βάση σύγκρισης. Με απλούστερα λόγια θα λέγαμε ότι οξύ κατά Λιούις είναι μια χημική ουσία δέκτης ζεύγους ηλεκτρονίων, ενώ βάση κατά Λιούις είναι μια χημική ουσία δότης ζεύγους ηλεκτρονίων. Στις δύο άλλες θεωρίες, η σχετική σειρά ισχύος των οξέων και βάσεων είναι η ίδια, ανεξάρτητα από τη βάση σύγκρισης.
Ταξινόμηση των οξέων
[Επεξεργασία | επεξεργασία κώδικα]

Τα οξέα[3] ταξινομούνται σε πολλές κατηγορίες και με διάφορα κριτήρια :
- Σε ανόργανα (π.χ. νιτρικό οξύ HNO3) και οργανικά (π.χ. αιθανικό οξύ CH3COOH) ανάλογα αν μελετώνται από την ανόργανη ή την οργανική χημεία αντίστοιχα.
- Σε οξυγονούχα, αν περιέχουν οξυγόνο (π.χ. Θειικό οξύ H2SO4), και μη οξυγονούχα, αν δεν περιέχουν (π.χ. υδρόθειο Η2S).
- Σε ισχυρά, αν ιοντίζονται πλήρως και σε ασθενή, αν ιοντίζονται εν μέρει, δηλαδή υπάρχουν στο διάλυμα και αδιάστατα μόρια και ιόντα. Ισχυρά είναι μόνο τα : υπερχλωρικό (HClO4), νιτρικό (ΗΝΟ3), υδροχλωρικό (HCl), υδροβρωμικό (HBr), υδροϊωδικό (ΗΙ), και θειικό (H2SO4, στο α' στάδιο ιοντισμού) π.χ. HCl + H2Ο → H3O+ + Cl-. Όλα τα άλλα οξέα είναι ασθενή π.χ.CH3COOH + H2Ο ⇆ CH3COO- + H3O+.
- Ο Πίαρσον (1963) υποδιαιρεί τα οξέα και τις βάσεις κατά Λιούις σε σκληρά και ήπια ή μαλακά. Τα σκληρά οξέα προέρχονται από άτομα μικρού ατομικού αριθμού με μικρή επιδεκτικότητα πόλωσης, ενώ τα μαλακά από άτομα μεγάλου ατομικού αριθμού με μεγάλη επιδεκτικότητα πόλωσης και συνήθως περιέχουν d ηλεκτρόνια. Σκληρά οξέα είναι τα H+, Na+, K+, RC+O, R+, BF3 κ.ά. Μαλακά οξέα είναι τα Cu+, Ag+, Hg+ κ.ά.
- Σε μονοπρωτικά (ή μονοβασικά), αν αποδίδουν πρωτόνιο σε ένα στάδιο ιοντισμού (π.χ. HCl), και σε πολυπρωτικά (ή πολυβασικά), αν αποδίδουν πρωτόνια σε πολλά στάδια (π.χ. φωσφορικό H3PO4).
- Σε ορθο-οξέα που περιέχουν τόσα άτομα οξυγόνου και υδρογόνου όσος είναι ο αριθμός οξείδωσης του κεντρικού στοιχείου του χημικού τους τύπου π.χ. ορθο-βορικό οξύ ή απλά βορικό οξύ (H3BO3), ορθο-πυριτικό οξύ (H4SiO4) κ.ά.
- Σε μετα-οξέα τα οποία προέρχονται από τα ορθο-οξέα με αφαίρεση ενός μορίου νερού π.χ. μετα-πυριτικό οξύ (H2SiO3) κ.ά.
- Σε σύμπλοκα οξέα που προκύπτουν θεωρητικά από τα οξυγονούχα οξέα αν αντικατασταθούν άτομα οξυγόνου από ίσο αριθμό ατόμων άλλου αμετάλλου ή ιόντος π.χ. εξαφθοριοπυριτικό οξύ (H2SiF6) κ.ά.
- ε υπεροξυ-οξέα αν περιέχουν υπεροξειδική γέφυρα (— Ο — Ο —) π.χ. υπεροξυνιτρικό οξύ (HNO4) κ.ά.
- Σε θειοξέα που προέρχονται από τα οξοοξέα με αντικατάσταση ατόμων οξυγόνου από θείο π.χ. θειοθειικό οξύ (H2S2O3), διθειοφωσφορικό οξύ (H3PO2S2) κ.ά.
- Σε πολυοξέα που προκύπτουν από τη συνένωση απλών οξέων με ταυτόχρονη απόσπαση μορίων νερού π.χ. τριπυριτικό οξύ (H8Si3O10) κ.ά.
Όξινος χαρακτήρας
[Επεξεργασία | επεξεργασία κώδικα]Τα οξέα όταν βρεθούν σε υδατικό διάλυμα παρουσιάζουν ένα σύνολο κοινών ιδιοτήτων που λέγεται όξινος χαρακτήρας ή όξινη αντίδραση :
- Έχουν ξινή γεύση.
- Αλλάζουν ομοιόμορφα το χρώμα των δεικτών.
- Αντιδρούν με πολλά μέταλλα σχηματίζοντας άλατα με ταυτόχρονη έκλυση υδρογόνου π.χ. 2HCl + Zn → ZnCl2 + H2 ↗. (↗ = αέριο). Δεν αντιδρούν με τα μέταλλα που βρίσκονται μετά το υδρογόνο στην ηλεκτροχημική σειρά των μετάλλων (χαλκός, υδράργυρος, άργυρος, λευκόχρυσος, χρυσός).
- Αντιδρούν με βάσεις σύμφωνα με το γενικό σχήμα : Οξύ + βάση → άλας + νερό. Η αντίδραση αυτή λέγεται εξουδετέρωση και έχει την αμφίδρομη ιοντική μορφή: : Η3Ο+ + ΟΗ- ⇆ 2Η2Ο. Με μοριακή μορφή μπορεί να γραφεί : NaOH + HCl → NaCl + H2O.
- Όταν ηλεκτρολύονται εκλύεται στην κάθοδο αέριο υδρογόνο: :2H+ + 2e → H2 ↗[4].
- Αντιδρούν με ανθρακικά άλατα οπότε εκλύεται διοξείδιο του άνθρακα : 2HCl + CaCO3 → CaCl2 + H2Ο + CO2↗.
- Τα υδατικά τους διαλύματα έχουν 0 ≤ pH < 7 στους 25 °C.
Ένα μέσο με πολύ μεγάλη οξύτητα, γενικά μεγαλύτερη από αυτήν του θειικού οξέος περιεκτικότητας 100 % w/w, ονομάζεται "σουπερ-οξύ". Η συνηθέστερη μέθοδος παρασκευής σουπερ-οξέων είναι με διάλυση ενός ισχυρού οξέος κατά Lewis όπως είναι π.χ. το πενταφθοριούχο αντιμόνιο, SbF5, σε κατάλληλο οξύ κατά Μπρόνστεντ-Λόουρυ όπως είναι το υδροφθορικό οξύ (HF).
Ονοματολογία ανόργανων οξέων
[Επεξεργασία | επεξεργασία κώδικα]Όταν τα ανόργανα οξέα είναι ενώσεις του υδρογόνου με τα μη οξυγονούχα ανιόντα F-, Cl-, Br-, I-, S2-, CN-, η ονομασία τους είναι γενικά "υδρο-ανιόν", ενώ όταν είναι ενώσεις του υδρογόνου με αρνητικά πολυατομικά ιόντα (εκτός του ΟΗ-) ονομάζονται με το γενικό σχήμα "όνομα ανιόντος οξύ" π.χ. HCl υδροχλώριο, Η2S υδρόθειο, HCN υδροκυάνιο, ΗΝΟ3 νιτρικό οξύ, Η2SO4 θειικό οξύ, H3PO4 φωσφορικό οξύ κ.ά.
Ορισμένα γνωστά ανόργανα μη οξυγονούχα οξέα : (όταν είναι υδατικά διαλύματα λέγονται υδρο-xxxx-ικό οξύ με εξαίρεση το υδρόθειο)
υδροχλώριο HCl (υδροχλωρικό οξύ), υδροφθόριο HF (υδροφθορικό οξύ), υδροϊώδιο HI (υδροϊωδικό οξύ), υυδροβρώμιο HBr (υδροβρωμικό οξύ) υδρόθειο H2S, υδροκυάνιο HCN (υδροκυανικό οξύ).
Ορισμένα γνωστά ανόργανα οξυγονούχα οξέα είναι:
φωσφορικό οξύ H3PO4, θειικό οξύ H2SO4, θειώδες οξύ H2SO3. νιτρικό οξύ HNO3, νιτρώδες οξύ HNO2.
Τα ορθο-, πυρο- και μετα-οξέα ονομάζονται με τα αντίστοιχα προθέματα μπροστά από το όνομα του κανονικού οξέος π.χ. H4SnO4 ορθοκασσιτερικό οξύ, H2S2O7 πυροθειικό οξύ, HPO3 μετα-φωσφορικό κ.ά.
Ονοματολογία οργανικών οξέων
[Επεξεργασία | επεξεργασία κώδικα]
Οι οργανικές ενώσεις με όξινο χαρακτήρα ανήκουν στις τάξεις των καρβοξυλικών οξέων, των φαινολών, των αλκοολών και των αλκινίων με τριπλό δεσμό C-C σε θέση-1. Αρκετά οργανικά οξέα έχουν εμπειρικά ονόματα π.χ. γαλακτικό, μυρμηκικό, οξικό, οξαλικό, κ.ά.). Η συστηματική όμως ονοματολογία τους ακολουθεί τους κανόνες της I.U.P.A.C.. Ορισμένα γνωστά οργανικά οξέα : μεθανικό ή μυρμηκικό οξύ HCOOH, αιθανικό ή οξικό οξύ CH3COOH, οξαλικό οξύ C2H2O4, ασκορβικό οξύ ή βιταμίνη C C6H8O6, ακετυλοσαλικυλικό οξύ C9H8O4(ασπιρίνη) κ.ά.
Γενικές μέθοδοι παρασκευής ανόργανων οξέων
[Επεξεργασία | επεξεργασία κώδικα]Τα οξέα του τύπου ΗΧ [5] που λέγονται και υδραλογόνα παρασκευάζονται :
α) Με απευθείας σύνθεση από τα στοιχεία τους κατά το σχήμα "υδρογόνο + αλογόνο → υδραλογόνο" π.χ. H2 + Cl2 → 2HCl. Έτσι παρασκευάζεται και το H2S : H2 + S → H2S.
β) Με απλή αντικατάσταση του αμετάλλου κατά τη σειρά F2→Cl2→Br2→I2→S. Κάθε αμέταλλο αντικαθιστά τα επόμενά του στις ενώσεις του κατά το σχήμα "Αμέταλλο + ένωση → υδραλογόνο + αμέταλλο" π.χ. F2 + 2HI → 2HF + I2, Cl2 + H2S → 2HCl + S.
γ) Από αλογονίδια με επίδραση νερού κατά το σχήμα "αλογονίδιο + νερό → οξυγονούχο οξύ + υδραλογόνο" π.χ. PCl5 + 4H2Ο → H3PO4 + 5HCl.
Τα οξυγονούχα οξέα μπορούν να παρασκευαστούν :
α) Με αντίδραση του τύπου "ανυδρίτης οξέος + νερό → οξύ" π.χ. P2O5 + H2Ο → H3PO4
β) Με επίδραση πυκνού ΗΝΟ3 σε αμέταλλο κατά το γενικό σχήμα "αμέταλλο + ΗΝΟ3 → οξύ + ΝΟ2 + Η2Ο" π.χ. P + 5HNO3 → H3PO4 + 5NO2 + H2O
Όλα τα οξέα (οξυγονούχα και μη) μπορούν να παρασκευαστούν :
α) Από αντίδραση του τύπου "άλας + οξύ → νέο άλας + νέο οξύ". Η αντίδραση είναι πραγματοποιήσιμη εφόσον το "νέο οξύ" μπορεί να απομονωθεί από τα άλλα προϊόντα της αντίδρασης π.χ. CaF2 + H2SO4 → CaSO4↘[6] + 2HF↗
Φυσική κατάσταση - Προέλευση - Χρήσεις διαφόρων ανόργανων οξέων
[Επεξεργασία | επεξεργασία κώδικα]| Χημικός τύπος | Φυσική κατάσταση | Προέλευση | Χρήσεις |
|---|---|---|---|
HF |
Υγρό |
Μόνο με μορφή αλάτων (φθορίτης, κρυόλιθος, απατίτης) | Υαλουργία, διύλιση πετρελαίου, τα άλατά του ως αντισηπτικά |
Αέριο |
Ηφαίστεια, γαστρικό υγρό, το άλας του (NaCl) βρίσκεται στο θαλασσινό νερό | Καθαριστικό, βιομηχανία χρωμάτων, παρασκευή Η2, Cl2, H2S, CO2 | |
HBr |
Αέριο |
Μόνο με μορφή αλάτων | Φωτογραφική, φαρμακευτική |
HI |
Αέριο |
Μόνο με μορφή αλάτων | Στις οργανικές συνθέσεις |
H2S |
Αέριο |
Ηφαίστεια, θερμές πηγές, σήψη οργανικών ενώσεων | Ποιοτική ανάλυση κατιόνων |
H2SO4 |
Υγρό |
Με μορφή αλάτων, θερμές πηγές | Το σημαντικότερο ανόργανο οξύ, βιομηχανία λιπασμάτων, διύλιση πετρελαίου, χρώματα, απορρυπαντικά, αφυδατικό, μπαταρίες αυτοκινήτων |
HNO3 |
Υγρό |
Ηλεκτρικές εκκενώσεις ατμόσφαιρας, με μορφή αλάτων | Εκρηκτικές ύλες, χρώματα, βιομηχανία λιπασμάτων |
H3PO4 |
Στερεό |
Μόνο με μορφή αλάτων | Λιπάσματα |
H3ΒΟ3 |
Δεν έχει απομονωθεί |
Ηφαίστεια, με μορφή αλάτων | Ήπιο αντιηπτικό |
Βιβλιογραφία
[Επεξεργασία | επεξεργασία κώδικα]- Μανουσάκης Γ.Ε. "Γενική και Ανόργανη Χημεία", Τόμοι 1ος και 2ος, Θεσσαλονίκη 1981.
- Μανωλκίδης Κ., Μπέζας Κ. "Στοιχεία Ανόργανης Χημείας", Έκδοση 14η, Αθήνα 1984.
- Μανωλκίδης Κ., Μπέζας Κ. "Χημικές Αντιδράσεις", Αθήνα 1976.
- Γιαννακουδάκης Δ. Α. "Φυσική Χημεία Ιονικών και Ηλεκτροδιακών Δράσεων", Θεσσαλονίκη 1986.
- Γιαννακουδάκης Δ. Α. "Φυσική Χημεία Ομογενών και Ετερογενών Συστημάτων", Θεσσαλονίκη 1986.
- Morrison R. T., Boyd R. N. "Οργανική Χημεία" Τόμοι 1ος,2ος,3ος, Μετάφραση:Σακαρέλλος-Πηλίδης-Γεροθανάσης, Ιωάννινα 1991.
- Meislich H., Nechamkin H., Sharefkin J. "Οργανική Χημεία", Μετάφραση:Βάρβογλης Α., Αθήνα 1983.
- Γεωργάτσος Ι. Ε. "Βιοχημεία, Τόμος Α', Δομή μακρομορίων-Ένζυμα-Βιολογικές Οξειδώσεις", Θεσσαλονίκη 1985.
- Τοσσίδης Ι. "Χημεία Ενώσεων Συναρμογής", Θεσσαλονίκη 1986.
- Μπόσκου Δ. "Χημεία τροφίμων με Στοιχεία Τεχνολογίας Τροφίμων", Θεσσαλονίκη 1986.