Υδροτελλούριο
| Υδροτελλούριο | |
|---|---|
| |

| |
| Γενικά | |
| Όνομα IUPAC | Υδροτελλούριο |
| Άλλες ονομασίες | Τελλάνιο Υδρίδιο του τελλουρίου Υδροτελλουρικό οξύ |
| Χημικά αναγνωριστικά | |
| Χημικός τύπος | H2Te |
| Μοριακή μάζα | 129,6158 amu |
| Αριθμός CAS | 7783-09-7 |
| SMILES | [TeH2] |
| InChI | 1S/H2Te/h1H2 |
| PubChem CID | 21785 |
| Δομή | |
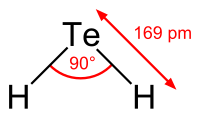
| Μήκος δεσμού | 169 pm |
| Είδος δεσμού | ομοιοπολικός |
| Πόλωση δεσμού | 5‰ (H--Te+) |
| Γωνία δεσμού | 90° |
| Μοριακή γεωμετρία | επίπεδη γωνιακή |
| Φυσικές ιδιότητες | |
| Σημείο τήξης | -49 °C |
| Σημείο βρασμού | -2,2 °C |
| Πυκνότητα | 3.310 kg/m3 (αέριο) 2.570 kg/m3 (υγρό στους -20°C) |
| Διαλυτότητα στο νερό |
7 kg/m3 |
| Χημικές ιδιότητες | |
| pKa | 2,64 |
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |
Το υδροτελλούριο[1] (αγγλικά: hydrogen telluride) είναι τριατομική ανόργανη χημική ένωση, που περιέχει υδρογόνο και τελλούριο, με μοριακό τύπο H2Te. Είναι το απλούστερο υδρίδιο του τελλουρίου. Σπάνια εμφανίζεται, γιατί διασπάται γρήγορα στα στοιχεία που το αποτελούν, ιδιαίτερα σε θερμοκρασία πάνω από τους -2°C. Οι περισσότερες ενώσεις με δεσμό Te-Η (τελλουρόλες), είναι (επίσης) ασταθείς, με την τάση να αποβάλλουν H2. Το υδροτελλούριο χημικά και δομικά είναι παρόμοιο με το υδροσελήνιο. Και τα δυο είναι όξινα. Η δεσμική γωνία H-Te-Η είναι περίπου 90°. Οι πτητικές ενώσεις του τελλουρίου συχνά έχουν δυσάρεστες οσμές, παρόμοιες με αυτές του πράσου ή του σκόρδου σε αποσύνθεση[2].
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
Το υδροτελλούριο παράγεται με οξύνιση αλάτων του τελλουρίου, όπως είναι το τελλουριούχο αργίλιο (Al2Te3) και το τελλουριούχο νάτριο (Na2Te).[3] Το τελλουριούχο νάτριο, με τη σειρά του, μπορεί να παραχθεί με αντίδραση μεταλλικού νατρίου και στοιχειακού τελλουρίου, σε άνυδρη αμμωνία. Το ενδιάμεσο της οξύνισης των τελλουριούχων αλάτων, δηλαδή το ανιόν HTe-, είναι σταθερό. Επίσης, το όξινο τελλουριούχο νάτριο (NaHTe) μπορεί να παραχθεί με αναγωγή τελλουρίου από νατριοβοριοτετραϋδρίδιο (NaBH4)[3].
Σε εργαστηριακή κλίμακα, το υδροτελλούριο συνήθως παράγεται με υδρόλυση ενώσεων του τελλουρίου με ηλεκτροθετικά μέταλλα[4]. Τυπικά χρησιμοποιείται υδρόλυση του τελλουριούχου αργιλίου:
Τελλουριούχο μαγνήσιο (MgTe) και τελλουριούχα αλκάλιμέταλλα επίσης μπορούν να υδρολυθούν παράγοντας υδροτελλούριο. Συνήθως οι υδρολύσεις αυτές απαιτούν την παρουσία οξέος, γιατί το ίδιο το υδροτελλούριο είναι αρκετά όξινο. Επίσης έχουν αναπτυχθεί και ηλεκτρολυτικές μέθοδοι παραγωγής υδροτελλουρίου[5].
Ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Το υδροτελλούριο είναι μια ενδοθερμική ένωση, ασταθής στον ατμοσφαιρικό αέρα, και εύκολα μπορεί να οξειδωθεί από το ατμοσφαιρικό οξυγόνο, παράγοντας νερό και στοιχειακό τελλούριο:[6]
Το υδροτελλούριο είναι σχεδόν το ίδιο όξινο με το φωσφορικό οξύ (με pKa1 2,64 έναντι 2,09)[6]. Το υδροτελλούριο αντιδρά με πολλά μέταλλα, σχηματίζοντας τα αντίστοιχα τελλουριούχα μέταλλα[7]. Π.χ.:
Παρατηρήσεις, υποσημειώσεις και αναφορές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Για εναλλακτικές ονομασίες δείτε τον πίνακα πληροφοριών.
- ↑ Greenwood, N. N.; & Earnshaw, A. (1997). Chemistry of the Elements (2η έκδοση), Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
- ↑ 3,0 3,1 Nicola Petragnani· Hélio A. Stefani (2007). Tellurium in organic synthesis. Best synthetic methods (2η έκδοση). Academic Press. σελ. 6. ISBN 0-08-045310-4.
- ↑ Shriver, Atkins. Inorganic Chemistry, Fifth Edition. W. H. Freeman and Company, New York, 2010; σσ. 407.
- ↑ F. Fehér, "Hydrogen Telluride" in Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY. Τόμ. 1. σσ. 438.
- ↑ 6,0 6,1 Egon Wiberg· Arnold Frederick Holleman (2001). Nils Wiberg, επιμ. Inorganic chemistry. Μτφρ. Mary Eagleson. Academic Press. σελ. 589. ISBN 0-12-352651-5.
- ↑ Henry Enfield Roscoe· Carl Schorlemmer (1878). A treatise on chemistry. 1. Appleton. σελίδες 367–368.
| |||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||



