Μεθυλοκυκλοπροπάνιο
| Μεθυλοκυκλοπροπάνιο | |||
|---|---|---|---|

| |||

| |||

| |||
| Γενικά | |||
| Όνομα IUPAC | Μεθυλοκυκλοπροπάνιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C4H8 | ||
| Μοριακή μάζα | 42,08 amu | ||
| Σύντομος συντακτικός τύπος |
|||
| Αριθμός CAS | 594-11-6 | ||
| SMILES | CC1CC1 | ||
| PubChem CID | 11657 | ||
| Δομή | |||
| Είδος δεσμού | C-H: σ(2sp2-1s) | ||
| Πόλωση δεσμού | C--H+: 3% | ||
| Μοριακή γεωμετρία | Τα ανθρακοάτομα του κυκλοπροπυλίου είναι σε επίπεδη τριγωνική θέση. | ||
| Ισομέρεια | |||
| Ισομερή θέσης | 4 Βουτένιο-1 (CH3CH2CH=CH2 Βουτένιο-2 (CH3CH=CHCH3) Μεθυλοπροπένιο (CH3CH=C(CH3)2) Κυκλοβουτάνιο ( | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | −117,2 °C | ||
| Σημείο βρασμού | 4–5 °C | ||
| Πυκνότητα | 691,2 kg/m3 (υγρό) | ||
| Εμφάνιση | Άχρωμο αέριο | ||
| Χημικές ιδιότητες | |||
| Θερμότητα πλήρους καύσης |
2.745 kJ/mole | ||
| Επικινδυνότητα | |||

| |||
| Εξαιρετικά εύφλεκτο (F+) | |||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Το μεθυλοκυκλοπροπάνιο (αγγλικά methylcyclopropane) είναι οργανική χημική ένωση, που περιέχει άνθρακα και υδρογόνο, με χημικό τύπο C4H8, αλλά συνήθως παριστάνεται με το γραμμικό του τύπο (![]() ). Το καθαρό μεθυλοκυκλοπροπάνιο, στις στις «συνηθισμένες συνθήκες», δηλαδή θερμοκρασία 25 °C και υπό πίεση 1 atm, είναι άχρωμο αέριο, που είναι διαθέσιμο για υγροποίηση (και μόνο με συμπίεση, δηλαδή είναι ένα από τα υγραέρια). Ανήκει στην ομόλογη σειρά των κυκλοαλκανίων, και πιο συγκεκριμένα στα κυκλοπροπάνια. Από τη μητρική του ένωση (κυκλοπροπάνιο) διαφέρει έχοντας μια μεθυλομάδα (CH3-) αντί για ένα άτομο υδρογόνου. Με βάση το χημικό τύπο του (C4H8) έχει τα ακόλουθα 4 ισομερή θέσης:
). Το καθαρό μεθυλοκυκλοπροπάνιο, στις στις «συνηθισμένες συνθήκες», δηλαδή θερμοκρασία 25 °C και υπό πίεση 1 atm, είναι άχρωμο αέριο, που είναι διαθέσιμο για υγροποίηση (και μόνο με συμπίεση, δηλαδή είναι ένα από τα υγραέρια). Ανήκει στην ομόλογη σειρά των κυκλοαλκανίων, και πιο συγκεκριμένα στα κυκλοπροπάνια. Από τη μητρική του ένωση (κυκλοπροπάνιο) διαφέρει έχοντας μια μεθυλομάδα (CH3-) αντί για ένα άτομο υδρογόνου. Με βάση το χημικό τύπο του (C4H8) έχει τα ακόλουθα 4 ισομερή θέσης:
- Κυκλοβουτάνιο
- 1-βουτένιο
- 2-βουτένιο (σε 2 γεωμερικά ισομερή)
- Μεθυλοπροπένιο
Ονοματολογία
[Επεξεργασία | επεξεργασία κώδικα]Η ονομασία «μεθυλοκυκλοπροπάνιο» από την ονοματολογία κατά IUPAC. Συγκεκριμένα, το αρχικό πρόθεμα «μεθυλο-»[1] δηλώνει την παρουσία διακλάδωσης ενός (1) ατόμου άνθρακα, το τμήμα «κυκλο-» δηλώνει την παρουσία ενός δακτυλίου στην κύρια ανθρακική αλυσίδα, το τμήμα «προπ-» δηλώνει την παρουσία τριών (3) ατόμων άνθρακα στην κύρια ανθρακική αλυσίδα της ένωσης, το ενδιάμεσο «-αν-» δείχνει την απουσία διπλών ή και τριπλών δεσμών μεταξύ ατόμων άνθρακα στο μόριο και η κατάληξη «-ιο» φανερώνει ότι δεν περιέχει χαρακτηριστικές ομάδες, δηλαδή ότι είναι υδρογονάνθρακας.
Κυκλοπροπάνια
[Επεξεργασία | επεξεργασία κώδικα]«Κυκλοπροπάνια» ονομάζονται τα κυκλοαλκάνια με τριμελή δακτύλιο, που αποτελεί και το χαρακτηριστικό της δομής τους. Οι πλευρικές αλυσίδες, όταν υπάρχουν, διαμορφώνονται όπως στα αλκάνια. Το ιδιαίτερο χαρακτηριστικό της μοριακής δομής τους είναι η εμφάνιση γωνίας δεσμού που είναι η συνηθισμένη γωνία δεσμού sp3-sp3 που αντιστοιχεί σε κορεσμένο. Ύστερα από ενεργειακή ανάλυση των πιθανών δομών - μοριακών μοντέλων με κβαντομηχανικές μεθόδους προέκυψε ως πιθανότερη η εκδοχή του sp2 υβριδισμού και της δημιουργίας δύο μοριακών τροχιακών τριών κέντρων (των τριών ατόμων C), σ (2sp2-2sp2-2sp2) και π (2p-2p-2p), με 3 ηλεκτρόνια ανά μοριακό τροχιακό, ώστε να χρησιμοποιηθούν τα 6 διαθέσιμα ηλεκτρόνια των 3 ατόμων C (τα άλλα 6 χρησιμοποούνται για τους 6 σ δεσμούς με τα 6 άτομα υδρογόνου ή και τα αλκύλια). Αντί δηλαδή των κλασσικών 3 ομοιοπολικών δεσμών δύο κέντρων μεταξύ των ατόμων C, υπάρχουν 2 ομοιοπολικοί δεσμοί τριών κέντρων[2].
Εξαιτίας αυτού του γεγονότος προκύπτει η λεγόμενη «ενέργεια τάσης δεσμών» που συνυπολογίζει την ενέργεια παραμόρφωσης δεσμικής γωνίας (κατά Baeyer), που οφείλεται στη διαφορά γωνίας από την κανονική, και την ενέργεια στρέψης (κατά Piltzer), που οφείλεται στην αδυναμία του συστήματος να στρέψει τους δεσμούς του και να πάρει διαμόρρφωση αποφυγής των απώσεων τύπου Van der Waals, που αναπτύσσονται από την προσέγγιση αλληλοαπωθούμενων ατόμων και ομάδων αυτών. Ενώ λοιπόν το ισομερές προπένιο έχει θερμότητα ολικής καύσης 1.971 kcal/mole το κυκλοπροπάνιο έχει 2.088 kcal/mole. Το ΔQ = 117 kJ/mole αντιστοιχεί ακριβώς στην επιπλέον ενέργεια που παγιδεύει η ιδιάζουσα δομή του τριμελή δατυλίου[3]. Αποτέλεσμα των παραπάνω είναι τα κυκλοπροπάνια να δείνουν αντιδράσεις προσθηκοδιάσπασης-1,3.
Δομή
[Επεξεργασία | επεξεργασία κώδικα]| Δεσμοί[4] | ||||
| Δεσμός | τύπος δεσμού | ηλεκτρονική δομή | Μήκος δεσμού | Ιονισμός |
|---|---|---|---|---|
| C#1΄-H | σ | 2sp3-1s | 109 pm | 3% C- H+ |
| C#1-#3-H | σ | 2sp2-1s | 108,7 pm | 3% C- H+ |
| C#1-C#1΄ | σ | 2sp2-2sp3 | 151 pm | |
| C-C-C | σ τριών ηλεκτρονίων και τριών κέντρων | 2sp2-2sp2-2sp2 | 151 pm (C-C) | |
| C-C-C | π τριών ηλεκτρονίων και τριών κέντρων | 2p-2p-2p | 151 pm (C-C) | |
| Κατανομή φορτίων σε ουδέτερο μόριο | ||||
| C#1΄ | -0,09 | |||
| C#2-#3 | -0,06 | |||
| C#1 | -0,03 | |||
| H | +0,03 | |||
Παρασκευές
[Επεξεργασία | επεξεργασία κώδικα]Ενδομοριακή αντίδραση Würz
[Επεξεργασία | επεξεργασία κώδικα]Με την τροποποιημένη αντίδραση Freund με Zn, που δίνει μεγαλύτερη απόδοση στην ενδομοριακή αντίδραση. Σ' αυτήν την περίπτωση η στοιχειομετρική εξίσωση της αντίδρασης γίνεται[5][6]:
Με χρήση καρβενίου
[Επεξεργασία | επεξεργασία κώδικα]1. Με προσθήκη μεθυλενίου σε προπένο και χρήση συστήματος διωδομεθάνιου (CH2I2), ψευδαργύρου (Zn) και χαλκού (Cu)[7]:
2. Παρεμβολή μεθυλενίου σε κυκλοπροπάνιο[8]:
Χημικές ιδιότητες
[Επεξεργασία | επεξεργασία κώδικα]Οξείδωση
[Επεξεργασία | επεξεργασία κώδικα]1. Όπως όλα τα κυκλοαλκάνια, το μεθυλοκυκλοπροπάνιο με περίσσεια οξυγόνου καίγεται προς διοξείδιο του άνθρακα και νερό [9][10]:
- Αν και η αντίδραση είναι μια έντονα εξώθερμη δεν συμβαίνει σε μέτριες θερμοκρασίες, γιατί για την έναρξή της πρέπει να υπερπηδηθεί πρώτα το εμπόδιο της διάσπασης των δεσμών C-C[11], των δεσμών C-H[12] και των δεσμών (Ο=Ο)[13] του O2:
2. Παραγωγή υδραερίου:
3. Με υπερμαγγανικό κάλιο προς 1-μεθυλοκυκλοπρονόλη:
Αλογόνωση
[Επεξεργασία | επεξεργασία κώδικα]1. Φωτοχημική αλογόνωση υποκατάστασης υδρογόνου: Το μεθυλοκυκλοπροπάνιο έχει 8 άτομα υδρογόνου για φωτοχημική αντικατάσταση από αλογόνα, οπότε προκύπτουν τα ακόλουθα τρία (3) ισομερή αλογονοπαράγωγα[14]:
- Δραστικότητα των X2: F2 > Cl2 > Br2 > Ι2.
- όπου 0<a,b,c<1, a + b + c = 0, διαφέρουν ανάλογα με το αλογόνο:
- Τα F και Cl είναι πιο δραστικά και λιγότερο εκλεκτικά. Η αναλογία των προπυλαλογονιδίων τους εξαρτάται κυρίως πό τη στατιστική αναλογία των προς αντικατάσταση ατόμων H. Ειδικά γοα το χλώριο θα έχουμε:
- 2-μεθυλο-1-χλωροκυκλοπροπάνιο (
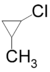 ): 4•3,8 = 15,2.
): 4•3,8 = 15,2. - 1-μεθυλο-1-χλωροκυκλοπροπάνιο (
 ): 1•5 = 5.
): 1•5 = 5. - κυκλοπροπυλομεθυλοχλωρίδιο (
 ): 3•1 = 3.
): 3•1 = 3.
- 2-μεθυλο-1-χλωροκυκλοπροπάνιο (
- Τα F και Cl είναι πιο δραστικά και λιγότερο εκλεκτικά. Η αναλογία των προπυλαλογονιδίων τους εξαρτάται κυρίως πό τη στατιστική αναλογία των προς αντικατάσταση ατόμων H. Ειδικά γοα το χλώριο θα έχουμε:
- Δηλαδή το μίγμα που προκύπτει είναι: 65,5% 2-μεθυλο-1-χλωροκυκλοπροπάνιο, 21,6% 1-μεθυλο-1-χλωροκυκλοπροπάνιο και 12,9% κυκλοπροπυλομεθυλοχλωρίδιο.
- Τα Br και I είναι πιο εκλεκτικά και λιγότερο δραστικά. Η αναλογία των βουτυλαλογονιδίων μεταβάλλεται προς όφελος του 1-αλο-1-μεθυλο-κυκλοπροπάνιο. Ειδικά για το βρώμιο θα έχουμε:
- 1-βρωμο-2-μεθυλοκυκλοπροπάνιο (
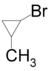 ): 4•82 = 328
): 4•82 = 328 - 1-βρωμο-1-μεθυλοκυκλοπροπάνιο (
 ): 1•1600=1600
): 1•1600=1600 - κυκλοπροπυλομεθυλοβρωμίδιο (
 ): 3•1 = 3.
): 3•1 = 3.
- 1-βρωμο-2-μεθυλοκυκλοπροπάνιο (
- Δηλαδή το μίγμα που προκύπτει είναι: 17% 1-βρωμο-2-μεθυλοκυκλοπροπάνιο, 82,9% 1-βρωμο-1-μεθυλοκυκλοπροπάνιο και 0,2% κυκλοπροπυλομεθυλοβρωμίδιο.
- Ανάλυση του μηχανισμού της χλωρίωσης του (
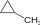 ):
): - 1. Έναρξη: Παράγονται ελεύθερες ρίζες.
- Η απαιτούμενη ενέργεια προέρχεται από το υπεριώδες φως (UV) ή θερμότητα (Δ).
- 2. Διάδοση: Καταναλώνονται οι παλιές ελεύθερες ρίζες, σχηματίζοντας νέες.
- 3. Τερματισμός: Καταναλώνονται μεταξύ τους οι ελεύθερες ρίζες, κατά τη στατιστικά σπάνια περίπτωση της συνάντησής τους.
- Η τριτοταγής ρίζα
 δεν μπορεί να ενωθεί με τον εαυτό της, λόγω στερεοχημικής παρεμπόδισης.
δεν μπορεί να ενωθεί με τον εαυτό της, λόγω στερεοχημικής παρεμπόδισης. - Είναι όμως πρακτικά δύσκολο να σταματήσει η αντίδραση στην παραγωγή μονοααλογονιδίων.
- Αν χρησιμοποιηθούν ισομοριακές ποσότητες
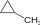 και Χ2 θα παραχθεί μίγμα όλων των αλογονοπαραγώγων του
και Χ2 θα παραχθεί μίγμα όλων των αλογονοπαραγώγων του 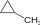 .
. - Αν όμως χρησιμοποιηθει περίσσεια
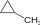 , τότε η απόδοση τωμ μονοπαραγώγων αυξάνεται πολύ, λόγω της αύξησης της στατιστική πιθανότητας συνάντισης
, τότε η απόδοση τωμ μονοπαραγώγων αυξάνεται πολύ, λόγω της αύξησης της στατιστική πιθανότητας συνάντισης 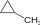 με X. σε σχέση με την πιθανότητα συνάντισης μονοπαραγώγου και X., που μπορεί να οδηγήσει στην παραγωγή των υπόλοιπων X-παραγώγων.
με X. σε σχέση με την πιθανότητα συνάντισης μονοπαραγώγου και X., που μπορεί να οδηγήσει στην παραγωγή των υπόλοιπων X-παραγώγων.
- Αν χρησιμοποιηθούν ισομοριακές ποσότητες
2. 1,3-Προσθηκοδιάσπαση παράγεται μίγμα 1,3-διαλοβουτάνιου και 1,3-διαλο-2-μεθυλοπροπάνιου:
Επίδραση καρβενίων
[Επεξεργασία | επεξεργασία κώδικα]- Η αντίδραση είναι ελάχιστα εκλεκτική και αυτό σημαίνει ότι κατά προσέγγιση έχουμε:
- 1. Παρεμβολή στους δύο (4) δεσμούς CH-H: 4.
- 2. Παρεμβολή στον (1) δεσμό C-H: 1.
- 3. Παρεμβολή στους τρεις (3) δεσμούς CH2-H: 3.
Προκύπτει επομένως μίγμα 1,2-διμεθυλοκυκλοπροπάνιου ~50%, αιθυλοκυκλοπροπάνιου 37,5% και 1,1-διμεθυλοκυκλοπροπάνιου ~12,5%.
Νίτρωση
[Επεξεργασία | επεξεργασία κώδικα]όπου 0<a,b,c<1, a + b + c = 1.
Καταλυτική υδρογόνωση με 1,3-κυκλοπροσθήκη
[Επεξεργασία | επεξεργασία κώδικα]- Ο όρος «1,3-κυκλοπροσθήκη» σημαίνει προσθήκη με διάνοιξη δακτυλίου.
Με καταλυτική υδρογόνωση. Παράγεται κυρίως βουτάνιο:
Υδραλογόνωση-1,3
[Επεξεργασία | επεξεργασία κώδικα]Με υδραλογόνο (ΗΧ) παράγεται κυρίως 2-αλοβουτάνιο:
Υδροξυαλογόνωση-1,3
[Επεξεργασία | επεξεργασία κώδικα]Με υπαλογονώδες οξύ (HOX) παράγεται κυρίως 4-αλο-2-βουτανόλη:
Ενυδάτωση-1,3
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση θειικού οξέως σε μεθυλοκυκλοπροπάνιo παράγεται τελικά κυρίως 2-βουτανόλη:
Διυδροξυλίωση-1,3
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση υπεροξείδιο του υδρογόνου σε μεθυλοκυκλοπροπάνιo, παρουσία καρβονικών οξέων παράγεται κυρίως 1,3-βουτανοδιόλη:
Αναφορές και σημειώσεις
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Ο αριθμός θέσης (1-) της διακλάδωσης παραλείπεται, επειδή δεν υπάρχει άλλο μεθυλοκυκλοπροπάνιο.
- ↑ Ν. Αλεξάνδρου, Γενική Οργανική Χημεία, ΘΕΣΣΑΛΟΝΙΚΗ 1985: Σελ.127-128, §6.2.
- ↑ Ν. Αλεξάνδρου, Γενική Οργανική Χημεία, ΘΕΣΣΑΛΟΝΙΚΗ 1985, Σελ. 125-126, §6.1.
- ↑ Τα δεδομένα προέρχονται εν μέρει από το «Table of periodic properties of thw Ellements», Sagrent-Welch Scientidic Company και Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, Σελ. 34.
- ↑ G. Gustavson (1887). "Ueber eine neue Darstellungsmethode des Trimethylens". J. Prakt. Chem. 36: 300–305. doi:10.1002/prac.18870360127. http://gallica.bnf.fr/ark:/12148/bpt6k90799n/f308.table.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 154, §6.5.Β1.
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, σελ. 138, §9.2Β5β.
- ↑ 8,0 8,1 SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, σελ. 46 §4.4.4.
- ↑ Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991, σελ.21, §1.1.
- ↑ Ν. Αλεξάνδρου, Γενική Οργανική Χημεία, ΘΕΣΣΑΛΟΝΙΚΗ 1985: Σελ.126, 6.1.
- ↑ ΔHC-C= +347 kJ/mol
- ↑ ΔHC-H = +415 kJ/mol
- ↑ ΔHO-O=+146 kJ/mol
- ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999, σελ. 43-46 §4.4.3.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982: Σελ. 244, §10.3.2.
Πηγές
[Επεξεργασία | επεξεργασία κώδικα]- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982







![{\displaystyle \mathrm {+3H_{2}O{\xrightarrow[{700-1100^{o}C}]{Ni}}3CO+6H_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/4092ba3a99c06c6660e229ed6517eb6aa67c6ac2)



![{\displaystyle \mathrm {+X_{2}{\xrightarrow[{\triangle }]{UV}}HX+a} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/8642789acc45d4b3d736594d5bb88f7e26b71e48)




![{\displaystyle \mathrm {Cl_{2}{\xrightarrow[{\triangle }]{UV}}2Cl^{\bullet }-239kJ} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/73fe9c8e7397e9e50d5b5a7ea91a25e26bed2f96)




























