Καίσιο
| Καίσιο | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ιστορία | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ταυτότητα του στοιχείου | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Όνομα, σύμβολο | Καίσιο (Cs) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ομάδα, περίοδος, τομέας |
1 ,6, | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Σχετική ατομική μάζα (Ar) |
132,9054519 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ατομικές ιδιότητες | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ατομική ακτίνα | 265 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ομοιοπολική ακτίνα | 244±11 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ακτίνα van der Waals | 343 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ηλεκτραρνητικότητα | 0,79 (κλίμακα Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Φυσικά χαρακτηριστικά | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Κρυσταλλικό σύστημα | κυβικό | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Κρυσταλλικό πλέγμα | χωροκεντρωμένο | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Σημείο τήξης | 301,59 Κ, 28,44 °C, 83,19 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Σημείο βρασμού | 944 K, 671 °C, 1240 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Κρίσιμο σημείο | 1938 K, 9,4 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Πυκνότητα | 1,93 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ενθαλπία τήξης | 2,09 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ενθαλπία εξάτμισης | 63,9 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Μαγνητική συμπεριφορά | παραμαγνητικό | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ειδική θερμική αγωγιμότητα |
35,9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Σκληρότητα Mohs | 0,2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Σκληρότητα Brinell | 0,14 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Μέτρο ελαστικότητας (Young's modulus) |
1,7 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Η κατάσταση αναφοράς είναι η πρότυπη κατάσταση (25°C, 1 Atm) εκτός αν σημειώνεται διαφορετικά | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Το καίσιο (αγγλικά ΗΒ και IUPAC: caesium,[1] αγγλικά ΗΠΑ cesium)[2] είναι το χημικό στοιχείο με το σύμβολο Cs και ατομικό αριθμό 55 και ατομικό βάρος 132,9054 amu.
Στις κανονικές συνθήκες περιβάλλοντος, το χημικά καθαρό καίσιο, είναι μαλακό, αργυρόχρυσο στερεό αλκαλιμέταλλο, με κανονική θερμοκρασία τήξης 28,5 °C, οπότε είναι ένα από τα πέντε μέταλλα χημικά στοιχεία που είναι υγρά μέσα ή κοντά στη θερμοκρασία δωματίου (20°C). Τα υπόλοιπα τέσσερα (4) είναι το ρουβίδιο (σ.τ. 39°C), το γάλλιο (σ.τ. 30 °C ), το φράγκιο (σ.τ. 27°C ) και ο υδράργυρος (σ.τ. -39°C)[3]. Βέβαια είναι και το βρώμιο (με σ.τ. -7,2°C), αλλά αυτό είναι αμέταλλο. Επίσης, προκαταρκτική εργασία προτείνει ότι το κοπερνίκιο και το φλερόβιο είναι αέρια μέταλλα στη θερμοκρασία δωματίου. Είναι το πιο δραστικό από όλα τα μέταλλα, πυροφορικό και αντιδρά με το νερό, ακόμη και στους -116°C. Είναι το πιο ηλεκτροθετικό από όλα τα χημικά στοιχεία, με ηλεκτραρνητικότητα 0,79 κατά Pauling. Το μόνο σταθερό ισότοπο του καισίου είναι το 133Cs. Το καίσιο εξορύσσεται κυρίως από τον πολλουκίτη, ενώ τα ραδιοϊσότοπά του, ιδιαίτερα το 137Cs που είναι προϊόν πυρηνικής σχάσης, εξάγονται από τα απόβλητα που παράγουν οι πυρηνικοί αντιδραστήρες.
Ο γερμανός χημικός Ρόμπερτ Μπούνσεν (Robert Bunsen) και ο επίσης γερμανός φυσικός Γκούσταβ Κίρχοφ (Gustav Kirchhoff) το 1860, ανακάλυψαν το καίσιο με την (τότε) πρόσφατα αναπτυγμένη μέθοδο της φασματοσκοπίας φλόγας. Οι πρώτες μικρής κλίμακας εφαρμογές του καισίου ήταν ως ιοντοανταλλάκτες για λυχνίες κενού και σε φωτοηλεκτρικά κύτταρα. Το 1967, λειτουργώντας ως απόδειξη της θεωρίας του Αϊνστάϊν ότι η ταχύτητα του φωτός είναι η πιο σταθερή διάσταση στο σύμπαν, το Διεθνές Σύστημα Μονάδων (SI) χρησιμοποίησε δυο ειδικά μήκη κύματος από το φάσμα εκπομπής του 133Cs για να επανορίσει το δευτερόλεπτο και το μέτρο. Από τότε, το καίσιο χρησιμοποιήθηκε ευρύτατα σε πολύ ακριβή ατομικά ρολόγια.
Από τη δεκαετία του 1990, η μεγαλύτερη εφαρμογή του στοιχείο είναι ως μυρμηκικό καίσιο (CsCO2H) σε υγρά γεώτρησης, αλλά έχει επίσης ένα εύρος εφαρμογών στην παραγωγή ηλεκτρισμού, στην ηλεκτρονική και στη χημεία.
Το ραδιοϊσότοπο 137Cs έχει ημιζωή περίπου 30 χρόνια και χρησιμοποιήθηκε σε ιατρικές εφαρμογές, σε βιομηχανικές μετρήσεις και στην υδρολογία. Οι μη ραδιενεργές ενώσεις του καισίου είναι μόνο ήπια τοξικές, αλλά η τάση του καθαρού μετάλλου να αντιδρά εκρηκτικά με το νερό το καθιστά σημαντικά επικίνδυνο υλικό, ενώ τα ραδιοϊσότοπά του, παρουσιάζουν σημαντικό κίνδυνο τόσο για την υγεία, όσο και για το περιβάλλον.
Ονομάστηκε έτσι (caesium) από αυτήν τη διπλή χαρακτηριστική κυανή γραμμή του φάσματος εκπομπής του, από τη λατινική λέξη "caesisus", που στα ελληνικά σημαίνει «ουρανί» (χρώμα), δηλαδή «κυανό του ουρανού».[4]
Το καίσιο εντοπίζεται μαζί με το κάλιο, σε πολλές ιαματικές πηγές, καθώς και σε κοιτάσματα αλάτων. Μέχρι 33% περιέχεται στο σπάνιο ορυκτό πολουσίτη ως αργιλοπυριτικό καίσιο, που απαντάται (για παράδειγμα) στη νήσο Έλβα. Επίσης απαντάται και στο λεπιδόλιθο (αργιλοπυριτικό λίθιο).
Τα άλατα καισίου λαμβάνονται από τα αλμόλοιπα της κρυστάλλωσης των αλάτων του λιθίου. Δύσκολα όμως διαχωρίζονται από τα συνοδεύοντα αυτών άλατα του ρουβιδίου. Το μέταλλο καίσιο λαμβάνεται είτε με ηλεκτρόλυση μίγματος τετηγμένων κυανιδίων καισίου και βορίου, είτε ευκολότερα δι' αναγωγής του υδροξειδίου του καισίου και του ανθρακικού καισίου με τη βοήθεια μαγνησίου μέσα σε ρεύμα υδρογόνου. Επίσης παρασκευάζεται και με απόσταξη χλωριούχου καισίου μετά του ασβεστίου, είτε δι' αναγωγής του οξειδίου του καισίου δια κόνεως μαγνησίου.
Ισότοπα[Επεξεργασία | επεξεργασία κώδικα]
Το καίσιο έχει 39 γνωστά ισότοπα, που ο μαζικός αριθμός τους κυμαίνεται από 112 ως 151. Αρκετά από αυτά συνθέτονται από ελαφρύτερα χημικά στοιχεία, με την αργή διεργασία σύλληψης νετρονίου (διεργασία S) μέσα στα γηραιά αστέρια και με τη διεργασία R, σε εκρήξεις υπερκαινοφανών αστέρων. Το μόνο σταθερό ισότοπο είναι το 133Cs, με 78 νετρόνια. Παρόλο που έχει μεγάλο πυρηνικό σπιν (7/2+), οι μελέτες πυρηνικού μαγνητικού συντονισμού αυτού του ισοτόπου μπορούν να χρησιμοποιούν τη λογική συχνότητα των 11,7 MHz.
Το ραδιοϊσότοπο 135Cs, με 80 νετρόνια, έχει πολύ μακρά ημιζωή, περί τα 2,3 εκατομμύρια έτη. Είναι το μακροβιότερο ραδιοϊσότοπο του καισίου. Αποτελεί ένα από τα μακροβιότερα προϊόντα πυρηνικής σχάσης του ουρανίου, που παράγεται σε πυρηνικούς αντιδραστήρες. Ωστόσο, αυτό το προϊόν σχάσης είναι μειωμένο στους περισσότερους αντιδραστήρες, γιατί ο προκάτοχός του, το 135Xe, είναι δυνατό δηλητήριο νετρονίων, ώστε συχνά μετατρέπεται στο σταθερό 136Xe, πριν προλάβει να (το 135Xe) μπορέσει να διασπαστεί σε 135Cs.
Το ραδιοϊσότοπο 137Cs, με 82 νετρόνια, έχει ημιζωή 30 έτη. Διασπάται αρχικά στο βραχύβιο 137mBa, με β-διάσπαση και έπειτα στο μη ραδιενεργό 137Ba. Η β-διάσπαση από 137Cs σε 137Cs συνοδεύεται από ισχυρή εκπομπή ακτίνων γ. Το 137Cs και το 90Sr είναι τα κύρια μεσαίας ημιζωής προϊόντα της πυρηνικής σχάσης, και οι κύριες πηγές της ραδιενέργειας που εκπέμπεται από τα πυρηνικά καύσιμα για εκατοντάδες χρόνια μετά την ψύξη τους. Αυτά τα δυο ραδιοϊσότοπα (137Cs και 90Sr) είναι οι μεγαλύτερες πηγές ραδιενέργειας στην περιοχή του Τσερνομπίλ, μετά από την καταστροφή. Εξαιτίας του χαμηλού βαθμού σύλληψης νετρονίων, η απαλλαγή μιας μολυσμένη περιοχής από το 137Cs μέσω αυτής της διεργασίας (δηλαδή της σύλληψης νετρονίων) είναι (πρακτικά) εφικτή. Η μόνο προς το παρόν ισχύουσα λύση είναι απλά να αφεθεί το ραδιοϊσότοπο να διασπαστεί ραδιενεργά, για όσο χρόνο αυτό χρειαστεί. Σχεδόν όλη η ποσότητα του καισίου που παράχθηκε με πυρηνική σχάση προέρχεται από τη β-διάσπαση αρχικά περισσότερο πλούσιων σε νετρόνια προϊόντων σχάσης, περνώντας ενδιάμεσα από διάφορα ισότοπα του ιωδίου και του ξένου. Επειδή τόσο το ιώδιο και το ξένο είναι πτητικά και μπορούν να διαφύγουν μέσω πυρηνικού καυσίμου ή του αέρα, το ραδιερνό καίσιο συχνά παράγεται μακριά από την αρχική τοποθεσία της σχάσης. Οι πυρηνικές δοκιμές από τη δεκαετία του 1950 ως τη δεκαετία του 1980, 137Cs που εκλύθηκε στην ατμόσφαιρα και γύρισε στην επιφάνεια της Γης ως ραδιενεργή σκόνη. Είναι ήδη καταγραφέας της κίνησης στο έδαφος και ίζημα από αυτές τις εποχές.
Το ραδιοϊσότοπο 134Cs, με 79 νετρόνια, έχει ημιζωή 2 έτη. Διασπάται απευθείας στο 134Ba.
Τα ραδιοϊσότοπα 129Cs, 131Cs, 132Cs και 136Cs, έχουν ημιζωές που κυμαίνονται μεταξύ μιας ημέρας και δύο εβδομάδων.
Τα υπόλοιπα ραδιοϊσότοπα του καισίου έχουν ημιζωές που κυμαίνονται μεταξύ 2 δευτερολέπτων και κλασμάτων του δευτερολέπτου. Υπάρχουν τουλάχιστον 21 μετασταθή πυρηνικά ισομερή καισίου. Εκτός από το 134mCs, που έχει ημιζωή κάτω των 3 ωρών, τα υπόλοιπα είναι πολύ ασταθή και έχουν ημιζωές λίγα λεπτά ή λιγότερο.
Χαρακτηριστικά[Επεξεργασία | επεξεργασία κώδικα]


Φυσικές ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Το καίσιο (στις κανονικές συνθήκες περιβάλλοντος) είναι το μαλακότερο (στερεό) χημικό στοιχείο, με σκληρότητα 0,2 Mohs. Είναι πολύ ελατό, χλωμό μέταλλο, που σκουραίνει με την παρουσία (έστω και ιχνών) οξυγόνου.[5][6][7]
Όταν είναι υπό την παρουσία ορυκτέλαιου, που είναι ο καλύτερος τρόπος διατήρησης για μετακίνηση, χάνει τη μεταλλική του λάμψη και αρχίζει να δημιουργείται μια στιλπνότητα, (που τείνει προς την γκρι εμφάνιση. Έχει κανονική θερμοκρασία τήξης 28,5 °C, καθιστώντας το ένα από τα λίγα μεταλλικά χημικά στοιχεία που υγροποιείται κοντά στη θερμοκρασία δωματίου. Συγκεκριμένα, ο υδράργυρος είναι το μόνο μεταλλικό χημικό στοιχείο που έχει μικρότερη γνωστή (μετρημένη) θερμοκρασία τήξης.[8] Βέβαια, το ραδιενεργό μεταλλικό χημικό στοιχείο φράγκιο υπολογίστηκε ότι μάλλον έχει μικρότερη κανονική θερμοκρασία τήξης, αλλά η ραδιενεργότητά του εμποδίζει την απομόνωση και επομένως τον έλεγχο ικανής ποσότητας του στοιχείου.[9] Επίσης, το κοπερνίκιο και το φλεβόριο μπορεί επίσης να έχουν ακόμη χαμηλότερες θερμοκρασίες τήξης. Επιπρόσθετα, το μεταλλικό καίσιο έχει μάλλον χαμηλή θερμοκρασία βρασμού, συγκεκριμένα 641°C, επίσης τη χαμηλότερη από όλα τα μεταλλικά χημικά στοιχεία πλην του υδραργύρου.[10]
Οι ενώσεις του καίγονται δίνοντας μπλε[11][12] ή ιώδη[12] φλόγα.
Το καίσιο σχηματίζει κράματα με τα άλλα αλκαλιμέταλλα, με το χρυσό και με τον υδράργυρο (αμαγάλματα). Σε θερμοκρασίες κάτω των 650 °C δεν σχηματίζει κράματα με το κοβάλτιο, με το σίδηρο, το μολυβδαίνιο, το νικέλιο, το λευκόχρυσο, το ταντάλιο και το βολφράμιο. Σχηματίζει καλά ορισμένες διαμεταλλικές ενώσεις με το αντιμόνιο, με το γάλλιο, με το ίνδιο και το θόριο, που είναι φωτοευαίσθητες.[5] Αναμειγνύεται με τα άλλα αλκαλιμέταλλα (εκτός από το λίθιο). Το κράμα με μοριακή σύνθεση 41% καίσιο, 47% κάλιο και 12% νάτριο έχει τη χαμηλότερη κανονική θερμοκρασία τήξης από κάθε άλλο γνωστό μεταλλικό κράμα, συγκεκριμένα -78 °C.[13][14]
Λίγα αμαγάλματα του καισίου έχουν μελετηθεί. Το διυδραργυριούχο καίσιο (CsHg2) είναι μαύρο με πορφυρή μεταλλική λάμψη, ενώ το υδραργυριούχο καίσιο (CsHg) είναι χρυσαφί, με επίσης μεταλλική λάμψη.[15]
Το χρυσαφί χρώμα του (μεταλλικού) καισίου προέρχεται από τη μειούμενη συχνότητα του φωτός που απαιτείται για να διεγείρει ηλεκτρόνια αλκαλιμετάλλων, καθώς κατεβαίνουμε στην ομάδα. Από το λίθιο ως και το ρουβίδιο η συχνότητα αντιστοιχεί στο υπεριώδες, αλλά στο καίσιο μπαίνει πια στο τέλος του ορατού φάσματος, δηλαδή στο μπλε-ιώδες. Το καίσιο μεταδίδει και μερικώς απορροφά το ιώδες φως επιλεκτικά σε σύγκριση με τα υπόλοιπα χρώματα του ορατού φάσματος, τα οποία ανακαλούνται, δίνοντας έτσι μια κιτρινωπή χροιά.[16]
Χημικές ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Το μεταλλικό καίσιο είναι πολύ δραστικό και πυροφορικό. Αναφλέγεται αυθόρμητα στον αέρα και αντιδρά εκρηκτικά με το νερό, ακόμη και σε χαμηλές θερμοκρασίες, περισσότερο από κάθε άλλο αλκαλιμέταλλο.[17][5]
Αντιδρά μάλιστα με τον πάγο σε θερμοκρασίες ως και −116 °C.[13]
Εξαιτίας αυτής της υψηλής δραστικότητάς του, το μεταλλικό καίσιο ταξινομήθηκε ως επικίνδυνο υλικό. Αποθηκεύεται και μεταφέρεται μέσα σε ξηρούς κορεσμένους υδρογονάνθρακες, όπως τα ορυκτέλαια. Μπορεί κανείς να το χειριστεί μόνο σε ατμόσφαιρα αδρανούς αερίου, όπως είναι για παράδειγμα το αργό. Ωστόσο, μια έκρηξη από την επίδραση νερού σε καίσιο είναι συχνά λιγότερο ισχυρό από την αντίστοιχη από την επίδραση νερού σε νάτριο. Αυτό συμβαίνει επειδή το καίσιο εκρήγνυται στιγμιαία με την επαφή του με το νερό, αφήνοντας λίγο χρόνο στο παραγόμενο υδρογόνο να συμμετάσχει στην έκρηξη.[18]
Το καίσιο μπορεί να αποθηκευθεί σε σφαγισμένες υπό κενό αμπούλες βοροπυριτικού γυαλιού. Σε ποσότητες άνω των περίπου 100 γραμμαρίων, το καίσιο μεταφέρεται σε ερμητικά σφραγισμένα δοχεία από ανοξείδωτο χάλυβα.[5]
Η χημεία του καισίου είναι παρόμοια με αυτήν των άλλων αλκαλιμετάλλων, και ειδικότερα με αυτήν του ρουβιδίου, που είναι το χημικό στοιχείο που βρίσκεται αμέσως πάνω από το καίσιο στον περιοδικό πίνακα.[19]
Όπως αναμένονταν για ένα αλκαλιμέταλλο, η μόνη συνηθισμένη βαθμίδα οξείδωσης του καισίου είναι +1.
Αυτό διαφέρει από την τιμή βαθμίδας οξείδωσης -1 που έχουν και καισίδια, δηλαδή ενώσεις που περιέχουν ανιόντα καισίου (Cs−).[20] Επιπρόσθετα, υπολογισμοί που έγιναν το 2013 από το Μάο-σενγκ Μιάο (Mao-sheng Miao) έδειξαν ότι υπό εξαιρετική πίεση (πάνω από 30 GPa), τα εσωτερικά 5p ηλεκτρόνια μπορούν να σχηματίσουν χημικούς δεσμούς, οπότε το καίσιο μπορεί σε αυτές τις περιπτώσεις να συμπεριφερθεί ως το έβδομο 5p χημικό στοιχείο. Αυτό δείχνει ότι υπό τέτοιες συνθήκες είναι δυνατό να υπάρξουν φθορίδια του καισίου με το καίσιο σε οξειδωτικές βαθμίδες +2 έως και +6.[21]
Κάποιες μικρές διαφορές προκύπτουν από το την υψηλότερη ατομική μάζα και τη μεγαλύτερη ηλεκτροθετικότερα από κάθε άλλο (μη ραδιενργό) αλκαλιμέταλλο.[22] Το καίσιο είναι το πιο ηλεκτροθετικό αλκαλιμέταλλο.[13] Η ηλεκτροθετικότητα του φραγκίου δεν έχει ακόμη μετρηθεί, εξαιτίας της ραδιενεργότητάς του, αλλά μετρήσεις πάνω στην ενέργεια πρώτου ιονισμού του προτείνουν ότι σχετικιστικά φαινόμενα μάλλον ελαττώνουν την ηλεκτροθετικότητά του και αυξάνουν την ηλεκτραρνητικότητά του πέρα από τη γενική τάση της ομάδας των αλκαλιμετάλλων.[23]
Το κατιόν του καισίου (Cs+) είναι ακόμη μεγαλύτερο και λιγότερο «σκληρό» σε σύγκριση με τα ελαφρύτερά του αλκαλιμέταλλα.
Ενώσεις του καισίου[Επεξεργασία | επεξεργασία κώδικα]
Οι περισσότερες ενώσεις του καισίου περιέχουν το κατιόν του (Cs+), τα οποία συνδέονται ιονικά με μια ευρεία ποικιλία ανιόντων. Μια αξιοσημείωτη εξαίρεση αποτελούν τα καισίδια, που περιέχουν το καισιούχο ανιόν (Cs−),[20] ενώ άλλες εξαιρέσεις αποτελούν διάφορα υποοξείδια (δείτε παρακάτω).
Τα άλατα του καισίου είναι συνήθως άχρωμα, εκτός αν το ίδιο το ανιόν είναι έγχρωμο. Πολλά απλά άλατα του καισίου είναι υγροσκοπικά, αλλά λιγότερο από τα αντίστοιχα άλατα των ελαφρύτερων αλκαλιμετάλλων. Τα φωσφορικά, τα οξικά, τα ανθρακικά, τα αλογονίδια, το οξείδιο, τα νιτρικά και τα θειικά άλατα του καισίου είναι υδατοδιαλυτά. Τα διπλά άλατα είναι λιγότερο συχνά υδατοδιαλυτά, ενώ η χαμηλή διαλυτότητα του θειικού αργιλιοκαισίου χρησιμεύει στον καθαρισμό του καισίου από ορυκτά του. Τα διπλά άλατα με αντιμόνιο, όπως το χλωριούχο αργιλιοκαίσιο (CsSbCl4), με βισμούθιο, με κάδμιο, με σίδηρο και με μόλυβδο έχουν επίσης φτωχή υδατοδιαλυτότητα.[5]
Το υδροξείδιο του καισίου (CsOH) είναι υγροσκοπικό και ισχυρά βασικό.[5] Τάχιστα χαράσει την επιφάνεια ημιαγωγών όπως το πυρίτιο.[24] Το υδροξείδιο του καισίου θεωρούνταν είναι η ισχυρότερη βάση, άποψη που αντανακλά την ασθενή έλξη ανάμεσα στα μεγάλα κατιόντα καισίου και στα ανιόντα υδροξυλίου (OH−).[11] Αυτό είναι πραγματικά αληθές για βάση κατ' Αρρένιους, αλλά υπάρχει ένας αριθμός μη υδατοδιαλυτών ενώσεων, όπως το βουτυλολίθιο (BuLi) και το νατραμίδιο (NaNH2),[5] που είναι πιο βασικές από το υδροξείδιο του καισίου.
Ένα στοιχειομετρικό μείγμα καισίου και χρυσού μετά από θέρμανση αντιδρά σχηματίζοντας κίτρινο χρυσιούχο καίσιο (Cs+Au−). Το χρυσιούχο ανιόν (Au−) συμπεριφέρεται ως ψευδοαλογόνο. Αυτή η ένωση (χρυσιούχο καίσιο) αντιδρά βίαια με το νερό, αποδίδοντας υδροξείδιο του καισίου, μεταλλικό χρυσό και αέριο υδρογόνο. Σε υγρή αμμωνία το χρυσιούχο καίσιο μπορεί να αντιδράσει με εξειδικευμένη ιοντεναλλακτική ρητίνη, παράγοντας χρυσιούχο τετραμεθυλαμμώνιο (Me4NAu). Το καίσιο σχηματίζει ανάλογη ένωση και με το λευκόχρυσο. Πρόκειται για το κόκκινο λευκοχρυσιούχο καίσιο (Cs2Pt), που περιέχει λευκοχρυσιούχο ανιόν (Pt2−), το οποίο συμπεριφέρεται ως ψευδοχαλκογόνο.[25]
Σύμπλοκα[Επεξεργασία | επεξεργασία κώδικα]
Όπως όλα τα μεταλλικά κατιόντα, τα Cs+ σχηματίζουν σύμπλοκα με διαλύματα βάσεων κατά Λιούις. Εξαιτίας του (σχετικά) μεγάλου μεγέθους τους, τα Cs+ υιοθετούν αριθμούς συναρμογής μεγαλύτερους από 6. Ο αριθμός αυτός συναρμογής είναι τυπικός για τα μικρότερα κατιόντα αλκαλιμετάλλων. Αυτή η διαφορά φαίνεται στον αριθμό συναρμογής 8 του χλωριούχου καισίου (CsCl). Αυτός ο υψηλός αριθμός συναρμογής και η «μαλακότητα» (τάση για σχηματισμό ομοιοπολικών δεσμών) είναι ιδιότητες που αξιοποιούνται στο διαχωρισμό των Cs+ από τα άλλα κατιόντα κατά τη διαχείριση των πυρηνικών αποβλήτων, από όπου τα κατιόντα 137Cs+ πρέπει να διαχωριστούν από μεγάλες ποσότητες μη ραδιενεργών κατιόντων K+.[26]
Αλογονίδια[Επεξεργασία | επεξεργασία κώδικα]
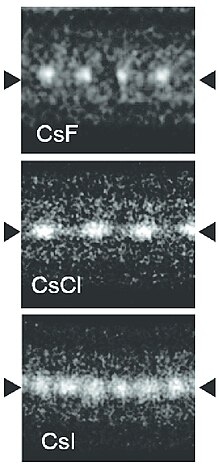
Το χημικά καθαρό φθοριούχο καίσιο (CsF), στις κανονικές συνθήκες περιβάλλοντος, είναι υγροσκοπικό λευκό στερεό που χρησιμοποιείται ευρύτατα στην οργανοφθοριούχα χημεία ως πηγή ανιόντων φθορίου.[28] Το φθοριούχο καίσιο έχει δομή αλίτη, που σημαίνει ότι τα ιόντα Cs+ και F- σχηματίζουν κυβική δομή που μοιάζει με την αντίστοιχη των ιόντων Na+ και Cl-, στο χλωριούχο νάτριο (NaCl).[5] Είναι αξιοσημείωτο ότι, στην ένωση φθοριούχο καίσιο, το καίσιο είναι το λιγότερο ηλεκτραρνητικό χημικό στοιχείο (0,79 κατά Πόλιγκ) και το φθόριο το περισσότερο ηλεκτραρνητικό (3,98 κατά Πόλιγκ), ανάμεσα σε όλα τα (γνωστά) χημικά στοιχεία. Επομένως, είναι η ένωση με τη μεγαλύτερη (γνωστή) διαφορά ηλεκτραρνητικότητας (3,19 κατά Πόλιγκ).
Το χλωριούχο καίσιο (CsCl) κρυσταλλώνεται στο απλό κυβικό σύστημα, που επίσης ονομάζεται «δομή χλωριούχου καισίου».[22] Αυτό το δομικό μοτίβο αποτελείται από πρωτόγονο κυβικό κρυσταλλικό πλέγμα με βάση δύο ιόντων, καθένα από αυτά έχει οκταπλή συναρμογή. Τα ανιόντα χλωρίου βρίσκονται πάνω από τα σημεία του πλέγματος, στις κορυφές των κύβων, ενώ τα κατιόντα καισίου βρίσκονται στις τρύπες που απομένουν στα κέντρα των κύβων. Την ίδια δομή μοιράζονται επίσης το βρωμιούχο καίσιο (CsBr), το ιωδιούχο καίσιο (CsI), καθώς και πολλές άλλες χημικές ενώσεις που δεν περιέχουν καίσιο. Σε αντιδιαστολή, όμως, τα περισσότερα άλλα αλογονίδια των αλκαλιμετάλλων έχουν τη δομή του NaCl.[22] Η δομή του χλωριούχου καισίου είναι προτιμητέα για αυτήν την ένωση επειδή τα κατιόντα Cs+ έχουν ιονική ακτίνα 174 pm και τα ανιόντα Cl− έχουν ιονική ακτίνα 181 pm.[29]
Χαλκογονίδια[Επεξεργασία | επεξεργασία κώδικα]

Περισσότερο από τα υπόλοιπα αλκαλιμέταλλα, το καίσιο σχηματίζει κάμποσες δυαδικές ενώσεις με το οξυγόνο, που συνονομάζονται οξείδια του καισίου, στα περισσότερα από τα οποία το καίσιο έχει παράξενους αριθμούς οξείδωσης.
Όταν το καίσιο καίγεται στον αέρα, το σουπεροξείδιο του καισίου (CsO2, με αριθμό οξείδωσης καισίου +4) είναι το κύριο προϊόν της καύσης.[30]
Το «κανονικό» οξείδιο του καισίου (Cs2O, με αριθμό οξείδωσης καισίου +1) σχηματίζει κιτρινοπορτοκαλί εξαγωνικούς κρυστάλλους.[31] Είναι το μόνο οξείδιο τύπου αντί-CdCl2.[32] Εξαερώνεται στους 250 °C και διασπάται σε μεταλλικό καίσιο και υπεροξείδιο του καισίου (Cs2O2, με αριθμό οξείδωσης καισίου +2) σε θερμοκρασίες άνω των 400 °C.[33] Επιπρόσθετα από το υπεροξείδιο και το οζονίδιο του καισίου[34][35] (CsO3, με αριθμό οξείδωσης καισίου +6), αρκετά έντονα χρωματισμένα υποξείδια έχουν επίσης μελετηθεί.[36] Αυτά συμπεριλαμβάνουν τα ακόλουθα:
- Το οξείδιο του επτακαισίου (Cs7O). Αριθμός οξείδωσης καισίου +2/7.
- Το οξείδιο του τετρακαισίου (Cs4O). Αριθμός οξείδωσης καισίου +1/2.
- Το τριοξείδιο του ενδεκακαισίου (Cs11O3), με αριθμό οξείδωσης καισίου +6/11.
- Το οξείδιο του τρικαισίου (Cs3O, σκούρο πράσινο).[37] Αριθμός οξείδωσης καισίου +2/3.
- Το μονοξείδιο του καισίου (CsO). Αριθμός οξείδωσης καισίου +2.
- Το διοξείδιο του τρικαισίου (Cs3O2).[38] Αριθμός οξείδωσης καισίου +4/3.
- Το διοξείδιο του επτακαισίου (Cs7O2).[39][40] Αριθμός οξείδωσης καισίου +4/7.
Το τελευταίο μπορεί να θερμανθεί σε κλίβανο παράγοντας Cs2O. Δυαδικές ενώσεις με θείο, σελήνιο και τελλούριο, επίσης υπάρχουν.[5]
Εφαρμογές[Επεξεργασία | επεξεργασία κώδικα]
Το μέταλλο καίσιο χρησιμοποιείται με περιορισμένη εφαρμογή στα φωτοηλεκτρικά κύτταρα, στα ηλεκτρικά τηλεσκόπια, κ.λπ. Τα δε άλατα καισίου χρησιμοποιούνται κυρίως στη παρασκευή τεχνικών ιαματικών υδάτων, ιδιαίτερα τα ανθρακικά, θειικά και χλωριούχα, καθώς και στην ιατρική, φαρμακευτική, αισθητική, κεραμευτική (το πυριτικό καίσιο) και παλαιότερα στις ραδιολυχνίες. Το 1967, μια συγκεκριμένη συχνότητα από το φάσμα εκπομπής του καισίου-133 επιλέχθηκε να χρησιμοποιηθεί στον ορισμό του δευτερολέπτου από το Διεθνές Σύστημα Μονάδων. Από τότε το καίσιο χρησιμοποιείται ευρέως σε ατομικά ρολόγια.
Από τη δεκαετία του 1990, η μεγαλύτερη εφαρμογή του στοιχείου έχει ως μυρμηκικού καίσιο για ρευστά γεώτρησης. Διαθέτει ένα ευρύ φάσμα εφαρμογών στον τομέα της παραγωγής ηλεκτρικής ενέργειας, στην ηλεκτρονική, και στη χημεία. Το ραδιενεργό ισότοπο Καίσιο-137 έχει χρόνο ημιζωής περίπου 30 χρόνια και χρησιμοποιείται σε ιατρικές εφαρμογές, βιομηχανικoύς μετρητές, και εφαρμογές υδρολογίας. Παρά το γεγονός ότι το στοιχείο χαρακτηρίζεται ήπια τοξικό, είναι ένα επικίνδυνο υλικό σαν μέταλλο και τα ραδιοϊσότοπα αυτού μπορεί να παρουσιάσουν υψηλό κίνδυνο για την υγεία σε περίπτωση διαρροής ακτινοβολίας.
Παρατήρηση[Επεξεργασία | επεξεργασία κώδικα]
- Πλοία που μεταφέρουν φορτία καισίου σε μεγάλες σχετικά ποσότητες θα πρέπει (υποχρεούνται) κατά τον κατάπλου τους και πριν την είσοδό τους σε λιμένες προς εκφόρτωση, ή ακόμα και διαπλέοντας στενούς διαύλους, διώρυγες κ.λπ. να ενημερώσουν σχετικά τις Αρχές.
Παραπομπές και σημειώσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ «IUPAC Periodic Table of Elements». International Union of Pure and Applied Chemistry.
- ↑ Coghill, Anne M.· Garson, Lorrin R., επιμ. (2006). The ACS Style Guide: Effective Communication of Scientific Information (3rd έκδοση). Washington, D.C.: American Chemical Society. σελ. 127. ISBN 978-0-8412-3999-9.
- ↑ Σημείωση: Έχουν σ.τ. μέχρι και το διπλάσιο (περίπου) της θερμοκρασίας δωματίου.
- ↑ Elements, American. «Cesium Permanganate». American Elements. Ανακτήθηκε στις 25 Φεβρουαρίου 2019.
- ↑ 5,0 5,1 5,2 5,3 5,4 5,5 5,6 5,7 5,8 Butterman, William C.· Brooks, William E.· Reese, Jr., Robert G. (2004). «Mineral Commodity Profile: Cesium» (PDF). United States Geological Survey. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 7 Φεβρουαρίου 2007. Ανακτήθηκε στις 27 Δεκεμβρίου 2009.
- ↑ Heiserman, David L. (1992). Exploring Chemical Elements and their Compounds. McGraw-Hill. σελίδες 201–203. ISBN 978-0-8306-3015-8.
- ↑ Addison, C. C. (1984). The Chemistry of the Liquid Alkali Metals. Wiley. ISBN 978-0-471-90508-0. Ανακτήθηκε στις 28 Σεπτεμβρίου 2012.
- ↑ Kaner, Richard (2003). «C&EN: It's Elemental: The Periodic Table – Cesium». American Chemical Society. Ανακτήθηκε στις 25 Φεβρουαρίου 2010.
- ↑ «Francium». Periodic.lanl.gov. Ανακτήθηκε στις 23 Φεβρουαρίου 2010.
- ↑ «Chemical Data – Caesium – Cs». Royal Society of Chemistry. Ανακτήθηκε στις 27 Σεπτεμβρίου 2010.
- ↑ 11,0 11,1 Lynch, Charles T. (1974). CRC Handbook of Materials Science. CRC Press. σελ. 13. ISBN 978-0-8493-2321-8.
- ↑ 12,0 12,1 Clark, Jim (2005). «Flame Tests». chemguide. Ανακτήθηκε στις 29 Ιανουαρίου 2012.
- ↑ 13,0 13,1 13,2 Kaner, Richard (2003). «C&EN: It's Elemental: The Periodic Table – Cesium». American Chemical Society. Ανακτήθηκε στις 25 Φεβρουαρίου 2010.
- ↑ Taova, T. M.· και άλλοι. (22 Ιουνίου 2003). «Density of melts of alkali metals and their Na-K-Cs and Na-K-Rb ternary systems» (PDF). Fifteenth symposium on thermophysical properties, Boulder, Colorado, United States. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 9 Οκτωβρίου 2006. Ανακτήθηκε στις 26 Σεπτεμβρίου 2010.
- ↑ Deiseroth, H. J. (1997). «Alkali metal amalgams, a group of unusual alloys». Progress in Solid State Chemistry 25 (1–2): 73–123. doi:.
- ↑ Addison, C. C. (1984). The chemistry of the liquid alkali metals. Wiley. σελ. 7. ISBN 9780471905080.
- ↑ Σημείωση: Και ναι στα όλα τα αλκαλιμέταλλα συμπεριλαμβάνεται και το φράγκιο.
- ↑ Gray, Theodore (2012) The Elements, Black Dog & Leventhal Publishers, p. 131, (ISBN 1-57912-895-5).
- ↑ Greenwood, N. N.· Earnshaw, A. (1984). Chemistry of the Elements. Oxford, UK: Pergamon Press. ISBN 978-0-08-022057-4.
- ↑ 20,0 20,1 Dye, J. L. (1979). «Compounds of Alkali Metal Anions». Angewandte Chemie International Edition 18 (8): 587–598. doi:.
- ↑ Moskowitz, Clara. «A Basic Rule of Chemistry Can Be Broken, Calculations Show». Scientific American. Ανακτήθηκε στις 22 Νοεμβρίου 2013.
- ↑ 22,0 22,1 22,2 Holleman, Arnold F.· Wiberg, Egon· Wiberg, Nils (1985). «Vergleichende Übersicht über die Gruppe der Alkalimetalle». Lehrbuch der Anorganischen Chemie (στα German) (91–100 έκδοση). Walter de Gruyter. σελίδες 953–955. ISBN 978-3-11-007511-3.
- ↑ Andreev, S. V.; Letokhov, V. S.; Mishin, V. I. (1987). «Laser resonance photoionization spectroscopy of Rydberg levels in Fr». Physical Review Letters 59 (12): 1274–76. doi:. PMID 10035190. Bibcode: 1987PhRvL..59.1274A.
- ↑ Köhler, Michael J. (1999). Etching in microsystem technology. Wiley-VCH. σελ. 90. ISBN 978-3-527-29561-6.
- ↑ Jansen, Martin (2005-11-30). «Effects of relativistic motion of electrons on the chemistry of gold and platinum». Solid State Sciences 7 (12): 1464–1474. doi:. Bibcode: 2005SSSci...7.1464J.
- ↑ Moyer, Bruce A.· Birdwell, Joseph F.· Bonnesen, Peter V.· Delmau, Laetitia H. (2005). Use of Macrocycles in Nuclear-Waste Cleanup: A Realworld Application of a Calixcrown in Cesium Separation Technology. Macrocyclic Chemistry. σελίδες 383–405. doi:10.1007/1-4020-3687-6_24. ISBN 978-1-4020-3364-3..
- ↑ Senga, Ryosuke; Suenaga, Kazu (2015). «Single-atom electron energy loss spectroscopy of light elements». Nature Communications 6: 7943. doi:. PMID 26228378. Bibcode: 2015NatCo...6E7943S.
- ↑ Evans, F. W.; Litt, M. H.; Weidler-Kubanek, A. M.; Avonda, F. P. (1968). «Reactions Catalyzed by Potassium Fluoride. 111. The Knoevenagel Reaction». Journal of Organic Chemistry 33 (5): 1837–1839. doi:.
- ↑ Wells, A. F. (1984). Structural Inorganic Chemistry (5th έκδοση). Oxford Science Publications. ISBN 978-0-19-855370-0.
- ↑ Cotton, F. Albert· Wilkinson, G. (1962). Advanced Inorganic Chemistry. John Wiley & Sons, Inc. σελ. 318. ISBN 978-0-471-84997-1.
- ↑ Lide, David R., επιμ. (2006). CRC Handbook of Chemistry and Physics (87th έκδοση). Boca Raton, FL: CRC Press. σελίδες 451, 514. ISBN 0-8493-0487-3.
- ↑ Tsai, Khi-Ruey; Harris, P. M.; Lassettre, E. N. (1956). «The Crystal Structure of Cesium Monoxide». Journal of Physical Chemistry 60 (3): 338–344. doi:. Αρχειοθετήθηκε από το πρωτότυπο στις 2017-09-24. https://web.archive.org/web/20170924131429/http://www.dtic.mil/get-tr-doc/pdf?AD=AD0026963. Ανακτήθηκε στις 2019-02-26.
- ↑ Nenoff, Tina M.; Nyman, May D. (2009-11-23). Information Bridge: DOE Scientific and Technical Information. Office of Scientific and Technical Information — U.S. Department of Energy. http://www.osti.gov/bridge/servlets/purl/770945-AFCMWR/webviewable/770945.pdf. Ανακτήθηκε στις 2010-02-15.
- ↑ Vol'nov, I. I.; Matveev, V. V. (1963). «Synthesis of cesium ozonide through cesium superoxide». Bulletin of the Academy of Sciences, USSR Division of Chemical Science 12 (6): 1040–1043. doi:.
- ↑ Tokareva, S. A. (1971). «Alkali and Alkaline Earth Metal Ozonides». Russian Chemical Reviews 40 (2): 165–174. doi:. Bibcode: 1971RuCRv..40..165T.
- ↑ Simon, A. (1997). «Group 1 and 2 Suboxides and Subnitrides — Metals with Atomic Size Holes and Tunnels». Coordination Chemistry Reviews 163: 253–270. doi:. https://archive.org/details/sim_coordination-chemistry-reviews_1997-07_163/page/253.
- ↑ Tsai, Khi-Ruey; Harris, P. M.; Lassettre, E. N. (1956). «The Crystal Structure of Tricesium Monoxide». Journal of Physical Chemistry 60 (3): 345–347. doi:.
- ↑ Okamoto, H. (2009). «Cs-Ο (Cesium-Oxygen)». Journal of Phase Equilibria and Diffusion 31: 86–87. doi:.
- ↑ Band, A.; Albu-Yaron, A.; Livneh, T.; Cohen, H.; Feldman, Y.; Shimon, L.; Popovitz-Biro, R.; Lyahovitskaya, V. και άλλοι. (2004). «Characterization of Oxides of Cesium». The Journal of Physical Chemistry B 108 (33): 12360–12367. doi:.
- ↑ Brauer, G. (1947). «Untersuchungen ber das System Csium-Sauerstoff». Zeitschrift für Anorganische Chemie 255 (1–3): 101–124. doi:.
Εξωτερικοί σύνδεσμοι[Επεξεργασία | επεξεργασία κώδικα]
| ||||||||
| Περιοδικός πίνακας | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | H | He | ||||||||||||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
|
| Αυτό το λήμμα σχετικά με ένα χημικό στοιχείο χρειάζεται επέκταση. Μπορείτε να βοηθήσετε την Βικιπαίδεια επεκτείνοντάς το. |




