Κατεχόλη
| Κατεχόλη | |||
|---|---|---|---|
| |||
| |||
| Γενικά | |||
| Όνομα IUPAC | 1,2-βενζο(λο)διόλη | ||
| Άλλες ονομασίες | Κατεχόλη Πυροκατεχόλη 2-υδροξυφαινόλη 1,2-διυδροξυβενζόλιο ο(ρθο)-βενζο(λο)διόλη ο(ρθο)-διυδροξυβενζόλιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C6H6O2 | ||
| Μοριακή μάζα | 110,1 amu | ||
| Σύντομος συντακτικός τύπος |
ο-C6H4(OH)2 | ||
| Αριθμός CAS | 120-80-9 | ||
| SMILES | Oc1c(O)cccc1 | ||
| Αριθμός EINECS | 204-427-5 | ||
| Αριθμός RTECS | UX1050000 | ||
| PubChem CID | 289 | ||
| ChemSpider ID | 283 | ||
| Δομή | |||
| Διπολική ροπή | 2,62±0,03 D | ||
| Ισομέρεια | |||
| Ισομερή θέσης | >100 | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | 105°C | ||
| Σημείο βρασμού | 245,5°C (εξαχνώνεται) | ||
| Πυκνότητα | 1.344 kg/m³ | ||
| Διαλυτότητα στο νερό |
430 kg/m³ | ||
| Δείκτης διάθλασης , nD |
1,604 | ||
| Τάση ατμών | 20 Pa (20 °C) | ||
| Χημικές ιδιότητες | |||
| pKa | 9,48 | ||
| Ελάχιστη θερμοκρασία ανάφλεξης |
127°C | ||
| Σημείο αυτανάφλεξης | 510°C | ||
| Επικινδυνότητα | |||
   
| |||
| Βλαβερη (Xn) | |||
| Φράσεις κινδύνου | 21/22, 36/38 | ||
| Φράσεις ασφαλείας | (2), 22, 26, 37 | ||
| LD50 | 300 mg/kg (αρουραίοι, στοματική λήψη) 270 mg/kg (ποντίκια, στοματική λήψη) | ||
| Κίνδυνοι κατά NFPA 704 |
|||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
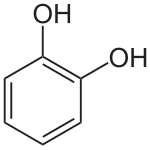
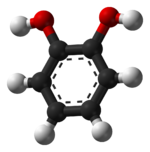
Η (πυρο)κατεχόλη[1] (αγγλικά: catechol) είναι αρωματική οργανική ένωση με μοριακό τύπο C6H6O2 , αν και συχνά παριστάνεται πιο αναλυτικά, ως o-C6H4(OH)2. Αποτελεί την ορθο- ισομερή, από τις τρεις (3) ισομερείς βενζο(λο)διόλες, που ανήκουν στις διφαινόλες. Η χημικά καθαρή κατεχόλη, στις κανονικές συνθήκες περιβάλλοντος, δηλαδή σε θερμοκρασία 25 °C και υπό πίεση 1 atm, είναι άχρωμο κρυσταλλικό στερεό, με λευκούς «φτερώδεις» κρυστάλλους, που είναι πολύ γρήγορα διαλυτοί στο νερό.
Εμφανίζεται και στη φύση, αλλά σε ίχνη. Ανακαλύφθηκε για πρώτη φορά στα προϊόντα της αποικοδομιτικής απόσταξης της κατεχίνης, που προέρχεται από φυτικό εκχύλισμα. Περίπου 20.000 τόνοι ετησίως κατεχόλης παράγονται στις μέρες μας από τη συνθετική χημική βιομηχανία, και αξιοποιείται κυρίως ως πρόδρομη ένωση για φυτοφάρμακα, προσθετικά γεύσης και αρώματα.
Ο όρος «κατεχόλη» αναφέρεται επίσης κατ' επέκταση και σε ομάδα «θυγατρικών» παραγώγων ή και υποκατεστημένων ενώσεων, που αποτελούν, με τη σειρά τους, γνήσιο υποσύνολο της ακόμη ευρύτερης ομάδας των κατεχινών, που αποτελούν θυγατρικές παράγωγες ενώσεις της προαναφερόμενης κατεχίνης.
Ιστορία[Επεξεργασία | επεξεργασία κώδικα]
Η κατεχόλη πρωτοαπομονώθηκε το 1839, από τον ΄Εντγκαρ Χούγκο Εμίλ Ρέινσχ (Edgar Hugo Emile Reinsch, 1809 - 1884), με αποικοδομιτική απόσταξη από το στερεό τανικό εκχύλισμα με την ονομασία κατεχίνη, το οποίο είναι το υπόλειμμα του βραμένου ή συμπυκνωμένου χυμού του φυτού Μιμόζα κατεχού (Acacia catechu L. f).[2] Κατά τη θέρμανση της κατεχίνης, πάνω από το σημείο αποσύνθεσής της, παράγεται μια ουσία που ο Ρέινσχ πρωτονόμασε Brenz-Katechusäure (που μπορεί να αποδοθεί στα ελληνικά ως «καμμένο κατεχοϊκό οξύ»), μετουσιωμένη ως λευκή εξάνθηση. Αυτή ήταν προϊόν της θερμικής αποσύνθεσης φλαβανολών σε κατεχίνη. Το 1841, τόσο ο Γουάκεροντερ (Wackenroder), όσο και ο Ζβένγκερ (Zwenger), ανεξάρτητα μεταξύ τους, ξανανακάλυψαν την κατεχόλη, και δημοσίευσαν την ανακάλυψή τους, με υποβολή αναφορών σχετικά με τα ευρήματά τους, στο Φιλοσοφικό Περιοδικό (Philosophical Magazine), επινοώντας την ονομασία «πυροκατεχίνη» (pyrocatechin).[3] Από το 1852, ο Έρντμαν (Erdman), συνειδητοποίησε ότι ο μοριακός τύπος της κατεχίνης είναι ίδιος με του βενζολίου συν δύο άτομα οξυγόνου. Το 1867, ο Αυγκούστ Κεκουλέ (August Kekulé) συνειδητοποίησε ότι κατεχολη είναι διόλη με βενζολικό πυρήνα, οπότε, από το 1868, η κατεχολη αναφέρονταν ως «πυροκατεχόλη».[4] Το 1879, η Εφημερίδα της Χημικής Κοινότητας (Journal of Chemical Society) , συνιστούσε η νέα (για τότε) ένωση να ονομάζεται πλέον με ως «κατεχόλη» και από το επόμενο έτος αναφέρεται σε λίστες ενώσεων με αυτήν την ονομασία.[5]
Ονοματολογία[Επεξεργασία | επεξεργασία κώδικα]
Αν και σπάνια συναντιέται, η επίσημη «προτιμώμενη συστηματική ονομασία IUPAC» (PIN) της κατεχόλης είναι 1,2-βενζο(λο)διόλη.[6] Το εμπειρικό όνομα πυροκατεχόλη είναι μια διατηρημένη ονομασία, κατά IUPAC, σύμφωνα με τις Συστάσεις 1993 για την Ονοματολογία της Οργανικής Χημείας.[7][8]
Φυσική παρουσία[Επεξεργασία | επεξεργασία κώδικα]
Η κατεχόλη από τότε αποδείχθηκε ότι υπάρχει φυσικά στο φυτό κίνο (Pterocarpus marsupium) και στην πίσσα από ξύλο οξιάς. Το αντίστοιχο σουλφονικό οξύ έχει ανιχνευθεί στα ούρα των αλόγων και των ανθρώπων.[9]
Μικρές ποσότητες κατεχολης εμφανίζονται φυσικά σε φρούτα και σε λαχανικά, μαζί με το ένζυμο πολυφαινόλη της μονοαμινοξειδάσης (επίσης γνωστό ως κατεχολάση, ή κατεχολική οξειδάση). Μετά την ανάμειξη του ενζύμου με το υπόστρωμα και την έκθεση σε οξυγόνο (όπως όταν μια πατάτα ή ένα μήλο εκτίθενται κομμένα στον αέρα), η άχρωμη κατεχόλη οξειδώνεται, αρχικά σε ερυθροκαστανές και τέλος σε μελανοειδείς χρωστικές ουσίες, που είναι παράγωγα της ορθοβενζοκινόνης. Το ένζυμο αδρανοποιείται, προσθέτοντας ένα οξύ, όπως το χυμό λεμονιού (περιέχει κιτρικό οξύ). Η αποφυγή της έκθεσης σε οξυγόνο επίσης αποτρέπει τις αντιδράσεις αμαύρωσης. Ωστόσο, η δραστηριότητα του ενζύμου αυξάνει σε χαμηλότερες θερμοκρασίες. Η βενζοκινόνη είναι αντιμικροβιακή, ιδιότητα που επιβραδύνει την αλλοίωση των τραυματισμένων φρούτων και άλλων φυτικών τμημάτων.
Είναι μία από τις κύριες φυσικές φαινόλες στο αργανέλαιο.[10]
Η πυροκατεχόλη βρίσκεται επίσης στα Agaricus bisporus.[11]
Είναι επίσης συστατικό του καστόριου, μιας ουσίας που παράγεραι από τον καστόιο αδένα των καστορών, που χρησιμοποιείται στην αρωματοποιία.
Παρουσία κατεχολικών παραγώγων[Επεξεργασία | επεξεργασία κώδικα]
Διάφορα κατεχολικά παράγωγα βρείσκονται επίσης ευρέως στο φυσικό κόσμο. Η επιδερμίδα των αρθροπόδων αποτελείται από χιτίνη, που συνδέεται μέσω κατεχολικού τμήματος σε πρωτεΐνη. Η επιδερμίδα μπορεί να ενισχυθεί με επιπρόσθετη σύνδεση (μαύρισμα και sclerotization), ιδίως, στα έντομα, και φυσικά με βιομινεραλισμό.[12] Οι κατεχόλες όπως η DHSA παράγονται από το μεταβολισμό της χοληστερόλης από βακτήρια όπως το Μυκοβακτηρίδιο της φυματίωσης.[13]
Οι ουρουσιόλες είναι φυσικά υφιστάμενες οργανικές ενώσεις, που έχουν την κατεχολική δομή του σκελετού και διφαινολική λειτουργικότητα, με αλλά αλκυλομάδες υποκατεστημένες στον αρωματικό δακτύλιο. Οι ουρουσιόλες είναι ερεθιστικά για το δέρμα δηλητήρια που βρίσκονται στα φυτά, όπως ο δηλητηριώδης κισσός, κτλ. Οι κατεχολαμίνες είναι βιοχημικά σημαντικές ορμόνες/νευροδιαβιβαστές που είναι φαιναιθυλαμίνες , στην οποία η φαινυλομάδα έχει κατεχολική δομή σκελετού.
Τμήματα του μορίου της κατεχίνης, ένα άλλο φυσικό συστατικό που υπάρχει φυσικά στο τσάι, περιέχει μια κατεχολική ομάδα.
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
Η κατεχόλη παράγεται βιομηχανικά με υδροξυλίωση της φαινόλης, χρησιμοποιώντας ως οξειδωτικό υπεροξείδιο του υδρογόνου (Η2O2).[14]:
Προηγουμένως, παράγονταν με υδροξυλίωση της σαλικυλαλδεΰδης, χρησιμοποιώντας και πάλι ως οξειδωτικό υπεροξείδιο του υδρογόνου,[15] :
Παράχθηκε επίσης και με υδρόλυση των 2-υποκατεστημένων φαινολών, και ειδικά της 2-χλωροφαινόλης, με θερμά υδατικά διαλύματα, που περιέχουν αλκαλικά υδροξείδια μετάλλων:
Τέλος, ο αντίστοιχος μεθυλαιθέρας, δηλαδή η ένωση 2-μεθοξυφαινόλη, που ονομάζεται γουαϊακόλη, μπορεί επίσης να μετατραπεί σε κατεχόλη, μέσω υδρόλυσης του δεσμού CH3-O , με υδροϊωδικό οξύ (HI):
Αντιδράσεις[Επεξεργασία | επεξεργασία κώδικα]
Οργανική χημεία[Επεξεργασία | επεξεργασία κώδικα]
Όπως και άλλα διλειτουργικά παράγωγα του βενζολίου, η κατεχόλη γρήγορα συμπυκνώνεται, σχηματίζοντας ετεροκυκλικές ενώσεις. Κυκλικοί εστέρες σχηματίζονται με την επίδραση τριχλωριούχου φωσφόρου (PCl3) και φωσφορυλοχλωρίδιου (POCl2), φωσγενίου (COCl2) και θειονυλοχλωριδίου (SOCl2):
όπου Α: PCl, POCl, CO και SO, αντιστοίχως, σχηματίζοντας έτσι τους αντίστοιχους ετεροκυκλικούς δακτυλίους.
Οι κατεχόλες παράγουν κινόνες, με την προσθήκη εξανιτροδημητριούχου διαμμωνίου [(NH4)2Ce(NO3)6].
Με ιόντα μετάλλων[Επεξεργασία | επεξεργασία κώδικα]
H κατεχόλη είναι το συζυγές οξύ ενός χηλικού μέσου που χρησιμοποιείται ευρέως στη χημεία συναρμογής. Σε βασικά διαλύματα, η κατεχόλη αντιδρά με τρισθενή σίδηρο (FeIII), δίνοντας ερυθρό ιόν με τύπο [Fe(C6H4O2)3]3−. Με τον τριχλωριούχο σίδηρο (FeCl3) δίνει ένα πράσινου χρώματος υδατικό διάλυμα, που σε αλκαλικό περιβάλλον αλλάζει γρήγορα το πράσινο χρώμα σε μαύρο, κατά την έκθεση στον αέρα.[16] Οι διοξυγονάσες, που είναι ένζυμα που περιέχουν σίδηρο, καταλύουν τη (βιο)διάσπαση της κατεχόλης.
Οξειδοαναγωγική χημεία[Επεξεργασία | επεξεργασία κώδικα]
Η κατεχόλη παράγεται με αντιστρέψιμη αναγωγή 1,2-βενζοκινόνης ( ) από δύο (2) πρωτόνια και δύο (2) ηλεκτρόνια [E° = +795 mV vs SHE; Em (pH 7) = +380 mV vs SHE].[17][18]
) από δύο (2) πρωτόνια και δύο (2) ηλεκτρόνια [E° = +795 mV vs SHE; Em (pH 7) = +380 mV vs SHE].[17][18]
Η οξειδοαναγωγική σειρά περιλαμβάνει κατεχολικό διανιόν, ημικινονικό μονοανιόν και βενζοκινόνη, που συλλογικά ονομάζονται διοξολένια (dioxolenes). Τα διοξολένια χρησιμοποιούνται ως συναρμοτές.[19]
Εφαρμογές[Επεξεργασία | επεξεργασία κώδικα]
Περίπου το 50% της συνθετικής κατεχόλης καταναλώνεται για την παραγωγή των φυτοφαρμάκων, και το υπόλοιπο να χρησιμοποιηθεί ως πρόδρομος για εκλεπτυσμένες χημικές ουσίες όπως αρώματα και φαρμακευτικά προϊόντα. Είναι μια συνηθισμένη δομική μονάδα στην οργανική σύνθεση.[20] Διάφορα βιομηχανικά σημαντικά πρόσθετα γεύσεων και τα αρώματα παρασκευάζονται ξεκινώντας από την κατεχόλη. Η γουαϊακόλη παρασκευάζεται με μεθυλίωση της κατεχόλης και στη συνέχεια μετατρέπεται σε βανιλίνη σε μια κλίμακα από περίπου 10.000 τόνων ανά έτος (1990). Ο συγγενικός μονοαιθυλαιθέρας της κατεχόλης, η γουαϊθόλη, μετατρέπεται σε αιθυλοβανιλίνη, ένα συστατικό της σοκολάτας σε ζαχαροπλαστεία. Η 3-trans-ισοκαμφυλυλοκυκλοεξανόλη, που χρησιμοποιείται ευρέως ως υποκατάστατο του σανταλοξυλέλαιου, παρασκευάζεται από την κατεχόλη μέσω γουαϊακόλης και καμφοράς. Η πυπερονάλη, ένα ανθώδες άρωμα, παράγεται από το μεθυλενοδιαιθέρα κατεχολης, ακολουθούμενη από συμπύκνωση με γλυοξάλη και αποκαρβοξυλίωση.[21]
Η κατεχόλη χρησιμοποιήθηκε ως ένας ασπρόμαυρος φωτογραφικός αναπτυκτής, αλλά, εκτός από μερικές ειδικού σκοπού εφαρμογές, η χρήση της είναι πια σε μεγάλο βαθμό απλά ιστορική. Φημολογείται ότι έχει χρησιμοποιηθεί για σύντομο χρονικό διάστημα από τον αναπτυκτή Eastman Kodak HC-110, και φημολογείται, ακόμη, ότι θα είναι ένα συστατικό του αναπτυκτή Tetenal Neofin.[22] Αυτό είναι βασικό στοιχείο για τη Finol από τη Moersch Photochemie, στη Γερμανία. Για τη σύγχρονη κατεχολική ανάπτυξη ήταν πρωτοπόρος ο αξιοσημείωτος φωτογράφος Sandy King. Το "PyroCat" είναι μια δημοφιλής διατύπωση μεταξύ σύγχρονων φωτογράφων ασπρόμαρου φιλμ.[23] Η εργασία του King ενέπνευσε την παραπέρα ανάπτυξη τέτοιας φωτογράφησης περαιτέρω στον 21ο αιώνα, από άλλους φωτογράφους, όπως ο Τζέι Ντε Φερ (Jay De Fehr) με Hypercat και Obsidian Acqua αναπτυκτές, και άλλους.
Εφαρμογές κατεχολικών παραγώγων[Επεξεργασία | επεξεργασία κώδικα]
Ο κατεχολικός σκελετός παρουσιάζεται σε μια ποικιλία από φυσικά προϊόντα όπως οι ουρουσιόλες. Υπάρχουν φάρμακα (όπως το MDMA) που τις μιμούνται.
Πολλές θυγατρικές πυροκατεχίνες έχουν προταθεί για θεραπευτικές εφαρμογές:
- Τα κοκκιδιοστατικά κινάτης (Quinate), συμπεριλαμβανομένων, για παράδειγμα, της δεκοκινάτης, της προκινολάτης, της κυπροκινάτης και της βουκινολάτης, γίνονται από την κατεχόλη.
- Ορισμένα αντικαταθλιπτικά, όπως π. χ. τα Azaloxan και Idazoxan.
- Ορισμένα συμπαθολογικά, όπως π. χ. το Guanoxan.
- Σύμφωνα με τους ισχυρισμούς, το πρώτο αντιισταμινικό που ανακαλύφθηκε το Piperoxan. Βλέπετε επίσης το Spiroxatrine, σε συνδυασμό με το Spirodecanone.
- Η ρετροσυνθετική ανάλυση των Eltoprazine μπορεί να εντοπιστεί σε κατεχολες, σε μία από τις (παραγωγικές) οδούς που λαμβάνονται.
- Το β-blocker και αγγειοδιασταλτικό στεφανιαίας oxprenolol είναι κατασκευασμένο από τον αλλυλαιθέρα της κατεχολης. Ο προπαργυλαιιθέρας της κατεχόλης ονομάζεται παργολόλη.
Δείτε επίσης[Επεξεργασία | επεξεργασία κώδικα]
Εξωτερικοί σύνδεσμοι[Επεξεργασία | επεξεργασία κώδικα]
- Το Διεθνές Χημικής Ασφάλειας Κάρτα 0411
- NIOSH Οδηγός Τσέπης για Χημικοί Κίνδυνοι
- IARC Μονογραφία: «Κατεχόλη»
- IUPAC Ονοματολογία της Οργανικής Χημείας (ηλεκτρονική έκδοση του "Blue Book")
Παραπομπές και σημειώσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Δείτε τις εναλλακτικές ονομασίες στον παρακείμενο πίνακα πληροφοριών χημικής ένωσης.
- ↑ Hugo Reinsch (1839) "Einige Bemerkungen über Catechu" (Some observations about catechu), Repertorium für die Pharmacie, 68 : 49-58.
- ↑ See:
- ↑ See:
- ↑ See:
- ↑ Preferred IUPAC Names.
- ↑ IUPAC, Commission on Nomenclature of Organic Chemistry.
- ↑ Panico, R., επιμ. (1994). A Guide to IUPAC Nomenclature of Organic Compounds 1993. Oxford: Blackwell Science. ISBN 0-632-03488-2.
- ↑ Zheng, L. T.; Ryu, G. M.; Kwon, B. M.; Lee, W. H.; Suk, K. (2008). «Anti-inflammatory effects of catechols in lipopolysaccharide-stimulated microglia cells: Inhibition of microglial neurotoxicity». European Journal of Pharmacology 588: 106–13. doi:. PMID 18499097.
- ↑ Charrouf, Z.; Guillaume, D. (2007). «Phenols and Polyphenols from Argania spinosa». American Journal of Food Technology 2 (7): 679–683. doi:.
- ↑ Delsignore, A; Romeo, F; Giaccio, M (1997). «Content of phenolic substances in basidiomycetes». Mycological Research 101 (5): 552–6. doi:.
- ↑ Briggs DEG (1999). «Molecular taphonomy of animal and plant cuticles: selective preservation and diagenesis». Philosophical Transactions of the Royal Society B: Biological Sciences 354 (1379): 7–17. doi:.
- ↑ PDB 2ZI8; «Studies of a ring-cleaving dioxygenase illuminate the role of cholesterol metabolism in the pathogenesis of Mycobacterium tuberculosis». PLoS Pathog. 5 (3): e1000344. March 2009. doi:. PMID 19300498.
- ↑ Fiegel, Helmut et al. (2002) "Phenol Derivatives" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH: Weinheim. doi:10.1002/14356007.a19_313.
- ↑ «http://www.orgsyn.org/demo.aspx?prep=CV1P0149». www.orgsyn.org. Ανακτήθηκε στις 17 Νοεμβρίου 2016. Εξωτερικός σύνδεσμος στο
|title=(βοήθεια) - ↑ Anderson, Bryan F.; Buckingham, David A.; Robertson, Glen B.; Webb, John; Murray, Keith S.; Clark, Paul E. (1976). «Models for the bacterial iron-transport chelate enterochelin». Nature 262: 722–724. doi:.
- ↑ Horner, Leopold; Geyer, Ekkehard (1965). «Zur Kenntnis der o-Chinone, XXVII: Redoxpotentiale von Brenzcatechin-Derivaten». Chemische Berichte 98 (6): 2016–2045. doi:.
- ↑ Nematollahi, D.; Rafiee, M. (2004-05-01). «Electrochemical oxidation of catechols in the presence of acetylacetone». Journal of Electroanalytical Chemistry 566 (1): 31–37. doi:.
- ↑ Griffith, W.P. (1993). «Recent advances in dioxolene chemistry». Transition Metal Chemistry 18 (2): 250–256. doi:.
- ↑ Barner, B. A. (2004) "Catechol" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette), J. Wiley & Sons, New York. doi:10.1002/047084289.
- ↑ Fahlbusch, Karl-Georg et al. (2003) "Flavors and Fragrances" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH: Weinheim doi:10.1002/14356007.a11_141.
- ↑ Stephen G. Anchell. The Darkroom Cookbook. ISBN 978-1136092770.
- ↑ Stephen G. Anchell· Bill Troop. The Film Developing Cookbook. ISBN 978-0240802770.
| ||||||||||||||||||||||||||||||||||||||||||||









