Κυκλοπροπυλομεθανόλη
| Κυκλοπροπυλομεθανόλη | |||
|---|---|---|---|

| |||
| Γενικά | |||
| Όνομα IUPAC | Κυκλοπροπυλομεθανόλη | ||
| Άλλες ονομασίες | Κυκλοπροπυλομεθυλική αλκοόλη Κυκλοπροπυλοκαρβινόλη Υδροξυμεθυλοκυκλοπροπάνιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C4H8O | ||
| Μοριακή μάζα | 72,10572 amu[1] | ||
| Σύντομος συντακτικός τύπος |
|||
| Αριθμός CAS | 2516-33-8[2] | ||
| SMILES | C1CC1CO | ||
| InChI | 1S/C4H8O/c5-3-4-1-2-4/h4-5H,1-3H2 | ||
| PubChem CID | 75644 | ||
| Δομή | |||
| Ισομέρεια | |||
| Ισομερή θέσης | 25 | ||
| Φυσικές ιδιότητες | |||
| Χημικές ιδιότητες | |||
| Επικινδυνότητα | |||

| |||
| Εύφλεκτη (F) | |||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Η κυκλομεθυλοπροπανόλη ή κυκλομρθυλική αλκοόλη ή κυκλομεθυλοκαρβινόλη ή υδροξυμεθυλοκυκλοπροπάνιο είναι ονομασία μιας κυκλοαλκανόλης, δηλαδή κορεσμένης μονοκυκλικής μονοσθενής αλκοόλης. Συνήθως αντιπροσωπεύεται από τον τύπο: ![]() . Με βάση το χημικό της τύπο, C4H8Ο έχει τα ακόλουθα εικοσιπέντε (25) ισομερή:
. Με βάση το χημικό της τύπο, C4H8Ο έχει τα ακόλουθα εικοσιπέντε (25) ισομερή:
- Βουτεν-1-όλη-1 (ελάσσων ταυτομερές της βουτανάλης) με σύντομο συντακτικό τύπο CH3CH2CH=CHOH.
- Βουτεν-2-όλη-1 ή 3-μεθυλαλλυλική αλκοόλη με σύντομο συντακτικό τύπο CH3CH=CHCH2OH.
- Βουτεν-3-όλη-1 με σύντομο συντακτικό τύπο CH2=CHCH2CH2OH.
- Βουτεν-1-όλη-2 (ελάσσων ταυτομερές της βουτανόνης) με σύντομο συντακτικό τύπο CH3CH2C(OH)=CH2.
- Βουτεν-2-όλη-2 (ελάσσων ταυτομερές της βουτανόνης) με σύντομο συντακτικό τύπο CH3CH=C(OH)CH3.
- Βουτεν-3-όλη-2 με σύντομο συντακτικό τύπο CH2=CHCH(OH)CH3.
- Μεθυλοπροπεν-1-όλη (ελάσσων ταυτομερές της μεθυλοπροπανάλης) με σύντομο συντακτικό τύπο (CH3)2C=CHOH.
- Μεθυλοπροπεν-2-όλη ή 2-μεθυλαλλυλική αλκοόλη με σύντομο συντακτικό τύπο CH2=C(CH3)CH2OH.
- Αιθυλοβινυλαιθέρας ή αιθοξυαιθένιο με σύντομο συντακτικό τύπο CH3CH2OCH=CH2.
- Μεθυλοπροπεν-1-υλαιθέρας ή 1-μεθοξυπροπένιο με σύντομο συντακτικό τύπο CH3OCH=CHCH3.
- Μεθυλοπροπεν-2-υλαιθέρας ή 3-μεθοξυπροπένιο με σύντομο συντακτικό τύπο CH3OCH2CH=CH2.
- Μεθυλο(μεθυλοβινυλ)αιθέρας ή 2-μεθοξυπροπένιο με σύντομο συντακτικό τύπο CH3OC(CH3)=CH2.
- Βουτανάλη (κύριο ταυτομερές) της βουτεν-1-όλης-1 με σύντομο συντακτικό τύπο CH3CH2CH2CHO.
- Μεθυλοπροπανάλη (κύριο ταυτομερές) της μεθυλοπροπεν-1-όλης με σύντομο συντακτικό τύπο (CH3)2CHCHO.
- Βουτανόνη (κύριο ταυτομερές) της βουτεν-2-όλης-2 και της βουτεν-3-όλης-2) με σύντομο συντακτικό τύπο CH3CH2COCH3.
- Μεθυλοκυκλοβουτανόλη με σύντομο συντακτικό τύπο
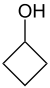 .
. - 1-μεθυλοκυκλοπροπανόλη με σύντομο συντακτικό τύπο
 .
. - 2-μεθυλοκυκλοπροπανόλη με σύντομο συντακτικό τύπο
 .
. - Κυκλοπροπυλομεθυλαιθέρας με σύντομο συντακτικό τύπο
 .
. - Οξολάνιο με σύντομο συντακτικό τύπο
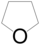 .
. - 2-μεθυλοξετάνιο με σύντομο συντακτικό τύπο
 .
. - 3-μεθυλοξετάνιο με σύντομο συντακτικό τύπο
 .
. - Αιθυλοξιράνιο με σύντομο συντακτικό τύπο
 .
. - 2,2-διμεθυλοξιράνιο με σύντομο συντακτικό τύπο
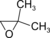 .
. - 2,3-διμεθυλοξιράνιο με σύντομο συντακτικό τύπο
 .
.
Κυκλοπροπάνια
[Επεξεργασία | επεξεργασία κώδικα]«Κυκλοπροπάνια» ονομάζονται τα κυκλοαλκάνια με τριμελή δακτύλιο, που αποτελεί και το χαρακτηριστικό της δομής τους. Οι πλευρικές αλυσίδες, όταν υπάρχουν, διαμορφώνονται όπως στα αλκάνια. Το ιδιαίτερο χαρακτηριστικό της μοριακής δομής τους είναι η εμφάνιση γωνίας δεσμού που είναι η συνηθισμένη γωνία δεσμού sp3-sp3 που αντιστοιχεί σε κορεσμένο. Ύστερα από ενεργειακή ανάλυση των πιθανών δομών - μοριακών μοντέλων με κβαντομηχανικές μεθόδους προέκυψε ως πιθανότερη η εκδοχή του sp2 υβριδισμού και της δημιουργίας δύο μοριακών τροχιακών τριών κέντρων (των τριών ατόμων C), σ (2sp2-2sp2-2sp2) και π (2p-2p-2p), με 3 ηλεκτρόνια ανά μοριακό τροχιακό, ώστε να χρησιμοποιηθούν τα 6 διαθέσιμα ηλεκτρόνια των 3 ατόμων C (τα άλλα 6 χρησιμοποούνται για τους 6 σ δεσμούς με τα 6 άτομα υδρογόνου ή και τα αλκύλια). Αντί δηλαδή των κλασσικών 3 ομοιοπολικών δεσμών δύο κέντρων μεταξύ των ατόμων C, υπάρχουν 2 ομοιοπολικοί δεσμοί τριών κέντρων[3].
Εξαιτίας αυτού του γεγονότος προκύπτει η λεγόμενη «ενέργεια τάσης δεσμών» που συνυπολογίζει την ενέργεια παραμόρφωσης δεσμικής γωνίας (κατά Baeyer), που οφείλεται στη διαφορά γωνίας από την κανονική, και την ενέργεια στρέψης (κατά Piltzer), που οφείλεται στην αδυναμία του συστήματος να στρέψει τους δεσμούς του και να πάρει διαμόρρφωση αποφυγής των απώσεων τύπου Van der Waals, που αναπτύσσονται από την προσέγγιση αλληλοαπωθούμενων ατόμων και ομάδων αυτών. Ενώ λοιπόν το ισομερές προπένιο έχει θερμότητα ολικής καύσης 1.971 kcal/mole το κυκλοπροπάνιο έχει 2.088 kcal/mole. Το ΔQ = 117 kJ/mole αντιστοιχεί ακριβώς στην επιπλέον ενέργεια που παγιδεύει η ιδιάζουσα δομή του τριμελή δακτυλίου[4]. Αποτέλεσμα των παραπάνω είναι τα κυκλοπροπάνια (και τα παράγωγά τους) να δείνουν αντιδράσεις προσθηκοδιάσπασης-1,3.
Σε σύγκριση με το κυκλοπροπάνιο, η κυκλοπροπυλομεθανόλη έχει ένα υδροξυμεθύλιο (CH2OH), αντί ενός ατόμου υδρογόνου, ενωμένο στο άτομο άνθρακα #1[5].
Παραγωγή
[Επεξεργασία | επεξεργασία κώδικα]Από 2,4-διαλοβουτανόλη-1
[Επεξεργασία | επεξεργασία κώδικα]Με επίδραση ψευδαργύρου σε 2,4-διαλοβουτανόλη-1 παράγεται κυκλοπροπυλομεθανόλη, με ενδομοριακή αντίδραση Wurtz [6]:
Από κυκλοπροπυλομεθυλαλογονίδιο
[Επεξεργασία | επεξεργασία κώδικα]1. Με επίδραση διαλύματος υδροξειδίου του αργύρου σε κυκλοπροπυλομεθυλαλογονίδιο παράγεται κυκλοπροπυλομεθανόλη[7]:
2. Με επίδραση διαλύματος αιθανικού νατρίου σε 1-αλο-1-μεθυλοκυκλοπροπάνιο παράγεται αρχικά αιθανικός 1'-μεθυλοκυκλοπροπυλεστέρας, που στη συνέχεια υδρολύεται σχηματίζοντας 1-μεθυλοκυκλοπροπανόλη [8]:
Αναφορές και σημειώσεις
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Δικτυακός τόπος PubChem
- ↑ Δικτυακός τόπος ChemIndustry.
- ↑ Ν. Αλεξάνδρου, Γενική Οργανική Χημεία, ΘΕΣΣΑΛΟΝΙΚΗ 1985: Σελ.127-128, §6.2.
- ↑ Ν. Αλεξάνδρου, Γενική Οργανική Χημεία, ΘΕΣΣΑΛΟΝΙΚΗ 1985, Σελ. 125-126, §6.1.
- ↑ Η αρίθμηση αρχίζει από το άτομο άνθρακα που είναι ενωμένο με το υδροξυμεθύλιο
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.154, §6.5.Β1
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.197, §8.2.3α
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.197, §8.2.3β
Πηγές
[Επεξεργασία | επεξεργασία κώδικα]- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
- Δημήτριου Ν. Νικολαΐδη: Ειδικά μαθήματα Οργανικής Χημείας, Θεσσαλονίκη 1983.
| ||||||||||||||||||||||||||||||||||||||||||||







