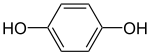
Υδροκινόνη
| Υδροκινόνη | |||
|---|---|---|---|
| |||

| |||

| |||
| Γενικά | |||
| Όνομα IUPAC | 1,4-βενζο(λο)διόλη | ||
| Άλλες ονομασίες | Υδροκινόνη Κινόλη 4-υδροξυφαινόλη 1,4-διυδροξυβενζόλιο π(αρα)-βενζο(λο)διόλη π(αρα)-διυδροξυβενζόλιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C6H6O2 | ||
| Μοριακή μάζα | 110,1 amu | ||
| Σύντομος συντακτικός τύπος |
π-C6H4(OH)2 | ||
| Αριθμός CAS | 123-31-9 | ||
| SMILES | c1cc(ccc1O)O | ||
| InChI | 1S/C6H6O2/c7-5-1-2-6(8)4-3-5/h1-4,7-8H | ||
| Αριθμός RTECS | MX3500000 | ||
| ChemSpider ID | 764 | ||
| Δομή | |||
| Διπολική ροπή | 1,4±0,1 D | ||
| Ισομέρεια | |||
| Ισομερή θέσης | >100 | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | 172°C | ||
| Σημείο βρασμού | 287°C (εξαχνώνεται) | ||
| Πυκνότητα | 1.300 kg/m³ | ||
| Διαλυτότητα στο νερό |
59 kg/m³ (15°C) | ||
| Τάση ατμών | 15 mPa (20°C) | ||
| Χημικές ιδιότητες | |||
| Ελάχιστη θερμοκρασία ανάφλεξης |
165°C | ||
| Επικινδυνότητα | |||
   
| |||
| Βλαβερη (Xn) Επικίνδυνη για το περιβάλλον (N) | |||
| Φράσεις κινδύνου | 22, 40, 41 43, 50, 68 | ||
| Φράσεις ασφαλείας | (2), 26 36/37/39, 61 | ||
| LD50 | 320 mg/kg (αρουραίοι, στοματική λήψη) 245 mg/kg (ποντίκια, στοματική λήψη) 490 mg/kg (θηλαστικά, στοματική λήψη) 200 mg/kg (κοννέλια, στοματική λήψη) 550 mg/kg (ινδικά χοιρίδια, στοματική λήψη) 200 mg/kg (σκύλοι, στοματική λήψη) 70 mg/kg (γάτες, στοματική λήψη) | ||
| Κίνδυνοι κατά NFPA 704 |
|||
| Άλλοι κίνδυνοι | Καρκινογόνο (κατηγορία 3) Μεταλλαξιογόνο (κατηγορία 3) | ||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Η υδροκινόνη[1] (αγγλικά hydroquinone) είναι αρωματική οργανική ένωση, με μοριακό τύπο C6H6O2, αν και συχνά παριστάνεται πιο αναλυτικά, με τον ημισυντακτικό τύπο π-C6H4(OH)2. Αποτελεί την παρα-ισομερή, από τις τρεις (3) ισομερείς βενζο(λο)διόλες, δηλαδή στις διφαινόλες, που αποτελούν υποσύνολο των αρενοδιολών. Η χημικά καθαρή υδροκινόνη, στις κανονικές συνθήκες περιβάλλοντος, δηλαδή σε θερμοκρασία 25 °C και υπό πίεση 1 atm, είναι κοκκώδες στερεό. Ο όρος «υδροκινόνη» αναφέρεται επίσης κατ' επέκταση και σε ομάδα «θυγατρικών» παραγώγων ή και υποκατεστημένων ενώσεων.
Ιστορία
[Επεξεργασία | επεξεργασία κώδικα]Η υδροκινόνη πρωτοπαράχθηκε το 1820 από τους Γάλλους χημικούς Πιερ Ζοζέφ Πελετιέ (Pierre Joseph Pelletier) και Ζοζέφ Μπιεναιμέ Καβεντού (Joseph Bienaimé Caventou), μέσω της ξηρής απόσταξης κινικού οξέος.
Το όνομα «υδροκινόνη» επινοήθηκε από τον Φρήντριχ Βέλερ το 1843.[2]
Ονοματολογία
[Επεξεργασία | επεξεργασία κώδικα]Αν και σπάνια συναντάται, η επίσημη «προτιμώμενη συστηματική ονομασία IUPAC» (PIN) της υδροκινόνης είναι 1,4-βενζο(λο)διόλη.[3]
Φυσική παρουσία
[Επεξεργασία | επεξεργασία κώδικα]Οι υδροκινόνες είναι από τα κύρια συστατικά του αμυντικού υγρού του βομβαρδιστή (μιας κατηγορίας σκαθαριών), σε συνδυασμό με υπεροξείδιο του υδρογόνου (H2O2), ίσως και με άλλες ενώσεις, ανάλογα με το είδος, που παράγεται από αδένες και μερικά από τα συστατικά συλλέγονται σε ειδική κύστη. Η κύστη αυτή ανοιγοκλείνει μέσω μιας βαλβίδας που ελέγχεται από ειδικό μυ, και το περιεχόμενό της πηγαίνει σε ένα θάλαμο αντίδρασης, με (σχετικά) χονδρά τοιχώματα, που περιέχει ειδικά κύτταρα, τα οποία παράγουν καταλάσες και υπεροξειδάσες. Αυτές καταλύουν την οξείδωση των υδροκινοκών στις αντίστοιχες κινόνες. Οι αντιδράσεις αυτές απελευθερώνουν οξυγόνο και παράγουν αρκετή θερμότητα, ώστε το μείγμα να φθάσει στην κανονική θερμοκρασία βρασμού του και έτσι να εξαερωθεί το 1/5 της ποσότητάς του, δημιουργώντας έτσι ένα ζεστό αερόλυμα, με το οποίο το σκαθάρι ψεκάζει τους εχθρούς του, από ειδικό άνοιγμα στην κοιλιακή του χώρα.[4]
Παράγωγα της φαρνεσυλυδροκινόνης αποτελούν τις κύριες ερεθιστικές ουσίες που αποπνέουν τα Eriodictyon parryi, οι οποίες μπορούν να προκαλέσουν σοβαρή δερματίτιδα, σε περίπτωση επαφής με το ανθρώπινο δέρμα.
Η υδροκινόνη θεωρείται ότι αποτελεί την ενεργή τοξίνη στα μανιτάρια agaricus hondensis.[5]
Η υδροκινόνη έχει αποδειχθεί ότι είναι ένα από τα χημικά συστατικά των φυσικών προϊόντων πρόπολης.[6]
Είναι επίσης μία από τις χημικές ενώσεις που βρίσκονται στο καστόριο. Αυτή η ένωση, μαζί με άλλες συλλέγονται από τις καστόριες κύστες των καστόρων .[7]
Στην κουμαριά (arctostaphylos uva-ursi), η αρβουτίνη μετατρέπεται σε υδροκινόνη.
Παραγωγή
[Επεξεργασία | επεξεργασία κώδικα]Η υδροκινόνη παράγεται βιομηχανικά από δύο κύριες παραγωγικές οδούς.[8]
1. Η ευρύτερα χρησιμοποιούμενη παραγωγική οδός διαδρομή είναι παρόμοια με τη διεργασία κουμενίου, σε μηχανισμό αντίδρασης, και εμπλέκει διαλκυλίωση του βενζολίου με προπένιο, που δίνει 1,4-διισοπροπυλοβενζόλιο. Η τελευταία ένωση αντιδρά με το οξυγόνο του ατμοσφαιρικού αέρα, δίνοντας το αντίστοιχο διυδροϋπεροξείδιο, που δομικά είναι παρόμοιο με το υπεροξείδιο του κουμενίου, οπότε ομοίως με μετάθεση δίνει προπανόνη και υδροκινόνη, μετά από επίδραση οξέος.
2. Μια δεύτερη παραγωγική οδός εμπλέκει υδροξυλίωση φαινόλης. Η μετατροπή αυτή γίνεται με επίδραση υπεροξειδίου του υδρογόνου (H2O2), που παρέχει ένα μείγμα υδροκινόνης και κατεχόλης:
Άλλες, λιγότερο συνηθισμένες μέθοδοι συμπεριλαμβάνουν:
- Την οξείδωση της ανιλίνης από διοξείδιο του μαγγανίου (MnO2), που ακολουθείται από αναγωγή της προκύπτουσας 1,4-βενζοκινόνης. Η διαδικασία έχει ορισμένα σημαντικά μειονεκτήματα: διεξάγεται ασυνεχώς κατά ποσότητες υλικού και επιπλέον δημιουργεί σημαντική ροή αποβλήτων.
- Μια δυνητικά σημαντική μέθοδος σύνθεσης υδροκινόνης που έχει προταθεί [9][10][11][12][13][14] χρησιμοποιεί αιθίνιο (HC≡CH) και πεντακαρβονυλοσίδηρο [Fe(CO)5]. Ο πεντακαρβονυλοσίδηρος λειτουργεί ως καταλύτης και όχι ως αντιδραστήριο, αν παρέχεται επιπλέον αέριο μονοξείδιο του άνθρακα (CO). Το ρόδιο ή το ρουθήνιο μπορούν να υποκαταστήσουν τον σίδηρο ως καταλύτες, με ευνοϊκές αποδόσεις, αλλά συνήθως δεν χρησιμοποιούνται λόγω του αυξημένου κόστους της αποκατάστασής τους στο αντιδρών μείγμα.
- Η υδροκινόνη και τα παράγωγά της μπορούν επίσης να παραχθούν με οξείδωση διάφορων φαινολών. Παραδείγματα περιλαμβάνουν τη μέθοδο της οξείδωσης με υπερθειικά κατά Ελμπς (Elbs persulfate) και τη μέθοδο της οξείδωση κατά Ντακίν.
Αντιδράσεις
[Επεξεργασία | επεξεργασία κώδικα]Η πηγή δραστικότητα της υδροκινόνης είναι οι δύο (2) υδροξυλομάδες. Η δράση της μοιάζει με αυτήν των υπόλοιπων φαινολών, που είναι ασθενώς όξινες. Το αποτέλεσμα είναι οι συζυγείς βάσεις να επιδέχονται εύκολη O-αλκυλίωση, δίνοντας τους αντίστοιχους μονο- και δι- αιθέρες. Ομοίως, η υδροκινόνη είναι ιδιαίτερα επιρεπής σε διάφορες αντιδράσεις υποκατάστασης στο βενζολικό δακτύλιό της κατά Friedel-Crafts, όπως είναι αλκυλίωση. Αυτή η αντίδραση αξιοποιείται για την παραγωγή δημοφιλών αντιοξειδωτικών, όπως η 2-τριτ. βουτυλο-4-μεθοξυφαινόλη (BHA). Η χρήσιμη χρωστική κινιζαρίνη παράγεται με διακυλίωση της υδροκινόνης με φθαλικό ανυδρίτη.
Οξειδοαναγωγής
[Επεξεργασία | επεξεργασία κώδικα]Η υδροκινόνη υφίσταται οξείδωση κάτω από ήπιες συνθήκες, δίνοντας ως προϊόν βενζοκινόνη. Αυτή η διαδικασία μπορεί να αντιστραφεί. Μερικά φυσικά παράγωγα της υδροκινόνης εμφανίζουν αυτό το είδος της αντιδραστικότητας, όπως για παράδειγμα το συνένζυμο Q. Η αντίδραση αξιοποιείται βιομηχανικά, τόσο με την ίδια την υδροκινόνη, όσο και με παράγωγά της
είναι η εκμετάλλευση και οι δύο με την υδροκινόνη ίδια, αλλά πιο συχνά με παράγωγά της, στα οποία το ένα (1) υδροξύλιο έχει αντικατασταθεί από αμινομάδα.
Αμίνωση
[Επεξεργασία | επεξεργασία κώδικα]Μια σημαντική αντίδραση είναι η μετατροπή της υδροκινόνης σε μονο- και διαμινο-παράγωγα. Η μεθυλαμινοφαινόλη, που χρησιμοποιούνται στη φωτογραφία, παράγεται με τον εξής τρόπο:
- C6H4(Ω)2 + CH3NH2 → C6H4(Ω)(N(H)CH3) + H2O
Ομοίως, διαμίνες χρήσιμες στη βιομηχανία ελαστικών, όπως antiozone παράγοντες, παράγονται με παρόμοιο τρόπο από την ανιλίνη:
- C6H4(Ω)2 + 2 C6H5NH2 → C6H4(N(H)C6H5)2 + 2 H2O
Χρήσεις
[Επεξεργασία | επεξεργασία κώδικα]Η υδροκινόνη έχει μια ποικιλία χρήσεων, κυρίως σχετικών με τη δράση της ως αναγωγικού παράγοντα που είναι διαλυτός στο νερό. Είναι ένα σημαντικό συστατικό στο πιο μαύρο και λευκό φωτογραφικό προγραμματιστές[ασαφές] για την ταινία και το έγγραφο, όπου, με την ένωση metol, ανάγει τα αλογονίδια του αργύρου σε στοιχειακό άργυρο.
Υπάρχουν διάφορες άλλες χρήσεις που συνδέονται με τη μείωση της δύναμης. Ως αναστολέας πολυμερισμού, υδροκινόνη εμποδίζει τον πολυμερισμό της ακρυλικό οξύ, μεθακρυλικό μεθύλιο, κυανοακρυλική κόλλα, και άλλα μονομερή τα οποία είναι ευαίσθητα σε ριζοσπαστική-ξεκίνησε πολυμερισμού. Αυτή η εφαρμογή εκμεταλλεύεται τις αντιοξειδωτικές ιδιότητες της υδροκινόνης.
Η υδροκινόνη μπορεί να υποστεί ήπια οξείδωση για να μετατραπεί στο σύνθετο παραβενζοκινόνη, C6H4O2, που συχνά ονομάζεται p-κινόνη ή απλά κινόνη. Αναγωγή της κινόνης αντιστρέφει αυτή την αντίδραση προς υδροκινόνη. Ορισμένες βιοχημικές ενώσεις στη φύση έχουν αυτό το είδος της υδροκινόνης ή κινόνης τμήμα τους δομές, όπως το Συνένζυμο Q, και μπορεί να υποβληθεί σε παρόμοιες οξειδοαναγωγικές μετατροπές.
Η υδροκινόνη μπορεί να χάσει ένα η+ από τα δύο για να σχηματίσουν ένα diphenolate ιόντων. Το diνατρίου diphenolate αλάτι της υδροκινόνης χρησιμοποιείται ως ένα εναλλασσόμενο coμονομερούς μονάδας για την παραγωγή του πολυμερές PEEK.
Αποχρωματισμός του δέρματος
[Επεξεργασία | επεξεργασία κώδικα]Η υδροκινόνη χρησιμοποιείται ως τοπική εφαρμογή στο δέρμα για να λευκάνει το χρώμα του. Δεν έχει την ίδια προδιάθεση να προκαλέσει δερματίτιδα, όπως το metol. Αυτή είναι μια συνταγή μόνο συστατικό[ασαφές] σε ορισμένες χώρες, συμπεριλαμβανομένων των κρατών μελών της Ευρωπαϊκής Ένωσης σύμφωνα με την οδηγία 76/768/ΕΟΚ:το 1976.[15][16]
Το 2006 η Υπηρεσία Τροφίμων και Φαρμάκων (FDA) των ΗΠΑ ανεκάλεσε την προηγούμενη έγκριση της υδροκινόνης και προτείνει την απαγόρευση όλων των σκευασμάτων που χορηγούνται χωρίς συνταγή.[17] Η FDA δήλωσε ότι η υδροκινόνη δεν μπορεί να αποκλειστεί ως πιθανή καρκινογόνος ουσία.[18] Στο συμπέρασμα αυτό κατέληξε με βάση την έκταση της απορρόφησης στον άνθρωπο και την επίπτωση των νεοπλασμάτων σε αρουραίους σε αρκετές μελέτες, όπου ενήλικες αρουραίοι βρέθηκαν να έχουν αυξημένα ποσοστά όγκων, συμπεριλαμβανομένων θυλακιώδη υπερπλασίες, anisokaryosis (παραλλαγή σε πυρήνες μεγέθη), μονοπύρηνων κυττάρων λευχαιμίας, ηπατοκυτταρικό αδένωμα και νεφρικό σωληνάριο κυτταρικά αδενώματα. Η Εκστρατεία για τα Ασφαλή Καλλυντικά ανέδειξε επίσης τις ανησυχίες τους.[19]
Πολυάριθμες μελέτες έχουν αποκαλύψει ότι η υδροκινόνη μπορεί να προκαλέσει εξωγενή ochronosis, μια παραμορφωτική ασθένεια στην οποία μπλε-μαύρο χρωστικές που εναποτίθενται πάνω στο δέρμα, αν ληφθεί από το στόμα, ωστόσο, το δέρμα παρασκευάσματα που περιέχουν το συστατικό που χορηγούνται τοπικά. Η FDA έχει ταξινομηθεί υδροκινόνη το 2006 ως ένα ασφαλές προϊόν - γενικά αναγνωρισμένη ως ασφαλής και αποτελεσματική (GRASE), ωστόσο συμπληρωματικές μελέτες σύμφωνα με το Εθνικό Πρόγραμμα Τοξικολογίας (NTP) προτάθηκαν προκειμένου να διαπιστωθεί αν υπάρχει κίνδυνος για τους ανθρώπους από τη χρήση της υδροκινόνης.[20] NTP αξιολόγηση έδειξε κάποια στοιχεία της μακροπρόθεσμης καρκινογόνων και των γονοτοξικών επιδράσεων[21]
Ενώ η χρήση υδροκινόνης ως παράγοντα λεύκανσης μπορεί να είναι αποτελεσματική με τη σωστή χρήση, μπορεί επίσης να προκαλέσει την ευαισθησία του δέρματος. Η καθημερινή χρήση αντιηλιακού με υψηλό PPD (persistent pigment) βαθμολογία μειώνει τον κίνδυνο της περαιτέρω βλάβης. Η υδροκινόνη είναι μερικές φορές σε συνδυασμό με άλφα υδροξύ οξέα που απολεπίζουν το δέρμα για να επιταχύνει την ελάφρυνση της διαδικασίας. Στις Ηνωμένες Πολιτείες, επίκαιρα θεραπείες που συνήθως περιέχει έως 2% υδροκινόνη. Διαφορετικά, υψηλότερες συγκεντρώσεις (μέχρι 4%) θα πρέπει να συνταγογραφείται και να χορηγείται με προσοχή.
Ενώ η υδροκινόνη παραμένει ευρέως συνταγογραφούμενη για τη θεραπεία της υπερμελάγχρωσης, ερωτήσεις που τέθηκαν σχετικά με το προφίλ ασφάλειας από ρυθμιστικών οργανισμών στην ΕΕ, την Ιαπωνία, και τις ΗΠΑ ενθαρρύνουν την αναζήτηση για άλλους παράγοντες με παρόμοια αποτελεσματικότητα.[22] Διάφοροι τέτοιοι παράγοντες είναι ήδη διαθέσιμοι ή υπό έρευνα[23], όπως το αζελαϊκό οξύ[24], το kojic οξύ, τα ρετινοειδή, η κυστεαμίνη,[25] τοπικά στεροειδή, το γλυκολικό οξύ και άλλες ουσίες.
Δείτε επίσης
[Επεξεργασία | επεξεργασία κώδικα]Εξωτερικοί σύνδεσμοι
[Επεξεργασία | επεξεργασία κώδικα]- Διεθνής Κάρτα Χημικής Ασφάλειας 0166
- NIOSH Οδηγός Τσέπης για Χημικούς Κινδύνους
- IARC Μονογραφία: «Υδροκινόνη»
Αναφορές και σημειώσεις
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Δείτε τις εναλλακτικές ονομασίες στον παρακείμενο πίνακα πληροφοριών χημικής ένωσης.
- ↑ F. Wöhler (1844) "Untersuchungen über das Chinon" (Investigations of quinone), Annalen der Chemie und Pharmacie, τόμ. 51, σσ. 145-163.
- ↑ Preferred IUPAC Names.
- ↑ Organic Chemistry, Solomon and Fryhle, 10th edition, Wiley Publishing, 2010.[Χρειάζεται σελίδα]
- ↑ Joval, E; Kroeger, P; N (Απρίλιος 1996). «Hydroquinone: the toxic compound of Agaricus hondensis». Planta Medica 62 (2): 185. doi:. PMID 17252436.
- ↑ Burdock, G.A. (1998). «Review of the biological properties and toxicity of bee propolis (propolis)». Food and Chemical Toxicology 36 (4): 347–363. doi:. PMID 9651052. https://archive.org/details/sim_food-and-chemical-toxicology_1998-04_36_4/page/347.
- ↑ The Beaver: Its Life and Impact.
- ↑ Phillip M. Hudnall "Hydroquinone" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. 2005 Wiley-VCH, Weinheim. doi:10.1002/14356007.a13_499.
- ↑ Reppe, Walter; Kutepow, N; Magin, A (1969). «Cyclization of Acetylenic Compounds». Angewandte Chemie International Edition in English 8 (10): 727–733. doi:. http://onlinelibrary.wiley.com/doi/10.1002/anie.196907271/abstract. Ανακτήθηκε στις 26 December 2013.
- ↑ Hubel, Karl· Braye, Henri (1960). Process for the preparation of substituted cyclic compounds and products resulting therefrom US3149138 A (PDF). Union Carbide Corp.
- ↑ Pino, Piero· Braca, Giuseppe (1964). Preparation of hydroquinone US3355503 A (PDF). Lonza Ag.
- ↑ Walter, Reppe· Magin, August (1966). Production of hydroquinones US3394193 A (PDF). Basf Ag.
- ↑ Piero, Pino· Giuseppe, Braca (1967). Preparation of hydroquinone US3459812 A (PDF). Lonza Ag.
- ↑ Holmes, J.· Hagemeyer, H. (1971). Process for the production of hydroquinone US 3742071 A (PDF). Eastman Kodak Co.
- ↑ 76/768/EEC:1976 Council Directive 76/768/EEC of 27 July 1976 on the approximation of the laws of the Member States relating to cosmetic products : http://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=CELEX:31976L0768:EN:HTML
- ↑ «Example of a product recall in Ireland». Αρχειοθετήθηκε από το πρωτότυπο στις 4 Οκτωβρίου 2011. Ανακτήθηκε στις 29 Μαΐου 2017.
- ↑ United States Food and Drug Administration (2006). Skin Bleaching Drug Products for Over-the-Counter Product Use; Proposed Rule (Report). 1978N-0065. http://www.fda.gov/OHRMS/DOCKETS/98fr/78n-0065-npr0003.pdf.
- ↑ Research, Center for Drug Evaluation and. «About the Center for Drug Evaluation and Research - Hydroquinone Studies Under The National Toxicology Program (NTP)». www.fda.gov (στα Αγγλικά). Ανακτήθηκε στις 12 Φεβρουαρίου 2017.
- ↑ «Campaign For Safe Cosmetics - Hydroquinone». Αρχειοθετήθηκε από το πρωτότυπο στις 27 Νοεμβρίου 2010. Ανακτήθηκε στις 29 Μαΐου 2017.
- ↑ Olumide, YM; Akinkugbe, AO; Altraide, D; Mohammed, T; Ahamefule, N; Ayanlowo, S; Onyekonwu, C; Essen, N (April 2008). «Complications of chronic use of skin lightening cosmetics». International Journal of Dermatology 47 (4): 344–53. doi:. PMID 18377596. https://archive.org/details/sim_international-journal-of-dermatology_2008-04_47_4/page/344.
- ↑ «Hydroquinone 10022-H». ntp.niehs.nih.gov (στα Αγγλικά). Ανακτήθηκε στις 12 Φεβρουαρίου 2017.
- ↑ Draelos, Zoe Diana (2007-09-01). «Skin lightening preparations and the hydroquinone controversy». Dermatologic Therapy 20 (5): 308–313. doi:. ISSN 1529-8019. PMID 18045355.
- ↑ Bandyopadhyay, Debabrata (2009-01-01). «TOPICAL TREATMENT OF MELASMA». Indian Journal of Dermatology 54 (4): 303–309. doi:. ISSN 0019-5154. PMID 20101327.
- ↑ Mazurek, Klaudia; Pierzchała, Ewa (2016-09-01). «Comparison of efficacy of products containing azelaic acid in melasma treatment». Journal of Cosmetic Dermatology 15 (3): 269–282. doi:. ISSN 1473-2165. PMID 27028014.
- ↑ Mansouri, P.; Farshi, S.; Hashemi, Z.; Kasraee, B. (2015-07-01). «Evaluation of the efficacy of cysteamine 5% cream in the treatment of epidermal melasma: a randomized double-blind placebo-controlled trial». The British Journal of Dermatology 173 (1): 209–217. doi:. ISSN 1365-2133. PMID 25251767.
| ||||||||||||||||||||||||||||||||||||||||||||


![{\displaystyle \mathrm {PhH+2CH_{3}CH=CH_{2}{\xrightarrow[{Al_{2}O_{3}}]{H_{3}PO_{4}}}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/08430a2efc9940406bcf97aeb1cfccec6d908262)