2-ναφθυλαμίνη
| 2-ναφθυλαμίνη | |||
|---|---|---|---|

| |||
| |||
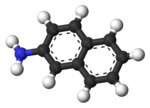
| Γενικά | |||
| Όνομα IUPAC | 2-ναφθαλιναμίνη | ||
| Άλλες ονομασίες | 2-ναφθυλαμίνη 2-αμινοναφθαλίνιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C10H9N | ||
| Μοριακή μάζα | 143,1852 ± 0,0088 amu | ||
| Αριθμός CAS | 91-59-8 | ||
| SMILES | c12ccccc1ccc(N)c2 | ||
| InChI | 1S/C10H9N/c11-10-6-5-8-3-1-2-4-9(8)7-10/h1-7H,11H2 | ||
| Αριθμός EINECS | 202-080-4 | ||
| ChemSpider ID | 6790 | ||
| Δομή | |||
| Ισομέρεια | |||
| Ισομερή θέσης | >100 | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | 111-113°C | ||
| Σημείο βρασμού | 306°C | ||
| Πυκνότητα | 1.061 kg/m³ | ||
| Διαλυτότητα στο νερό |
Αδιάλυτη | ||
| Τάση ατμών | 1 mmHg (104°C) | ||
| Χημικές ιδιότητες | |||
| pKa | 3,92 | ||
| Ελάχιστη θερμοκρασία ανάφλεξης |
157°C | ||
| Επικινδυνότητα | |||
 
| |||
| Τοξική (T) Βλαβερή για το περιβάλλον (N) Καρκινογόνα για τον άνθρωπο (ομάδα 1) | |||
| Φράσεις κινδύνου | 22, 45, 51/53 | ||
| Φράσεις ασφαλείας | 45, 53, 61 | ||
| LD50 | 727 mg/kg | ||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Η 2-ναφθυλαμίνη[1] (αγγλικά 2-naphthylamine) είναι αρωματική οργανική ένωση, που περιέχει άνθρακα, υδρογόνο και άζωτο, με μοριακό τύπο C10H9N. Πιο συγκεκριμένα, είναι μια αρωματική αμίνη, που ανήκει στα «θυγατρικά» ναφθαλίνια.
Χρησιμοποιείται για την παραγωγή αζωχρωμάτων. Είναι ένα γνωστό καρκινογόνο και γι' αυτό σε μεγάλο βαθμό έχει αντικατασταθεί από λιγότερο τοξικές ενώσεις.
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
2-Ναφθυλαμίνη παράγεται με συνθέρμανση 2-ναφθόλης με ψευδαργυροτετραχλωριούχο αμμώνιο {(NH4)2[ZnCl4]} στους 200-210°C, σύμφωνα με την αντίδραση Μπάχιρερ (Bucherer reaction).
Μπορεί να παραχθεί επίσης από ένα ακετυλοπαράγωγο της 2-ναφθόλης με οξικό αμμώνιο (CH3COONH4), στους 270-280 °C.
Αντιδράσεις[Επεξεργασία | επεξεργασία κώδικα]
Δίνει έγχρωμο προϊόν με τριχλωριούχο σίδηρο (FeCl3). Όταν αναχθεί με νάτριο διαλυμένο σε βραστή αμυλική αλκοόλη, δίνει τετραϋδρο-2-ναφθυλαμίνη, η οποία παρουσιάζει τις ιδιότητες των αλειφατικών αμινών, που είναι έντονα αλκαλική αντίδραση, έχει αμμωνιακή οσμή και δεν μπορεί να δώσει διαζωνιακές ενώσεις.
Οξειδώνεται δίνοντας 2-καρβοξυδροκινναμικό οξύ [(2-HOOC(C6H4)CH2CH2COOH] .
Εφαρμογές[Επεξεργασία | επεξεργασία κώδικα]
Πολλά παράγωγα της 2-ναφθυλαμίνης με θειικό οξύ χρησιμοποιούνται στο εμπόριο, ως πρόδρομες ενώσεις για χρωστικές. Επειδή, όμως, η 2-ναφθυλαμίνη είναι καρκινογόνα, συνήθως οι χρωστικές αυτές παράγονται με αμίνωση των αντιστοίχων ναφθολών (συνήθως της 2-ναφθόλης). Από αυτά τα παράγωγα, αυτό που έχει τη μεγαλύτερη τεχνική αξία είναι το δ-οξύ (δ-acid) και το οξύ του οξύ του Μπρόνερ (Bronner's acid), καθώς συνδυάζονται με ορθοτετραζωδιοτολυλομάδα, για να δώσουν μια θαυμάσια κόκκινη χρωστική ουσία για τρόφιμα.
Ασφάλεια[Επεξεργασία | επεξεργασία κώδικα]
Η 2-ναφθυλαμίνη βρίσκεται στα τσιγάρα και υπάρχει υποψία ότι συμβάλει στην ανάπτυξη του καρκίνου της ουροδόχου κύστης.[2]
Ενεργοποιείται στο ήπαρ, αλλά γρήγορα απενεργοποιείται από την σύζευξη με γλυκουρονικό οξύ. Στην κύστη, το ένζυμο γλυκουρονιδάση την επανενεργοποιεί τη 2-ναφθυλαμίνη με υδρόλυση του ενδιάμεσα σχηματισμένου αμιδίου, οδηγώντας στην (πιθανή) ανάπτυξη του καρκίνου της ουροδόχου κύστης.
Δείτε επίσης[Επεξεργασία | επεξεργασία κώδικα]
| |||||||||||||||||||||||||||||||||||
Αναφορές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Για εναλλακτικές ονομασίες δείτε τον πίνακα πληροφοριών.
- ↑ CDC - NIOSH Οδηγός Τσέπης για Χημικοί Κίνδυνοι
