Ετεροκυκλικές ενώσεις


Ετεροκυκλικές ονομάζονται οι κυκλικές χημικές ενώσεις των οποίων ο δακτύλιος περιέχει άτομα τουλάχιστον δύο διαφορετικών χημικών στοιχείων, σύμφωνα με τον ορισμό της IUPAC[1] Σε αντιδιαστολή, οι κυκλικές χημικές ενώσεις των οποίων ο δακτύλιος περιέχει αποκλειστικά άτομα ενός και μόνο στοιχείου ονομάζονται ομοκυκλικές ή ισοκυκλικές.[2][3].
Παρ' όλο που υπάρχουν και ανόργανες ετεροκυκλικές ενώσεις (δείτε παρακάτω), οι περισσότερες, οι πιο γνωστές και οι πιο χρήσιμες είναι οι οργανικές. Και επειδή, στην οργανική ένωση, όταν σε αυτήν υπάρχουν άτομα και άλλων χημικών στοιχείων, εκτός του άνθρακα και του υδρογόνου στην ένωση, θεωρείται συχνά ότι αντικαθιστούν άτομα άνθρακα ή και υδρογόνου, γι' αυτό τα άτομα αυτά ονομάζονται «ετεροάτομα». Έτσι, τα «ετεροατόμα» έχουν την έννοια των ατόμων που δεν είναι άτομα του άνθρακα ή του υδρογόνου. Είναι, ωστόσο, δυνατό μια ένωση να περιέχει δακτύλιο από ένα είδος ετεροατόμων, οπότε είναι ομοκυκλική. Η IUPAC συνιστά τη χρήση της συστηματικής ονοματολογίας Hantzsch-Widman, για την ονοματοδοσία των ετεροκυκλικών ενώσεων, για μονοκυκλικές ενώσεις που περιέχουν μέχρι και δεκαμελή δακτύλιο. Υπάρχουν, επίσης, μερικές ετεροκυκλικές ενώσεις με εμπειρικές ή ημιεμπιρικές ονομασίες, που διατηρούνται επίσημα. Τέλος, οι υπόλοιπες ονομάζονται σύμφωνα με την ονοματολογία αντικατάστασης, δηλαδή παίρνουν τη συστηματική ονομασία των αντίστοιχων ομοκυκλικών ενώσεων και τα ετεροάτομα τοποθετούνται μπροστά, με τους αριθμούς θέσης τους (αν απαιτείται), ως υποκαταστάτες.
Οι οργανικές ετεροκυκλικές ενώσεις ιδιαίτερα αυτές που περιέχουν άτομα αζώτου, οξυγόνου και θείου, απαντώνται συχνά και σε ενώσεις βιολογικής προέλευσης (είναι δηλαδή βιοχημικές) όπως τα νουκλεϊκά οξέα, πρωτεϊνογόνα αμινοξέα, υδατάνθρακες, αλκαλοειδή και φυσικές χρωστικές. Έχουν μεγάλη σημασία για τις επιστήμες της χημείας, της βιοχημείας, της βιολογίας, της φαρμακολογίας και της τοξικολογίας.
Ο κλάδος της χημείας που ασχoλείται με τις ετεροκυκλικές ενώσεις ονομάζεται ετεροκυκλική χημεία, και ασχολείται με τη σύνθεση, τις ιδιότητες και τις εφαρμογές των ετεροκυκλικών ενώσεων.
Ταξινόμηση[Επεξεργασία | επεξεργασία κώδικα]
Οι ετεροκυκλικές ενώσεις ταξινομούνται με διάφορους τρόπους ανάλογα με την ιδιότητα (χημική σύσταση, δομή, μέγεθος, ηλεκτρονιακή διαμόρφωση, βιολογικός ρόλος, κλπ) στην οποία επιδιώκεται να δοθεί έμφαση ή η οποία εξυπηρετεί μια δεδομένη διάκριση. Ακολούθως αναφέρονται μερικές από τις κυριότερες ταξινομήσεις.
- Οι ετεροκυκλικές ενώσεις διακρίνονται σε ανόργανες, όταν ο δακτύλιος και οι υποκαταστάτες δεν περιέχουν κανένα άτομο άνθρακα, και σε οργανικές, όταν ο δακτύλιος ή οι υποκαταστάτες περιέχουν τουλάχιστον ένα άτομο άνθρακα. Λόγω του πολύ μεγαλύτερου αριθμού των οργανικών ετεροκυκλικών ενώσεων σε σύγκριση με τις ανόργανες, καθώς και της σπουδαιότητάς τους σε πολλούς κλάδους της χημείας, ο όρος «ετεροκυκλική ένωση» χωρίς άλλο προσδιοριστικό χρησιμοποιείται συχνά ως συνώνυμο του «οργανική ετεροκυκλική ένωση», οπότε είναι προφανές ότι ο δακτύλιος ή οι υποκαταστάτες περιέχουν ένα τουλάχιστον άτομο άνθρακα. Στην περίπτωση των οργανικών ετεροκυκλικών ενώσεων τα άτομα του δακτυλίου που ανήκουν σε στοιχεία εκτός του άνθρακα (π.χ. άζωτο, οξυγόνο, θείο) αποκαλούνται ετεροάτομα.
-
2,4,6,1,3,5-τριβορατριαζινίνη, ανόργανη ετεροκυκλική ένωση
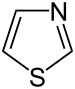
-
1,3-θειαζόλιο, οργανική ετεροκυκλική ένωση
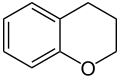
-
Χρωμάνιο, οργανική ετεροκυκλική ένωση
- Κατατάσσονται ως προς το μέγεθος, ανάλογα με τον αριθμό των ατόμων του ετεροκυκλικού δακτυλίου.
- Διακρίνονται σε μονοκυκλικές, όταν στο μόριό τους υπάρχει μόνο ένας δακτύλιος, και πολυκυκλικές όταν στο μόριό τους περιλαμβάνονται περισσότεροι του ενός δακτύλιοι, εκ των οποίων τουλάχιστον ένας είναι ετεροκυκλικός. Οι πολυκυκλικές ενώσεις διακρίνονται επίσης σε ενώσεις με συμπυκνωμένους δακτυλίους, όταν οι δακτύλιοι έχουν έναν δεσμό από κοινού, και σε σπειροενώσεις, όταν οι δακτύλιοι έχουν κοινό μόνο ένα άτομο.
-
Πυριμιδίνη, μονοκυκλική ετεροκυκλική ένωση
-
Κινοξαλίνη, δικυκλική ετεροκυκλική ένωση
-
7-αζασπειρο[5,4]δεκάνιο, δικυκλική ετεροκυκλική σπειροένωση
- Ένας οργανικός ετεροκυκλικός δακτύλιος μπορεί να είναι κορεσμένος, όταν κανένα από τα άτομα του δακτυλίου δεν συμμετέχει σε πολλαπλό δεσμό, ή ακόρεστος, όταν τουλάχιστον ένα άτομο συμμετέχει σε πολλαπλό δεσμό. Με σημείο αναφοράς έναν κορεσμένο δακτύλιο, ο αριθμός ζευγών υδρογόνου που απομακρύνονται για να παραχθούν σταδιακά τα ακόρεστα παράγωγά του ονομάζεται βαθμός ακορεστότητας. Σημειώνεται ότι το μόριο μιας οργανικής ετεροκυκλικής ένωσης μπορεί να περιέχει και άλλες ανθρακικές αλυσίδες εκτός του ετεροκυκλικού δακτυλίου, γι' αυτό και είναι δυνατό μια ένωση να έχει τον χαρακτηρισμό ακόρεστη (για παράδειγμα, να περιέχει έναν διπλό δεσμό C=C) αλλά με κορεσμένο ετεροκυκλικό δακτύλιο (δηλαδή ο εν λόγω διπλός δεσμός δεν είναι μέρος του δακτυλίου αλλά μιας πλευρικής αλυσίδας που ενώνεται με αυτόν).
-
Πιπεριδίνη, κορεσμένη ετεροκυκλική ένωση
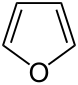
-
Φουράνιο, ακόρεστη ετεροκυκλική ένωση
- Οι ετεροκυκλικές ενώσεις μπορεί να είναι αρωματικές, οπότε ονομάζονται ετεροαρωματικές ενώσεις, εφόσον ο ετεροκυκλικός δακτύλιος περιέχει 4n+2 απεντοπισμένα ηλεκτρόνια (όπου n φυσικός αριθμός) σε π συζυγή τροχιακά του δακτυλίου που προσδίδουν στην ένωση αρωματικό χαρακτήρα, αντιαρωματικές (4n π ηλεκτρόνια) ή μη αρωματικές. Για να δηλωθεί ταυτόχρονα ο αρωματικός χαρακτήρας και η ετεροκυκλική φύση μιας ένωσης χρησιμοποιείται ο όρος ετεροαρωματικότητα και οι αντίστοιχες ενώσεις χαρακτηρίζονται ετεροαρωματικές. Όπως στις καρβοκυκλικές[4] αρωματικές ενώσεις (π.χ. το βενζόλιο και τα παράγωγά του), ο συνηθέστερος αριθμός π ηλεκτρονίων των οργανικών ετεροκυκλικών αρωματικών ενώσεων είναι 6. Εκτός των ατόμων άνθρακα, στις ετεροκυκλικές ενώσεις π ηλεκτρόνια μπορούν να συνεισφέρουν και τα ετεροάτομα που έχουν ασύζευκτο ζεύγος ηλεκτρονίων σε p ατομικά τροχιακά κάθετα στο επίπεδο του δακτυλίου, όπως το άτομο του αζώτου στο πυρρόλιο.
Ονοματολογία[Επεξεργασία | επεξεργασία κώδικα]
Οι πρώτες προσπάθεις δημιουργίας συστηματικών κανόνων ονοματολογίας των ετεροκυκλικών ενώσεων έγιναν τον 19ο αιώνα από τους Α. Χαντς[5] και Ο. Βίντμαν.[6] Η βασική λογική του συστήματος Χαντς-Βίντμαν, το οποίο έκτοτε αναθεωρήθηκε και επεκτάθηκε, είναι η παραγωγή της ονομασίας με συνδυασμό ενός ή περισσότερων προθεμάτων που δηλώνουν το είδος των ατόμων που περιέχονται στον δακτύλιο, και μιας κατάληξης που δηλώνει το μέγεθος του δακτυλίου.[7]
Το σύγχρονο σύστημα ονοματολογίας ετεροκυκλικών ενώσεων κατά IUPAC ενσωματώνει το σύστημα κανόνων Χαντς-Βίντμαν (Hantzsch-Widman) για μονοκυκλικές ενώσεις με μέγεθος δακτυλίου μέχρι 10 άτομα, ενώ για μεγαλύτερους δακτυλίους και πολυκυκλικές ενώσεις ή πιο σύνθετες περιπτώσεις ακολουθείται το τυποποιημένο σύστημα της οργανικής ονοματολογίας αντικατάστασης. Παράλληλα, το σύστημα περιλαμβάνει έναν κατάλογο με εμπειρικές και ημιεμπειρικές ονομασίες οι οποίες είναι επισήμως αποδεκτές και χρησιμοποιούνται αντί των ονομασιών που θα προέκυπταν από τους συστηματικούς κανόνες.[8] Οι κανόνες περιγράφονται στο τρία πρώτα τμήματα του λεγόμενου «Blue Book» της IUPAC, το οποίο πρωτοεκδόθηκε το 1979[9] και αναθεωρήθηκε μερικώς το 1983.[10] Κάθε ονομασία ετεροκυκλικής ένωσης που βρισκόταν σε χρήση πριν τη δημοσίευση των δύο αυτών οδηγιών, που δεν προκύπτει από τους συστηματικούς κανόνες και δεν περιλαμβάνεται στον επίσημο κατάλογο εξαιρέσεων, θεωρείται ακατάλληλη.
Μονοκυκλικές ενώσεις[Επεξεργασία | επεξεργασία κώδικα]
- Το είδος του ετεροατόμου ή των ετεροατόμων δηλώνεται με τα προθέματα του πίνακα 1, τα οποία συνδυάζονται με την κατάλληλη κατάληξη από τον πίνακα 2. Όταν ακολουθεί φωνήεν, το τελικό α του προθέματος εκθλίβεται και παραμένει το αρχικό φωνήεν της επόμενης συλλαβής (π.χ. αζα + -ετιδίνη = αζετιδίνη).
| Ετεροάτομο | Σθένος | Πρόθεμα | Ετεροάτομο | Σθένος | Πρόθεμα | |
|---|---|---|---|---|---|---|
| F | I | Φθορα | As | III | Αρσα ή Αρσεν | |
| Cl | I | Χλωρα | Sb | III | Στιμπα ή Αντιμον | |
| Br | I | Βρωμα | Bi | III | Βισμα | |
| I | I | Ιωδα | Si | IV | Σιλα | |
| O | II | Οξα | Ge | IV | Γερμα | |
| S | II | Θεια | Sn | IV | Σταννα | |
| Se | II | Σεληνα | Pb | IV | Πλουμπα | |
| Te | II | Τελλουρα | B | III | Βορα | |
| N | III | Αζα | Hg | II | Μερκουρα | |
| P | III | Φωσφα ή Φωσφορ |
| Μέλη δακτυλίου | Κορεσμένος | Ακόρεστος[α] | |
|---|---|---|---|
| 3 | -ιράνιο (-ιριδίνη)[β] |
-ιρένιο (-ιρίνη)[β] | |
| 4 | -ετάνιο (-ετιδίνη)[β] |
-έτιο | |
| 5 | -ολάνιο (-ολιδίνη)[β] |
-όλιο | |
| 6Α | O, S, Se, Te, Bi, Hg | -άνιο | -ίνιο |
| 6Β | N, Si, Ge, Sn, Pb | -ινάνιο | -ίνιο (-ίνη)[β] |
| 6Γ | B, F, Cl, Br, I, P, As, Sb | -ινάνιο | -ινίνιο |
| 7 | -επάνιο | -επίνιο (-επίνη)[β] | |
| 8 | -οκάνιο | -οκίνιο (-οκίνη)[β] | |
| 9 | -ονάνιο | -ονίνιο (-ονίνη)[β] | |
| 10 | -εκάνιο | -εκίνιο (-εκίνη)[β] | |
- Στον πρώτο αριστερά πίνακα, τα δεύτερα προθέματα, όπου υπάρχουν, χρησιμοποιούνται όταν ακολουθεί η συλλαβή «-ιν-». Π.χ. αρσεπάνιο (δηλαδή αρσ, αφού δεν ακολουθεί ιν) και αρσενίνιο (δηλαδή αρσεν, αφού ακολουθεί ιν).
- Όταν υπάρχουν διαφορετικά ετεροάτομα, τότε τα προθέματα παρατάσσονται ακολουθώντας ως σειρά προτεραιότητας τη σειρά με την οποία τα στοιχεία αναγράφονται στον Πίνακα 1 (π.χ. «θειαζάνιο» και όχι «αζαθειάνιο»).
- Περισσότερα του ενός ετεροάτομα του ίδιου στοιχείου δηλώνονται με τα αριθμητικά προθέματα δι-, τρι- κλπ που προτάσσονται των αντίστοιχων προθεμάτων του πίνακα 1 (π.χ. «διαζόλιο»). Όταν το αριθμητικό πρόθεμα τελειώνει σε α και ακολουθεί φωνήεν, το α εκθλίβεται.
- Για δακτυλίους με ένα ετεροάτομο, η αρίθμηση του δακτυλίου ξεκινά από το ετεροάτομο. Για δακτυλίους με διαφορετικά ετεροάτομα η αρίθμηση ξεκινά με το ετεροάτομο που προηγείται στον πίνακα 1. Για δακτυλίους με δύο ή περισσότερα ετεροάτομα η αρίθμηση ακολουθεί φορά τέτοια ώστε οι αριθμοί θέσης ετεροατόμων να είναι οι μικρότεροι δυνατοί. Τα αριθμητικά θέσης πάντοτε προηγούνται της ονομασίας ή του προθέματος που προσδιορίζουν.
-
1,3-θειαζόλιο
-
1,2,4-τριαζίνη
-
1,2,5-τριθειεπάνιο
- Σχετικά με τον πίνακα 2 σημειώνεται ότι η επίσημη ονοματολογία της IUPAC ορίζεται στα αγγλικά, μια γλώσσα που δεν έχει γραμματικά γένη. Στην ελληνική γλώσσα οι καταλήξεις των ετεροκυκλικών ενώσεων αποδίδονται γενικά σε ουδέτερο γένος, εκτός από τις περιπτώσεις που αναφέρονται ρητά στον πίνακα (κορεσμένες αζωτούχες ενώσεις με δακτύλιο 3-5 μελών και ακόρεστες τριμελείς αζωτούχες ενώσεις). Μια εξαίρεση αφορά στις αζωτούχες ενώσεις με εξαμελείς και μεγαλύτερους δακτυλίους: στα ελληνικά συνήθως (αλλά όχι πάντα) οι αζωτούχες ενώσεις είναι γένους θηλυκού, οπότε οι αναγραφόμενες στον πίνακα καταλήξεις παίρνουν την ανάλογη μορφή (π.χ. αλλάζουν από «-ίνιο» σε «-ίνη», από «-επίνιο» σε «-επίνη» κλπ). Τονίζεται ότι η κατάληξη «-όλη» αναφέρεται στην τάξη των αλκοολών και η χρήση της είτε σε συστηματικές είτε σε εμπειρικές ονομασίες αζωτούχων ετεροκυκλικών ενώσεων αντί της κατάληξης «-όλιο» είναι πάντοτε λανθασμένη. Οι ενώσεις που δεν έχουν άζωτο παίρνουν τις ουδέτερες καταλήξεις του πίνακα 2, χωρίς αυτό να σημαίνει ότι δεν εντοπίζονται και αποκλίσεις στην βιβλιογραφία λόγω ευρείας διάδοσης μιας μη συστηματικής ονομασίας (π.χ. «διοξίνη» αντί του ορθότερου «διοξίνιο»).
- Για τους εξαμελείς δακτυλίους η κατάληξη προσδιορίζεται ανάλογα με την ομάδα (6Α, 6Β, 6Γ) στην οποία ανήκει το μοναδικό ετεροάτομο, ή ανάλογα με την ομάδα στην οποία ανήκει το ετεροάτομο το οποίο βρίσκεται πιο χαμηλά στην κατάταξη του πίνακα 2 (και το οποίο ως εκ τούτου συντάσσεται στην ονομασία της ένωσης αμέσως πριν την κατάληξη).
- Τα μερικώς υδρογονωμένα παράγωγα των ακόρεστων ετεροκυκλικών ενώσεων ονομάζονται με προθέματα όπως «διυδρο», «τετραϋδρο» κλπ, στο μητρικό όνομα. Για τα ολικώς υδρογονωμένα αζωτούχα παράγωγα, με δακτύλιο μεγαλύτερο από πενταμελή, χρησιμοποιείται το όνομα της πλήρως ακόρεστης ένωσης και το πρόθεμα «περυδρο». Όπως και στις ομοκυκλικές ενώσεις η θέση ενός επιπλέον υδρογόνου δηλώνεται με πρόθεση αριθμητικού δείκτη και του γράμματος Η (π.χ. 2Η-διοξίνιο). Παλαιότερα η θέση του διπλού δεσμού δηλωνόταν με το γράμμα Δ και έναν εκθέτη που αντιστοιχούσε στο πρώτο αριθμητικά άτομο του διπλού δεσμού, αλλά το σύστημα αυτό δεν είναι πλέον σε χρήση.
- Υπάρχουν πολλές ενώσεις για τις οποίες διατηρούνται επισήμως συγκεκριμένες εμπειρικές και ημιεμπειρικές ονομασίες.[8]
- Για δακτυλίους μεγαλύτερους από δεκαμελείς το σύστημα Χαντς-Βίντμαν παύει να ισχύει και οι ονομασίες προκύπτουν από αυτές των αντίστοιχων δακτυλίων χωρίς ετεροάτομα (π.χ. κυκλικών υδρογονανθράκων) με αριθμητικούς συντελεστές και προθέματα που δηλώνουν τη θέση και το είδος των ετεροατόμων.
Στον ακόλουθο πίνακα παρατίθενται οι απλούστερες περιπτώσεις οργανικών μονοκυκλικών ετεροκυκλικών ενώσεων με ένα ετεροάτομο αζώτου, οξυγόνου ή θείου, ταξινομημένες ανάλογα με το μέγεθος και την ακορεστότητα του δακτυλίου. Οι ονομασίες είναι αυτές που ορίζονται από τους κανόνες της IUPAC.
| Κορεσμένοι δακτύλιοι | Ακόρεστοι δακτύλιοι | |||||
|---|---|---|---|---|---|---|
| Ετεροάτομο | Άζωτο | Οξυγόνο | Θείο | Άζωτο | Οξυγόνο | Θείο |
| τριμελείς δακτύλιοι | ||||||
| Ονομασία | Αζιριδίνη | Οξιράνιο | Θειιράνιο | N-αζιρίνη | Οξιρένιο | Θειιρένιο |
| Δομή | ||||||
| τετραμελείς δακτύλιοι | ||||||
| Ονομασία | Αζετιδίνη | Οξετάνιο | Θειετάνιο | Αζέτιο | Οξέτιο | Θειέτιο |
| Δομή | ||||||
| πενταμελείς δακτύλιοι | ||||||
| Ονομασία | Αζολιδίνη Πυρρολιδίνη[α] |
Οξολάνιο | Θειολάνιο | Αζόλιο Πυρρόλιο[α] |
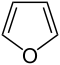
Οξόλιο Φουράνιο[α] |
Θειόλιο Θειοφαίνιο[α] |
| Δομή | 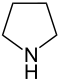 |
 |
 |
 |
 |

|
| εξαμελείς δακτύλιοι | ||||||
| Ονομασία | Αζινάνιο Πιπεριδίνη[α] |
Οξάνιο | Θειάνιο | Αζίνη[β] Πυριδίνη[α] |
Οξίνιο[β] Πυράνιο[α] |
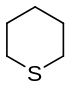
Θειίνιο Θειοπυράνιο[α] |
| Δομή | 
|

|
|

|

|

|
| επταμελείς δακτύλιοι | ||||||
| Ονομασία | Αζεπάνιο | Οξεπάνιο | Θειεπάνιο | Αζεπίνη | Οξεπίνιο | Θειεπίνιο |
| Δομή |  |
 |
 |
 |
 |

|
| ||||||
Μονοκυκλικές ενώσεις με δύο ή περισσότερα ετεροάτομα είναι επίσης συνηθισμένες, με σπουδαιότερες τις αζωτούχες ενώσεις. Μερικά παραδείγματα μονοκυκλικών ενώσεων με δύο ετεροάτομα είναι τα ακόλουθα:
| Πενταμελείς με 2 ετεροάτομα | ||||
|---|---|---|---|---|
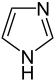
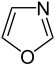
| Πυραζόλιο | Ιμιδαζόλιο | Οξαζόλιο | Ισοξαζόλιο | Θειαζόλιο |
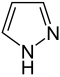 |
 |
 |
 |

|
| Εξαμελείς με 2 ετεροάτομα | ||||
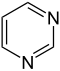
| Πυριδαζίνη | Πυραμιδίνη | Πυραζίνη | Πιπεραζίνη | Μορφολίνη |
 |
 |
 |
 |

|
Μια ειδική κατηγορία ετεροκυκλικών ενώσεων είναι εκείνες στις οποίες τον ρόλο του ετεροατόμου έχει αναλάβει ένα μέταλλο των στοιχείων μετάπτωσης. Οι ενώσεις αυτές ονομάζονται μεταλλοκυκλικές και αποτελούν ένα από τα αντικείμενα μελέτης της οργανομεταλλικής χημείας, όπου απαντώνται ως ενδιάμεσες ενώσεις σε καταλυτικές αντιδράσεις.[12] Οι δακτύλιοι των ενώσεων αυτών ονομάζονται συνήθως με πρόθεση του ονόματος του μετάλλου στο όνομα του μητρικού οργανικού δακτυλίου, π.χ. «οσμαβενζόλιο» για έναν δακτύλιο βενζολίου όπου το ένα άτομο άνθρακα έχει αντικατασταθεί από ένα ιόν οσμίου.
Πολυκυκλικές ενώσεις[Επεξεργασία | επεξεργασία κώδικα]
Για τα συμπυκνωμένα ετεροκυκλικά συστήματα ισχύουν οι ίδιοι κανόνες που εφαρμόζονται στους συμπυκνωμένους υδρογονάνθρακες. Λόγω της πολυπλοκότητας που παρουσιάζει η ονοματολογία στα συστήματα αυτά, εδώ αναφέρονται μόνο τα κριτήρια που ακολουθούνται για την επιλογή του βασικού συστήματος, κατά σειρά προτεραιότητας:
- δακτύλιος που περιέχει ετεροάτομο
- δακτύλιος που περιέχει άτομο αζώτου
- δακτύλιος με ετεροάτομο που προηγείται στην κατάταξη του πίνακα 1
- δακτύλιος με το μεγαλύτερο μέγεθος
- για ενώσεις με πάνω από δύο δακτυλίους, το μητρικό υποσύστημα με τον μεγαλύτερο αριθμό συμπυκνωμένων δακτυλίων, τον μεγαλύτερο αριθμό ετεροατόμων, ή τα περισσότερα διαφορετικά ετεροάτομα
Παρά τους συστηματικούς κανόνες ονοματολογίας, για τις συνηθέστερα απαντώμενες πολυκυκλικές ενώσεις κυριαρχούν οι εμπειρικές και ημιεμπειρικές ονομασίες. Στον ακόλουθο πίνακα δίνονται παραδείγματα ετεροκυκλικών ενώσεων με δύο και τρεις συμπυκνωμένους δακτυλίους.
| Με δύο δακτυλίους | |||||
|---|---|---|---|---|---|
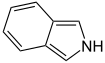
| Ινδόλιο | Ισοϊνδόλιο | Κινολίνη | Ισοκινολίνη | Πτεριδίνη | Πουρίνη |
 |
 |
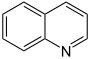 |
 |
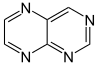 |

|
| Με τρεις δακτυλίους | |||||
| Καρβαζόλιο | Φαινανθρολίνη | Ακριδίνη | |||
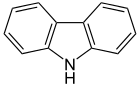
|

|

| |||
Μονοκυκλικές ετεροκυκλικές ενώσεις με τριμελή δακτύλιο[Επεξεργασία | επεξεργασία κώδικα]
Οι ετεροκυκλικές ενώσεις που περιέχουν τριμελή δακτύλιο είναι περισσότερο δραστικές, εξαιτίας αποθήκευσης επιπλέον χημικής ενέργειας σε αυτές, με τη μορφή ενέργειας παραμόρφωσης λόγω δακτυλίου. Όσες από αυτές περιέχουν ένα (μόνο) ετεροάτομο είναι γενικά (σχετικά) σταθερές. Αυτές που περιέχουν δύο (2) ετεροάτομα, το πιθανότερο είναι να είναι τόσο ασταθείς ώστε να χρειάζεται να παραχθούν in situ, όταν απαιτείται η χρήση τους ή και υπάρχουν μόνο ως ενδιάμεσα (και πολύ προσωρινά) προϊόντα αντιδράσεων.
Οι πιο συνηθισμένες μονοκυκλικές ετεροκυκλικές ενώσεις με τριμελή δακτύλιο και ένα (1) ετεροάτομο είναι οι ακόλουθες:
| Ετεροάτομο | Κορεσμένη ένωση | Ακόρεστη ένωση |
|---|---|---|
| Άζωτο | Αζιριδίνη ( |
Αζιριδίνες [1Η-αζιρίνη ( |
| Οξυγόνο | Οξιράνιο ( |
Οξιρένιο ( |
| Θείο | Θειιράνιο ( |
Θειιρένιο ( |
| Βόριο | Βοριράνιο ( |
Βοριρένια [1H-βοριρένιο () και 2H-βοριρένιο () ] |
Οι πιο συνηθισμένες μονοκυκλικές ετεροκυκλικές ενώσεις με τριμελή δακτύλιο και δύο (2) ετεροάτομα είναι οι ακόλουθες:
| Ετεροάτομο | Κορεσμένη ένωση | Ακόρεστη ένωση |
|---|---|---|
| Άζωτο | Διαζιριδίνη ( |
Διαζιριδίνες (1Η-διαζιρίνη και 3H-διαζιρίνη) |
| Οξυγόνο | Διοξιράνιο ( |
|
| Άζωτο και οξυγόνο | Οξαζιριδίνη ( |
Μονοκυκλικές ετεροκυκλικές ενώσεις με τετραμελή δακτύλιο[Επεξεργασία | επεξεργασία κώδικα]
Οι πιο συνηθισμένες μονοκυκλικές ετεροκυκλικές ενώσεις με τετραμελή δακτύλιο και ένα (1) ετεροάτομο είναι οι ακόλουθες:
| Ετεροάτομο | Κορεσμένη ένωση | Ακόρεστη ένωση |
|---|---|---|
| Άζωτο | Αζετιδίνη ( |
Αζέτιο ( |
| Οξυγόνο | Οξετάνιο ( |
Οξετένιο ( |
| Θείο | Θειετάνιο ( |
Θειετένιο ( ) )
|
Οι πιο συνηθισμένες μονοκυκλικές ετεροκυκλικές ενώσεις με τετραμελή δακτύλιο και δύο (2) ετεροάτομα είναι οι ακόλουθες:
| Ετεροάτομο | Κορεσμένη ένωση | Ακόρεστη ένωση |
|---|---|---|
| Άζωτο | Διαζετιδίνες [ 1,2-διαζετιδίνη () και 1,3-διαζετιδίνη ()] | Διαζέτια |
| Οξυγόνο | Διοξετάνια [ 1,2-διοξετάνιο ( |
Διοξέτια |
| Θείο | Διθειετάνια [ 1,2-διοθειετάνιο ( )] )]
|
Διθειέτια |
Μονοκυκλικές ετεροκυκλικές ενώσεις με πενταμελή δακτύλιο[Επεξεργασία | επεξεργασία κώδικα]
Στις ετεροκυκλικές ενώσεις που περιέχουν πενταμελείς δακτυλίους συχνά οι ακόρεστες είναι σταθερότερες, γιατί συχνά συμβαόνει να είναι ετεροαρωματικές.
Οι πιο συνηθισμένες μονοκυκλικές ετεροκυκλικές ενώσεις με πενταμελή δακτύλιο και ένα (1) ετεροάτομο είναι οι ακόλουθες:
| Ετεροάτομο | Κορεσμένη ένωση | Ακόρεστη ένωση |
|---|---|---|
| Άζωτο | Πυρρολιδίνη ( |
Πυρρόλιο ( ) )
|
| Οξυγόνο | Τετραϋδροφουράνιο ( |
Φουράνιο ( |
| Θείο | Τετραϋδροθειοφαίνιο ( |
Θειοφαίνιο ( ) )
|
| Βόριο | Βορολάνιο ( |
1H-βορόλιο ( |
| Φωσφόρος | Φωσφολάνιο ( |
Φωσφόλιο ( |
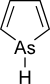
| Αρσενικό | Αρσολάνιο ( |
Αρσόλιο ( |
| Αντιμόνιο | Αντιμονάνιο ( |
Αντιμονόλιο ( |
| Βισμούθιο | Βισμολάνιο () | Βισμόλιο ( |
| Πυρίτιο | Σιλολάνιο ( |
Σιλόλιο ( |
| Κασσίτερος | Σταννολάνιο ( |
Σταννόλιο ( |
Οι πιο συνηθισμένες μονοκυκλικές ετεροκυκλικές ενώσεις με πενταμελή δακτύλιο και δύο (2) ετεροάτομα είναι οι ακόλουθες:
| Ετεροάτομο | Κορεσμένη ένωση | Ακόρεστη ένωση |
|---|---|---|
| Άζωτο | Ιμιδαζολιδίνη ( |
Ιμιδαζόλιο ( Πυραζόλιο () |
| Οξυγόνο | 1,3-διοξολάνιο ( |
|
| Θείο | 1,2-διθειολάνιο ( |
|
| Άζωτο και οξυγόνο | 1,2-οξαζολιδίνη ( |
1,2-οξαζόλιο ( ) )
|
| Άζωτο και θείο | 1,3-θειαζολιδίνη ( |
1,2-θειαζόλιο ( ) )
|
Οι πιο συνηθισμένες μονοκυκλικές ετεροκυκλικές ενώσεις με πενταμελή δακτύλιο και τρία (3) ετεροάτομα είναι οι ακόλουθες:
| Ετεροάτομο | Κορεσμένη ένωση | Ακόρεστη ένωση |
|---|---|---|
| Άζωτο | 1,2,3-τριαζόλη ( | |
| 2 άτομα αζώτου + 1 άτομο οξυγόνου | Φουραζάνιο ( ) )
| |
| 2 άτομα αζώτου + 1 άτομο θείου | Θειαδιαζόλια | |
| 1 άτομο αζώτου + 2 άτομα θείου | 1,4,2-διθειαζόλιο ( |
Η πιο συνηθισμένη μονοκυκλική ετεροκυκλική ένωση με πενταμελή δακτύλιο και τέσσερα (4) ετεροάτομα είναι η ακόλουθη:
| Ετεροάτομο | Κορεσμένη ένωση | Ακόρεστη ένωση |
|---|---|---|
| Άζωτο | Τετραζόλιο ( ) )
|
Οι πιο συνηθισμένες ανόργανες μονοκυκλικές ετεροκυκλικές ενώσεις (η τελευταία είναι μάλιστα ισοκυκλική) με πενταμελή δακτύλιο και πέντε (5) ετεροάτομα είναι οι ακόλουθες:
| Ετεροάτομο | Κορεσμένη ένωση | Ακόρεστη ένωση |
|---|---|---|
| 4 άτομα αζώτου + 1 άτομο οξυγόνου | Οξατετραζόλιο | |
| 4 άτομα αζώτου + 1 άτομο θείου | Θειατετραζόλιο | |
| Άζωτο | Πενταζόλιο ( ) )
|
Ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Η πληθώρα και η πολυμορφία των ετεροκυκλικών ενώσεων συνεπάγεται ότι δεν υπάρχει κοινό σύνολο φυσικών ή χημικών ιδιοτήτων. Από γενική σκοπιά, μια χρήσιμη προσέγγιση για την κατανόηση των διαφορών μεταξύ ενός οργανικού ετεροκυκλικού δακτυλίου και του αντίστοιχου ομοκυκλικού συστήματος, είναι να θεωρήσουμε το ομοκυκλικό σύστημα ως σημείο αναφοράς και να εξετάσουμε τί αλλαγές επιφέρει η αντικατάσταση ενός ατόμου άνθρακα από ένα ετεροάτομο. Οι ιδιότητες του μορίου επηρεάζονται κυρίως με τρεις τρόπους:
- Το ετεροάτομο έχει διαφορετική (συνήθως μεγαλύτερη) ηλεκτραρνητικότητα από τον άνθρακα, με αποτέλεσμα να επέρχεται πόλωση στην κατανομή του ηλεκτρικού φορτίου εντός του μορίου
- Το ετεροάτομο έχει διαφορετικό μέγεθος ατομικών τροχιακών από τον άνθρακα, με συνέπεια να ελαττώνεται η αλληλεπικάλυψη των τροχιακών μεταξύ αυτού και των γειτονικών του ατόμων
- Το ετεροάτομο ενδεχομένως φέρει μονήρες ζεύγος ηλεκτρονίων, οπότε μπορεί να δράσει ως βάση κατά Lewis (δότης ζεύγους ηλεκτρονίων) ή ως βάση κατά Brønsted (δέκτης πρωτονίου).
Ο συνδυασμός των παραπάνω παραγόντων καθορίζει τόσο τις στατικές φυσικοχημικές ιδιότητες μιας ετεροκυκλικής ένωσης (δομή, θερμοδυναμική σταθερότητα, φασματοσκοπικές ιδιότητες, διαλυτότητα κλπ), όσο και τους τρόπους με τους οποίους αντιδρά με άλλες ενώσεις.
Πηγές[Επεξεργασία | επεξεργασία κώδικα]
- W. H. Powell, Revision of the Extended Hantzsch-Widman System of Nomenclature for Heteromonocycles, Pure Appl. Chem., 1983, 55, 409-416. Copyright 1979 IUPAC. (PDF).
- Συστάσεις ονοματολογίας IUPAC, 1979 και 1993
- Καραγκιοζίδη Σ. Πολυχρόνη, «Ονοματολογία Οργανικών Ενώσεων στα Ελληνικά & Αγγλικά» Β΄ Έκδοση, Εκδόσεις Ζήτη, Θεσσαλονίκη 1991[13].
- M. B. Smith, J. March, March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, 6η Έκδοση, Wiley, 2007.
- Παπαγεωργίου, Β.Π., Εφαρμοσμένη Οργανική Χημεία, Εκδόσεις Παρατηρητής, Θεσσαλονίκη 2005, ISBN 960-260-342-7
- SCHAUM'S OUTLINE SERIES, «ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ», Μτφ. Α. Βάρβογλη, 1999
- «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982
- Αναστάσιου Βάρβογλη, «Χημεία Οργανικών Ενώσεων», Παρατηρητής, Θεσσαλονίκη 1991
- Νικολάου Ε. Αλεξάνδρου, «Γενική Οργανική Χημεία», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985
- Δημητρίου Ν. Νικολαΐδη, «Ειδικά Μαθήματα Οργανικής Χημείας», ΑΠΘ, θεσσαλονίκη 1983
- Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Φαίδωνα Χατζημηχαλάκη, «Εργαστηριακός Οδηγός», Εκδόσεις Ζήτη, Θεσσαλονίκη 1986
- Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Δημητρίου Ν. Νικολαΐδη: «Χημεία Ετεροκυκλικών Ενώσεων», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985
- Διαδικτυακοί τόποι που αναφέρονται στις «Αναφορές και παρατηρήσεις».
Αναφορές και παρατηρήσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ A. D. McNaught, A. Wilkinson, IUPAC. Compendium of Chemical Terminology, 2η έκδοση, Blackwell Scientific Publications, Oxford, 1997. XML on-line corrected version: http://goldbook.iupac.org (2006-) created by M. Nic, J. Jirat, B. Kosata; updates compiled by A. Jenkins. IUPAC Gold Book: heterocyclic compounds.
- ↑ IUPAC Gold Book: homocyclic compounds
- ↑ Ο όρος «ισοκυκλικές» χρησιμοποιείται επί χρόνια περισσότερο στην ελληνική βιβλιογραφία, αν και ο όρος «ομοκυκλικές» είναι ακριβέστερος.
- ↑ IUPAC Gold Book: carbocyclic compounds
- ↑ A. Hantzsch, J. H. Weber, Ber. Dtsch. Chem. Ges., 1887, 20, 3118-3132.
- ↑ O. Widman, J. Prakt. Chem., 1888, 38, 185-201
- ↑ IUPAC Gold Book: Hantzsch–Widman name
- ↑ 8,0 8,1 Κανόνας IUPAC Β-2.
- ↑ Nomenclature of Organic Chemistry, Sections A, B, C, D, E, F, and H, Pergamon Press, Oxford, 1979.
- ↑ W. H. Powell, Revision of the Extended Hantzsch-Widman System of Nomenclature for Heteromonocycles, Pure Appl. Chem., 1983, 55, 409-416.
- ↑ «Κανόνας IUPAC: FR-2.2. Heterocyclic Components». 27 Δεκεμβρίου 2020.
- ↑ J. F. Hartwig, Organotransition Metal Chemistry: from Bonding to Catalysis, University Science Books, 2010.
- ↑ Το βιβλίο του Πολυχρόνη Καραγκιοζίδη είναι σημείο αναφοράς στην ελληνική βιβλιογραφία της οργανικής χημείας. Ένα από τα ελάχιστα προβλήματά του είναι ότι (μέχρι και την 2η έκδοση) δεν λαμβάνει υπ'όψη τις αναθεωρήσεις των κανόνων της IUPAC από το 1983 και έπειτα, επομένως υπάρχουν μερικά (λίγα) σημεία που σύμφωνα με τους ισχύοντες κανόνες εμπίπτουν στην "παρωχημένη χρήση".