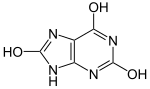
Ουρικό οξύ
| Ουρικό οξύ | |
|---|---|

| |
| Γενικά | |
| Όνομα IUPAC | Ουρικό οξύ |
| Άλλες ονομασίες | 7,9-διυδρο-1H-πουρινο-2,6,8(3H)-τριόνη, 2,6,8-τριοξοπουρίνη |
| Χημικά αναγνωριστικά | |
| Χημικός τύπος | C5H4N4O3 |
| Μοριακή μάζα | 168,028 amu |
| Φυσικές ιδιότητες | |
| Σημείο τήξης | 300 °C |
| Πυκνότητα | 1,89 g/cm3 |
| Διαλυτότητα στο νερό |
60 mg/dm3 (στους 20 °C) |
| Εμφάνιση | λευκοί κρύσταλλοι |
| Χημικές ιδιότητες | |
| pKa1 | 5,4 |
| pKa2 | 10,3 |
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |
Το ουρικό οξύ είναι μια ετεροκυκλική χημική ένωση με χημικό τύπο C5H4N4O3, που αποτελεί παράγωγο της πουρίνης. Σχηματίζεται στον οργανισμό κυρίως από τον καταβολισμό πουρινικών βάσεων (αδενίνη, γουανίνη και ουρακίλη) των νουκλεϊκών οξέων. Υψηλές συγκεντρώσεις ουρικού οξέος στο αίμα σχετίζονται με την εμφάνιση ουρικής αρθρίτιδας («ποδάγρας») και λίθων στα νεφρά (νεφρολιθίαση, ουρολιθίαση).
Χημικές ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Το ουρικό οξύ είναι διπρωτικό οξύ με σταθερές οξύτητας pKa1 = 5,4 και pKa2 = 10,3.[1] Σε υψηλό pH συμπεριφέρεται σαν ισχυρή βάση κατά Lewis και σχηματίζει το διπλώς αρνητικά φορτισμένο ουρικό ιόν. Ωστόσο, σε φυσιολογικό pH χάνει μόνο ένα πρωτόνιο και σχηματίζει το απλώς φορτισμένο ουρικό ανιόν, γνωστό και ως «όξινο ουρικό».
Η ένωση μπορεί να εμφανίζεται με ταυτομερείς κετονικές και ενολικές μορφές (ταυτομέρεια κετο-ενόλης), που διαφέρουν στην κατανομή των πρωτονίων μεταξύ των χαρακτηριστικών ομάδων του μορίου. Οι δύο ακραίες περιπτώσεις ταυτομερών είναι οι εξής:
Το ουρικό οξύ και τα άλατά του έχουν γενικά χαμηλή διαλυτότητα στο νερό, γεγονός που ευνοεί την δημιουργία κρυστάλλων.[2][1]
Βιολογία[Επεξεργασία | επεξεργασία κώδικα]
Η σύνθεση του ουρικού οξέος στον οργανισμό γίνεται από τα προϊόντα πουρινικών ενώσεων ξανθίνη και υποξανθίνη, με μεσολάβηση του ενζύμου ξανθινοξειδάση (οξειδάση της ξανθίνης). Στους ανθρώπους το ουρικό οξύ είναι το τελικό προϊόν μεταβολισμού των πουρινών και αποβάλλεται κυρίως (σε ποσοστό περίπου 70%) μέσω των νεφρών στα ούρα. Στα πτηνά και στα ερπετά το ουρικό οξύ είναι επίσης το τελικό προϊόν του μεταβολισμού των πουρινών, αλλά εκκρίνεται σε στερεά μορφή με τα κόπρανα.[3] Σε άλλα θηλαστικά ο μεταβολισμός συνεχίζεται εντός του οργανισμού, με το ένζυμο ουρικάση να οξειδώνει το ουρικό οξύ σε αλλαντοΐνη.[4] Το ουρικό οξύ είναι ισχυρά αναγωγική ένωση (δότης ηλεκτρονίων) και επομένως μπορεί να δράσει ως αντιοξειδωτικός παράγοντας.[5][6]
Παθολογία[Επεξεργασία | επεξεργασία κώδικα]
Αυξημένα επίπεδα ουρικού οξέος στο αίμα οδηγούν στην κατάσταση που ονομάζεται υπερουριχαιμία. Αυτή δηλώνει ότι η ισορροπία μεταξύ της διάσπασης των πουρινών εντός του οργανισμού και της αποβολής του ουρικού οξέος έχει διαταραχθεί, δηλαδή είτε παράγεται περισσότερο ουρικό οξύ από το φυσιολογικό (ή, ισοδύναμα, εισάγεται στον οργανισμό μεγάλη ποσότητα πουρινών), είτε η αποβολή του ουρικού οξέος είναι ατελής με αποτέλεσμα τη συσσώρευσή του. Η κατάσταση αυτή δεν συνιστά από μόνη της νόσο, ούτε έχει παθολογικά συμπτώματα. Σχετίζεται όμως με την ουρική αρθρίτιδα, η οποία εμφανίζεται με μορφή φλεγμονής και πόνου στα άκρα (κυρίως στα πόδια), και με την νεφρολιθίαση (λίθοι ουρικού οξέως), η οποία μπορεί να εκδηλωθεί με μορφή κωλικού ή αιματουρίας.
Τα αίτια της υπερουριχαιμίας μπορεί να είναι είτε η αυξημένη παραγωγή ουρικού οξέος (π.χ. λόγω γενετικών/κληρονομικών παραγόντων ή διατροφής) είτε η μειωμένη απέκκρισή του (π.χ. λόγω νεφρικής δυσλειτουργίας που προσβάλλει ένα ποσοστό 5-25% των ανθρώπων[7], ή λήψης κάποιων φαρμάκων).
Η αντίθετη κατάσταση (υποουριχαιμία) είναι πιο σπάνια και σχετίζεται με έλλειψη σιδήρου (αναιμία) ή μολυβδαινίου, δύο στοιχείων που είναι απαραίτητα για την λειτουργία της ξανθινοξειδάσης.
Δείτε επίσης[Επεξεργασία | επεξεργασία κώδικα]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 McCrudden, Francis H. (2008). Uric Acid. BiblioBazaar.
- ↑ CRC Handbook of Chemistry and Physics (62η έκδοση).
- ↑ Hazard, Lisa C. (2004). Sodium and Potassium Secretion by Iguana Salt Glands. Iguanas: Biology and Conservation. University of California Press. σελίδες 84–85.
- ↑ Angstadt, Carol N. (1997-12-04). Purine and Pyrimidine Metabolism: Purine Catabolism. NetBiochem, 4 December 1997.
- ↑ Proctor, P. «Similar functions of uric acid and ascorbate in man?». Nature 228 (5274): 868.
- ↑ Glantzounis G. K., Tsimoyiannis E. C., Kappas A. M., Galaris D. A. (2005). «Uric acid and oxidative stress». Current Pharmaceutical Design 11 (32): 4145–4151.
- ↑ Vitart V., Rudan I., Hayward C., et al. «SLC2A9 is a newly identified urate transporter influencing serum urate concentration, urate excretion and gout». Nature Genetics 40 (4): 437–442.
|