Τροπόνη
| Το λήμμα δεν περιέχει πηγές ή αυτές που περιέχει δεν επαρκούν. |
| Τροπόνη | |||
|---|---|---|---|

| |||

| |||
| Γενικά | |||
| Όνομα IUPAC | 2,4,6-κυκλοεπτατριενόνη | ||
| Άλλες ονομασίες | Τροπόνη | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C7H6O | ||
| Μοριακή μάζα | 106,12 amu | ||
| Αριθμός CAS | 539-80-0 | ||
| SMILES | O=C\1/C=C\C=C/C=C/1 | ||
| InChI | 1S/C7H6O/c8-7-5-3-1-2-4-6-7/h1-6H | ||
| PubChem CID | 10881 | ||
| ChemSpider ID | 10419 | ||
| Δομή | |||
| Ισομέρεια | |||
| Φυσικές ιδιότητες | |||
| Σημείο βρασμού | 113°C | ||
| Πυκνότητα | 1.094 kg/m³ | ||
| Εμφάνιση | Άχρωμο υγρό | ||
| Χημικές ιδιότητες | |||
| Ελάχιστη θερμοκρασία ανάφλεξης |
>113°C | ||
| Επικινδυνότητα | |||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Η τροπόνη[1] (αγγλικά tropone) είναι αρωματική οργανική χημική ένωση, που περιέχει άνθρακα, υδρογόνο και οξυγόνο, με μοριακό τύπο C7H6O, Αποτελεί σημαντική ένωση για την οργανική χημεία και γιατί αποτελεί σχετικά σπάνιο παράδειγμα μη βενζοειδούς αρωματικής ένωσης.[2] Δομικά, το μόριο της ένωσης αποτελείται από έναν επταμελή ισοκυκλικό δακτύλιο, με τρεις (3) συζυγείς (δηλαδή εναλλάξ) διπλούς δεσμούς και μια κετονομάδα (>C=O). Εκτός από τη «μητρική» τροπόνη, ο όρος επεκτείνεται και σε μια σειρά «θυγατρικά» παράγωγα αυτής. Η «θυγατρική» τροπολόνη περιέχει επιπλέον μια υδροξυλομάδα (-OH), ακριβώς δίπλα από την κετονομάδα. Οι «θυγατρικές» τροπόνες συμπεριλαμβάνουν βιομόρια, όπως η κολχικίνη, το στιπτατικό οξύ και η ινοκτιόλη.
Η τροπόνη είχε γίνει γνωστή από το 1951 και ονομάζεται επίσης «οξείδιο του κυκλοεπτανοτριυλίου». Η ονομασία «τροπολόνη» επινοήθηκε από το Μάικλ Ντιούαρ (M. J. S. Dewar) το 1945.[3]
Σύνθεση
[Επεξεργασία | επεξεργασία κώδικα]Πολλές μέθοδοι υπάρχουν για την οργανική σύνθεση των τροπονών. Μερικά επιλεγμένα παραδείγματα μεθόδων σύνθεσης τροπονών είναι τα ακόλουθα:
- Το 1,3,5-κυκλοεπτατριένιο μπορεί να οξειδωθεί με διοξείδιο του σεληνίου (SeO2), σχηματίζοντας τροπόνη.
- Επίσης, η τροπινόνη μπορεί να μετατραπεί με ιωδομεθάνιο (CH3I) και θέρμανση σε 1,2-κυκλοεπταδιενόνη, η οποία μπορεί, με τη σειρά της, να οξειδωθεί με διάλυμα στοιχειακού βρωμίου (Br2) σε τετραχλωράνθρακα (CCl4), σχηματίζοντας, επίσης, τροπόνη.

Ιδιότητες
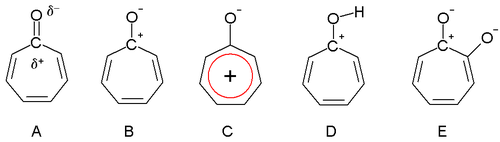
[Επεξεργασία | επεξεργασία κώδικα]Ο Ντιούαρ, το 1945 πρότεινε ότι οι τροπόνες θα μπορούσαν να έχουν αρωματικές ιδιότητες. Το καρβονύλιο της ομάδας είναι πολωμένο με ένα μερικό θετικό (δ+) ηλεκτρικό φορτίο στο άτομο άνθρακα (σχήμα Α) και ένα μερικό αρνητικό φορτίο (δ-) στο άτομο οξυγόνου. Σε μια ακραία μεσομορφή της ένωσης, το άτομο άνθρακα έχει πλήρες θετικό φορτίο (C+, σχήμα Β), το οποίο διασπείρεται σε όλο το δακτύλιο του σχηματιζόμενου κατιόντος τροπυλίου, που αποτελεί αρωματικό σύστημα 6 ηλεκτρονίων (σχήμα C).
Η τροπολόνη είναι όξινη (η συζυγής της βάση δείχνεται στο σχήμα E), με pKa =7, που είναι ενδιάμεσο μεταξύ του αντίστοιχο της φαινόλης (PhOH, με pKa=10) και του βενζοϊκού οξέος (PhCOOH, με pKa = 4). Η αυξημένη οξύτητα, σε σύγκριση με τη φαινόλη, οφείλεται πολύ στην κανονική μεσομερή σταθεροποίηση. Οι τροπόνες είναι βασικές (σχήμα D, ενώ και οι τροπολόνες δίνουν και βασικές αντιδράσεις), γεγονός που οφείλεται πολύ στην αρωματική σταθεροποίηση. Η ιδιότητα αυτή μπορεί εύκολα να παρατηρηθεί, με το σχηματισμό αντίστοιχων αλάτων, μετά από την επίδραση οξέων. Η διπολική ροπή της τροπόνης είναι 4,17 D, σε σύγκριση με 3,04 D, της διπολικής ροπής της κυκλοεπτανόνης. Οι τιμές αυτές μπορούν επίσης να ληφθούν ως αποδεικτικές ενδείξεις για την αρωματικότητα της τροπόνης.
Αντιδράσεις
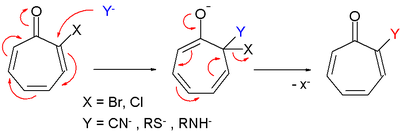
[Επεξεργασία | επεξεργασία κώδικα]- Η ‹μητρική› τροπόνη δίνει αντιδράσεις ηλεκτρονιόφιλης υποκατάστασης, για παράδειγμα με βρώμιο (Br2), αλλά η αντίδραση προχωρά μέσα από προσωρινή (έστω) παραγωγή προϊόντος 1,2-προσθήκης και δεν πρόκειται για αυθεντική ηλεκτρονιόφιλη αρωματική υποκατάσταση.
- Αρκετές «θυγατρικές» τροπόνες δίνουν, επίσης, αντιδράσεις πυρηνόφιλης υποκατάστασης, που λειτουργεί όπως η πυρηνόφιλη αρωματική υποκατάσταση.
- Η «μητρική» τροπόνη δίνει αντιδράσεις Ντιλς-Άλντερ, όπως τα διένια, με το μηλεϊνικό ανυδρίτη, για παράδειγμα.
- Η «μητρική» τροπόνη βρέθηκε ότι αντιδρά με [8+3] αννουλίωση με κινναμοναλδεΰδες (PhCH=CHCHO)[4]
Αναφορές και σημειώσεις
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Δείτε τις εναλλακτικές ονομασίες στον παρακείμενο πίνακα πληροφοριών χημικής ένωσης.
- ↑ Tropones and Tropolones Peter L. Pauson. Chemical Reviews.
- ↑ M. J. S. Dewar (1945). «Structure of Stipitatic Acid». Nature 155 (3924): 50–51. doi:.
- ↑ An N-Heterocyclic Carbene-Catalyzed [8 + 3] Annulation of Tropone and Enals via Homoenolate Vijay Nair, Manojkumar Poonoth, Sreekumar Vellalath, Eringathodi Suresh, and Rajasekaran Thirumalai "The Journal of Organic Chemistry".
| |||||||||||||||||