Ογκανέσσιο: Διαφορά μεταξύ των αναθεωρήσεων
| Γραμμή 137: | Γραμμή 137: | ||
Κατά συνέπεια, ορισμένοι αναμένουν το ουνουνόκτιο να έχει παρόμοιες φυσικές και χημικές ιδιότητες με τα άλλα μέλη της ομάδας του, πιο στενή ομοιότητα με το ευγενές αέριο από πάνω του στον περιοδικό πίνακα, το [[ραδόνιο]] <ref>{{cite web|url=http://lenntech.com/Periodic-chart-elements/Uuo-en.htm|title=Ununoctium (Uuo) – Chemical properties, Health and Environmental effects|publisher=Lenntech|accessdate=2008-01-18|archiveurl = http://web.archive.org/web/20080116172028/http://lenntech.com/Periodic-chart-elements/Uuo-en.htm |archivedate = January 16, 2008|deadurl=yes}}</ref>. Ακολουθώντας την [[περιοδική τάση]], το ουνουνόκτιο αναμένεται να είναι ελαφρώς πιο δραστικό από το ραδόνιο. Ωστόσο, θεωρητικοί υπολογισμοί έχουν δείξει ότι θα μπορούσε να είναι τόσο δραστικό, έτσι ώστε πιθανώς να μην μπορεί να θεωρηθεί [[Ευγενή αέρια|ευγενές αέριο]] <ref name=Kaldor>{{cite book|title=Theoretical Chemistry and Physics of Heavy and Superheavy Elements|first1=Uzi|last1=Kaldor|first2=Stephen|last2=Wilson|page=105|year=2003|publisher=Springer|isbn=1-4020-1371-X}}</ref>. Πέραν του ότι μπορεί να είναι πολύ πιο δραστικό από το ραδόνιο, το ουνουνόκτιο μπορεί να είναι ακόμη πιο αντιδραστικό απ´ ότι τα στοιχεία [[φλερόβιο]] και [[κοπερνίκιο]] <ref name=Nash>{{cite journal|title=Atomic and Molecular Properties of Elements 112, 114, and 118|first=Clinton S.|last=Nash|journal=Journal of Physical Chemistry A|year=2005|volume=109|issue=15|pages=3493–3500|doi=10.1021/jp050736o|pmid=16833687|last1=Nash|first1=CS}}</ref>. Ο λόγος για την εμφανή αύξηση της χημικής δραστικότητας σε σχέση με το ραδόνιο είναι μία ενεργητική αποσταθεροποίηση και μία ακτινική διαστολή του τελευταίου κατεχόμενου 7b υποφλοιού.<ref name=Nash/><ref group="Σημ.">Η ακριβής φράση είναι "Ο λόγος για την εμφανή ενίσχυση της χημικής δραστηριότητας του στοιχείου 118 σε σχέση με το ραδόνιο είναι η ενεργειακή αποσταθεροποίηση και ακτινική διαστολή του κατεχόμενου 7b περιβλήματος."</ref> Ακριβέστερα, σημαντικές αλληλεπιδράσεις τροχιάς μεταξύ των ηλεκτρονίων 7p με τα αδρανή 7s<sup>2</sup> ηλεκτρόνια, έχει ως αποτέλεσμα ένα δεύτερο κλείσιμο κελύφους στο φλερόβιο, και μια σημαντική μείωση στην σταθερότητα του κλειστού περιβλήματος του στοιχείου 118 <ref name="Nash"/>. Επίσης, έχει υπολογιστεί ότι το ουνουνόκτιο, σε αντίθεση με άλλα ευγενή αέρια, δεσμεύει ένα ηλεκτρόνιο με την απελευθέρωση της ενέργειας ή με άλλα λόγια, εμφανίζει θετική ηλεκτρονκή συγγένεια <ref name=Pyykko>{{cite journal|title=QED corrections to the binding energy of the eka-radon (Z=118) negative ion|first1=Igor|last1=Goidenko|first2=Leonti|last2=Labzowsky|first3=Ephraim|last3=Eliav|first4=Uzi|last4=Kaldor|first5= Pekka |last5=Pyykko¨|journal=Physical Review A|volume=67|year=2003|pages=020102(R)|doi=10.1103/PhysRevA.67.020102|bibcode = 2003PhRvA..67b0102G|issue=2}}</ref><ref>{{cite journal|volume=77|issue=27|journal=Physical Review Letters|year=1996|title=Element 118: The First Rare Gas with an Electron Affinity|first1=Ephraim |last1=Eliav |first2=Uzi |last2=Kaldor|doi=10.1103/PhysRevLett.77.5350|pages=5350–5352|pmid=10062781|last3=Ishikawa|first3=Y|last4=Pyykkö|first4=P |bibcode=1996PhRvL..77.5350E}}</ref><ref group="Σημ.">Παρ 'όλα αυτά, κβαντικές ηλεκτροδυναμικές διορθώσεις έχουν αποδείξει ότι είναι αρκετά σημαντικό για τη μείωση της συνάφειας με τη μείωση της δέσμευσης του ανιόντος Uuo<sup>-</sup> κατά 9%, επιβεβαιώνοντας έτσι τη σημασία αυτών των διορθώσεων στο βαρέα στοιχεία. Δείτε το Pyykkö.</ref> |
Κατά συνέπεια, ορισμένοι αναμένουν το ουνουνόκτιο να έχει παρόμοιες φυσικές και χημικές ιδιότητες με τα άλλα μέλη της ομάδας του, πιο στενή ομοιότητα με το ευγενές αέριο από πάνω του στον περιοδικό πίνακα, το [[ραδόνιο]] <ref>{{cite web|url=http://lenntech.com/Periodic-chart-elements/Uuo-en.htm|title=Ununoctium (Uuo) – Chemical properties, Health and Environmental effects|publisher=Lenntech|accessdate=2008-01-18|archiveurl = http://web.archive.org/web/20080116172028/http://lenntech.com/Periodic-chart-elements/Uuo-en.htm |archivedate = January 16, 2008|deadurl=yes}}</ref>. Ακολουθώντας την [[περιοδική τάση]], το ουνουνόκτιο αναμένεται να είναι ελαφρώς πιο δραστικό από το ραδόνιο. Ωστόσο, θεωρητικοί υπολογισμοί έχουν δείξει ότι θα μπορούσε να είναι τόσο δραστικό, έτσι ώστε πιθανώς να μην μπορεί να θεωρηθεί [[Ευγενή αέρια|ευγενές αέριο]] <ref name=Kaldor>{{cite book|title=Theoretical Chemistry and Physics of Heavy and Superheavy Elements|first1=Uzi|last1=Kaldor|first2=Stephen|last2=Wilson|page=105|year=2003|publisher=Springer|isbn=1-4020-1371-X}}</ref>. Πέραν του ότι μπορεί να είναι πολύ πιο δραστικό από το ραδόνιο, το ουνουνόκτιο μπορεί να είναι ακόμη πιο αντιδραστικό απ´ ότι τα στοιχεία [[φλερόβιο]] και [[κοπερνίκιο]] <ref name=Nash>{{cite journal|title=Atomic and Molecular Properties of Elements 112, 114, and 118|first=Clinton S.|last=Nash|journal=Journal of Physical Chemistry A|year=2005|volume=109|issue=15|pages=3493–3500|doi=10.1021/jp050736o|pmid=16833687|last1=Nash|first1=CS}}</ref>. Ο λόγος για την εμφανή αύξηση της χημικής δραστικότητας σε σχέση με το ραδόνιο είναι μία ενεργητική αποσταθεροποίηση και μία ακτινική διαστολή του τελευταίου κατεχόμενου 7b υποφλοιού.<ref name=Nash/><ref group="Σημ.">Η ακριβής φράση είναι "Ο λόγος για την εμφανή ενίσχυση της χημικής δραστηριότητας του στοιχείου 118 σε σχέση με το ραδόνιο είναι η ενεργειακή αποσταθεροποίηση και ακτινική διαστολή του κατεχόμενου 7b περιβλήματος."</ref> Ακριβέστερα, σημαντικές αλληλεπιδράσεις τροχιάς μεταξύ των ηλεκτρονίων 7p με τα αδρανή 7s<sup>2</sup> ηλεκτρόνια, έχει ως αποτέλεσμα ένα δεύτερο κλείσιμο κελύφους στο φλερόβιο, και μια σημαντική μείωση στην σταθερότητα του κλειστού περιβλήματος του στοιχείου 118 <ref name="Nash"/>. Επίσης, έχει υπολογιστεί ότι το ουνουνόκτιο, σε αντίθεση με άλλα ευγενή αέρια, δεσμεύει ένα ηλεκτρόνιο με την απελευθέρωση της ενέργειας ή με άλλα λόγια, εμφανίζει θετική ηλεκτρονκή συγγένεια <ref name=Pyykko>{{cite journal|title=QED corrections to the binding energy of the eka-radon (Z=118) negative ion|first1=Igor|last1=Goidenko|first2=Leonti|last2=Labzowsky|first3=Ephraim|last3=Eliav|first4=Uzi|last4=Kaldor|first5= Pekka |last5=Pyykko¨|journal=Physical Review A|volume=67|year=2003|pages=020102(R)|doi=10.1103/PhysRevA.67.020102|bibcode = 2003PhRvA..67b0102G|issue=2}}</ref><ref>{{cite journal|volume=77|issue=27|journal=Physical Review Letters|year=1996|title=Element 118: The First Rare Gas with an Electron Affinity|first1=Ephraim |last1=Eliav |first2=Uzi |last2=Kaldor|doi=10.1103/PhysRevLett.77.5350|pages=5350–5352|pmid=10062781|last3=Ishikawa|first3=Y|last4=Pyykkö|first4=P |bibcode=1996PhRvL..77.5350E}}</ref><ref group="Σημ.">Παρ 'όλα αυτά, κβαντικές ηλεκτροδυναμικές διορθώσεις έχουν αποδείξει ότι είναι αρκετά σημαντικό για τη μείωση της συνάφειας με τη μείωση της δέσμευσης του ανιόντος Uuo<sup>-</sup> κατά 9%, επιβεβαιώνοντας έτσι τη σημασία αυτών των διορθώσεων στο βαρέα στοιχεία. Δείτε το Pyykkö.</ref> |
||
Το ουνουνόκτιο αναμένεται να έχει κατά πολύ ευρύτατη πολωσιμότητα, πιο πολύ από όλα τα προηγούμενα στοιχεία, και σχεδόν διπλάσια από του ραδονίου <ref name="Nash"/>. Σε παρέκταση από τα άλλα ευγενή αέρια, αναμένεται ότι το ουνουνόκτιο έχει ένα σημείο βρασμού μεταξύ 320 και 380 Κ (50 - 80°C) <ref name="Nash"/>. Αυτό είναι πολύ διαφορετικό από τις προηγούμενες εκτιμώμενες τιμές (263 K <ref name=Seaborg>{{cite book|title=Modern Alchemy|authorlink=Glenn Theodore Seaborg|first=Glenn Theodore|last=Seaborg|year=1994|isbn=981-02-1440-5|publisher=World Scientific|page =172}}</ref> ή 247 K <ref>{{cite journal|journal=Journal of Radioanalytical and Nuclear Chemistry|volume=251|issue=2|year=2002|pages=299–301|title=Boiling points of the superheavy elements 117 and 118|first=N. |last=Takahashi|doi=10.1023/A:1014880730282}}</ref>). Ακόμη και δεδομένων των μεγάλων αβεβαιοτήτων των υπολογισμών, φαίνεται εξαιρετικά απίθανο ότι το ουνουνόκτιο θα είναι αέριο υπό κανονικές συνθήκες <ref name="Nash"/><ref group="Σημ.">Είναι αμφίβολο εάν το όνομα της ομάδας "ευγενή αέρια" θα αλλάξει, εάν το ουνουνόκτιο φαίνεται να είναι μη πτητικό</ref>, και καθώς το υγρό φάσμα των άλλων αερίων είναι πολύ περιορισμένο, μεταξύ 2 και 9 °Kelvin, το στοιχείο αυτό πρέπει να είναι [[στερεό]] υπό κανονικές συνθήκες. Αν το ουνουνόκτιο σχηματίζει [[αέριο]] κάτω από τυπικές συνθήκες, ωστόσο, θα ήταν ένα από τις πυκνότερες αέριες ουσίες υπό κανονικές συνθήκες (ακόμη και αν είναι μονοατομικό όπως και τα άλλα ευγενή αέρια). |
|||
Λόγω της τεράστιας πόλωσής του, το ουνουνόκτιο αναμένεται να έχει μια αφύσικα χαμηλή ενέργεια ιονισμού (παρόμοια με εκείνη του [[Μόλυβδος|μολύβδου]], η οποία είναι 70% περισσότερη από αυτήν του [[Ραδόνιο|ραδονίου]] <ref name=hydride/> και σημαντικά μικρότερη από εκείνη του [[Φλερόβιο|φλεροβίου]] <ref>{{cite journal|journal=Journal of Physical Chemistry A|volume=1999|issue=3|pages=402–410|title=Spin-Orbit Effects, VSEPR Theory, and the Electronic Structures of Heavy and Superheavy Group IVA Hydrides and Group VIIIA Tetrafluorides. A Partial Role Reversal for Elements 114 and 118|first=Clinton S.|last=Nash|doi=10.1021/jp982735k|year=1999|last2=Bursten|first2=Bruce E.}}</ref>) και μια τυπική κατάσταση συμπυκνωμένης φάσης <ref name=Nash/>. |
|||
== Δείτε επίσης == |
== Δείτε επίσης == |
||
Έκδοση από την 20:21, 1 Μαΐου 2013
| Ουνουνόκτιο | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ιστορία | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Πρόβλεψη | από τον Robert Smolańczuk το 1998 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ανακαλύφθηκε | από το Κοινό Ινστιτούτο Πυρηνικής Έρευνας και το Εθνικό Εργαστήριο Λώρενς της Λίβερμορ το 2002 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ταυτότητα του στοιχείου | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Όνομα, σύμβολο | Ουνουνόκτιο (Uuo) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ατομικός αριθμός (Ζ) | 118 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ομάδα, περίοδος, τομέας |
18 ,7, p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Σχετική ατομική μάζα (Ar) |
294 g/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ηλεκτρονική διαμόρφωση |
[Rn] 5f14 6d10 7s2 7p6
(προβλεπόμενη) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Αριθμός CAS | 54144-19-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ατομικές ιδιότητες | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ατομική ακτίνα | 152 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Κυριότεροι αριθμοί οξείδωσης |
0, 2, 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Φυσικά χαρακτηριστικά | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Σημείο βρασμού | 80 ± 30°C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Η κατάσταση αναφοράς είναι η πρότυπη κατάσταση (25°C, 1 Atm) εκτός αν σημειώνεται διαφορετικά | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ουνουνόκτιο είναι η προσωρινή ονομασία από την IUPAC [1] για το υπερβαρύ χημικό στοιχείο με τον ατομικό αριθμό 118 και προσωρινό σύμβολο το Uuo. Ανήκει στα στοιχεία του τομέα p και είναι το τελευταίο στοιχείο της έβδομης περιόδου. Είναι αυτή τη στιγμή το πρώτο συνθετικό μέλος της ομάδας 18. Έχει τον υψηλότερο ατομικό αριθμό και ατομική μάζα από οποιοδήποτε ανακαλυφθέν στοιχείο.
Το ραδιενεργό άτομο του ουνουνοκτίου είναι πολύ ασταθές, και από το 2002 μόνο τρία άτομα (ενδεχομένως τέσσερα) του 294Uuo έχουν εντοπιστεί.[2] Aυτό δεν επιτρέπει παρά πολύ περιορισμένο πειραματικό χαρακτηρισμό των ιδιοτήτων και των πιθανών ενώσεών του. Παρ' όλ' αυτά, θεωρητικοί υπολογισμοί έχουν καταλήξει σε αρκετές προβλέψεις, μεταξύ των οποίων και μερικές απροσδόκητες. Για παράδειγμα, εάν το ουνουνόκτιο είναι μέλος της ομάδας 18, μπορεί ενδεχομένως να μην είναι ευγενές αέριο, σε αντίθεση με όλα τα άλλα χημικά στοιχεία της δεκάτης εβδόμης ομάδας.[3] Στο παρελθόν πιστευόταν ότι είναι αέριο, τώρα όμως οι προβλέψεις το θέλουν, υπό κανονικές συνθήκες, στερεό.
Ιστορία
Ανεπιτυχείς προσπάθειες σύνθεσης
Στα τέλη του 1998 ο Πολωνός φυσικός Robert Smolańczuk δημοσίευσε υπολογισμούς σχετικά με την σύντηξη των ατομικών πυρήνων για τη σύνθεση βαρέων ατόμων, στα οποία συμπεριλαμβάνεται και το ουνουνόκτιο.[4] Σύμφωνα με τους υπολογισμούς του θα ήταν δυνατό να συντεθεί ουνουνόκτιο μέσω πυρηνικής σύντηξης μολύβδου με κρυπτό υπό εξαιρετικά ελεγχόμενες συνθήκες.[4]
Το 1999 ερευνητές στο Εθνικό Εργαστήριο του Λώρενς στο Μπέρκλεϋ έκαναν χρήση αυτών των προβλέψεων και ανακοίνωσαν την ανακάλυψη του ουνουνέξιου (τώρα Λιβερμόριο) και του ουνουνόκτιου, σε εργασία που δημοσιεύθηκε στο Physical Review Letters,[5] και πολύ σύντομα τα αποτελέσματα αναφέρθηκαν στο Science. Οι ερευνητές ανέφεραν ότι είχαν πραγματοποιήσει την αντίδραση:
Την επόμενη χρονιά όμως δημοσίευσαν αναίρεση της ανακοίνωσής τους, μια και ερευνητές σε άλλα εργαστήρια δεν μπόρεσαν να επαναλάβουν τα αποτελέσματα, ενώ και το ίδιο το εργαστήριο του Μπέρκλεϋ δεν μπόρεσε να τα επαναλάβει.[6] Τον Ιούλιο του 2002 ο διευθυντής του εργαστηρίου ανακοίνωσε ότι ο αρχικός ισχυρισμός της ανακάλυψης των δύο αυτών στοιχείων βασιζόταν σε δεδομένα που είχε χαλκεύσει ο κυριότερος συγγραφέας της ανακοίνωσης Victor Nunin.[7][8]
Αναφορές ανακάλυψης
Η πρώτη διπάσπαση ατόμων ουνουνοκτίου παρατηρήθηκε στο Κοινό Ινστιτούτο Πυρηνικής Έρευνας από τον Γιούρι Ογκανεσσιάν και την ομάδα του στην Ντούμπνα της Ρωσίας, το 2002 [9]. Στις 6 Οκτωβρίου του 2006, ερευνητές από το Κ.Ι.Π.Ε. (Κοινό Ινστιτούτο Πυρηνικής Έρευνας) και από το Εθνικό Εργαστήριο Λώρενς της Λίβερμορ στην Καλιφόρνια στις Η.Π.Α. δουλεύοντας στο Κ.Ι.Π.Ε. της Ντούμπνας, ανακοίνωσαν [10] ότι είχαν ανιχνεύσει έμμεσα συνολικά τρεις (ενδεχομένως τέσσερις) πυρήνες του ουνουνοκτίου-294 (ένα ή δύο το 2002 [11] και δύο παραπάνω το 2005) παραγόμενους μέσω σύγκρουσης ατόμων καλιφορνίου-249 και ιόντων ασβεστίου-48: [12][13][14][15][16]
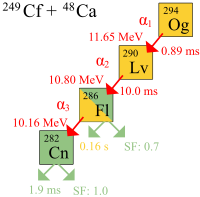
Το 2011, η IUPAC αξιολόγησε τα αποτελέσματα του 2006 της συνεργασίας Ντούμπνα-Λίβερμορ και κατέληξε: «Οι τρεις ενέργειες που αναφέρθηκαν για το ισότοπο Ζ = 118 έχει πολύ καλό εσωτερικὀ πλεονασμό, αλλά χωρίς άγκυρα οι γνωστοί πυρήνες δεν πληρούν τα κριτήρια για την ανακάλυψη" [17].
Λόγω της πολύ μικρής πιθανότητας αντίδρασης σύντηξης (η διατομή σύντηξης είναι ~ 0,3-0,6 pb = (3-6) × 10-41 m2), το πείραμα πήρε 4 μήνες και περιλάμβανε μια δόση δέσμης των 4 × 1019 ιόντων ασβεστίου που έπρεπε να να πυροβόλησουν στο στόχο από καλιφόρνιο για να παράξει το πρώτο καταγεγραμμένο συμβάν που πιστεύετο ότι ήταν η σύνθεση του ουνουνοκτίου [18]. Παρ' όλα αυτά, οι ερευνητές είναι πολύ σίγουροι ότι τα αποτελέσματα δεν είναι ψευδώς θετικά, δεδομένου ότι η πιθανότητα οι ανιχνεύσεις να ήταν τυχαία γεγονότα είναι λιγότερο από 0,001‰ [19].
Στα πειράματα, παρατηρήθηκε η άλφα-διάσπαση των τριών ατόμων ουνουνοκτίου παρατηρήθηκε. Μία τέταρτη αποσύνθεση με άμεση αυθόρμητη σχάση προτάθηκε επίσης. Μία διάρκεια ημιζωής 0,89 ms υπολογίστηκε: Το 294Uuo διασπάται σε 290Lv από την άλφα διάσπαση. Επειδή υπήρχαν μόνο τρεις πυρήνες, ο χρόνος ημισείας ζωής που προέρχεται από τις παρατηρούμενες διάρκειες ζωής έχει μία μεγάλη αβεβαιότητα: 0.89+1.07
−0.31 ms [10]
Η ταυτοποίηση των πυρήνων 294Uuo επαληθεύθηκε με χωριστή δημιουργία των υποτιθέμενων θυγατρικών πυρήνων 290Lv άμεσα μέσω ενός βομβαρδισμού του 245Cm με ιόντα 48Ca,
και με έλεγχο ότι η αποσύνθεση του 290Lv ταίριαζε με την αλυσίδα διάσπασης των πυρήνων του 294Uuo [10].
Σε ένα μοντέλο κβαντικής σήραγγας, η α διάσπαση του 294Uuo προβλεπόταν να είχε χρόνο ημιζωής είναι 0.66+0.23
−0.18ms [20] με την πειραματική τιμή Q που δημοσιεύθηκε το 2004 [21]. Ο υπολογισμός με τις θεωρητικές τιμές Q-από το μακροσκοπικό - μικροσκοπικό μοντέλο της Muntian-Hofman-Patyk-Sobiczewski δίνει κάπως χαμηλά, αλλά συγκρίσιμα αποτελέσματα [22].
Μετά την επιτυχία της απόκτησης ουνουνοκτίου, οι ερευνητές έχουν αρχίσει παρόμοια πειράματα με την ελπίδα της δημιουργίας ουνμπινιλίου (στοιχείο 120) από 58Fe και 244Pu [23]. Τα ισότοπα του ουνμπινιλίου αναμένεται να έχουν άλφα διάσπαση με ημίσεια ζωή της τάξης των μικροδευτερολέπτων [24][25].
Ονομασία
Από τη δεκαετία του 1960 το ουνουνόκτιο ήταν γνωστό ως εκα-emanation (emanation είναι το παλαιό όνομα για το ραδόνιο [26]. Το 1979 η IUPAC δημοσίευσε προτάσεις σύμφωνα με τις οποίες το στοιχείο θα ονομαζόταν ουνουνόκτιο, που θα ήταν μία συστηματική όνομασία του στοιχείου [27], ως σύμβολο κράτησης θέσης έως ότου η ανακάλυψη του στοιχείου επιβεβαιωθεί και η IUPAC αποφασίσει ένα όνομα.
Πριν από την ανάκληση, το 2002, οι ερευνητές από το Μπέρκλεϋ είχε την πρόθεση να αναφέρει το στοιχείο γκιόρσιο, ghiorsium (Gh), μετά από Albert Ghiorso (ηγετικό μέλος της ερευνητικής ομάδας) [28].
Οι Ρώσοι ερευνητές ανέφεραν τη σύνθεση τους το 2006. Το 2007, ο επικεφαλής του Ρωσικού Ινστιτούτου δήλωσε ότι η ομάδα εξέταζε δύο ονόματα για το νέο στοιχείο: φλυόριο, flyorium (Fy), προς τιμήν του Γκεόργκι Φλυόριοβ, ιδρυτή του ερευνητικού εργαστηρίου στην Ντούμπνα· και μοσκόβιο, moskovium (Mk), σε αναγνώριση της περιφέρειας της Μόσχας, όπου βρίσκεται η Ντούμπνα [29]. Ανέφερε επίσης ότι, αν και το στοιχείο ανακαλύφθηκε με αμερικανική συνεργασία, η οποία παρείχε το στόχο καλιφορνίου, το στοιχείο θα πρέπει δικαίως να ονομαστεί προς τιμήν της Ρωσίας από το Εργαστήριο Flerov των πυρηνικών αντιδράσεων στο Κ.Ι.Π.Ε. ήταν η μόνη εγκατάσταση στον κόσμο που θα μπορούσε να επιτευχθεί αυτό το αποτέλεσμα [30]. Αυτά τα ονόματα πρότεινε αργότερα για το στοιχείο 114 (φλερόβιο) και για το στοιχείο 116 (μοσκόβιο) [31]. Ωστόσο, η τελική ονομασία που προτάθηκε για το στοιχείο 116 ήταν αντί αυτού το λιβερμόριο [32].
Καμία ονομασία δεν έχει προταθεί ακόμα για το στοιχείο αφού καμία από τις απαιτήσεις για την ανακάλυψή του δεν έχουν γίνει ακόμα δεκτές από την IUPAC. Σύμφωνα με τις ισχύουσες κατευθυντήριες γραμμές της IUPAC, το απόλυτο όνομα για όλα τα νέα στοιχεία θα πρέπει να τελειώνει σε «-ιο», όχι «-ον», ακόμη κι αν αποδειχτεί ότι το ουνουνόκτιο είναι ένα ευγενές αέριο, που παραδοσιακά έχουν ονόματα που τελειώνουν σε «-ον» (με την εξαίρεση του ηλίου, το οποίο όταν ανακαλύφθηκε δεν ήταν γνωστό ότι είναι ένα ευγενές αέριο) [33].
Χαρακτηριστικά
Πυρηνική σταθερότητα και ισότοπα

Κύριο Άρθρο: Ισότοπα του Ουνουνοκτίου
Δείτε Επίσης: Νησί της σταθερότητας
Η σταθερότητα των πυρήνων μειώνεται σημαντικά με την αύξηση του ατομικού αριθμού μετά το πλουτώνιο, το βαρύτερο αρχέγονο χημικό στοιχείο, έτσι ώστε όλα τα ισότοπα με ατομικό αριθμό πάνω από 101 να αποσυντίθονται ραδιενεργώς με ημιζωή κάτω από μία ημέρα, με εξαίρεση το Ντούμπνιο-268. Δεν υπάρχουν στοιχεία με ατομικό αριθμό πάνω από 82 (μετά από τον μόλυβδο) που να έχουν σταθερά ισότοπα [34]. Παρ 'όλα αυτά, για τον λόγο ότι δεν είναι πολύ καλά κατανοητό ακόμα, υπάρχει μια ελαφρά αύξηση της πυρηνικής σταθερότητας γύρω από ατομικούς αριθμούς 110-114, η οποία οδηγεί στην εμφάνιση του τι είναι γνωστό στην πυρηνική φυσική ως το «νησί της σταθερότητας». Αυτή η ιδέα, που προτάθηκε στο Πανεπιστήμιο της Καλιφόρνια από τον καθηγητής Glenn Seaborg, εξηγεί γιατί τα βαρέα στοιχεία διαρκούν περισσότερο απ´ ότι είχε προβλεφθεί [35]. Το ουνουνόκτιο είναι ραδιενεργό και έχει ημιζωή που φαίνεται ότι είναι λιγότερη από ένα χιλιοστό του δευτερολέπτου. Παρ' όλα αυτά, εξακολουθεί να είναι μεγαλύτερη απ´ ότι κάποιες προβλεπόμενες τιμές [20][36], δίνοντας έτσι περαιτέρω υποστήριξη στην ιδέα της «νησίδας της σταθερότητας» [37].
Οι υπολογισμοί που χρησιμοποιούν μοντέλου κβαντικής διάνοιξης σηράγγων προβλέπει την ύπαρξη των διαφόρων ισοτόπων ουνουνοκτίου πλουσίων σε νετρόνια με άλφα-διάσπαση και ημιζωή κοντά στο 1 ms [24][25].
Οι θεωρητικοί υπολογισμοί που έγιναν για τις συνθετικές οδούς, και ο χρόνος ημιζωής άλλων ισοτόπων έχουν δείξει ότι κάποια θα μπορούσαν να είναι λίγο πιο σταθερά από το συντεθιμένο ισότοπο 294Uuo, πιθανότατα τα ισότοπα 293Uuo, 295Uuo, 296Uuo, 297Uuo, 298Uuo, 300Uuo και 302Uuo [20][38]. Από αυτά, το 297Uuo μπορεί να παρέχει τις καλύτερες πιθανότητες για την απόκτηση μακροβιότερων πυρήνων [20][38], και έτσι το επίκεντρο των μελλοντικών εργασιών θα μπορούσε να γίνει με αυτό το ισότοπο. Μερικά ισότοπα με πολλά περισσότερα νετρόνια, όπως ορισμένα που βρίσκονται γύρω από το 313Uuo θα μπορούσαν επίσης να παράσχουν μακροβιότερους πυρήνες [39].
Υπολογισμένες ατομικές και φυσικές ιδιότητες
Το Ουνουνόκτιο είναι μέλος της ομάδας 18, των στοιχείων μηδενικού σθένους. Τα μέλη της ομάδας αυτής είναι συνήθως αδρανή στις πιο κοινές χημικές αντιδράσεις (για παράδειγμα, η καύση), επειδή το εξωτερικό κέλυφος είναι εντελώς γεμάτο με οκτώ ηλεκτρόνια. Αυτό παράγει μια σταθερή, ελάχιστη ενεργειακή διαμόρφωση στην οποία τα εξωτερικά ηλεκτρόνια δεσμεύονται σφικτά [40]. Θεωρείται ότι ομοίως, το ουνουνόκτιο έχει κλειστά εξωτερικό κέλυφος στο οποίο το ηλεκτρονικό σθένος είναι τοποθετημένο σε 7s2 7p6 [3].
Κατά συνέπεια, ορισμένοι αναμένουν το ουνουνόκτιο να έχει παρόμοιες φυσικές και χημικές ιδιότητες με τα άλλα μέλη της ομάδας του, πιο στενή ομοιότητα με το ευγενές αέριο από πάνω του στον περιοδικό πίνακα, το ραδόνιο [41]. Ακολουθώντας την περιοδική τάση, το ουνουνόκτιο αναμένεται να είναι ελαφρώς πιο δραστικό από το ραδόνιο. Ωστόσο, θεωρητικοί υπολογισμοί έχουν δείξει ότι θα μπορούσε να είναι τόσο δραστικό, έτσι ώστε πιθανώς να μην μπορεί να θεωρηθεί ευγενές αέριο [42]. Πέραν του ότι μπορεί να είναι πολύ πιο δραστικό από το ραδόνιο, το ουνουνόκτιο μπορεί να είναι ακόμη πιο αντιδραστικό απ´ ότι τα στοιχεία φλερόβιο και κοπερνίκιο [3]. Ο λόγος για την εμφανή αύξηση της χημικής δραστικότητας σε σχέση με το ραδόνιο είναι μία ενεργητική αποσταθεροποίηση και μία ακτινική διαστολή του τελευταίου κατεχόμενου 7b υποφλοιού.[3][Σημ. 1] Ακριβέστερα, σημαντικές αλληλεπιδράσεις τροχιάς μεταξύ των ηλεκτρονίων 7p με τα αδρανή 7s2 ηλεκτρόνια, έχει ως αποτέλεσμα ένα δεύτερο κλείσιμο κελύφους στο φλερόβιο, και μια σημαντική μείωση στην σταθερότητα του κλειστού περιβλήματος του στοιχείου 118 [3]. Επίσης, έχει υπολογιστεί ότι το ουνουνόκτιο, σε αντίθεση με άλλα ευγενή αέρια, δεσμεύει ένα ηλεκτρόνιο με την απελευθέρωση της ενέργειας ή με άλλα λόγια, εμφανίζει θετική ηλεκτρονκή συγγένεια [43][44][Σημ. 2]
Το ουνουνόκτιο αναμένεται να έχει κατά πολύ ευρύτατη πολωσιμότητα, πιο πολύ από όλα τα προηγούμενα στοιχεία, και σχεδόν διπλάσια από του ραδονίου [3]. Σε παρέκταση από τα άλλα ευγενή αέρια, αναμένεται ότι το ουνουνόκτιο έχει ένα σημείο βρασμού μεταξύ 320 και 380 Κ (50 - 80°C) [3]. Αυτό είναι πολύ διαφορετικό από τις προηγούμενες εκτιμώμενες τιμές (263 K [45] ή 247 K [46]). Ακόμη και δεδομένων των μεγάλων αβεβαιοτήτων των υπολογισμών, φαίνεται εξαιρετικά απίθανο ότι το ουνουνόκτιο θα είναι αέριο υπό κανονικές συνθήκες [3][Σημ. 3], και καθώς το υγρό φάσμα των άλλων αερίων είναι πολύ περιορισμένο, μεταξύ 2 και 9 °Kelvin, το στοιχείο αυτό πρέπει να είναι στερεό υπό κανονικές συνθήκες. Αν το ουνουνόκτιο σχηματίζει αέριο κάτω από τυπικές συνθήκες, ωστόσο, θα ήταν ένα από τις πυκνότερες αέριες ουσίες υπό κανονικές συνθήκες (ακόμη και αν είναι μονοατομικό όπως και τα άλλα ευγενή αέρια).
Λόγω της τεράστιας πόλωσής του, το ουνουνόκτιο αναμένεται να έχει μια αφύσικα χαμηλή ενέργεια ιονισμού (παρόμοια με εκείνη του μολύβδου, η οποία είναι 70% περισσότερη από αυτήν του ραδονίου [47] και σημαντικά μικρότερη από εκείνη του φλεροβίου [48]) και μια τυπική κατάσταση συμπυκνωμένης φάσης [3].
Δείτε επίσης
Αναφορές και Σημειώσεις
- ↑ Η ακριβής φράση είναι "Ο λόγος για την εμφανή ενίσχυση της χημικής δραστηριότητας του στοιχείου 118 σε σχέση με το ραδόνιο είναι η ενεργειακή αποσταθεροποίηση και ακτινική διαστολή του κατεχόμενου 7b περιβλήματος."
- ↑ Παρ 'όλα αυτά, κβαντικές ηλεκτροδυναμικές διορθώσεις έχουν αποδείξει ότι είναι αρκετά σημαντικό για τη μείωση της συνάφειας με τη μείωση της δέσμευσης του ανιόντος Uuo- κατά 9%, επιβεβαιώνοντας έτσι τη σημασία αυτών των διορθώσεων στο βαρέα στοιχεία. Δείτε το Pyykkö.
- ↑ Είναι αμφίβολο εάν το όνομα της ομάδας "ευγενή αέρια" θα αλλάξει, εάν το ουνουνόκτιο φαίνεται να είναι μη πτητικό
Παραπομπές
- ↑ Wieser, M.E. (2006). «Atomic weights of the elements 2005 (IUPAC Technical Report)». Pure Appl. Chem. 78 (11): 2051–2066. doi:.
- ↑ «The Top 6 Physics Stories of 2006». Discover Magazine. 7 Ιανουαρίου 2007. Ανακτήθηκε στις 18 Ιανουαρίου 2008.
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 3,6 3,7 3,8 Nash, CS (2005). «Atomic and Molecular Properties of Elements 112, 114, and 118». Journal of Physical Chemistry A 109 (15): 3493–3500. doi:. PMID 16833687.
- ↑ 4,0 4,1 Smolanczuk, R. (1999). «Production mechanism of superheavy nuclei in cold fusion reactions». Physical Review C 59 (5): 2634–2639. doi:. Bibcode: 1999PhRvC..59.2634S.
- ↑ Ninov, Viktor; et al. (1999). «Observation of Superheavy Nuclei Produced in the Reaction of 86Kr with 208Pb». Physical Review Letters 83 (6): 1104–1107. doi:. Bibcode: 1999PhRvL..83.1104N.
- ↑ Public Affairs Department (2001-07-21). «Results of element 118 experiment retracted». Berkeley Lab. http://enews.lbl.gov/Science-Articles/Archive/118-retraction.html. Ανακτήθηκε στις 2008-01-18.
- ↑ Dalton, R (2002). «Misconduct: The stars who fell to Earth». Nature 420 (6917): 728–729. doi:. PMID 12490902.
- ↑ Element 118 disappears two years after it was discovered. Physicsworld.com. Retrieved on 2012-04-02.
- ↑ Oganessian, Yu. T. et al. (2002). «Results from the first 249Cf+48Ca experiment». JINR Communication (JINR, Dubna). http://www.jinr.ru/publish/Preprints/2002/287(D7-2002-287)e.pdf.
- ↑ 10,0 10,1 10,2 10,3 Oganessian, Yu. T.; et al. (2006). «Synthesis of the isotopes of elements 118 and 116 in the 249Cf and 245Cm + 48Ca fusion reactions». Physical Review C 74 (4): 044602. doi:. Bibcode: 2006PhRvC..74d4602O. Σφάλμα αναφοράς: Μη έγκυρη ετικέτα
<ref>• όνομα " full " ορίζεται πολλές φορές με διαφορετικό περιεχόμενο - ↑ Oganessian, Yu. T.· και άλλοι. (2002). «Element 118: results from the first 249Cf + 48Ca experiment». Communication of the Joint Institute for Nuclear Research.
- ↑ «Livermore scientists team with Russia to discover element 118». Livermore press release. 2006-12-03. https://www.llnl.gov/news/newsreleases/2006/NR-06-10-03.html. Ανακτήθηκε στις 2008-01-18.
- ↑ Oganessian, Yu. T. (2006). «Synthesis and decay properties of superheavy elements». Pure Appl. Chem. 78 (5): 889–904. doi:.
- ↑ Sanderson, K. (2006). «Heaviest element made – again». Nature News (Nature). doi:.
- ↑ Schewe, P. and Stein, B. (17 Οκτωβρίου 2006). «Elements 116 and 118 Are Discovered». Physics News Update. American Institute of Physics. Ανακτήθηκε στις 18 Ιανουαρίου 2008.
- ↑ Weiss, R. (17 Οκτωβρίου 2006). «Scientists Announce Creation of Atomic Element, the Heaviest Yet». Washington Post. Ανακτήθηκε στις 18 Ιανουαρίου 2008.
- ↑ Barber, Robert C.; Karol, Paul J.; Nakahara, Hiromichi; Vardaci, Emanuele; Vogt, Erich W. (2011). «Discovery of the elements with atomic numbers greater than or equal to 113 (IUPAC Technical Report)». Pure and Applied Chemistry 83 (7): 1. doi:.
- ↑ «Ununoctium». WebElements Periodic Table. Ανακτήθηκε στις 18 Ιανουαρίου 2008.
- ↑ «Element 118 Detected, With Confidence». Chemical and Engineering news. 17 Οκτωβρίου 2006. Ανακτήθηκε στις 18 Ιανουαρίου 2008.
I would say we're very confident.
- ↑ 20,0 20,1 20,2 20,3 Chowdhury, Roy P.; Samanta, C.; Basu, D. N. (2006). «α decay half-lives of new superheavy elements». Phys. Rev. C 73: 014612. doi:. Bibcode: 2006PhRvC..73a4612C.
- ↑ doi:10.1103/PhysRevC.70.064609
- ↑ Samanta, C.; Chowdhury, R. P.; Basu, D.N. (2007). «Predictions of alpha decay half-lives of heavy and superheavy elements». Nucl. Phys. A 789: 142–154. doi:. Bibcode: 2007NuPhA.789..142S.
- ↑ «A New Block on the Periodic Table» (PDF). Lawrence Livermore National Laboratory. April 2007. https://www.llnl.gov/str/April07/pdfs/04_07.4.pdf. Ανακτήθηκε στις 2008-01-18.
- ↑ 24,0 24,1 Chowdhury, Roy P.; Samanta, C.; Basu, D. N. (2008). «Search for long lived heaviest nuclei beyond the valley of stability». Physical Reviews C 77 (4): 044603. doi:. Bibcode: 2008PhRvC..77d4603C.
- ↑ 25,0 25,1 Chowdhury, R. P.; Samanta, C.; Basu, D.N. (2008). «Nuclear half-lives for α -radioactivity of elements with 100 ≤ Z ≤ 130». At. Data & Nucl. Data Tables 94 (6): 781–806. doi:. Bibcode: 2008ADNDT..94..781C.
- ↑ Grosse, A. V. (1965). «Some physical and chemical properties of element 118 (Eka-Em) and element 86 (Em)». Journal of Inorganic and Nuclear Chemistry (Elsevier Science Ltd.) 27 (3): 509–19. doi:.
- ↑ Chatt, J. (1979). «Recommendations for the Naming of Elements of Atomic Numbers Greater than 100». Pure Appl. Chem. 51 (2): 381–384. doi:.
- ↑ «Discovery of New Elements Makes Front Page News». Berkeley Lab Research Review Summer 1999. 1999. Ανακτήθηκε στις 18 Ιανουαρίου 2008.
- ↑ «New chemical elements discovered in Russia`s Science City». 12 Φεβρουαρίου 2007. Ανακτήθηκε στις 9 Φεβρουαρίου 2008.
- ↑ Yemel'yanova, Asya (17 Δεκεμβρίου 2006). «118-й элемент назовут по-русски (118th element will be named in Russian)» (στα Russian). vesti.ru. Ανακτήθηκε στις 18 Ιανουαρίου 2008.
- ↑ «Российские физики предложат назвать 116 химический элемент московием (Russian Physicians Will Suggest to Name Element 116 Moscovium)» (στα Russian). rian.ru. 2011. Ανακτήθηκε στις 8 Μαΐου 2011.
- ↑ «News: Start of the Name Approval Process for the Elements of Atomic Number 114 and 116». International Union of Pure and Applied Chemistry. Ανακτήθηκε στις 2 Δεκεμβρίου 2011.
- ↑ Koppenol, W. H. (2002). «Naming of new elements (IUPAC Recommendations 2002)». Pure and Applied Chemistry 74 (5): 787. doi:. http://media.iupac.org/publications/pac/2002/pdf/7405x0787.pdf.
- ↑ Marcillac, Pierre de; Noël Coron, Gérard Dambier, Jacques Leblanc, and Jean-Pierre Moalic (April 2003). «Experimental detection of α-particles from the radioactive decay of natural bismuth». Nature 422 (6934): 876–878. doi:. PMID 12712201. Bibcode: 2003Natur.422..876D.
- ↑ Considine, Glenn D.· Kulik, Peter H. (2002). Van Nostrand's scientific encyclopedia (9 έκδοση). Wiley-Interscience. ISBN 978-0-471-33230-5. OCLC 223349096.
- ↑ Oganessian, Yu. T. (2007). «Heaviest nuclei from 48Ca-induced reactions». Journal of Physics G: Nuclear and Particle Physics 34 (4): R165–R242. doi:. Bibcode: 2007JPhG...34..165O.
- ↑ «New Element Isolated Only Briefly». The Daily Californian. 18 Οκτωβρίου 2006. Ανακτήθηκε στις 18 Ιανουαρίου 2008. [νεκρός σύνδεσμος]
- ↑ 38,0 38,1 Royer, G.; Zbiri, K.; Bonilla, C. (2004). «Entrance channels and alpha decay half-lives of the heaviest elements». Nuclear Physics A 730 (3–4): 355–376. doi:. Bibcode: 2004NuPhA.730..355R.
- ↑ Duarte, S. B.; Tavares, O. A. P.; Gonçalves, M.; Rodríguez, O.; Guzmán, F.; Barbosa, T. N.; García, F.; Dimarco, A. (2004). «Half-life predictions for decay modes of superheavy nuclei». Journal of Physics G: Nuclear and Particle Physics 30 (10): 1487–1494. doi:. Bibcode: 2004JPhG...30.1487D.
- ↑ Bader, Richard F.W. «An Introduction to the Electronic Structure of Atoms and Molecules». McMaster University. Ανακτήθηκε στις 18 Ιανουαρίου 2008.
- ↑ «Ununoctium (Uuo) – Chemical properties, Health and Environmental effects». Lenntech. Αρχειοθετήθηκε από το πρωτότυπο στις 16 Ιανουαρίου 2008. Ανακτήθηκε στις 18 Ιανουαρίου 2008.
- ↑ Kaldor, Uzi· Wilson, Stephen (2003). Theoretical Chemistry and Physics of Heavy and Superheavy Elements. Springer. σελ. 105. ISBN 1-4020-1371-X.
- ↑ Goidenko, Igor; Labzowsky, Leonti; Eliav, Ephraim; Kaldor, Uzi; Pyykko¨, Pekka (2003). «QED corrections to the binding energy of the eka-radon (Z=118) negative ion». Physical Review A 67 (2): 020102(R). doi:. Bibcode: 2003PhRvA..67b0102G.
- ↑ Eliav, Ephraim; Kaldor, Uzi; Ishikawa, Y; Pyykkö, P (1996). «Element 118: The First Rare Gas with an Electron Affinity». Physical Review Letters 77 (27): 5350–5352. doi:. PMID 10062781. Bibcode: 1996PhRvL..77.5350E.
- ↑ Seaborg, Glenn Theodore (1994). Modern Alchemy. World Scientific. σελ. 172. ISBN 981-02-1440-5.
- ↑ Takahashi, N. (2002). «Boiling points of the superheavy elements 117 and 118». Journal of Radioanalytical and Nuclear Chemistry 251 (2): 299–301. doi:.
- ↑ Σφάλμα αναφοράς: Σφάλμα παραπομπής: Λανθασμένο
<ref>. Δεν υπάρχει κείμενο για τις παραπομπές με όνομαhydride. - ↑ Nash, Clinton S.; Bursten, Bruce E. (1999). «Spin-Orbit Effects, VSEPR Theory, and the Electronic Structures of Heavy and Superheavy Group IVA Hydrides and Group VIIIA Tetrafluorides. A Partial Role Reversal for Elements 114 and 118». Journal of Physical Chemistry A 1999 (3): 402–410. doi:.
Περαιτέρω ανάγνωση
- Eric Scerri, The Periodic Table, Its Story and Its Significance, Oxford University Press, New York, 2007.
Εξωτερικοί σύνδεσμοι
- Στοιχείο 118: πειράματα για την ανακάλυψη, archive of discoverers' official web page
- Chemistry Blog: Independent analysis of 118 claim
- Είναι στοιχειακό: Ουνουνόκτιο
- Ουνουνόκτιο στον Περιοδικό Πίνακα των μαγνητοσκοπήσεων (Πανεπιστήμιο του Νόττιγχαμ)
- On the Claims for Discovery of Elements 110, 111, 112, 114, 116, and 118 (IUPAC Technical Report)
- "Element 118, Βαρύτερο από ποτέ, αναφερόμενο για ένα χιλιοστό του δευτερολέπτου", NYTimes.com.
- WebElements: Ουνουνόκτιο
| Περιοδικός πίνακας | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | H | He | ||||||||||||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||||||||
| ||||||||||||||||||||||||||||||||||||||||||




