Μπακμίνστερφουλερένιο
Το Μπακμίνστερφουλερένιο είναι ένας τύπος φουλερενίου με τύπο C 60 . Έχει μια δομή συντηγμένου δακτυλίου που μοιάζει με κλουβί ( κολοβό εικοσάεδρο ) από είκοσι εξάγωνα και δώδεκα πεντάγωνα και μοιάζει με ποδόσφαιρο . Κάθε ένα από τα 60 άτομα άνθρακα του είναι συνδεδεμένο με τους τρεις γείτονές του.
Το Buckminsterfullerene είναι ένα μαύρο στερεό που διαλύεται σε διαλύτες υδρογονανθράκων για να παραχθεί ένα ιώδες διάλυμα. Η ένωση ανακαλύφθηκε το 1985 και έχει μελετηθεί εντατικά, αν και έχουν βρεθεί λίγες εφαρμογές στον πραγματικό κόσμο.
Ένα κοινό, συντομευμένο όνομα για το buckminsterfullerene είναι buckyballs. [1]
Περιστατικό[Επεξεργασία | επεξεργασία κώδικα]
Το Μπακμίνστερφουλερένιο είναι το πιο κοινό φυσικό φουλερένιο. Μικρές ποσότητες του μπορούν να βρεθούν στην αιθάλη . [2] [3]
Υπάρχει και στο διάστημα . Ουδέτερο C 60 έχει παρατηρηθεί σε πλανητικά νεφελώματα [4] και σε αρκετούς τύπους αστεριών . [5] Η ιονισμένη μορφή, C 60 +, έχει εντοπιστεί στο διαστρικό μέσο [6] όπου είναι η αιτία πολλών χαρακτηριστικών απορρόφησης γνωστών ως διάχυτες διαστρικές ζώνες στο εγγύς υπέρυθρο. [7]
Ιστορία[Επεξεργασία | επεξεργασία κώδικα]
Πρότυπο:Molecules detected in outer spaceΠρότυπο:Buckminster Fuller

Οι θεωρητικές προβλέψεις των μορίων Μπακμίνστερφουλερένιο εμφανίστηκαν στα τέλη της δεκαετίας του 1960 και στις αρχές της δεκαετίας του 1970. [8] [9] [10] [11] Δημιουργήθηκε για πρώτη φορά το 1984 από τους Eric Rohlfing, Donald Cox και Andrew Kaldor [11] [12] χρησιμοποιώντας ένα λέιζερ για την εξάτμιση του άνθρακα σε μια υπερηχητική δέσμη ηλίου, αν και η ομάδα δεν συνειδητοποίησε ότι είχε παραχθεί Μπακμίνστερφουλερένιο. Το 1985 η δουλειά τους επαναλήφθηκε από τους Harold Kroto, James R. Heath, Sean C. O'Brien, Robert Curl και Richard Smalley στο Πανεπιστήμιο Rice, οι οποίοι αναγνώρισαν τη δομή του C 60 ως buckminsterfullerene. [13]
Ταυτόχρονα, αλλά άσχετα με το έργο Kroto-Smalley, οι αστροφυσικοί εργάζονταν με φασματογράφους για να μελετήσουν τις υπέρυθρες εκπομπές από γιγάντια αστέρια κόκκινου άνθρακα. [14] [15] [16] Ο Smalley και η ομάδα μπόρεσαν να χρησιμοποιήσουν μια τεχνική εξάτμισης με λέιζερ για να δημιουργήσουν σμήνη άνθρακα που θα μπορούσαν ενδεχομένως να εκπέμπουν υπέρυθρες στο ίδιο μήκος κύματος που είχε εκπέμπει το κόκκινο αστέρι άνθρακα. [14] [17] Ως εκ τούτου, η έμπνευση ήρθε στον Smalley και στην ομάδα να χρησιμοποιήσουν την τεχνική λέιζερ στον γραφίτη για να δημιουργήσουν φουλερένια.
Χρησιμοποιώντας εξάτμιση γραφίτη με λέιζερ, η ομάδα Smalley βρήκε C n συστάδες (όπου n > 20 και ζυγά) από τα οποία τα πιο κοινά ήταν τα C 60 και C 70 . Ένας συμπαγής περιστρεφόμενος δίσκος γραφίτη χρησιμοποιήθηκε ως η επιφάνεια από την οποία εξατμίστηκε ο άνθρακας χρησιμοποιώντας μια δέσμη λέιζερ δημιουργώντας καυτό πλάσμα που στη συνέχεια διοχετεύθηκε μέσω ενός ρεύματος αερίου ηλίου υψηλής πυκνότητας. [18] Τα είδη άνθρακα στη συνέχεια ψύχθηκαν και ιονίστηκαν με αποτέλεσμα το σχηματισμό συστάδων. Τα σμήνη κυμαίνονταν σε μοριακές μάζες, αλλά οι Kroto και Smalley βρήκαν κυριαρχία σε ένα σύμπλεγμα C 60 που θα μπορούσε να ενισχυθεί περαιτέρω επιτρέποντας στο πλάσμα να αντιδράσει περισσότερο. Ανακάλυψαν επίσης ότι το C 60 είναι ένα μόριο που μοιάζει με κλουβί, ένα κανονικό κολοβωμένο εικοσάεδρο . [14] [18]
Οι Kroto, Curl και Smalley τιμήθηκαν με το Νόμπελ Χημείας το 1996 για τον ρόλο τους στην ανακάλυψη του buckminsterfullerene και της σχετικής κατηγορίας μορίων, των φουλερενίων . [8]
Τα πειραματικά στοιχεία, μια ισχυρή κορυφή στις 720 μονάδες ατομικής μάζας, έδειξε ότι σχηματιζόταν ένα μόριο άνθρακα με 60 άτομα άνθρακα, αλλά δεν παρείχε δομικές πληροφορίες. Η ερευνητική ομάδα κατέληξε στο συμπέρασμα μετά από πειράματα αντιδραστικότητας, ότι η πιο πιθανή δομή ήταν ένα σφαιροειδές μόριο. Η ιδέα εκλογικεύτηκε γρήγορα ως βάση μιας δομής κλειστού κλουβιού με εικοσαεδρική συμμετρία . Ο Κρότο ανέφερε τις γεωδαιτικές δομές θόλου του διάσημου μελλοντολόγο και εφευρέτη Buckminster Fuller ως επιρροές στην ονομασία αυτής της συγκεκριμένης ουσίας ως buckminsterfullerene. [8]
Το 1989 οι φυσικοί Wolfgang Krätschmer, Κωνσταντίνος Φωστηρόπουλος και Donald R. Huffman παρατήρησαν ασυνήθιστες οπτικές απορροφήσεις σε λεπτές μεμβράνες σκόνης άνθρακα (αιθάλη). Η αιθάλη είχε δημιουργηθεί με μια διεργασία τόξου μεταξύ δύο ηλεκτροδίων γραφίτη σε μια ατμόσφαιρα ηλίου όπου το υλικό του ηλεκτροδίου εξατμίζεται και συμπυκνώνεται σχηματίζοντας αιθάλη στην ατμόσφαιρα σβέσης. Μεταξύ άλλων χαρακτηριστικών, τα φάσματα IR της αιθάλης έδειξαν τέσσερις διακριτές ζώνες σε στενή συμφωνία με εκείνες που προτάθηκαν για το C 60 . [19]
Μια άλλη εργασία σχετικά με τον χαρακτηρισμό και την επαλήθευση της μοριακής δομής ακολούθησε την ίδια χρονιά (1990) από τα πειράματά τους σε λεπτή μεμβράνη, και λεπτομερώς επίσης την εκχύλιση ενός εξατμιζόμενου καθώς και διαλυτού σε βενζόλιο υλικού από την αιθάλη που δημιουργείται με τόξο. Αυτό το εκχύλισμα είχε ανάλυση TEM και κρυστάλλων ακτίνων Χ σύμφωνα με συστοιχίες σφαιρικών μορίων C 60, περίπου 1,0 nm σε διάμετρο van der Waals καθώς και την αναμενόμενη μοριακή μάζα 720 Da για C 60 (και 840 Da για C 70 ) στα φάσματα μάζας τους . [20] Η μέθοδος ήταν απλή και αποτελεσματική για την παρασκευή του υλικού σε ποσότητες σε γραμμάρια την ημέρα (1990), γεγονός που ενίσχυσε την έρευνα για το φουλλερένιο και εφαρμόζεται ακόμη και σήμερα για την εμπορική παραγωγή φουλερενίων.
Η ανακάλυψη πρακτικών διαδρομών προς το C 60 οδήγησε στην εξερεύνηση ενός νέου πεδίου χημείας που περιελάμβανε τη μελέτη των φουλερενίων.
Ετυμολογία[Επεξεργασία | επεξεργασία κώδικα]
Οι ανακαλύψεις του αλλοτρόπου ονόμασαν το νεοανακαλυφθέν μόριο από τον Buckminster Fuller, ο οποίος σχεδίασε πολλές γεωδαιτικές δομές θόλου που μοιάζουν με το C 60 και ο οποίος είχε πεθάνει το 1983, ένα έτος πριν από την ανακάλυψη. Αυτό είναι ελαφρώς παραπλανητικό, ωστόσο, καθώς οι γεωδαιτικοί θόλοι του Fuller κατασκευάζονται μόνο με περαιτέρω διαίρεση εξαγώνων ή πενταγώνων σε τρίγωνα, τα οποία στη συνέχεια παραμορφώνονται μετακινώντας κορυφές ακτινικά προς τα έξω για να ταιριάζουν στην επιφάνεια μιας σφαίρας. [21] Γεωμετρικά μιλώντας, το buckminsterfullerene είναι ένα φυσικό παράδειγμα πολυέδρου Goldberg . Ένα κοινό, συντομευμένο όνομα για το buckminsterfullerene είναι buckyballs. [22]
Σύνθεση[Επεξεργασία | επεξεργασία κώδικα]
Η αιθάλη παράγεται με αφαίρεση γραφίτη με λέιζερ ή με πυρόλυση αρωματικών υδρογονανθράκων . Τα φουλερένια εξάγονται από την αιθάλη με οργανικούς διαλύτες χρησιμοποιώντας έναν εκχυλιστή Soxhlet . [23] Αυτό το στάδιο δίνει ένα διάλυμα που περιέχει έως και 75% C60, καθώς και άλλα φουλλερένια. Αυτά τα κλάσματα διαχωρίζονται χρησιμοποιώντας χρωματογραφία . [24] Γενικά, τα φουλλερένια διαλύονται σε υδρογονάνθρακα ή αλογονωμένο υδρογονάνθρακα και διαχωρίζονται χρησιμοποιώντας στήλες αλουμίνας. [25]
Δομή[Επεξεργασία | επεξεργασία κώδικα]
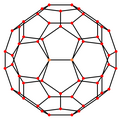
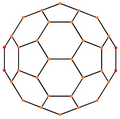
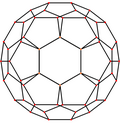
Το Buckminsterfullerene είναι ένα κολοβωμένο εικοσάεδρο με 60 κορυφές, 32 όψεις (20 εξάγωνα και 12 πεντάγωνα όπου κανένα πεντάγωνο δεν μοιράζεται κορυφή) και 90 άκρες (60 άκρες μεταξύ 5μελών & 6μελών δακτυλίων και 30 μοιρών άκρων 6-μελείς δακτύλιοι), με άτομο άνθρακα στις κορυφές κάθε πολυγώνου και δεσμό κατά μήκος κάθε ακμής πολυγώνου. Η διάμετρος van der Waals ενός C60</br> C60 μόριο είναι περίπου 1,01 νανόμετρα (nm). Η διάμετρος πυρήνα σε πυρήνα ενός C60</br> Το μόριο C60 είναι περίπου 0,71 nm. Το C60</br> Το μόριο C60 έχει δύο μήκη δεσμού. Οι δεσμοί δακτυλίου 6:6 (μεταξύ δύο εξαγώνων) μπορούν να θεωρηθούν " διπλοί δεσμοί " και είναι βραχύτεροι από τους δεσμούς 6:5 (μεταξύ ενός εξαγώνου και ενός πενταγώνου). Το μέσο μήκος δεσμού του είναι 0,14 nm. Κάθε άτομο άνθρακα στη δομή συνδέεται ομοιοπολικά με 3 άλλα. [26] Ένα άτομο άνθρακα στο C60</br> C60 μπορεί να αντικατασταθεί από ένα άτομο αζώτου ή βορίου που παράγει C59N</br> C59N ή C 59 B αντίστοιχα. [27]

Χημικές αντιδράσεις και ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
| Στο κέντρο από | Κορυφή | Ακρη </br> 5–6 |
Ακρη </br> 6–6 |
Πρόσωπο </br> Εξάγωνο |
Πρόσωπο </br> Πεντάγωνο |
|---|---|---|---|---|---|
| Εικόνα |  </img> </img>
|
 </img> </img>
|
 </img> </img>
|
 </img> </img>
|
 </img> </img>
|
| Προβολικός συμμετρία |
[2] | [2] | [2] | [6] | [10] |
Για ένα διάστημα το buckminsterfullerene ήταν το μεγαλύτερο γνωστό μόριο που παρατηρήθηκε ότι παρουσίαζε δυαδικότητα κύματος-σωματιδίου . θεωρητικά κάθε αντικείμενο εμφανίζει αυτή τη συμπεριφορά. [28] Το 2020 το μόριο της βαφής φθαλοκυανίνη παρουσίασε τη δυαδικότητα που αποδίδεται πιο διάσημα στο φως, τα ηλεκτρόνια και άλλα μικρά σωματίδια και μόρια. [29]
Διάλυμα[Επεξεργασία | επεξεργασία κώδικα]

| Διαλυτικό μέσο | Διαλυτότητα </br> (g/L) |
|---|---|
| 1-χλωροναφθαλίνη | 51 |
| 1-μεθυλοναφθαλίνιο | 33 |
| 1,2-διχλωροβενζόλιο | 24 |
| 1,2,4-τριμεθυλοβενζόλιο | 18 |
| τετραϋδροναφθαλίνη | 16 |
| δισουλφίδιο του άνθρακα | 8 |
| 1,2,3-τριβρωμοπροπάνιο | 8 |
| ξυλόλιο | 5 |
| βρωμομορφικό | 5 |
| cumene | 4 |
| τολουΐνη | 3 |
| βενζόλιο | 1.5 |
| τετραχλωράνθρακα | 0,447 |
| χλωροφόρμιο | 0,25 |
| n - εξάνιο | 0,046 |
| κυκλοεξάνιο | 0,035 |
| τετραϋδροφουράνιο | 0,006 |
| ακετονιτρίλιο | 0,004 |
| μεθανόλη | 0,00004 |
| νερό | 1.3 × 10 −11 |
| πεντάνιο | 0,004 |
| οκτάνιο | 0,025 |
| ισοοκτάνιο | 0,026 |
| δεκανός | 0,070 |
| δωδεκάνησα | 0,091 |
| τετραδεκάνιο | 0,126 |
| διοξάνη | 0,0041 |
| μεσιτιλένιο | 0,997 |
| διχλωρομεθάνιο | 0,254 |
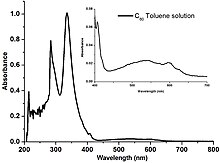
Τα φουλερένια είναι ελάχιστα διαλυτά σε αρωματικούς διαλύτες και δισουλφίδιο του άνθρακα, αλλά αδιάλυτα στο νερό. Τα διαλύματα καθαρού C 60 έχουν βαθύ μωβ χρώμα που αφήνει ένα καφέ υπόλειμμα κατά την εξάτμιση. Ο λόγος για αυτήν την αλλαγή χρώματος είναι το σχετικά στενό ενεργειακό πλάτος της ζώνης των μοριακών επιπέδων που είναι υπεύθυνες για την απορρόφηση του πράσινου φωτός από μεμονωμένα μόρια C 60 . Έτσι μεμονωμένα μόρια εκπέμπουν λίγο μπλε και κόκκινο φως με αποτέλεσμα ένα μωβ χρώμα. Κατά την ξήρανση, η διαμοριακή αλληλεπίδραση έχει ως αποτέλεσμα την επικάλυψη και τη διεύρυνση των ζωνών ενέργειας, εξαλείφοντας έτσι τη μετάδοση του μπλε φωτός και προκαλώντας την αλλαγή του χρώματος του μωβ σε καφέ. [14]
Το C60 κρυσταλλίζεται με ορισμένα διαλύτρια στο πλέγμα ("σολβές"). Για παράδειγμα, η κρυσταλλοποίηση του C60 από λύση βενζίνης παράγει τρικλινικά κρύσταλλα με τον τύπο C60·4C6H6. Όπως και άλλες σολβές, αυτή απελευθερώνει ευκολότερα βενζίνη για να δώσει το συνήθες κυβικό κέντρο προσώπου C60. Κρύσταλλα μεγέθους χιλιοστομέτρων του C60 και του C70 μπορούν να καλλιεργηθούν από λύση τόσο για σολβές όσο και για καθαρά φουλερένια.
Στερεός[Επεξεργασία | επεξεργασία κώδικα]


Στο στερεό buckminsterfullerene, τα μόρια C 60 υιοθετούν το μοτίβο fcc ( πρόσωπο-κεντρικό κυβικό ). Αρχίζουν να περιστρέφονται με περίπου -20 °C. Αυτή η αλλαγή σχετίζεται με μια μετάβαση φάσης πρώτης τάξης σε μια δομή fcc και μια μικρή, αλλά απότομη αύξηση στη σταθερά του πλέγματος από 1,411 σε 1,4154 nm. [33]
Το στερεό C60 είναι τόσο μαλακό όσο και ο γραφίτης, αλλά όταν συμπιεστεί σε λιγότερο από 70% του όγκου του, μετατρέπεται σε μια υπερσκληρή μορφή διαμαντιού (δείτε συγκεντρωμένο νανοκορδόνι διαμαντιού). Τα φιλμ και οι λύσεις C60 έχουν ισχυρές μη γραμμικές οπτικές ιδιότητες· ειδικότερα, η οπτική απορρόφησή τους αυξάνεται με την ένταση του φωτός (κορεσμένη απορρόφηση).
Το C60 δημιουργεί ένα καφετί στερεό με ένα οπτικό όριο απορρόφησης στα περίπου 1,6 eV. Είναι ένα n-τύπου ημιαγωγός με χαμηλή ενεργοποίηση της ενέργειας από 0,1 έως 0,3 eV· αυτή η αγωγιμότητα αποδίδεται σε ελλείψεις που σχετίζονται με το εσωτερικό ή το οξυγόνο. Το κυβικό κέντρο προσώπου (Fcc) C60 περιέχει κενά στις οκταεδρικές και τετραεδρικές θέσεις του, τα οποία είναι αρκετά μεγάλα (0,6 και 0,2 nm αντίστοιχα) για να φιλοξενήσουν ακαθαρσίες. Όταν αλκαλικά μέταλλα προστίθενται σε αυτά τα κενά, το C60 μετατρέπεται από ημιαγωγό σε αγωγό ή ακόμη και υπεραγωγό.
Οξειδοαναγωγή (αντιδράσεις μεταφοράς ηλεκτρονίων)[Επεξεργασία | επεξεργασία κώδικα]
Υδρογόνωση[Επεξεργασία | επεξεργασία κώδικα]
Το C 60 παρουσιάζει έναν μικρό βαθμό αρωματικού χαρακτήρα, αλλά εξακολουθεί να αντανακλά εντοπισμένους διπλούς και απλούς χαρακτήρες δεσμού C–C. Επομένως, το C 60 μπορεί να υποβληθεί σε προσθήκη με υδρογόνο για να δώσει πολυϋδροφουλλερένια. Το C 60 υφίσταται επίσης αναγωγή Birch . Για παράδειγμα, το C 60 αντιδρά με λίθιο σε υγρή αμμωνία, ακολουθούμενο από τριτ -βουτανόλη για να δώσει ένα μείγμα πολυϋδροφουλλερενίων όπως C 60 H 18, C 60 H 32, C 60 H 36, με το C 60 H 32 να είναι το κυρίαρχο προϊόν. Αυτό το μείγμα πολυϋδροφουλλερενίων μπορεί να επαναοξειδωθεί με 2,3-διχλωρο-5,6-δικυανο-1,4-βενζοκινόνη για να δώσει ξανά C60 .
Υπάρχει μια μέθοδος επιλεκτικής υδρογόνωσης. Η αντίδραση του C 60 με 9,9', 10, 10'-διυδροανθρακένιο υπό τις ίδιες συνθήκες, ανάλογα με το χρόνο αντίδρασης, δίνει C 60 H 32 και C 60 H 18 αντίστοιχα και επιλεκτικά. [34]
Το C 60 μπορεί να υδρογονωθεί, υποδηλώνοντας ότι ένα τροποποιημένο buckminsterfullerene που ονομάζεται οργανομεταλλικά buckyballs (OBBs) θα μπορούσε να γίνει όχημα για αποθήκευση υδρογόνου σε υψηλή πυκνότητα, θερμοκρασία δωματίου, πίεση περιβάλλοντος. Αυτά τα OBB δημιουργούνται δεσμεύοντας άτομα ενός μετάλλου μετάπτωσης (TM) σε C 60 ή C 48 B 12 και στη συνέχεια συνδέοντας πολλά άτομα υδρογόνου σε αυτό το άτομο TM, διασκορπίζοντάς τα ομοιόμορφα σε όλο το εσωτερικό του οργανομεταλλικού buckyball. Η μελέτη διαπίστωσε ότι η θεωρητική ποσότητα H 2 που μπορεί να ανακτηθεί από το OBB σε πίεση περιβάλλοντος πλησιάζει το 9 wt<span typeof="mw:Entity" id="mwAhA"> </span>%, ένα κλάσμα μάζας που έχει χαρακτηριστεί ως βέλτιστο για καύσιμο υδρογόνου από το Υπουργείο Ενέργειας των ΗΠΑ . </link>[ <span title="This claim needs references to reliable sources. (January 2022)">απαιτείται παραπομπή</span> ]
Προσθήκη φθορίου, χλωρίου και βρωμίου συμβαίνει για το C60 . Τα άτομα φθορίου είναι αρκετά μικρά για προσθήκη 1,2, ενώ το Cl 2 και το Br 2 προστίθενται σε απομακρυσμένα άτομα C λόγω στερικών παραγόντων . Για παράδειγμα, στα C 60 Br 8 και C 60 Br 24, τα άτομα Br βρίσκονται σε θέσεις 1,3 ή 1,4 το ένα ως προς το άλλο. Κάτω από διάφορες συνθήκες μπορεί να παραχθεί ένας τεράστιος αριθμός αλογονωμένων παραγώγων του C 60, μερικά με εξαιρετική εκλεκτικότητα σε ένα ή δύο ισομερή έναντι των άλλων πιθανών. Η προσθήκη φθορίου και χλωρίου συνήθως οδηγεί σε ισοπέδωση του πλαισίου C 60 σε ένα μόριο σε σχήμα τυμπάνου. [34]
Προσθήκη ατόμων οξυγόνου[Επεξεργασία | επεξεργασία κώδικα]
Τα διαλύματα του C 60 μπορούν να οξυγονωθούν στο εποξείδιο C 60 O. Η οζονοποίηση του C 60 σε 1,2-ξυλόλιο στους 257 K δίνει ένα ενδιάμεσο όζον C 60 O 3, το οποίο μπορεί να αποσυντεθεί σε 2 μορφές C 60 O. Αποσύνθεση του C 60 O 3 στο 296 Το K δίνει το εποξείδιο, αλλά η φωτόλυση δίνει ένα προϊόν στο οποίο το άτομο Ο γεφυρώνει μια ακμή 5,6. [34]

Η αντίδραση Diels-Alder χρησιμοποιείται συνήθως για τη λειτουργικότητα του C 60 . Η αντίδραση του C 60 με κατάλληλο υποκατεστημένο διένιο δίνει το αντίστοιχο προϊόν προσθήκης.
Η αντίδραση Diels-Alder μεταξύ C 60 και 3,6-διαρυλ-1,2,4,5-τετραζινών αποδίδει C62 . Το C 62 έχει τη δομή στην οποία ένας τετραμελής δακτύλιος περιβάλλεται από τέσσερις εξαμελείς δακτυλίους.

Τα μόρια C 60 μπορούν επίσης να συζευχθούν μέσω μιας [2+2] κυκλοπροσθήκης, δίνοντας την ένωση σε σχήμα αλτήρα C 120 . Η σύζευξη επιτυγχάνεται με δονούμενη άλεση υψηλής ταχύτητας C 60 με καταλυτική ποσότητα KCN . Η αντίδραση είναι αναστρέψιμη καθώς το C 120 διασπάται σε δύο μόρια C 60 όταν θερμαίνεται στους 450 K (177 °C; 350 °F) . Υπό υψηλή πίεση και θερμοκρασία, η επαναλαμβανόμενη [2+2] κυκλοπροσθήκη μεταξύ του C 60 οδηγεί σε πολυμερισμένες αλυσίδες φουλερενίου και δίκτυα. Αυτά τα πολυμερή παραμένουν σταθερά στην πίεση και τη θερμοκρασία περιβάλλοντος μόλις σχηματιστούν, και έχουν εξαιρετικά ενδιαφέρουσες ηλεκτρονικές και μαγνητικές ιδιότητες, όπως είναι σιδηρομαγνητικά πάνω από τη θερμοκρασία δωματίου. [34]
Αντιδράσεις ελεύθερων ριζών[Επεξεργασία | επεξεργασία κώδικα]
Αντιδράσεις του C 60 με ελεύθερες ρίζες συμβαίνουν εύκολα. Όταν το C 60 αναμιγνύεται με ένα δισουλφιδικό RSSR, η ρίζα C 60 SR• σχηματίζεται αυθόρμητα κατά την ακτινοβόληση του μείγματος.
Η σταθερότητα του είδους ρίζας C 60 Y • εξαρτάται σε μεγάλο βαθμό από τους στερικούς παράγοντες του Y. Όταν το τριτ -βουτυλο αλογονίδιο φωτολύεται και αφήνεται να αντιδράσει με το C 60, σχηματίζεται ένας αναστρέψιμος δεσμός C–C μεταξύ των κλωβών: [34]

Κυκλοπροπανίωση (αντίδραση Bingel)[Επεξεργασία | επεξεργασία κώδικα]
Η κυκλοπροπανίωση ( αντίδραση Bingel ) είναι μια άλλη κοινή μέθοδος για την ενεργοποίηση του C 60 . Η κυκλοπροπανοποίηση του C 60 συμβαίνει κυρίως στη διασταύρωση 2 εξαγώνων λόγω στερικών παραγόντων.
Η πρώτη κυκλοπροπανοποίηση διεξήχθη με επεξεργασία του β-βρωμομηλονικού με C60 παρουσία μιας βάσης. Η κυκλοπροπανίωση συμβαίνει επίσης εύκολα με τα διαζομεθάνια . Για παράδειγμα, το διφαινυλοδιαζομεθάνιο αντιδρά εύκολα με το C 60 για να δώσει την ένωση C 61 Ph 2 . [34] Το παράγωγο μεθυλεστέρα του φαινυλο- <sub id="mwAnc">C61</sub> -βουτυρικού οξέος που παρασκευάζεται μέσω κυκλοπροπανίωσης έχει μελετηθεί για χρήση σε οργανικά ηλιακά κύτταρα .
Αντιδράσεις οξειδοαναγωγής – ανιόντα και κατιόντα C 60[Επεξεργασία | επεξεργασία κώδικα]
C 60 ανιόντα[Επεξεργασία | επεξεργασία κώδικα]
Το LUMO στο C 60 είναι τριπλά εκφυλισμένο, με το διαχωρισμό HOMO – LUMO σχετικά μικρό. Αυτό το μικρό κενό υποδηλώνει ότι η μείωση του C 60 θα πρέπει να συμβεί σε ήπια δυναμικά που οδηγούν σε ανιόντα φουλεριδίου, [C 60 ] n - ( n = 1–6). Τα μεσαία δυναμικά της αναγωγής 1 ηλεκτρονίου του buckminsterfullerene και των ανιόντων του δίνονται στον παρακάτω πίνακα:
| Δυνατότητα μείωσης C 60 στα 213 κ | |
|---|---|
| Ημιαντίδραση | E ° (V) |
| C 60 + e − ⇌ C− 60</br> C− 60 |
−0,169 |
| C− 60</br> C− 60 + e − ⇌ C2− 60</br> C2− 60 |
−0,599 |
| C2− 60</br> C2− 60 + e − ⇌ C3− 60</br> C3− 60 |
−1,129 |
| C3− 60</br> C3− 60 + e − ⇌ C4− 60</br> C4− 60 |
−1.579 |
| C4− 60</br> C4− 60 + e − ⇌ C5− 60</br> C5− 60 |
−2.069 |
| C5− 60</br> C5− 60 + e − ⇌ C6− 60</br> C6− 60 |
−2.479 |
Το C 60 σχηματίζει μια ποικιλία συμπλεγμάτων μεταφοράς φορτίου, για παράδειγμα με τετρακις(διμεθυλαμινο)αιθυλένιο :
- C 60 + C 2 (NMe 2 ) 4 → [C 2 (NMe 2 ) 4 ] + [C 60 ] −
Αυτό το άλας παρουσιάζει σιδηρομαγνητισμό στο 16 Κ.
C 60 κατιόντα[Επεξεργασία | επεξεργασία κώδικα]
Το C 60 οξειδώνεται με δυσκολία. Τρεις αναστρέψιμες διεργασίες οξείδωσης έχουν παρατηρηθεί χρησιμοποιώντας κυκλική βολταμετρία με εξαιρετικά ξηρό μεθυλενοχλωρίδιο και έναν υποστηρικτικό ηλεκτρολύτη με εξαιρετικά υψηλή αντίσταση στην οξείδωση και χαμηλή πυρηνοφιλικότητα, όπως [ n Bu 4 N] [AsF 6 ]. [35]
| Δυνατότητες μείωσης οξείδωσης C 60 σε χαμηλές θερμοκρασίες | |
|---|---|
| Ημιαντίδραση | E ° (V) |
| C 60 ⇌ C+ 60</br> C+ 60 |
+1,27 |
| C+ 60</br> C+ 60 ⇌ C2+ 60</br> C2+ 60 |
+1,71 |
| C2+ 60</br> C2+ 60 ⇌ C3+ 60</br> C3+ 60 |
+2.14 |
Συμπλέγματα μετάλλων[Επεξεργασία | επεξεργασία κώδικα]
Το C 60 σχηματίζει σύμπλοκα παρόμοια με τα πιο κοινά αλκένια. Έχουν αναφερθεί σύμπλοκα μολυβδαίνιο, βολφράμιο, πλατίνα, παλλάδιο, ιρίδιο και τιτάνιο . Τα είδη πεντακαρβονυλίου παράγονται με φωτοχημικές αντιδράσεις .
- M(CO) 6 + C 60 → M( η 2 -C 60 )(CO) 5 + CO (M = Mo, W)
Στην περίπτωση του συμπλόκου πλατίνας, το ασταθές πρόσδεμα αιθυλενίου είναι η αποχωρούσα ομάδα σε μια θερμική αντίδραση:
- Pt( η 2 -C 2 H 4 )(PPh 3 ) 2 + C 60 → Pt( η 2 -C 60 )(PPh 3 ) 2 + C 2 H 4
- ( η 5 - Cp ) 2 Ti( η 2 -(CH 3 ) 3 SiC≡CSi(CH 3 ) 3 ) + C 60 → ( η 5 -Cp) 2 Ti( η 2 -C 60 ) + (CH 3 ) 3 SiC≡CSi(CH 3 ) 3
Συντονικά ακόρεστες πρόδρομες ουσίες, όπως το σύμπλεγμα Vaska, για προϊόντα προσθήκης με C 60 :
- trans -Ir(CO)Cl(PPh 3 ) 2 + C 60 → Ir(CO)Cl( η 2 -C 60 )(PPh 3 ) 2
Ένα τέτοιο σύμπλοκο ιριδίου, [Ir( η 2 -C 60 )(CO)Cl(Ph 2 CH 2 C 6 H 4 OCH 2 Ph) 2 ] έχει παρασκευαστεί όπου το μεταλλικό κέντρο προβάλλει δύο πλούσιους σε ηλεκτρόνια «βραχίονες» που αγκαλιάζουν ο καλεσμένος του C 60 . [36]
Ενδοεδρικά φουλλερένια[Επεξεργασία | επεξεργασία κώδικα]
Πρότυπο:Buckminster FullerΆτομα μετάλλου ή ορισμένα μικρά μόρια όπως το Η 2 και το ευγενές αέριο μπορούν να εγκλωβιστούν εντός του κλωβού C 60 . Αυτά τα ενδοεδρικά φουλλερένια συνήθως συντίθενται με ντόπινγκ στα άτομα μετάλλου σε έναν αντιδραστήρα τόξου ή με εξάτμιση λέιζερ. Αυτές οι μέθοδοι δίνουν χαμηλές αποδόσεις ενδοεδρικών φουλλερενίων και μια καλύτερη μέθοδος περιλαμβάνει το άνοιγμα του κλωβού, τη συσκευασία στα άτομα ή τα μόρια και το κλείσιμο του ανοίγματος χρησιμοποιώντας ορισμένες οργανικές αντιδράσεις . Αυτή η μέθοδος, ωστόσο, είναι ακόμη ανώριμη και μόνο λίγα είδη έχουν συντεθεί με αυτόν τον τρόπο. [37]
Τα ενδοεδρικά φουλλερένια παρουσιάζουν διακριτές και ενδιαφέρουσες χημικές ιδιότητες που μπορεί να είναι εντελώς διαφορετικές από το ενθυλακωμένο άτομο ή μόριο, καθώς και από το ίδιο το φουλερένιο. Τα ενθυλακωμένα άτομα έχουν αποδειχθεί ότι εκτελούν κυκλικές κινήσεις μέσα στον κλωβό C 60 και η κίνησή τους έχει παρακολουθηθεί χρησιμοποιώντας φασματοσκοπία NMR . [36]
Δυνητικές εφαρμογές στην τεχνολογία[Επεξεργασία | επεξεργασία κώδικα]
Οι ιδιότητες οπτικής απορρόφησης του C 60 ταιριάζουν με το ηλιακό φάσμα με τρόπο που υποδηλώνει ότι τα φιλμ με βάση το C 60 θα μπορούσαν να είναι χρήσιμα για φωτοβολταϊκές εφαρμογές. Λόγω της υψηλής ηλεκτρονικής του συγγένειας [38] είναι ένας από τους πιο κοινούς δέκτες ηλεκτρονίων που χρησιμοποιούνται σε ηλιακά κύτταρα με βάση δότη/δέκτη. Αποδόσεις μετατροπής έως και 5,7% έχουν αναφερθεί σε κύτταρα πολυμερούς C 60 . [39]
Κατάποση και κίνδυνοι[Επεξεργασία | επεξεργασία κώδικα]
Το C 60 είναι ευαίσθητο στο φως, επομένως αφήνοντας το C 60 κάτω από έκθεση στο φως προκαλείται υποβάθμιση του, καθιστώντας επικίνδυνο. Η κατάποση διαλυμάτων C 60 που έχουν εκτεθεί στο φως μπορεί να οδηγήσει σε ανάπτυξη καρκίνου (όγκων). [40] [41] Επομένως, η διαχείριση των προϊόντων C 60 για ανθρώπινη κατάποση απαιτεί προληπτικά μέτρα [41] όπως: επεξεργασία σε πολύ σκοτεινά περιβάλλοντα, περιτύλιξη σε μπουκάλια μεγάλης αδιαφάνειας και αποθήκευση σε σκοτεινά μέρη, και άλλα όπως η κατανάλωση σε συνθήκες χαμηλού φωτισμού και η χρήση ετικετών για προειδοποιήστε για τα προβλήματα με το φως.
Διαλύματα C 60 διαλυμένα σε ελαιόλαδο ή νερό, εφόσον διατηρούνται από το φως, έχουν βρεθεί μη τοξικά για τα τρωκτικά. [42]
Διαφορετικά, μια μελέτη διαπίστωσε ότι το C 60 παραμένει στο σώμα για μεγαλύτερο χρονικό διάστημα από το συνηθισμένο, ειδικά στο ήπαρ, όπου τείνει να συσσωρεύεται, και επομένως έχει τη δυνατότητα να προκαλέσει επιβλαβείς επιπτώσεις στην υγεία. [43]
Λάδια με C60 και κινδύνους[Επεξεργασία | επεξεργασία κώδικα]
Ένα πείραμα το 2011-2012 χορήγησε διάλυμα C 60 σε ελαιόλαδο σε αρουραίους, επιτυγχάνοντας σημαντική παράταση της διάρκειας ζωής τους. [42] Έκτοτε, πολλά έλαια με C 60 έχουν πωληθεί ως αντιοξειδωτικά προϊόντα, αλλά δεν αποφεύγεται το πρόβλημα της ευαισθησίας τους στο φως, που μπορεί να τα κάνει τοξικά. Μια μεταγενέστερη έρευνα επιβεβαίωσε ότι η έκθεση στο φως αποδομεί διαλύματα C 60 σε λάδι, καθιστώντας το τοξικό και οδηγώντας σε «μαζική» αύξηση του κινδύνου ανάπτυξης καρκίνου (όγκων) μετά την κατανάλωσή του. [40] [41]
Για να αποφευχθεί η υποβάθμιση από την επίδραση του φωτός, τα λάδια C 60 πρέπει να παρασκευάζονται σε πολύ σκοτεινά περιβάλλοντα, να φυλάσσονται σε μπουκάλια μεγάλης αδιαφάνειας και να διατηρούνται στο σκοτάδι, να καταναλώνονται σε συνθήκες χαμηλού φωτισμού και να συνοδεύονται από ετικέτες που προειδοποιούν για τους κινδύνους του φωτός για το C. 60 . [41]
Μερικοί παραγωγοί μπόρεσαν να διαλύσουν το C 60 στο νερό για να αποφύγουν πιθανά προβλήματα με τα λάδια, αλλά αυτό δεν θα προστατεύει το C 60 από το φως, επομένως απαιτούνται οι ίδιες προφυλάξεις.
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ The AZo Journal of Materials Online.
- ↑ Howard, Jack B.; McKinnon, J. Thomas; Makarovsky, Yakov; Lafleur, Arthur L.; Johnson, M. Elaine (1991). «Fullerenes C60 and C70 in flames». Nature 352 (6331): 139–141. doi:. PMID 2067575. Bibcode: 1991Natur.352..139H.
- ↑ Howard, J; Lafleur, A; Makarovsky, Y; Mitra, S; Pope, C; Yadav, T (1992). «Fullerenes synthesis in combustion». Carbon 30 (8): 1183–1201. doi:. https://archive.org/details/sim_carbon_1992_30_8/page/1183.
- ↑ Cami, J.; Bernard-Salas, J.; Peeters, E.; Malek, S. E. (2010). «Detection of C60 and C70 in a Young Planetary Nebula». Science 329 (5996): 1180–1182. doi:. PMID 20651118. Bibcode: 2010Sci...329.1180C.
- ↑ Roberts, Kyle R. G.; Smith, Keith T.; Sarre, Peter J. (2012). «Detection of C60 in embedded young stellar objects, a Herbig Ae/Be star and an unusual post-asymptotic giant branch star». Monthly Notices of the Royal Astronomical Society 421 (4): 3277–3285. doi:. Bibcode: 2012MNRAS.421.3277R.
- ↑ Berné, O.; Mulas, G.; Joblin, C. (2013). «Interstellar C60+». Astronomy & Astrophysics 550: L4. doi:. Bibcode: 2013A&A...550L...4B.
- ↑ Maier, J. P.; Gerlich, D.; Holz, M.; Campbell, E. K. (July 2015). «Laboratory confirmation of C60+ as the carrier of two diffuse interstellar bands». Nature 523 (7560): 322–323. doi:. ISSN 1476-4687. PMID 26178962. Bibcode: 2015Natur.523..322C.
- ↑ 8,0 8,1 8,2 Katz, 363
- ↑ Osawa, E. (1970).
- ↑ Jones, David E. H. (1966). «Hollow molecules». New Scientist (32): 245.
- ↑ 11,0 11,1 Smalley, Richard E. (1997-07-01). «Discovering the fullerenes». Reviews of Modern Physics 69 (3): 723–730. doi:.
- ↑ Rohlfing, Eric A; Cox, D. M; Kaldor, A (1984). «Production and characterization of supersonic carbon cluster beams». Journal of Chemical Physics 81 (7): 3322. doi:. Bibcode: 1984JChPh..81.3322R.
- ↑ Kroto, H. W.; Heath, J. R.; O'Brien, S. C.; Curl, R. F.; Smalley, R. E. (1985). «C60: Buckminsterfullerene». Nature 318 (6042): 162–163. doi:. Bibcode: 1985Natur.318..162K.
- ↑ 14,0 14,1 14,2 14,3 Dresselhaus, M. S.· Dresselhaus, G. (1996). Science of Fullerenes and Carbon Nanotubes. San Diego, CA: Academic Press. ISBN 978-012-221820-0.
- ↑ Herbig, E. (1975). «The diffuse interstellar bands. IV – the region 4400-6850 A». Astrophys. J. 196: 129. doi:. Bibcode: 1975ApJ...196..129H.
- ↑ Leger, A.; d'Hendecourt, L.; Verstraete, L.; Schmidt, W. (1988). «Remarkable candidates for the carrier of the diffuse interstellar bands: C60+ and other polyhedral carbon ions». Astron. Astrophys. 203 (1): 145. Bibcode: 1988A&A...203..145L. https://archive.org/details/sim_astronomy-and-astrophysics_1988-09_203_1/page/145.
- ↑ Dietz, T. G.; Duncan, M. A.; Powers, D. E.; Smalley, R. E. (1981). «Laser production of supersonic metal cluster beams». J. Chem. Phys. 74 (11): 6511. doi:. Bibcode: 1981JChPh..74.6511D.
- ↑ 18,0 18,1 Kroto, H. W.; Health, J. R.; O'Brien, S. C.; Curl, R. F.; Smalley, R. E. (1985). «C60: Buckminsterfullerene». Nature 318 (6042): 162–163. doi:. Bibcode: 1985Natur.318..162K.
- ↑ Krätschmer, W. (1990). «The infrared and ultraviolet absorption spectra of laboratory-produced carbon dust: evidence for the presence of the C60 molecule». Chemical Physics Letters 170 (2–3): 167–170. doi:. Bibcode: 1990CPL...170..167K.
- ↑ Krätschmer, W.; Lamb, Lowell D.; Fostiropoulos, K.; Huffman, Donald R. (1990). «Solid C60: A new form of carbon». Nature 347 (6291): 354–358. doi:. Bibcode: 1990Natur.347..354K.
- ↑ «What is a geodesic dome?». R. Buckminster Fuller Collection: Architect, Systems Theorist, Designer, and Inventor. Stanford University. 6 Απριλίου 2017. Αρχειοθετήθηκε από το πρωτότυπο στις 12 Ιανουαρίου 2020. Ανακτήθηκε στις 10 Ιουνίου 2019.
- ↑ The AZo Journal of Materials Online.
- ↑ Girolami, G. S.· Rauchfuss, T. B. (1999). Synthesis and Teknique in Inorganic Chemistry. Mill Valley, CA: University Science Books. ISBN 978-0935702484.
- ↑ Katz, 369–370
- ↑ Shriver· Atkins (2010). Inorganic Chemistry (Fifth έκδοση). New York: W. H. Freeman. σελ. 356. ISBN 978-0-19-923617-6.
- ↑ Katz, 364
- ↑ Katz, 374
- ↑ Arndt, Markus; Nairz, Olaf; Vos-Andreae, Julian; Keller, Claudia; Van Der Zouw, Gerbrand; Zeilinger, Anton (1999). «Wave–particle duality of C60». Nature 401 (6754): 680–682. doi:. PMID 18494170. Bibcode: 1999Natur.401..680A.
- ↑ Lee, Chris (2020-07-21). «Wave-particle duality in action—big molecules surf on their own waves». Ars Technica. Αρχειοθετήθηκε από το πρωτότυπο στις 2021-09-26. https://web.archive.org/web/20210926144828/https://arstechnica.com/science/2020/07/wave-particle-duality-in-action-big-molecules-surf-on-their-own-waves/. Ανακτήθηκε στις 26 September 2021.
- ↑ Beck, Mihály T.; Mándi, Géza (1997). «Solubility of C60». Fullerenes, Nanotubes and Carbon Nanostructures 5 (2): 291–310. doi:.
- ↑ Bezmel'nitsyn, V. N.; Eletskii, A. V.; Okun', M. V. (1998). «Fullerenes in solutions». Physics-Uspekhi 41 (11): 1091–1114. doi:. Bibcode: 1998PhyU...41.1091B.
- ↑ Ruoff, R. S.; Tse, Doris S.; Malhotra, Ripudaman; Lorents, Donald C. (1993). «Solubility of fullerene (C60) in a variety of solvents». Journal of Physical Chemistry 97 (13): 3379–3383. doi:.
- ↑ Katz, 372
- ↑ 34,0 34,1 34,2 34,3 34,4 34,5 Catherine E. Housecroft· Alan G. Sharpe (2008). «Chapter 14: The group 14 elements». Inorganic Chemistry (3rd έκδοση). Pearson. ISBN 978-0-13-175553-6.
- ↑ Reed, Christopher A.; Bolskar, Robert D. (2000). «Discrete Fulleride Anions and Fullerenium Cations». Chemical Reviews 100 (3): 1075–1120. doi:. PMID 11749258. https://escholarship.org/uc/item/60b5m71z.
- ↑ 36,0 36,1 Jonathan W. Steed· Jerry L. Atwood (2009). Supramolecular Chemistry (2nd έκδοση). Wiley. ISBN 978-0-470-51233-3.
- ↑ Rodríguez-Fortea, Antonio; Balch, Alan L.; Poblet, Josep M. (2011). «Endohedral metallofullerenes: a unique host–guest association». Chem. Soc. Rev. 40 (7): 3551–3563. doi:. PMID 21505658.
- ↑ Ryuichi, Mitsumoto (1998). «Electronic Structures and Chemical Bonding of Fluorinated Fullerenes Studied». J. Phys. Chem. A 102 (3): 552–560. doi:. Bibcode: 1998JPCA..102..552M.
- ↑ Shang, Yuchen; Liu, Zhaodong; Dong, Jiajun; Yao, Mingguang; Yang, Zhenxing; Li, Quanjun; Zhai, Chunguang; Shen, Fangren και άλλοι. (November 2021). «Ultrahard bulk amorphous carbon from collapsed fullerene». Nature 599 (7886): 599–604. doi:. ISSN 1476-4687. PMID 34819685. Bibcode: 2021Natur.599..599S. Αρχειοθετήθηκε από το πρωτότυπο στις 2021-11-26. https://web.archive.org/web/20211126104002/https://www.nature.com/articles/s41586-021-03882-9. Ανακτήθηκε στις 2021-11-26.
- ↑ 40,0 40,1 Grohn, Kristopher J. «Comp grad leads research». WeyburnReview. Αρχειοθετήθηκε από το πρωτότυπο στις 17 Απριλίου 2021. Ανακτήθηκε στις 17 Απριλίου 2021.
- ↑ 41,0 41,1 41,2 41,3 Grohn, Kristopher J.· και άλλοι. «C60 in olive oil causes light-dependent toxicity» (PDF). Αρχειοθετήθηκε (PDF) από το πρωτότυπο στις 15 Απριλίου 2021. Ανακτήθηκε στις 15 Απριλίου 2021.
- ↑ 42,0 42,1 Baati, Tarek; Moussa, Fathi (June 2012). «The prolongation of the lifespan of rats by repeated oral administration of [60]fullerene». Biomaterials 33 (19): 4936–4946. doi:. PMID 22498298.
- ↑ Shipkowski, K. A.; Sanders, J. M.; McDonald, J. D.; Walker, N. J.; Waidyanatha, S. (2019). «Disposition of fullerene C60 in rats following intratracheal or intravenous administration». Xenobiotica; the Fate of Foreign Compounds in Biological Systems 49 (9): 1078–1085. doi:. PMID 30257131.
Βιβλιογραφικές αναφορές[Επεξεργασία | επεξεργασία κώδικα]
- Katz, E. A. (2006). «Fullerene Thin Films as Photovoltaic Material». Στο: Sōga, Tetsuo. Nanostructured materials for solar energy conversion. Elsevier. σελίδες 361–443. ISBN 978-0-444-52844-5.
Περαιτέρω ανάγνωση[Επεξεργασία | επεξεργασία κώδικα]
- Kroto, H. W.; Heath, J. R.; O'Brien, S. C.; Curl, R. F.; Smalley, R. E. (November 1985). «C60: Buckminsterfullerene». Nature 318 (14): 162–163. doi:. Bibcode: 1985Natur.318..162K. – describing the original discovery of C60
- Hebgen, Peter; Goel, Anish; Howard, Jack B.; Rainey, Lenore C.; Vander Sande, John B. (2000). «Fullerenes and Nanostructures in Diffusion Flames». Proceedings of the Combustion Institute 28: 1397–1404. doi:. http://web.mit.edu/anish/www/Peter-JBH.pdf. – report describing the synthesis of C60 with combustion research published in 2000 at the 28th International Symposium on Combustion
Εξωτερικοί σύνδεσμοι[Επεξεργασία | επεξεργασία κώδικα]
- Η ιστορία της ανακάλυψης της δεκαετίας του '60 πραγματοποιήθηκε από το Τμήμα Χημείας του Πανεπιστημίου του Μπρίστολ
- Μια σύντομη επισκόπηση του buckminsterfullerene που περιγράφεται από το Πανεπιστήμιο του Wisconsin-Madison
- Μια αναφορά από το Ming Kai College που περιγράφει λεπτομερώς τις ιδιότητες του buckminsterfullerene
- Η εργασία των Donald R. Huffman και Wolfgang Krätschmer σχετικά με τη σύνθεση του C 60 στο Nature που δημοσιεύτηκε το 1990
- Μια λεπτομερής περιγραφή του C 60 από το Εθνικό Εργαστήριο Oak Ridge
- Ένα άρθρο σχετικά με το buckminsterfullerene στο Connexions Science Encyclopaedia
- Εκτεταμένα στατιστικά δεδομένα που συγκεντρώθηκαν από το Πανεπιστήμιο του Sussex σχετικά με τις αριθμητικές ποσοτικές ιδιότητες του buckminsterfullerene
- Μια διαδικτυακή πύλη αφιερωμένη στο buckminsterfullerene, που συντάχθηκε και υποστηρίζεται από το Πανεπιστήμιο του Μπρίστολ
- Μια άλλη διαδικτυακή πύλη αφιερωμένη στο buckminsterfullerene, που συντάχθηκε και υποστηρίζεται από το Τμήμα Χημείας του Πανεπιστημίου του Μπρίστολ
- Ένα σύντομο άρθρο αφιερωμένο εξ ολοκλήρου στο C 60 και την ανακάλυψη, τη δομή, την παραγωγή, τις ιδιότητες και τις εφαρμογές του
- Το πλήρες άρθρο της Αμερικανικής Χημικής Εταιρείας για το buckminsterfullerene
- Buckminsterfullerene στον περιοδικό πίνακα των βίντεο (Πανεπιστήμιο του Nottingham).mw-parser-output .reflist{font-size:90%;margin-bottom:0.5em;list-style-type:decimal}.mw-parser-output .reflist .references{font-size:100%;margin-bottom:0;list-style-type:inherit}.mw-parser-output .reflist-columns-2{column-width:30em}.mw-parser-output .reflist-columns-3{column-width:25em}.mw-parser-output .reflist-columns{margin-top:0.3em}.mw-parser-output .reflist-columns ol{margin-top:0}.mw-parser-output .reflist-columns li{page-break-inside:avoid;break-inside:avoid-column}.mw-parser-output .reflist-upper-alpha{list-style-type:upper-alpha}.mw-parser-output .reflist-upper-roman{list-style-type:upper-roman}.mw-parser-output .reflist-lower-alpha{list-style-type:lower-alpha}.mw-parser-output .reflist-lower-greek{list-style-type:lower-greek}.mw-parser-output .reflist-lower-roman{list-style-type:lower-roman}
|

