Διοξάνιο
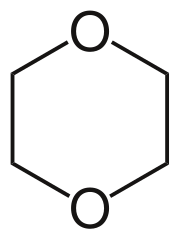
Το διοξάνιο είναι μία ετεροκυκλική οργανική ένωση, που ταξινομείται ως αιθέρας.[1] Είναι ένα άχρωμο υγρό χημικό, με ελαφρά γλυκιά οσμή, παρόμοια με αυτή του διαιθυλαιθέρα. Η ένωση συχνά ονομάζεται απλώς διοξάνιο ή χημικώς ορθά 1,4- διοξάνιο επειδή τα άλλα ισομερή του (ήτοι: 1,2- διοξάνιο και 1,3- διοξάνιο) σπάνια συναντώνται.
Το διοξάνιο χρησιμοποιείται ως διαλύτης για ποικίλες πρακτικές εφαρμογές, καθώς και στο εργαστήριο, όπως και ως σταθεροποιητής για τη μεταφορά χλωριωμένων υδρογονανθράκων σε δοχεία αλουμινίου.[2]
Σύνθεση[Επεξεργασία | επεξεργασία κώδικα]
Το διοξάνιο παράγεται με αφυδάτωση μιας γλυκόλης, συγκεκριμένα με καταλυόμενη από οξύ αφυδάτωση της διαιθυλενογλυκόλης, η οποία με τη σειρά της λαμβάνεται από υδρόλυση του αιθυλενοξειδίου.
Δομή[Επεξεργασία | επεξεργασία κώδικα]
Το μόριο του διοξανίου είναι κεντροσυμμετρικό, που σημαίνει ότι έχει στερεοχημική δομή (chair) καρέκλας, χαρακτηριστική των συγγενών του κυκλοεξανίου. Ωστόσο, το μόριο είναι δομικώς εύκαμπτο και η διαμόρφωση του υλοποιείται εύκολα, λ.χ. στη χηλικοποίηση κατιόντων μετάλλων. Το διοξάνιο ομοιάζει με έναν μικρότερο αιθέρα κορώνας με μόνο δύο μονάδες αιθυλενοξυλίου.
Χρήσεις[Επεξεργασία | επεξεργασία κώδικα]
Για τη μεταφορά του τριχλωροαιθανίου[Επεξεργασία | επεξεργασία κώδικα]
Στη δεκαετία του 1980, το μεγαλύτερο μέρος του παραγόμενου διοξανίου χρησιμοποιήθηκε ως σταθεροποιητής για το χημικό συστατικό, 1,1,1-τριχλωροαιθάνιο για αποθήκευση και μεταφορά μέσα σε δοχεία αλουμινίου.[3]
Ως διαλύτης[Επεξεργασία | επεξεργασία κώδικα]
Το διοξάνιο χρησιμοποιείται σε ποικίλες εφαρμογές ως ευέλικτος απρωτικός διαλύτης, π.χ. για μελάνια, κόλλες και εστέρες κυτταρίνης.[4] Δύναται να αντικαθιστά το τετραϋδροφουράνιο (THF) σε ορισμένες διεργασίες, λόγω της χαμηλότερης τοξικότητας που έχει και του υψηλότερου σημείου βρασμού (δηλ. 101°C, έναντι 66°C του THF).
Φασματοσκοπία[Επεξεργασία | επεξεργασία κώδικα]
Το διοξάνιο χρησιμοποιείται ως πρότυπος διαλύτης για τη φασματοσκοπία NMR σε οξείδιο του δευτερίου.[5]
Τοξικολογία[Επεξεργασία | επεξεργασία κώδικα]
Το διοξάνιο έχει μέση θανατηφόρο δόση -LD50- 5170 mg/kg σε αρουραίους.[3] Είναι χημικό ερεθιστικό για τους οφθαλμούς και την αναπνευστική οδό.[6] Η έκθεση μπορεί να προκαλέσει βλάβη στο κεντρικό νευρικό σύστημα, στο ήπαρ και στα νεφρά.[7] Ταξινομείται από το Εθνικό Πρόγραμμα Τοξικολογίας ως "αναμενόμενα καρκινογόνος ουσία για τον άνθρωπο".[8] Επίσης ταξινομείται από την διεθνή ένωση IARC ως πιθανώς καρκινογόνος για τον άνθρωπο επειδή είναι γνωστό καρκινογόνο σε άλλα ζώα (θηλαστικά).[9]
Ισομερή[Επεξεργασία | επεξεργασία κώδικα]
Το διοξάνιο έχει τυπικά τρία διαφορετικά ισομερή, εκ των οποίων μόνον το ένα είναι το συχνά απαντώμενο.
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ «Dioxane». PubChem. Ανακτήθηκε στις 17 Νοεμβρίου 2021.
- ↑ Wisconsin Department of Health Services (2013) 1,4-Dioxane Fact Sheet Αρχειοθετήθηκε 2020-10-16 στο Wayback Machine..
- ↑ 3,0 3,1 Surprenant, Kenneth S. (2000). «Dioxane». Dioxane in Ullmann's Encyclopedia of Industrial Chemistry. ISBN 978-3527306732.
- ↑ Klaus Weissermel, Hans-Jürgen Arpe (2003) "Industrial Organic Chemistry".
- ↑ Shimizu, A.; Ikeguchi, M.; Sugai, S. (1994). «Appropriateness of DSS and TSP as internal references for 1H NMR studies of molten globule proteins in aqueous media». Journal of Biomolecular NMR 4 (6): 859–62. doi:. PMID 22911388.
- ↑ «Εκατοντάδες καλλυντικά για παιδιά ύποπτα για καρκινογόνες ουσίες». Think Organic. 8 Ιανουαρίου 2020. Ανακτήθηκε στις 17 Νοεμβρίου 2021.
- ↑ «International Chemical Safety Card». National Institute for Occupational Safety and Health. Αρχειοθετήθηκε από το πρωτότυπο στις 29 Απριλίου 2005. Ανακτήθηκε στις 6 Φεβρουαρίου 2006.
- ↑ «12th Report on Carcinogens». United States Department of Health and Human Services' National Toxicology Program. Αρχειοθετήθηκε από το πρωτότυπο στις 14 Ιουλίου 2014. Ανακτήθηκε στις 11 Ιουλίου 2014.
- ↑ IARC Monographs Volume 71 (PDF). International Agency for Research on Cancer. Ανακτήθηκε στις 11 Ιουλίου 2014.
