Σύνδρομο Στίβενς-Τζόνσον
| Σύνδρομο Στίβενς-Τζόνσον | |
|---|---|
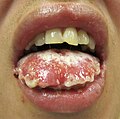
 Βλάβες προσώπου σε άτομο σύνδρομο Στίβενς-Τζόνσον | |
| Ειδικότητα | δερματολογία |
| Ταξινόμηση | |
| ICD-10 | L51.1 |
| ICD-9 | 695.13 |
| OMIM | 608579 |
| DiseasesDB | 4450 |
| MedlinePlus | 000851 |
| eMedicine | emerg/555 derm/405 |
| MeSH | D013262 |
Το σύνδρομο Στίβενς-Τζόνσον (SJS) είναι τύπος σοβαρής δερματικής αντίδρασης.[1] Μαζί με την τοξική επιδερμική νεκρόλυση (TEN) και τo σύνδρομο Στίβενς-Τζόνσον/τοξική επιδερμική νεκρόλυση (SJS/TEN), σχηματίζει ένα φάσμα ασθενειών, με το SJS να είναι το λιγότερο σοβαρό.[1][2] Το πολύμορφο ερύθημα θεωρείται γενικά ξεχωριστή πάθηση.[3] Τα πρώιμα συμπτώματα του SJS περιλαμβάνουν πυρετό και συμπτώματα που μοιάζουν με γρίπη.[1] Λίγες μέρες αργότερα, το δέρμα αρχίζει να βγάζει φουσκάλες και να ξεφλουδίζει, σχηματίζοντας επώδυνες εκτεθειμένες περιοχές.[1] Οι βλεννογόνοι, όπως το στόμα, εμπλέκονται επίσης τυπικά.[1] Οι επιπλοκές περιλαμβάνουν αφυδάτωση, σήψη, πνευμονία και πολυοργανική ανεπάρκεια.[1]
Η πιο κοινή αιτία είναι ορισμένα φάρμακα όπως η λαμοτριγίνη, η καρβαμαζεπίνη, η αλλοπουρινόλη, τα αντιβιοτικά σουλφοναμίδης και η νεβιραπίνη.[1] Άλλες αιτίες μπορεί να περιλαμβάνουν λοιμώξεις όπως το Mycoplasma pneumoniae και ο κυτταρομεγαλοϊός ή η αιτία μπορεί να παραμείνει άγνωστη.[4][1] Οι παράγοντες κινδύνου περιλαμβάνουν το HIV/AIDS και τον συστηματικό ερυθηματώδη λύκο.[1]
Η διάγνωση του συνδρόμου Στίβενς-Τζόνσον βασίζεται σε προσβολή λιγότερο από το 10% του δέρματος.[4] Αναφέρεται ως TEN όταν εμπλέκεται περισσότερο από το 30% του δέρματος και θεωρείται ενδιάμεση μορφή όταν εμπλέκεται το 10-30%.[2] Οι νόσοι SJS/TEN πιστεύεται ότι ακολουθούν μηχανισμό υπερευαισθησίας τύπου IV.[5] Περιλαμβάνεται επίσης με φαρμακευτική αντίδραση με ηωσινοφιλία και συστηματικά συμπτώματα (σύνδρομο DRESS), οξεία γενικευμένη εξανθηματώδη φλυκταίνωση (AGEP) και τοξική επιδερμική νεκρόλυση σε μια ομάδα καταστάσεων γνωστών σοβαρών δερματικών ανεπιθύμητων αντιδράσεων (SCAR).[6]
Η θεραπεία λαμβάνει χώρα συνήθως στο νοσοκομείο, όπως σε μονάδα εγκαυμάτων ή μονάδα εντατικής θεραπείας.[4] Η αντιμετώπιση περιλαμβάνει απομάκρυνση της αιτίας, παυσίπονα, αντιισταμινικά, αντιβιοτικά, ενδοφλέβιες ανοσοσφαιρίνες ή κορτικοστεροειδή.[4] Μαζί με το TEN, το SJS επηρεάζει 1 έως 2 άτομα ανά εκατομμύριο ετησίως.[1] Η τυπική έναρξη είναι κάτω των 30 ετών.[4] Το δέρμα αναγεννάται συνήθως σε διάστημα δύο έως τριών εβδομάδων. Ωστόσο, η πλήρης αποκατάσταση μπορεί να διαρκέσει μήνες.[4] Συνολικά, ο κίνδυνος θανάτου λόγω SJS είναι 5 έως 10%.[1][7]
Σημεία και συμπτώματα
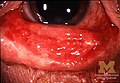
[Επεξεργασία | επεξεργασία κώδικα]Το SJS συνήθως ξεκινά με πυρετό, πονόλαιμο και κόπωση, που συνήθως διαγιγνώσκεται εσφαλμένα και επομένως αντιμετωπίζεται με αντιβιοτικά. Τα SJS, SJS/TEN και TEN συχνά προαναγγέλλονται από πυρετό, πονόλαιμο, βήχα και κάψιμο στα μάτια για 1 έως 3 ημέρες.[8] Οι ασθενείς με αυτές τις διαταραχές συχνά εμφανίζουν καυστικό πόνο στο δέρμα τους στην αρχή της νόσου.[8] Έλκη και άλλες βλάβες αρχίζουν να εμφανίζονται στους βλεννογόνους, σχεδόν πάντα στο στόμα και τα χείλη, αλλά και στις περιοχές των γεννητικών οργάνων και του πρωκτού. Αυτά στο στόμα είναι συνήθως εξαιρετικά επώδυνα και μειώνουν την ικανότητα του ασθενούς να φάει ή να πιει. Η επιπεφυκίτιδα εμφανίζεται στο 30% περίπου των παιδιών που αναπτύσσουν SJS.[9] Ένα εξάνθημα με τη μορφή στρογγυλών βλαβών διαμέτρου περίπου δύο εκατοστών στο πρόσωπο, τον κορμό, τα χέρια και τα πόδια και τα πέλματα, αλλά συνήθως όχι στο τριχωτό της κεφαλής.[10]
-
Απολέπιση του βλεννογόνου σε άτομο με σύνδρομο Στίβενς-Τζόνσον
-
Φλεγμονή και ξεφλούδισμα των χειλιών - με πληγές που εμφανίζονται στη γλώσσα και τους βλεννογόνους στο SJS
-
Επιπεφυκίτιδα σε SJS
Αιτίες
[Επεξεργασία | επεξεργασία κώδικα]Το σύνδρομο Στίβενς-Τζόνσον πιστεύεται ότι προκύπτει από διαταραχή του ανοσοποιητικού συστήματος.[10] Η ανοσολογική αντίδραση μπορεί να προκληθεί από φάρμακα ή λοιμώξεις.[11] Γενετικοί παράγοντες σχετίζονται με προδιάθεση για SJS.[12] Η αιτία του SJS είναι άγνωστη στο ένα τέταρτο έως το μισό των περιπτώσεων.[12] Τα SJS, SJS/TEN και TEN θεωρούνται μια μεμονωμένη ασθένεια με κοινά αίτια και μηχανισμούς.[8]
Άτομα που εκφράζουν συγκεκριμένους ορότυπους (δηλαδή γενετικά αλληλόμορφα) ανθρώπινου αντιγόνου λευκοκυττάρων (π.χ. HLA), υποδοχείς Τ-λεμφοκυττάρων ή διακυμάνσεις της αποτελεσματικότητάς τους να απορροφούν, να διανέμουν στους ιστούς, να μεταβολίζουν ή να εκκρίνουν ένα φάρμακο έχουν προδιάθεση για ανάπτυξη του SJS.
Φάρμακα
[Επεξεργασία | επεξεργασία κώδικα]Αν και το SJS μπορεί να προκληθεί από ιογενείς λοιμώξεις και κακοήθειες, η κύρια αιτία είναι τα φάρμακα.[13] Η κύρια αιτία φαίνεται να είναι η χρήση αντιβιοτικών, ιδιαίτερα θειικών φαρμάκων.[12][14] Μεταξύ 100 και 200 διαφορετικών φαρμάκων μπορεί να σχετίζονται με το SJS.[15] Δεν υπάρχει αξιόπιστο τεστ που να αποδεικνύει τη σχέση μεταξύ ενός συγκεκριμένου φαρμάκου και του SJS για κάθε περίπτωση.[13] Ο προσδιορισμός του φαρμάκου που προκαλείται βασίζεται στο χρονικό διάστημα μεταξύ της πρώτης χρήσης του φαρμάκου και της έναρξης της δερματικής αντίδρασης. Φάρμακα που διακόπτονται περισσότερο από ένα μήνα πριν από την εμφάνιση των βλεννογονοδερματικών φυσικών ευρημάτων είναι πολύ απίθανο να προκαλέσουν SJS και TEN.[8] Το SJS και το TEN ξεκινούν συχνότερα μεταξύ 4 και 28 ημερών μετά τη χορήγηση του ένοχου φαρμάκου.[8] Ένας δημοσιευμένος αλγόριθμος (ALDEN) για την αξιολόγηση της αιτιότητας των φαρμάκων παρέχει δομημένη βοήθεια στον εντοπισμό του υπεύθυνου φαρμάκου.[13][16]
SJS μπορεί να προκληθεί από τα φάρμακα ριβαροξαμπάνη, [17] βανκομυκίνη, αλλοπουρινόλη, βαλπροϊκό άλας, λεβοφλοξασίνη, δικλοφενάκη, ετραβιρίνη, ισοτρετινοΐνη, φλουκοναζόλη,[18] βαλδεκοξίμπη, σιταγλιπτίνη, οσελταμιξινοξινοξίνη, πενθολαμιβιρίνη, βαζουλταμιβιρίνη, βαζουλταμιβιρίνη, βαζουλταμιβιρίνη , βαζουλταμιβιρίνη, μοδαφινίλη,[19] λαμοτριγίνη, νεβιραπίνη,[8] πυριμεθαμίνη, ιβουπροφαίνη,[20] αιθοσουξιμίδη, καρβαμαζεπίνη, βουπροπιόνη, τελαπρεβίρη[21] και νυστατίνη.[22][23]
Φάρμακα που παραδοσιακά είναι γνωστό ότι οδηγούν σε SJS, πολύμορφο ερύθημα και τοξική επιδερμική νεκρόλυση περιλαμβάνουν τα σουλφοναμιδικά αντιβιοτικά,[8] αντιβιοτικά πενικιλλίνης, κεφιξίμη (αντιβιοτικό), βαρβιτουρικά, λαμοτριγίνη, φαινυτοΐνη και τριμεθοπρίμη. Ο συνδυασμός λαμοτριγίνης με βαλπροϊκό νάτριο αυξάνει τον κίνδυνο SJS.[24]
Τα μη στεροειδή αντιφλεγμονώδη φάρμακα (ΜΣΑΦ) είναι μια σπάνια αιτία SJS σε ενήλικες. Ο κίνδυνος είναι υψηλότερος για τους ηλικιωμένους ασθενείς, τις γυναίκες και όσους ξεκινούν θεραπεία.[25] Τυπικά, τα συμπτώματα του SJS που προκαλείται από φάρμακα εμφανίζονται εντός μιας εβδομάδας από την έναρξη της φαρμακευτικής αγωγής. Παρόμοια με τα ΜΣΑΦ, η παρακεταμόλη (ακεταμινοφένη) έχει επίσης προκαλέσει σπάνιες περιπτώσεις[26][27] SJS. Τα άτομα με συστηματικό ερυθηματώδη λύκο ή λοιμώξεις HIV είναι πιο επιρρεπή σε φαρμακογενές SJS.[10]
Λοιμώξεις
[Επεξεργασία | επεξεργασία κώδικα]Η δεύτερη πιο κοινή αιτία SJS και TEN είναι η λοίμωξη, ιδιαίτερα στα παιδιά. Αυτό περιλαμβάνει λοιμώξεις του ανώτερου αναπνευστικού, μέση ωτίτιδα, φαρυγγίτιδα και ιούς Epstein-Barr, Mycoplasma pneumoniae και λοιμώξεις από κυτταρομεγαλοϊό. Η τακτική χρήση φαρμάκων όπως αντιβιοτικά, αντιπυρετικά και αναλγητικά για τη διαχείριση λοιμώξεων μπορεί να καταστήσει δύσκολο τον εντοπισμό εάν τα κρούσματα προκλήθηκαν από τη μόλυνση ή τα φάρμακα που ελήφθησαν.[28]
Οι ιογενείς ασθένειες που έχουν αναφερθεί ότι προκαλούν SJS περιλαμβάνουν: τον ιό του απλού έρπητα (πιθανώς; είναι υπό συζήτηση), το AIDS, τον ιό κοξάκι, τη γρίπη, την ηπατίτιδα και την παρωτίτιδα.[12]
Σε παιδιατρικές περιπτώσεις, ο ιός Επστάιν-Μπαρ και οι εντεροϊοί έχουν συσχετιστεί με SJS.[12]
Πρόσφατες λοιμώξεις του ανώτερου αναπνευστικού έχουν αναφερθεί σε περισσότερους από τους μισούς ασθενείς με SJS.[12]
Οι βακτηριακές λοιμώξεις που συνδέονται με το SJS περιλαμβάνουν β-αιμολυτικούς στρεπτόκοκκους ομάδας Α, διφθερίτιδα, βρουκέλλωση, αφροδίσιο λεμφοκοκκίωμα, μυκοβακτήρια, Mycoplasma pneumoniae, ρικετσιώσεις, τουλαραιμία και τυφοειδή πυρετό.[12]
Μυκητιασικές λοιμώξεις με κοκκιδιοειδομυκητίαση, δερματοφύτωση και ιστοπλάσμωση θεωρούνται επίσης πιθανές αιτίες.[12] Η ελονοσία και η τριχομονάδωση, λοιμώξεις από πρωτόζωα, έχουν επίσης αναφερθεί ως αίτια.[12]
Παθοφυσιολογία
[Επεξεργασία | επεξεργασία κώδικα]Το SJS είναι μια αντίδραση υπερευαισθησίας τύπου IV στην οποία ένα φάρμακο ή μεταβολίτης του διεγείρει κυτταροτοξικά Τ κύτταρα (π. CD8 + Τ κύτταρα) και Τ βοηθητικά κύτταρα (δηλ, CD4+ Τ κύτταρα) για την έναρξη αυτοάνοσων αντιδράσεων που επιτίθενται στους ιστούς του εαυτού τους. Ειδικότερα, πρόκειται για αντίδραση τύπου IV, υποτύπου IVc, καθυστερημένης υπερευαισθησίας που εξαρτάται εν μέρει από τις δράσεις των φυσικών φονικών κυττάρων που βλάπτουν τους ιστούς.[29] Αυτό έρχεται σε αντίθεση με τους άλλους τύπους δερματικών διαταραχών, π.χ., το σύνδρομο DRESS που είναι τύπου IV, υποτύπου IVb, φαρμακευτική αντίδραση υπερευαισθησίας που εξαρτάται εν μέρει από τη δράση των ηωσινοφίλων που τραυματίζουν τους ιστούς[29][30] και την οξεία γενικευμένη εξανθηματώδη φλυκταίνωση που είναι μια αντίδραση υπερευαισθησίας Τύπου IV, υποτύπου IVd, η οποία εξαρτάται εν μέρει από τις δράσεις των ουδετερόφιλων που βλάπτουν τους ιστούς.[29][31]
Όπως και άλλα φάρμακα που προκαλούν SCAR, τα φάρμακα που προκαλούν SJS ή οι μεταβολίτες τους διεγείρουν τα CD8+ T κύτταρα ή τα CD4+ T κύτταρα για να ξεκινήσουν αυτοάνοσες αποκρίσεις. Μελέτες δείχνουν ότι ο μηχανισμός με τον οποίο ένα φάρμακο ή οι μεταβολίτες του το επιτυγχάνουν αυτό περιλαμβάνει την ανατροπή των οδών παρουσίασης αντιγόνου του έμφυτου ανοσοποιητικού συστήματος. Το φάρμακο ή ο μεταβολίτης δεσμεύεται ομοιοπολικά με μια πρωτεΐνη ξενιστή για να σχηματίσει έναν μη αυτο-σχετικό με το φάρμακο επίτοπο. Ένα κύτταρο που παρουσιάζει αντιγόνο (APC) προσλαμβάνει αυτές τις μεταβαλλόμενες πρωτεΐνες, τις χωνεύει σε μικρά πεπτίδια, τις τοποθετεί τα πεπτίδια σε μια αυλάκωση στο αντιγόνο των ανθρώπινων λευκοκυττάρων (δηλ. HLA) του κύριου συμπλέγματος ιστοσυμβατότητάς τους (δηλ. MHC) και παρουσιάζει τα συνδεδεμένα με MHC πεπτίδια σε υποδοχείς Τ-κυττάρων σε CD8+ Τ κύτταρα ή CD4+ Τ κύτταρα. Αυτά τα πεπτίδια που εκφράζουν ένα σχετιζόμενο με το φάρμακο, μη αυτοεπιτόπιο σε μία από τις διάφορες μορφές πρωτεΐνης HLA (HLA-A, HLA-B, HLA-C, HLA-DM, HLA-DO, HLA-DP, HLA-DQ, ή HLA-DR) μπορεί να συνδεθεί με έναν υποδοχέα Τ-κυττάρων και έτσι να διεγείρει το μητρικό Τ κύτταρο που φέρει τον υποδοχέα να ξεκινήσει επιθέσεις στους ιστούς του εαυτού τους. Εναλλακτικά, ένα φάρμακο ή ο μεταβολίτης του μπορεί να διεγείρει αυτά τα Τ κύτταρα εισάγοντας στην αυλάκωση μιας πρωτεΐνης HLA για να χρησιμεύσει ως μη-επίτοπος ή να συνδεθεί έξω από αυτήν την αύλακα για να αλλάξει μια πρωτεΐνη HLA έτσι ώστε να σχηματίσει έναν μη αυτο-επίτοπο. Σε όλες αυτές τις περιπτώσεις, ωστόσο, ένας μη αυτο-επίτοπος πρέπει να συνδέεται με έναν συγκεκριμένο ορότυπο HLA (δηλαδή παραλλαγή) προκειμένου να διεγείρει Τ κύτταρα. Δεδομένου ότι ο ανθρώπινος πληθυσμός εκφράζει περίπου 13.000 διαφορετικούς ορότυπους HLA ενώ ένα άτομο εκφράζει μόνο ένα κλάσμα από αυτούς και δεδομένου ότι ένα φάρμακο ή μεταβολίτης που προκαλεί SJS αλληλεπιδρά μόνο με έναν ή μερικούς ορότυπους HLA, η ικανότητα ενός φαρμάκου να προκαλεί δερματικές αντιδράσεις περιορίζεται σε εκείνα τα άτομα που εκφράζουν ορότυπους HLA που στοχεύουν το φάρμακο ή τον μεταβολίτη του.[32][33] Συνεπώς, μόνο σπάνια άτομα έχουν προδιάθεση να αναπτύξουν σοβαρές δερματικές αντιδράσεις ως απόκριση σε ένα συγκεκριμένο φάρμακο με βάση την έκφραση των ορότυπων HLA:[34] μελέτες έχουν εντοπίσει αρκετούς ορότυπους HLA που σχετίζονται με την ανάπτυξη SJS, SJS/TEN ή TEN ως απόκριση σε ορισμένα φάρμακα.[29][35] Γενικά, αυτές οι συσχετίσεις περιορίζονται στους αναφερόμενους πληθυσμούς.[36]
Υποδοχείς Τ-κυττάρων
[Επεξεργασία | επεξεργασία κώδικα]Εκτός από τη δράση μέσω πρωτεϊνών HLA για τη σύνδεση με έναν υποδοχέα Τ-κυττάρων, ένα φάρμακο ή ο μεταβολίτης του μπορεί να παρακάμψει τις πρωτεΐνες HLA για να συνδεθεί απευθείας σε έναν υποδοχέα Τ-κυττάρων και έτσι να διεγείρει τα CD8+ T ή CD4+ Τ κύτταρα για να ξεκινήσουν αυτοάνοσες αποκρίσεις. Και στις δύο περιπτώσεις, αυτή η δέσμευση φαίνεται να αναπτύσσεται μόνο σε ορισμένους υποδοχείς Τ κυττάρων. Δεδομένου ότι τα γονίδια για αυτούς τους υποδοχείς είναι σε μεγάλο βαθμό επεξεργασμένα, δηλ. τροποποιημένα ώστε να κωδικοποιούν πρωτεΐνες με διαφορετικές αλληλουχίες αμινοξέων, και επειδή ο ανθρώπινος πληθυσμός μπορεί να εκφράζει περισσότερα από 100 τρισεκατομμύρια διαφορετικούς (δηλ. διαφορετικές αλληλουχίες αμινοξέων) υποδοχείς Τ-κυττάρων ενώ ένα άτομο εκφράζει μόνο κλάσμα αυτών, η ικανότητα ενός φαρμάκου ή του μεταβολίτη του να επάγει το σύνδρομο DRESS αλληλεπιδρώντας με έναν υποδοχέα Τ κυττάρου περιορίζεται σε εκείνα τα άτομα των οποίων τα Τ κύτταρα εκφράζουν έναν ή περισσότερους υποδοχείς Τ κυττάρου που μπορούν να αλληλεπιδράσουν με το φάρμακο ή τον μεταβολίτη του.[32][37] Έτσι, μόνο σπάνια άτομα έχουν προδιάθεση να αναπτύξουν SJS ως απόκριση σε ένα συγκεκριμένο φάρμακο με βάση την έκφρασή τους συγκεκριμένων τύπων υποδοχέων Τ-κυττάρων.[34] Ενώ τα στοιχεία που υποστηρίζουν αυτήν την εκλεκτικότητα των Τ-κυττάρων είναι περιορισμένα, μια μελέτη εντόπισε την προτιμώμενη παρουσία του TCR-Vb και της περιοχής 3 που καθορίζει τη συμπληρωματικότητα σε υποδοχείς Τ-κυττάρων που βρέθηκαν στα Τ κύτταρα στις φουσκάλες ασθενών με DRESS που προκλήθηκε από αλλοπουρινόλη. Αυτό το εύρημα είναι συμβατό με την ιδέα ότι συγκεκριμένοι τύποι υποδοχέων Τ κυττάρων εμπλέκονται στην ανάπτυξη ειδικών SCAR που προκαλούνται από φάρμακα.[35]
ADME
[Επεξεργασία | επεξεργασία κώδικα]Παραλλαγές στην ADME, δηλ. η αποτελεσματικότητα ενός ατόμου στην απορρόφηση, την κατανομή στους ιστούς, τον μεταβολισμό ή την απέκκριση ενός φαρμάκου, έχει βρεθεί ότι συμβαίνουν σε διάφορες σοβαρές δερματικές ανεπιθύμητες ενέργειες (SCARS) καθώς και σε άλλους τύπους ανεπιθύμητων ενεργειών φαρμάκου.[38] Αυτές οι παραλλαγές επηρεάζουν τα επίπεδα και τη διάρκεια ενός φαρμάκου ή του μεταβολίτη του στους ιστούς και συνεπώς επηρεάζουν την ικανότητα του φαρμάκου ή του μεταβολίτη να προκαλεί αυτές τις αντιδράσεις.[6] Για παράδειγμα, το CYP2C9 είναι ένα σημαντικό κυτόχρωμα P450 που μεταβολίζει φάρμακα: μεταβολίζει και έτσι αδρανοποιεί τη φαινυτοΐνη. Ταϊβανοί, Ιάπωνες και Μαλαισιανοί εκφράζουν την παραλλαγή του CYP2C9*3[39] του CYP2C9, η οποία έχει μειωμένη μεταβολική δραστηριότητα σε σύγκριση με τον άγριο τύπο (π.χ. CYP2c9*1), έχουν αυξημένα επίπεδα φαινυτοΐνης στο αίμα και υψηλή συχνότητα εμφάνισης SJS (καθώς και SJS/TEN και TEN) κατά τη λήψη του φαρμάκου.[6][40] Εκτός από τις ανωμαλίες στα ένζυμα που μεταβολίζουν τα φάρμακα, οι δυσλειτουργίες των νεφρών, του ήπατος ή του γαστρεντερικού σωλήνα που αυξάνουν τα επίπεδα ενός φαρμάκου ή μεταβολίτη που προκαλούν ουλές ουλές προτείνονται για την προώθηση των αποκρίσεων SCAR.[6][7] Αυτές οι ανωμαλίες ADME, προτείνεται επίσης, μπορεί να αλληλεπιδράσουν με συγκεκριμένες πρωτεΐνες HLA και υποδοχείς Τ κυττάρων για να προάγουν μια σοβαρή δερματική αντίδραση.[6][41]
Διάγνωση
[Επεξεργασία | επεξεργασία κώδικα]Η διάγνωση βασίζεται σε προσβολή λιγότερο από το 10% του δέρματος.[4] Είναι γνωστό ως TEN όταν εμπλέκεται περισσότερο από το 30% του δέρματος και μια ενδιάμεση μορφή με συμμετοχή 10 έως 30%.[2] Ένα θετικό σημείο Νικόλσκι είναι χρήσιμο στη διάγνωση του SJS και του TEN.[8] Η βιοψία δέρματος είναι χρήσιμη, αλλά δεν απαιτείται, για τη διάγνωση SJS και TEN.[8]
Παθολογοανατομία
[Επεξεργασία | επεξεργασία κώδικα]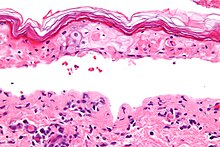
Το SJS, όπως το TEN και το πολύμορφο ερύθημα, χαρακτηρίζεται από συρρέουσα επιδερμική νέκρωση με ελάχιστη σχετική φλεγμονή. Η οξύτητα είναι εμφανής από το (κανονικό) μοτίβο που μοιάζει με πλέξη καλαθιού της κεράτινης στιβάδας.
Ταξινόμηση
[Επεξεργασία | επεξεργασία κώδικα]Το σύνδρομο Στίβενς-Τζόνσον (SJS) είναι μια ηπιότερη μορφή τοξικής επιδερμικής νεκρόλυσης (TEN).[42] Αυτές οι παθήσεις αναγνωρίστηκαν για πρώτη φορά το 1922.[25] Μια ταξινόμηση που δημοσιεύθηκε για πρώτη φορά το 1993, η οποία υιοθετήθηκε ως συναινετικός ορισμός, προσδιορίζει το σύνδρομο Στίβενς-Τζόνσον, την τοξική επιδερμική νεκρόλυση και την επικάλυψη SJS/TEN. Και τα τρία αποτελούν μέρος ενός φάσματος σοβαρών δερματικών αντιδράσεων (SCAR) που επηρεάζουν το δέρμα και τους βλεννογόνους.[13] Η διάκριση μεταξύ SJS, SJS/TEN επικάλυψης και TEN βασίζεται στον τύπο των βλαβών και στην ποσότητα της επιφάνειας του σώματος με φυσαλίδες και διαβρώσεις.[13] Συμφωνείται ότι η πιο αξιόπιστη μέθοδος για την ταξινόμηση των EM, SJS και TEN βασίζεται στη μορφολογία της βλάβης και στην έκταση της επιδερμικής αποκόλλησης.[8] Οι φουσκάλες και οι διαβρώσεις καλύπτουν μεταξύ 3% και 10% του σώματος σε SJS, 11–30% σε επικάλυψη SJS/TEN και πάνω από 30% σε TEN.[13] Το μοτίβο του δέρματος που σχετίζεται συχνότερα με το SJS είναι ευρέως διαδεδομένο, συχνά ενωμένο (συρρέον), βλατιδώδεις κηλίδες ή επίπεδες μικρές ή μεγάλες φουσκάλες που μπορεί επίσης να ενωθούν.[13] Αυτά εμφανίζονται κυρίως στον κορμό.[13]
Η επικάλυψη SJS, TEN και SJS/TEN μπορεί να θεωρηθεί εσφαλμένα ως πολύμορφο ερύθημα.[43] Το πολύμορφο ερύθημα, το οποίο είναι επίσης εντός του φάσματος SCAR, διαφέρει ως προς το κλινικό μοτίβο και την αιτιολογία.[13]
Θεραπευτική αγωγή
[Επεξεργασία | επεξεργασία κώδικα]Το SJS αποτελεί δερματολογική επείγουσα ανάγκη. Οι ασθενείς με τεκμηριωμένες λοιμώξεις από μυκόπλασμα μπορούν να αντιμετωπιστούν με μακρολίδη ή δοξυκυκλίνη από το στόμα.[10]
Αρχικά, η θεραπεία είναι παρόμοια με αυτή των ασθενών με θερμικά εγκαύματα και η συνεχιζόμενη φροντίδα μπορεί να είναι μόνο υποστηρικτική (π.χ. ενδοφλέβια υγρά και ρινογαστρική ή παρεντερική σίτιση) και συμπτωματική (π.χ. αναλγητικό στοματικό διάλυμα για στοματικό έλκος). Οι δερματολόγοι και οι χειρουργοί τείνουν να διαφωνούν σχετικά με το εάν το δέρμα πρέπει να καθαριστεί.[10]
Πέρα από αυτό το είδος υποστηρικτικής φροντίδας, καμία θεραπεία για SJS δεν θεωρείται ευρέως αποδεκτή. Η θεραπεία με κορτικοστεροειδή είναι αμφιλεγόμενη. Οι πρώιμες αναδρομικές μελέτες υπέδειξαν ότι τα κορτικοστεροειδή αύξησαν την παραμονή στο νοσοκομείο και τα ποσοστά επιπλοκών. Δεν έχουν διεξαχθεί τυχαιοποιημένες δοκιμές κορτικοστεροειδών για το SJS και μπορεί να αντιμετωπιστεί επιτυχώς χωρίς αυτά.[10]
Πρόγνωση
[Επεξεργασία | επεξεργασία κώδικα]Το SJS (με λιγότερο από το 10% της επιφάνειας του σώματος που εμπλέκεται) έχει ποσοστό θνησιμότητας περίπου 5%. Η θνησιμότητα για τοξική επιδερμική νεκρόλυση (TEN) είναι 30-40%. Ο κίνδυνος θανάτου μπορεί να εκτιμηθεί χρησιμοποιώντας την κλίμακα SCORTEN, η οποία λαμβάνει υπόψη έναν αριθμό προγνωστικών δεικτών.[44] Είναι χρήσιμο να υπολογίσετε ένα SCORTEN εντός των πρώτων 3 ημερών νοσηλείας.[8] Άλλα αποτελέσματα περιλαμβάνουν βλάβη/ανεπάρκεια οργάνων, ξύσιμο κερατοειδούς και τύφλωση. Περιοριστική πνευμονοπάθεια μπορεί να αναπτυχθεί σε ασθενείς με SJS και TEN μετά από αρχική οξεία πνευμονική προσβολή.[8] Οι ασθενείς με SJS ή TEN που προκαλούνται από ένα φάρμακο έχουν καλύτερη πρόγνωση όσο νωρίτερα αποσυρθεί το αιτιολογικό φάρμακο.[8]
Επιδημιολογία
[Επεξεργασία | επεξεργασία κώδικα]Το SJS είναι μια σπάνια πάθηση, με αναφερόμενη συχνότητα εμφάνισης περίπου 2,6[10] έως 6,1[25] περιπτώσεων ανά εκατομμύριο άτομα ανά έτος. Στις Ηνωμένες Πολιτείες γίνονται περίπου 300 νέες διαγνώσεις κάθε χρόνο. Η πάθηση είναι πιο συχνή στους ενήλικες παρά στα παιδιά.
Ιστορία
[Επεξεργασία | επεξεργασία κώδικα]Το SJS πήρε το όνομά του από τον ΄Άλμπερτ Μέισον Στίβενς και τον Φρανκ Τσέιμπλις Τζόνσον, Αμερικανούς παιδίατρους που δημοσίευσαν από κοινού μια περιγραφή της διαταραχής στο American Journal of Diseases of Children το 1922.[45][46]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 «Stevens-Johnson syndrome/toxic epidermal necrolysis». Genetics Home Reference (στα Αγγλικά). Ιουλίου 2015. Αρχειοθετήθηκε από το πρωτότυπο στις 27 Απριλίου 2017. Ανακτήθηκε στις 26 Απριλίου 2017.
- ↑ 2,0 2,1 2,2 «Orphanet: Toxic epidermal necrolysis». Orphanet (στα Αγγλικά). Νοεμβρίου 2008. Αρχειοθετήθηκε από το πρωτότυπο στις 27 Απριλίου 2017. Ανακτήθηκε στις 26 Απριλίου 2017.
- ↑ Schwartz, RA; McDonough, PH; Lee, BW (August 2013). «Toxic epidermal necrolysis: Part I. Introduction, history, classification, clinical features, systemic manifestations, etiology, and immunopathogenesis.». Journal of the American Academy of Dermatology 69 (2): 173.e1–13; quiz 185–6. doi:. PMID 23866878.
- ↑ 4,0 4,1 4,2 4,3 4,4 4,5 4,6 «Stevens-Johnson syndrome». GARD. Αρχειοθετήθηκε από το πρωτότυπο στις 28 Αυγούστου 2016. Ανακτήθηκε στις 26 Αυγούστου 2016.
- ↑ Hyzy, Robert C. (2017). Evidence-Based Critical Care: A Case Study Approach (στα Αγγλικά). Springer. σελ. 761. ISBN 9783319433417.
- ↑ 6,0 6,1 6,2 6,3 6,4 «Recent advances in the understanding of severe cutaneous adverse reactions». The British Journal of Dermatology 177 (5): 1234–1247. 2017. doi:. PMID 28256714.
- ↑ 7,0 7,1 «Current Perspectives on Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis». Clinical Reviews in Allergy & Immunology 54 (1): 147–176. 2017. doi:. PMID 29188475.
- ↑ 8,00 8,01 8,02 8,03 8,04 8,05 8,06 8,07 8,08 8,09 8,10 8,11 8,12 Maverakis, Emanual; Wang, Elizabeth A.; Shinkai, Kanade; Mahasirimongkol, Surakameth; Margolis, David J.; Avigan, Mark; Chung, Wen-Hung; Goldman, Jennifer και άλλοι. (2017). «Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis Standard Reporting and Evaluation Guidelines» (στα αγγλικά). JAMA Dermatology 153 (6): 587–592. doi:. PMID 28296986. Αρχειοθετήθηκε από το πρωτότυπο στις 2019-12-03. https://web.archive.org/web/20191203081548/https://www.zora.uzh.ch/id/eprint/144140/1/LF_2017_Stevens-Johnson_Syndrome_and_Toxic_Necrolysis_Standard_Reporting_and_Evaluation_Guidlines_-_Results_of_a_National_Institutes_of_Health_Working_Group.pdf. Ανακτήθηκε στις 2022-11-27.
- ↑ «Drug Reaction with Eosinophilia and Systemic Symptoms (DRESS) Syndrome and the Rheumatologist». Current Rheumatology Reports 19 (1): 3. January 2017. doi:. PMID 28138822.
- ↑ 10,0 10,1 10,2 10,3 10,4 10,5 10,6 Tigchelaar, H.· Kannikeswaran, N.· Kamat, D. (Δεκεμβρίου 2008). «Stevens–Johnson Syndrome: An intriguing diagnosis». pediatricsconsultantlive.com. UBM Medica. Αρχειοθετήθηκε από το πρωτότυπο στις 17 Αυγούστου 2012.
- ↑ Tan SK, Tay YK; Tay (2012). «Profile and pattern of Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis in a general hospital in Singapore: Treatment outcomes». Acta Dermato-Venereologica 92 (1): 62–6. doi:. PMID 21710108.
- ↑ 12,0 12,1 12,2 12,3 12,4 12,5 12,6 12,7 12,8 Foster, C. StephenΣφάλμα έκφρασης: Μη αναγνωρισμένη λέξη "etal" (12 August 2013). Roy, Hampton Sr. (article editor). «Stevens-Johnson Syndrome». Medscape Reference: Etiology. Αρχειοθετήθηκε από το πρωτότυπο στις 22 January 2013. https://web.archive.org/web/20130122091022/http://emedicine.medscape.com/article/1197450-overview#aw2aab6b2b3.
- ↑ 13,0 13,1 13,2 13,3 13,4 13,5 13,6 13,7 13,8 Mockenhaupt M (2011). «The current understanding of Stevens–Johnson syndrome and toxic epidermal necrolysis». Expert Review of Clinical Immunology 7 (6): 803–15. doi:. PMID 22014021.
- ↑ Teraki Y, Shibuya M, Izaki S; Shibuya; Izaki (2010). «Stevens-Johnson syndrome and toxic epidermal necrolysis due to anticonvulsants share certain clinical and laboratory features with drug-induced hypersensitivity syndrome, despite differences in cutaneous presentations». Clin. Exp. Dermatol. 35 (7): 723–8. doi:. PMID 19874350.
- ↑ Cooper KL (2012). «Drug reaction, skin care, skin loss». Crit Care Nurse 32 (4): 52–9. doi:. PMID 22855079. https://archive.org/details/sim_critical-care-nurse_2012-08_32_4/page/52.
- ↑ Sassolas B, Haddad C, Mockenhaupt M, Dunant A, Liss Y, Bork K, Haustein UF, Vieluf D, Roujeau JC, Le Louet H; Haddad; Mockenhaupt; Dunant; Liss; Bork; Haustein; Vieluf και άλλοι. (2010). «ALDEN, an algorithm for assessment of drug causality in Stevens-Johnson Syndrome and toxic epidermal necrolysis: Comparison with case-control analysis». Clinical Pharmacology & Therapeutics 88 (1): 60–8. doi:. PMID 20375998. https://semanticscholar.org/paper/c4eadf168aee2afb5e2a14a46068b26384ba3fc3.
- ↑ «Scientific conclusions and grounds for the variation to the terms of the marketing authorisation(s)» (PDF) (data sheet). European Medicines Agency. 6 Απριλίου 2017.
- ↑ «Diflucan One» (data sheet). Medsafe; New Zealand Ministry of Health. 29 Απριλίου 2008. Αρχειοθετήθηκε από το πρωτότυπο στις 3 Ιουνίου 2010.
- ↑ «Provigil (modafinil) Tablets». MedWatch. US Food and Drug Administration. 24 Οκτωβρίου 2007. Αρχειοθετήθηκε από το πρωτότυπο στις 11 Δεκεμβρίου 2013.
- ↑ Raksha MP, Marfatia YS; Marfatia (2008). «Clinical study of cutaneous drug eruptions in 200 patients». Indian Journal of Dermatology, Venereology and Leprology 74 (1): 80. doi:. PMID 18193504. http://www.bioline.org.br/pdf?dv08031.
- ↑ «Incivek prescribing information» (PDF) (package insert). Vertex Pharmaceuticals. Δεκεμβρίου 2012. Αρχειοθετήθηκε (PDF) από το πρωτότυπο στις 15 Μαρτίου 2013.
- ↑ Fagot JP, Mockenhaupt M, Bouwes-Bavinck JN, Naldi L, Viboud C, Roujeau JC; Mockenhaupt; Bouwes-Bavinck; Naldi; Viboud; Roujeau; Euroscar Study (2001). «Nevirapine and the risk of Stevens–Johnson syndrome or toxic epidermal necrolysis». AIDS 15 (14): 1843–8. doi:. PMID 11579247.
- ↑ Devi K, George S, Criton S, Suja V, Sridevi PK; George; Criton; Suja; Sridevi (2005). «Carbamazepine – The commonest cause of toxic epidermal necrolysis and Stevens–Johnson syndrome: A study of 7 years». Indian Journal of Dermatology, Venereology and Leprology 71 (5): 325–8. doi:. PMID 16394456.
- ↑ «Stevens-Johnson syndrome due to concomitant use of lamotrigine and valproic acid». Am J Clin Dermatol 8 (2): 107–11. 2007. doi:. PMID 17428116.
- ↑ 25,0 25,1 25,2 Ward KE, Archambault R, Mersfelder TL; Archambault; Mersfelder (2010). «Severe adverse skin reactions to nonsteroidal antiinflammatory drugs: A review of the literature». American Journal of Health-System Pharmacy 67 (3): 206–213. doi:. PMID 20101062.
- ↑ Khawaja A, Shahab A, Hussain SA; Shahab; Hussain (2012). «Acetaminophen induced Steven Johnson syndrome-Toxic Epidermal Necrolysis overlap». Journal of Pakistan Medical Association 62 (5): 524–7. PMID 22755330. Αρχειοθετήθηκε από το πρωτότυπο στις 30 December 2014. https://web.archive.org/web/20141230130734/http://www.jpma.org.pk/full_article_text.php?article_id=3419.
- ↑ Trujillo C, Gago C, Ramos S; Gago; Ramos (2010). «Stevens-Jonhson syndrome after acetaminophen ingestion, confirmed by challenge test in an eleven-year-old patient». Allergol Immunopathol (Madr) 38 (2): 99–100. doi:. PMID 19875224.
- ↑ Bentley, John; Sie, David (8 October 2014). «Stevens-Johnson syndrome and toxic epidermal necrolysis». The Pharmaceutical Journal 293 (7832). Αρχειοθετήθηκε από το πρωτότυπο στις 12 October 2014. https://web.archive.org/web/20141012190345/http://www.pharmaceutical-journal.com/learning/cpd-article/stevens-johnson-syndrome-and-toxic-epidermal-necrolysis/20066728.cpdarticle. Ανακτήθηκε στις 8 October 2014.
- ↑ 29,0 29,1 29,2 29,3 «Adverse cutaneous drug eruptions: current understanding». Seminars in Immunopathology 38 (1): 75–86. January 2016. doi:. PMID 26553194.
- ↑ «Chapter 28: Classification of hypersensitivity reactions». Allergy and Asthma Proceedings 33 Suppl 1 (3): S96–9. 2012. doi:. PMID 22794701.
- ↑ «Acute Generalized Exanthematous Pustulosis: Pathogenesis, Genetic Background, Clinical Variants and Therapy». International Journal of Molecular Sciences 17 (8): 1214. 2016. doi:. PMID 27472323.
- ↑ 32,0 32,1 «Severe cutaneous adverse reactions to drugs». Lancet 390 (10106): 1996–2011. 2017. doi:. PMID 28476287.
- ↑ «Pustular psoriasis and related pustular skin diseases». The British Journal of Dermatology 178 (3): 614–618. January 2018. doi:. PMID 29333670.
- ↑ 34,0 34,1 «Classification of Drug Hypersensitivity into Allergic, p-i, and Pseudo-Allergic Forms». International Archives of Allergy and Immunology 171 (3–4): 166–179. 2016. doi:. PMID 27960170.
- ↑ 35,0 35,1 «Immunopathogenesis and risk factors for allopurinol severe cutaneous adverse reactions». Current Opinion in Allergy and Clinical Immunology 16 (4): 339–45. 2016. doi:. PMID 27362322.
- ↑ «HLA Association with Drug-Induced Adverse Reactions». Journal of Immunology Research 2017: 3186328. 2017. doi:. PMID 29333460.
- ↑ «Pharmacogenomics of off-target adverse drug reactions». British Journal of Clinical Pharmacology 83 (9): 1896–1911. September 2017. doi:. PMID 28345177.
- ↑ «Genomics of Adverse Drug Reactions». Trends in Pharmacological Sciences 38 (1): 100–109. January 2017. doi:. PMID 27955861.
- ↑ snpdev. «Reference SNP (refSNP) Cluster Report: rs1057910 ** With drug-response allele **». www.ncbi.nlm.nih.gov.
- ↑ «Genetic variants associated with phenytoin-related severe cutaneous adverse reactions». JAMA 312 (5): 525–34. August 2014. doi:. PMID 25096692. https://archive.org/details/sim_jama_2014-08-06_312_5/page/n69.
- ↑ «Severe cutaneous adverse drug reactions». The Journal of Dermatology 43 (7): 758–66. 2016. doi:. PMID 27154258.
- ↑ Rehmus, W. E. (Νοεμβρίου 2013). «Stevens–Johnson Syndrome (SJS) and Toxic Epidermal Necrolysis (TEN)». Στο: Porter, R. S., επιμ. The Merck Manual ((online version) 19th έκδοση). Whitehouse Station, NJ: Merck & Co.
- ↑ Auquier-Dunant A, Mockenhaupt M, Naldi L, Correia O, Schröder W, Roujeau JC; Mockenhaupt; Naldi; Correia; Schröder; Roujeau; SCAR Study Group. Severe Cutaneous Adverse Reactions (2002). «Correlations between clinical patterns and causes of Erythema Multiforme Majus, Stevens-Johnson Syndrome, and Toxic Epidermal Necrolysis results of an international prospective study». Archives of Dermatology 138 (8): 1019–24. doi:. PMID 12164739. https://archive.org/details/sim_jama-dermatology_2002-08_138_8/page/1019.
- ↑ Foster et al. 2013.
- ↑ Enerson, Ole Daniel, επιμ.., «Stevens-Johnson syndrome», Whonamedit?, http://www.whonamedit.com/synd.cfm/1501.html
- ↑ Stevens, A.M.; Johnson, F.C. (1922). «A new eruptive fever associated with stomatitis and ophthalmia; Report of two cases in children». American Journal of Diseases of Children 24 (6): 526–33. doi:. Αρχειοθετήθηκε από το πρωτότυπο στις 3 January 2014. https://web.archive.org/web/20140103023904/http://books.google.com/books?id=E90fAAAAIAAJ&pg=PA526.