Φαινοφιμπράτη
 | |
| Ονομασία IUPAC | |
|---|---|
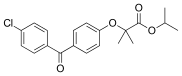
propan-2-yl 2-[4-(4-chlorobenzoyl)phenoxy]-2-methylpropanoate | |
| Κλινικά δεδομένα | |
| Εμπορικές ονομασίες | Fenoglide, Lipofen, Lipidil, άλλες |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a601052 |
| Δεδομένα άδειας |
|
| Κατηγορία ασφαλείας κύησης | |
| Οδοί χορήγησης | Από το στόμα |
| Κυκλοφορία | |
| Κυκλοφορία |
|
| Φαρμακοκινητική | |
| Πρωτεϊνική σύνδεση | 99% |
| Μεταβολισμός | Γλυκουρονιδίωση |
| Βιολογικός χρόνος ημιζωής | 20 ώρες |
| Απέκκριση | ούρα (60%), κόπρανα (25%) |
| Κωδικοί | |
| Αριθμός CAS | 49562-28-9 |
| Κωδικός ATC | C10AB05 C10BA03 C10BA04 |
| PubChem | CID 3339 |
| IUPHAR/BPS | 7186 |
| DrugBank | DB01039 |
| ChemSpider | 3222 |
| UNII | U202363UOS |
| KEGG | D00565 |
| ChEBI | CHEBI:5001 |
| ChEMBL | CHEMBL672 |
| Χημικά στοιχεία | |
| Χημικός τύπος | C20H21ClO4 |
| Μοριακή μάζα | 360,83 g·mol−1 |
O=C(c1ccc(Cl)cc1)c2ccc(OC(C(=O)OC(C)C)(C)C)cc2 | |
InChI=1S/C20H21ClO4/c1-13(2)24-19(23)20(3,4)25-17-11-7-15(8-12-17)18(22)14-5-9-16(21)10-6-14/h5-13H,1-4H3 Key:YMTINGFKWWXKFG-UHFFFAOYSA-N | |
| Φυσικά στοιχεία | |
| Σημείο τήξης | 80 to 81 °C (176 to 178 °F) |
| (verify) | |
Η φαινοφιμπράτη ή φαινοφιβράτη, που πωλείται με την επωνυμία Tricor μεταξύ άλλων, είναι φάρμακο της κατηγορίας των φιμπρατών που χρησιμοποιείται για τη θεραπεία των μη φυσιολογικών επιπέδων λιπιδίων στο αίμα.[2] Προτιμάται λιγότερο από τις στατίνες, καθώς δεν φαίνεται να μειώνει τον κίνδυνο θανατηφόρου καρδιαγγειακής νόσου.[3] Η χρήση της συνιστάται μαζί με διατροφικές αλλαγές. Λαμβάνεται από το στόμα.[2]
Συχνές ανεπιθύμητες ενέργειες περιλαμβάνουν ηπατικά προβλήματα, αναπνευστικά προβλήματα, κοιλιακό άλγος, μυϊκά προβλήματα και ναυτία. Σοβαρές παρενέργειες μπορεί να περιλαμβάνουν τοξική επιδερμική νεκρόλυση, ραβδομυόλυση, χολόλιθους, θρόμβους αίματος και παγκρεατίτιδα.[2] Δεν συνιστάται η χρήση κατά την εγκυμοσύνη και τον θηλασμό.[3][4] Λειτουργεί με διάφορους μηχανισμούς.[2]
Το δίπλωμα ευρεσιτεχνίας για τη φαινοφιμπράτη κατοχυρώθηκε το 1969 και τέθηκε σε ιατρική χρήση το 1975.[5] Διατίθεται ως γενόσημο φάρμακο.[3] Το 2017, ήταν η 70η πιο συχνά συνταγογραφούμενη φαρμακευτική αγωγή στις Ηνωμένες Πολιτείες, με περισσότερες από έντεκα εκατομμύρια συνταγές.[6][7]
Ιατρικές χρήσεις[Επεξεργασία | επεξεργασία κώδικα]
Η φαινοφιμπράτη χρησιμοποιείται μαζί με τη διατροφή για τη μείωση της αυξημένης χοληστερόλης λιποπρωτεϊνών χαμηλής πυκνότητας (LDL), της ολικής χοληστερόλης, των τριγλυκεριδίων (TG) και της απολιποπρωτεΐνης Β (apo B), και για την αύξηση της χοληστερόλης λιποπρωτεΐνης υψηλής πυκνότητας (HDL) σε ενήλικες με πρωτογενή υπερχοληστερολαιμία ή μικτή δυσλιπιδαιμία,[8] και φαίνεται να είναι πιο αποτελεσματική στη δεύτερη.[9] Παρ'όλα αυτά, οι στατίνες παραμένουν η πρώτη γραμμή για τη θεραπεία της υψηλής χοληστερόλης στο αίμα. Οι οδηγίες του AHA από το 2013 δεν βρήκαν στοιχεία υπέρ της συνήθους χρήσης πρόσθετων φαρμάκων.[10] Επίσης, η βελτίωση του γλυκαιμικού ελέγχου σε διαβητικούς που παρουσιάζουν χυλομικροναιμία νηστείας συνήθως θα μειώσει την ανάγκη για φαρμακολογική παρέμβαση.[8][ασαφές]
Στην κλινική μελέτη FIELD, η φαινοφιμπράτη φάνηκε να μειώνει τον κίνδυνο του μη θανατηφόρου εμφράγματος του μυοκαρδίου καθώς και των καρδιακών συμβαμάτων σε άτομα με σακχαρώδη διαβήτη, όμως αυτό δεν αντικατοπτρίστηκε σε στατιστικά σημαντική μείωση της θνητότητας από καρδιαγγειακή νόσο ή της συνολικής θνητότητας.[9] Επίσης πιθανώς βελτιώνει την έκβαση διαβητικής αμφιβληστροειδοπάθειας,[11][12] και έχει εγκριθεί για να εμποδίσει την εξέλιξη της διαβητικής αμφιβληστροειδοπάθειας σε ασθενείς με διαβήτη τύπου 2 και υπάρχουσα διαβητική αμφιβληστροειδοπάθεια στην Αυστραλία.[13] Φαίνεται επίσης ότι βοηθά στη μείωση των ακρωτηριασμών των κάτω άκρων σε αυτήν την ίδια ομάδα ανθρώπων.[14]
Η φαινοφιμπράτη έχει χρησιμοποιηθεί επίσης εκτός ετικέτας ως πρόσθετη θεραπεία των υψηλών επιπέδων ουρικού οξέος στο αίμα σε άτομα που έχουν ουρική αρθρίτιδα.[15]
Σε ζωικά μοντέλα έχει δειχθεί ότι έχει αντιεπιληπτική δράση, αν και δεν χρησιμοποιείται κλινικά γι'αυτή τη δράση του.[16]
Αντενδείξεις[Επεξεργασία | επεξεργασία κώδικα]
Η φαινοφιμπράτη αντενδείκνυται σε:[8]
- Ασθενείς με σοβαρή νεφρική δυσλειτουργία, συμπεριλαμβανομένων εκείνων που υποβάλλονται σε αιμοκάθαρση (2,7 φορές αύξηση της έκθεσης και αυξημένη συσσώρευση κατά τη διάρκεια χρόνιας δόσης σε ασθενείς με εκτιμώμενο ρυθμό σπειραματικής διήθησης <30 mL / min)
- Ασθενείς με ενεργή ηπατική νόσο, συμπεριλαμβανομένων εκείνων με πρωτοπαθή χολική κίρρωση και ανεξήγητες επίμονες ανωμαλίες στις εξετάσεις ηπατικών ενζύμων
- Ασθενείς με προϋπάρχουσα νόσο της χοληδόχου κύστης
- Μητέρες που θηλάζουν
- Ασθενείς με γνωστή υπερευαισθησία στη φαινοφιμπράτη ή φαινοφιμπρικό οξύ
Παρενέργειες[Επεξεργασία | επεξεργασία κώδικα]
Οι πιο συχνές ανεπιθύμητες ενέργειες (> 3% των ασθενών με συγχορηγούμενες στατίνες) είναι[17]
- Κεφαλαλγία
- Ραχιαλγία
- Ρινοφαρυγγίτιδα
- Ναυτία
- Μυαλγία
- Αρθραλγία
- Διάρροια
- Λοίμωξη ανώτερου αναπνευστικού συστήματος
- Νεφρολιθίαση
Προφυλάξεις[Επεξεργασία | επεξεργασία κώδικα]
Όταν η φαινοφιμπράτη και μια στατίνη χορηγούνται ως συνδυαστική θεραπεία, συνιστάται η χορήγηση φαινοφιμπράτης το πρωί και της στατίνης τη νύχτα, έτσι ώστε οι μέγιστες δόσεις να μην αλληλεπικαλύπτονται.[18]
- Μυοπάθεια και ραβδομυόλυση: αυξημένος κίνδυνος όταν συγχορηγείται με στατίνη, ιδιαίτερα σε ηλικιωμένους και ασθενείς με διαβήτη, νεφρική ανεπάρκεια, υποθυρεοειδισμό[17]
- Μπορεί να αυξήσει τις τρανσαμινάσες του ορού. Οι εξετάσεις ήπατος πρέπει να παρακολουθούνται περιοδικά[17]
- Μπορεί να αυξήσει τα επίπεδα κρεατινίνης στον ορό. Η νεφρική λειτουργία πρέπει να παρακολουθείται περιοδικά σε ασθενείς με χρόνια νεφρική νόσο[17]
- Μπορεί να αυξήσει την απέκκριση χοληστερόλης στη χολή, οδηγώντας σε κίνδυνο χολολιθίασης. Εάν υπάρχει υποψία, ενδείκνυνται έλεγχος της χοληδόχου κύστης.[17]
Υπερβολική δόση[Επεξεργασία | επεξεργασία κώδικα]
Δεν υπάρχει ειδική θεραπεία για υπερδοσολογία με δισκία παρατεταμένης αποδέσμευσης φαινοφιβρικού οξέος. Υποδεικνύεται γενική υποστηρικτική φροντίδα, συμπεριλαμβανομένης της παρακολούθησης ζωτικών σημείων και της παρατήρησης της κλινικής κατάστασης. Επιπλέον, η αιμοκάθαρση δεν πρέπει να θεωρείται ως επιλογή θεραπείας υπερδοσολογίας επειδή η φαινοφιμπράτη συνδέεται έντονα με τις πρωτεΐνες του πλάσματος και δεν διαλύεται καλά.[17]
Αλληλεπιδράσεις[Επεξεργασία | επεξεργασία κώδικα]
Αυτές οι αλληλεπιδράσεις φαρμάκων με τη φαινοφιμπράτη θεωρούνται σημαντικές και μπορεί να χρειάζονται τροποποιήσεις θεραπείας:
- Διαχωριστικά χολικού οξέος (π.χ. χολεστυραμίνη, κολεστιπόλη κ.λπ. ): Εάν ληφθούν μαζί, οι ρητίνες χολικού οξέος μπορεί να προσδεθούν στη φαινοφιμπράτη, με αποτέλεσμα τη μείωση της απορρόφησης φαινοφιμπράτης. Για να μεγιστοποιηθεί η απορρόφηση, οι ασθενείς πρέπει να διαχωρίσουν τη χορήγηση τουλάχιστον 1 ώρα πριν ή 4 ώρες έως 6 ώρες μετά τη λήψη του ρητινών χολικού οξέος.[17][19]
- Ανοσοκατασταλτικά (π.χ. κυκλοσπορίνη ή τακρόλιμους): Υπάρχει αυξημένος κίνδυνος νεφρικής δυσλειτουργίας με ταυτόχρονη χρήση ανοσοκατασταλτικών και φαινοφιμπράτης. Προσεγγίστε με προσοχή κατά τη συγχορήγηση πρόσθετων φαρμάκων που μειώνουν τη νεφρική λειτουργία.[20]
- Ανταγωνιστές της βιταμίνης Κ (π.χ. βαρφαρίνη): Όπως αναφέρθηκε προηγουμένως, η φαινοφιμπράτη αλληλεπιδρά με αντιπηκτικά κουμαρίνης για να αυξήσει τον κίνδυνο αιμορραγίας. Μπορεί να είναι απαραίτητη η προσαρμογή της δοσολογίας του ανταγωνιστή της βιταμίνης Κ.
- Στατίνες: Ο συνδυασμός στατινών και φαινοφιβράτης μπορεί να αυξήσει τον κίνδυνο ραβδομυόλυσης ή μυοπάθειας.[21]
Μηχανισμός δράσης[Επεξεργασία | επεξεργασία κώδικα]
"Συνοπτικά, ο αυξημένος καταβολισμός σωματιδίων πλούσιων σε τριγλυκερίδια και η μειωμένη έκκριση της VLDL αποτελούν το υποτριγλυκεριδικό αποτέλεσμα των φιβρατών, ενώ η επίδρασή τους στον μεταβολισμό HDL σχετίζεται με αλλαγές στην έκφραση της απολιποπρωτεΐνης HDL."[22]
Η φαινοφιβράτη είναι παράγωγο ινώδους οξέος, ένα προφάρμακο που περιλαμβάνει φαινοφιβρικό οξύ συνδεδεμένο με έναν ισοπροπυλεστέρα. Μειώνει τα επίπεδα λιπιδίων ενεργοποιώντας τον ενεργοποιημένο από τον πολλαπλασιαστή υπεροξειδοσώματος υποδοχέα άλφα (PPARa). Ο PPARα ενεργοποιεί τη λιπάση λιποπρωτεΐνης και μειώνει την αποπρωτεΐνη CIII, η οποία αυξάνει την λιπόλυση και την απομάκρυνση των πλούσιων σε τριγλυκερίδια σωματιδίων από το πλάσμα.[22]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ «Fenofibrate 267mg Capsules - Summary of Product Characteristics (SmPC)». (emc). 12 Φεβρουαρίου 2020. Ανακτήθηκε στις 13 Απριλίου 2020.
- ↑ 2,0 2,1 2,2 2,3 «Fenofibric Acid/Fenofibrate Monograph for Professionals». Drugs.com. American Society of Health-System Pharmacists. Ανακτήθηκε στις 3 Μαρτίου 2019.
- ↑ 3,0 3,1 3,2 British national formulary : BNF 76 (76 έκδοση). Pharmaceutical Press. 2018. σελ. 198. ISBN 9780857113382.
- ↑ «Fenofibrate Pregnancy and Breastfeeding Warnings». Drugs.com (στα Αγγλικά). Ανακτήθηκε στις 3 Μαρτίου 2019.
- ↑ Fischer, Jnos· Ganellin, C. Robin (2006). Analogue-based Drug Discovery (στα Αγγλικά). John Wiley & Sons. σελ. 474. ISBN 9783527607495.
- ↑ «The Top 300 of 2020». ClinCalc. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ «Fenofibrate - Drug Usage Statistics». ClinCalc. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ 8,0 8,1 8,2 Package Insert: Abbot Laboratories (October 2010)
- ↑ 9,0 9,1 «Fenofibrate Intervention and Event Lowering in Diabetes». American College of Cardiology. 19 Αυγούστου 2014. Ανακτήθηκε στις 21 Οκτωβρίου 2020.
- ↑ «2013 ACC/AHA guideline on the treatment of blood cholesterol to reduce atherosclerotic cardiovascular risk in adults: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines». Circulation 129 (25 Suppl 2): S1–45. 2014. doi:. PMID 24222016.
- ↑ «Fenofibrate - a potential systemic treatment for diabetic retinopathy?». Am J Ophthalmol 154 (1): 6–12. Jul 2012. doi:. PMID 22709833. https://archive.org/details/sim_american-journal-of-ophthalmology_2012-07_154_1/page/6.
- ↑ «More clinical lessons from the FIELD study». Cardiovasc Drugs Ther 23 (3): 235–41. 2009. doi:. PMID 19160032.
- ↑ «Australian Public Assessment Report for fenofibrate». TGA. TGA. Αρχειοθετήθηκε από το πρωτότυπο στις 29 Ιουνίου 2015. Ανακτήθηκε στις 27 Ιουνίου 2015.
- ↑ «How can we improve the management of vascular risk in type 2 diabetes: insights from FIELD». Cardiovasc Drugs Ther 23 (5): 403–8. 2009. doi:. PMID 19757004.
- ↑ «2012 American College of Rheumatology guidelines for management of gout. Part 1: systematic nonpharmacologic and pharmacologic therapeutic approaches to hyperuricemia». Arthritis Care Res (Hoboken) 64 (10): 1431–46. 2012. doi:. PMID 23024028.
- ↑ Porta N, Vallée L, Lecointe C, Bouchaert E, Staels B, Bordet R, Auvin S. Fenofibrate, a peroxisome proliferator-activated receptor-alpha agonist, exerts anticonvulsive properties. Epilepsia. 2009 Apr;50(4):943–8. doi:10.1111/j.1528-1167.2008.01901.x. PubMed.
- ↑ 17,0 17,1 17,2 17,3 17,4 17,5 17,6 Fenofibric Acid FDA Label Prescribing Information«FDA Label Information» (PDF). FDA.
- ↑ «Statin-fibrate combination: therapy for hyperlipidemia: a review». Curr Med Res Opin 19 (3): 155–68. 2003. doi:. PMID 12814127. https://archive.org/details/sim_current-medical-research-and-opinion_2003_19_3/page/155.
- ↑ Product Information: TriCor(TM), fenofibrate. Abbott Laboratories, North Chicago, IL, 1998.
- ↑ Product Information: Sandimmune(R) oral capsules, oral solution, intravenous injection, cyclosporine oral capsules, oral solution, intravenous injection. Novartis Pharmaceuticals Corporation, East Hanover, NJ, 2010.
- ↑ Product Information: TRICOR(R) oral tablets, fenofibrate oral tablets. Abbott Laboratories, North Chicago, IL, 2007.
- ↑ 22,0 22,1 «Mechanism of action of fibrates on lipid and lipoprotein metabolism». Circulation 98 (19): 2088–93. 1998. doi:. PMID 9808609. https://circ.ahajournals.org/content/98/19/2088.full.
