Μαστικός αδένας
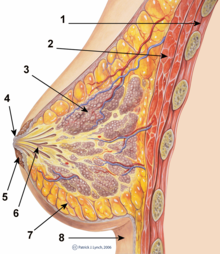
Ο μαστικός αδένας είναι εξωκρινής αδένας στον άνθρωπο και σε άλλα θηλαστικά που παράγει γάλα για να ταΐσει τους νεαρούς απογόνους. Οι μαστικοί αδένες είναι διατεταγμένοι σε όργανα τα οποία ονομάζονται μαστοί. Η γαλακτόρροια, η περιστασιακή παραγωγή γάλακτος από τους αδένες, μπορεί να εμφανιστεί σε οποιοδήποτε θηλαστικό, αλλά στα περισσότερα θηλαστικά, η γαλουχία, η παραγωγή αρκετού γάλακτος για θηλασμό, εμφανίζεται μόνο σε φαινοτυπικά θηλυκά που έχουν κυοφορήσει τους τελευταίους μήνες ή χρόνια. Κατευθύνεται με ορμονική καθοδήγηση από τα σεξουαλικά στεροειδή. Σε λίγα είδη θηλαστικών, μπορεί να εμφανιστεί αρσενική γαλουχία. Στους ανθρώπους, ο αρσενικός θηλασμός μπορεί να συμβεί μόνο υπό συγκεκριμένες συνθήκες.
Τα θηλαστικά χωρίζονται σε 3 ομάδες: πρωτοθήρια, μεταθήρια και ευθήρια. Στην περίπτωση των πρωτοθήριων, τόσο τα αρσενικά όσο και τα θηλυκά έχουν λειτουργικούς μαστικούς αδένες, αλλά οι μαστικοί αδένες τους είναι χωρίς θηλές. Αυτοί οι μαστικοί αδένες είναι τροποποιημένοι σμηγματογόνοι αδένες. Όσον αφορά τα μεταθήρια και τα ευθήρια, μόνο τα θηλυκά έχουν λειτουργικούς μαστικούς αδένες. Οι μαστικοί αδένες τους μπορούν να ονομαστούν μαστοί. Μπορεί ο κάθε μαστικός αδένας να έχει τη δική του θηλή (π.χ. ανθρώπινοι μαστικοί αδένες) ή τα ζεύγη των μαστικών αδένων να αποτελούν μια ενιαία μάζα, με περισσότερες από μία θηλές να κρέμονται από αυτήν. Για παράδειγμα, οι αγελάδες και οι βούβαλοι έχουν το καθένα έναν μαστό με τέσσερις θηλές, ενώ τα πρόβατα και οι κατσίκες έχουν το καθένα δύο θηλές που προεξέχουν από τον μαστό. Αυτοί οι μαστικοί αδένες είναι τροποποιημένοι ιδρωτοποιοί αδένες.
Δομή[Επεξεργασία | επεξεργασία κώδικα]
Τα βασικά συστατικά ενός ώριμου μαστικού αδένα είναι οι κυψελίδες (κούφιες κοιλότητες, μεγέθους μερικών χιλιοστών), οι οποίες είναι επενδεδυμένες με κυβοειδή κύτταρα που εκκρίνουν γάλα και περιβάλλονται από μυοεπιθηλιακά κύτταρα. Αυτές οι κυψελίδες ενώνονται για να σχηματίσουν ομάδες γνωστές ως λοβούς. Κάθε λοβός έχει έναν γαλακτοφόρο αγωγό που παροχετεύεται σε ανοίγματα στη θηλή. Τα μυοεπιθηλιακά κύτταρα συστέλλονται υπό τη διέγερση της ωκυτοκίνης, αποβάλλοντας το γάλα που εκκρίνεται από τις κυψελιδικές μονάδες στον αυλό του λοβού προς τη θηλή. Καθώς το βρέφος αρχίζει να πιπιλάει, ακολουθεί το «αντανακλαστικό απελευθέρωσης» που προκαλείται από την ωκυτοκίνη και εκκρίνεται το μητρικό γάλα. — δεν αναρροφάται — από τον αδένα στο στόμα του μωρού.[1]
Όλος ο ιστός που εκκρίνει το γάλα που οδηγεί σε έναν μόνο γαλακτοφόρο πόρο ονομάζεται συλλογικά «απλός μαστικός αδένας». σε έναν «σύνθετο μαστικό αδένα», όλοι οι απλοί μαστικοί αδένες εξυπηρετούν μία θηλή. Οι άνθρωποι έχουν συνήθως δύο σύνθετους μαστικούς αδένες, έναν σε κάθε μαστό, και κάθε σύνθετος μαστικός αδένας αποτελείται από 10-20 απλούς αδένες. Το άνοιγμα κάθε απλού αδένα στην επιφάνεια της θηλής ονομάζεται «πόρος».[2] Η παρουσία περισσότερων από δύο θηλών είναι γνωστή ως πολυθηλία και η παρουσία περισσότερων από δύο πολύπλοκων μαστικών αδένων ως πολυμαστία.
Η διατήρηση της σωστής πολωμένης μορφολογίας του δέντρου του γαλακτοφόρου πόρου απαιτεί ένα άλλο βασικό συστατικό - την εξωκυτταρική μήτρα (ΕΚΜ) των επιθηλιακών κυττάρων του μαστού που, μαζί με τα λιποκύτταρα, τους ινοβλάστες, τα φλεγμονώδη κύτταρα και άλλα, αποτελούν το στρώμα του μαστού. [3] Η ΕΚΜ του επιθηλίου του μαστού περιέχει κυρίως τη μυοεπιθηλιακή βασική μεμβράνη και τον συνδετικό ιστό. Δεν βοηθούν μόνο στην υποστήριξη της βασικής δομής του μαστού, αλλά χρησιμεύουν επίσης ως γέφυρα επικοινωνίας μεταξύ του επιθηλίου του μαστού και του περιβάλλοντος του καθ' όλη τη διάρκεια της ανάπτυξης αυτού του οργάνου.[4][5]
Ιστολογία[Επεξεργασία | επεξεργασία κώδικα]

Ο μαστικός αδένας είναι ειδικός τύπος αποκρινών αδένων που ειδικεύεται στην παραγωγή πρωτογάλακτος κατά τον τοκετό. Οι μαστικοί αδένες μπορούν να αναγνωριστούν ως αποκρινείς επειδή εμφανίζουν έκκριση «αποκεφαλισμού». Πολλές πηγές υποστηρίζουν ότι οι μαστικοί αδένες είναι τροποποιημένοι ιδρωτοποιοί αδένες.[6][7][8] Μερικοί συγγραφείς το αμφισβητούν και υποστηρίζουν ότι είναι σμηγματογόνοι αδένες.[6]
Ανάπτυξη[Επεξεργασία | επεξεργασία κώδικα]
Οι μαστικοί αδένες αναπτύσσονται κατά τη διάρκεια διαφορετικών κύκλων ανάπτυξης. Υπάρχουν και στα δύο φύλα κατά το εμβρυϊκό στάδιο, σχηματίζοντας μόνο ένα στοιχειώδες δέντρο αγωγών κατά τη γέννηση. Σε αυτό το στάδιο, η ανάπτυξη του μαστικού αδένα εξαρτάται από τις συστημικές (και τις μητρικές) ορμόνες,[3] αλλά είναι επίσης υπό την (τοπική) ρύθμιση της παρακρινής επικοινωνίας μεταξύ γειτονικών επιθηλιακών και μεσεγχυματικών κυττάρων από την σχετιζόμενη με την παραθυρεοειδική ορμόνη πρωτεΐνη (PTHrP).[9] Αυτός ο τοπικά εκκρινόμενος παράγοντας προκαλεί μια σειρά θετικών ανατροφοδοτήσεων από έξω και μέσα προς τα έξω μεταξύ αυτών των δύο τύπων κυττάρων, έτσι ώστε τα επιθηλιακά κύτταρα των μαστών να μπορούν να πολλαπλασιαστούν και να αναπτυχθούν προς τα κάτω στο μεσεγχυματικό στρώμα μέχρι να φτάσουν στο λίπος για να ξεκινήσουν πρώτος γύρος διακλάδωσης.[3] Ταυτόχρονα, τα εμβρυϊκά μεσεγχυματικά κύτταρα γύρω από την επιθηλιακή μάζα δέχονται παράγοντες έκκρισης που ενεργοποιούνται από την PTHrP, όπως το BMP4. Αυτά τα μεσεγχυματικά κύτταρα μπορούν να μετατραπούν σε ένα πυκνό, ειδικό για το μαστό μεσέγχυμα, το οποίο αργότερα εξελίσσεται σε συνδετικό ιστό με ινώδη νήματα, σχηματίζοντας αιμοφόρα αγγεία και το λεμφικό σύστημα.[10] Η βασική μεμβράνη, που περιέχει κυρίως λαμινίνη και κολλαγόνο, που σχηματίζεται στη συνέχεια από διαφοροποιημένα μυοεπιθηλιακά κύτταρα, διατηρεί την πολικότητα αυτού του κύριου δέντρου αγωγού. Αυτά τα συστατικά της εξωκυτταρικής μήτρας είναι ισχυροί καθοριστικοί παράγοντες της μορφογένεσης του πόρου.[11]
Βιοχημεία[Επεξεργασία | επεξεργασία κώδικα]
Τα οιστρογόνα και η αυξητική ορμόνη (GH) είναι απαραίτητα για την ανάπτυξη του πόρου του μαστικού αδένα και δρουν συνεργικά για να το μεσολαβήσουν.[12][13][14][15][16] Ούτε τα οιστρογόνα ούτε η GH είναι ικανά να επάγουν την ανάπτυξη του πόρου από μόνα τους.[13][14][15][16] Ο ρόλος της GH στην ανάπτυξη του πόρου έχει βρεθεί ότι μεσολαβείται κυρίως από την επαγωγή της έκκρισης του αυξητικού παράγοντα 1 που μοιάζει με ινσουλίνη (IGF-1), ο οποίος εμφανίζεται τόσο συστηματικά (κυρίως προερχόμενος από το ήπαρ) όσο και τοπικά στο μαστικό λίπος μέσω της ενεργοποίησης του υποδοχέα αυξητικής ορμόνης (GHR).[13][14][15][16][17] Ωστόσο, η ίδια η GH δρα επίσης ανεξάρτητα από τον IGF-1 για να διεγείρει την ανάπτυξη του πόρου ρυθμίζοντας προς τα πάνω την έκφραση του υποδοχέα οιστρογόνου (ER) στον ιστό του μαστικού αδένα, η οποία είναι μια κατάντη επίδραση της ενεργοποίησης της GHR του μαστικού αδένα.[16] Σε κάθε περίπτωση, σε αντίθεση με τον IGF-1, η ίδια η GH δεν είναι απαραίτητη για την ανάπτυξη του μαστικού αδένα και ο IGF-1 σε συνδυασμό με τα οιστρογόνα μπορεί να προκαλέσει φυσιολογική ανάπτυξη μαστικού αδένα χωρίς την παρουσία GH.[16] Εκτός από τον IGF-1, άλλοι παρακρινικοί αυξητικοί παράγοντες όπως ο επιδερμικός αυξητικός παράγοντας (EGF), ο αυξητικός παράγοντας μετασχηματισμού βήτα (TGF-β),[18] η αμφιρεγκουλίνη,[19] ο αυξητικός παράγοντας ινοβλαστών (FGF) και ο αυξητικός παράγοντας ηπατοκυττάρων (HGF)[20] εμπλέκονται στην ανάπτυξη του μαστού ως μεσολαβητές κατάντη των ορμονών του φύλου και της GH/IGF-1.[21][22][23]
Κατά τη διάρκεια της εμβρυϊκής ανάπτυξης, τα επίπεδα IGF-1 είναι χαμηλά και σταδιακά αυξάνονται από τη γέννηση έως την εφηβεία.[24] Στην εφηβεία, τα επίπεδα της GH και του IGF-1 φτάνουν στα υψηλότερα επίπεδα στη ζωή και τα οιστρογόνα αρχίζουν να εκκρίνονται σε υψηλές ποσότητες στις γυναίκες, οπότε λαμβάνει χώρα κυρίως η ανάπτυξη των πόρων.[24] Υπό την επίδραση των οιστρογόνων, αναπτύσσεται επίσης στρωματικός και λιπώδης ιστός που περιβάλλει το σύστημα του πόρου στους μαστικούς αδένες.[25] Μετά την εφηβεία, τα επίπεδα GH και IGF-1 μειώνονται προοδευτικά, γεγονός που περιορίζει την περαιτέρω ανάπτυξη μέχρι την εγκυμοσύνη, εάν συμβεί.[24] Κατά τη διάρκεια της εγκυμοσύνης, η προγεστερόνη και η προλακτίνη είναι απαραίτητες για τη διαμεσολάβηση της λοβοκυψελιδικής ανάπτυξης στον ιστό του μαστικού αδένα, η οποία εμφανίζεται κατά την προετοιμασία της γαλουχίας και του θηλασμού.[12] [26]
Τα ανδρογόνα όπως η τεστοστερόνη αναστέλλουν την ανάπτυξη των μαστικών αδένων με τη μεσολάβηση οιστρογόνων (π.χ. μειώνοντας την τοπική έκφραση υποδοχέων οιστρογόνων) μέσω της ενεργοποίησης των υποδοχέων ανδρογόνων που εκφράζονται στον ιστό του μαστικού αδένα[26][27] και σε συνδυασμό με σχετικά χαμηλά επίπεδα οιστρογόνων, είναι η αιτία η έλλειψη αναπτυγμένων μαστικών αδένων στους άνδρες.[28]
Χρονοδιάγραμμα[Επεξεργασία | επεξεργασία κώδικα]
Πριν τη γέννηση[Επεξεργασία | επεξεργασία κώδικα]
Η ανάπτυξη του μαστικού αδένα χαρακτηρίζεται από τη μοναδική διαδικασία κατά την οποία το επιθήλιο εισβάλλει στο στρώμα. Η ανάπτυξη του μαστικού αδένα συμβαίνει κυρίως μετά τη γέννηση. Κατά την εφηβεία, ο σχηματισμός σωληναρίων μαζί με τη διακλαδούμενη μορφογένεση δημιουργεί το βασικό κυψελιδικό δίκτυο αγωγών που ξεκινάει από τη θηλή.[29]
Αναπτυξιακά, το επιθήλιο του μαστικού αδένα παράγεται και διατηρείται συνεχώς από σπάνια επιθηλιακά κύτταρα, που ονομάζονται πρόγονοι του μαστού, τα οποία τελικά πιστεύεται ότι προέρχονται από βλαστοκύτταρα που βρίσκονται στον ιστό.[30]
Η ανάπτυξη του εμβρυϊκού μαστικού αδένα μπορεί να χωριστεί σε μια σειρά από συγκεκριμένα στάδια. Αρχικά, ο σχηματισμός των γαλακτικών γραμμών που εκτείνονται μεταξύ του μπροστινού και του οπίσθιου άκρου αμφίπλευρα σε κάθε πλευρά της μέσης γραμμής συμβαίνει γύρω στην εμβρυϊκή ημέρα 10,5 (Ε10,5). Το δεύτερο στάδιο εμφανίζεται στην E11.5 όταν αρχίζει ο σχηματισμός των πλακωδών κατά μήκος της γραμμής της μαστικής γαλακτικής γραμμής. Αυτό τελικά θα δημιουργήσει τη θηλή. Τέλος, το τρίτο στάδιο συμβαίνει την E12,5 και περιλαμβάνει την εισβολή κυττάρων εντός του πλακώδιους στο μεσέγχυμα.[31]
Ανάπτυξη[Επεξεργασία | επεξεργασία κώδικα]
Μεταγεννητικά, οι μαστικοί πόροι επιμηκύνονται μέσα στο μαστικό λίπος. Στη συνέχεια, ξεκινώντας περίπου από την ηλικία των τεσσάρων εβδομάδων, η ανάπτυξη του μαστικού πόρου αυξάνεται σημαντικά με τους πόρους να εισβάλλουν προς τον λεμφαδένα. Οι τερματικοί οφθαλμοί, οι εξαιρετικά πολλαπλασιαστικές δομές που βρίσκονται στις άκρες των αγωγών εισβολής, διαστέλλονται και αυξάνονται πολύ σε αυτό το στάδιο. Αυτή η αναπτυξιακή περίοδος χαρακτηρίζεται από την εμφάνιση των τερματικών ακραίων οφθαλμών και διαρκεί μέχρι την ηλικία των 7-8 εβδομάδων περίπου.
Μέχρι το στάδιο της εφηβείας, οι μαστικοί πόροι έχουν εισβάλει μέχρι το τέλος του μαστικού λίπους. Σε αυτό το σημείο, οι τερματικοί ακραίοι οφθαλμοί γίνονται λιγότερο πολλαπλασιαστικοί και μειώνονται σε μέγεθος. Οι πλευρικοί κλάδοι σχηματίζονται από τους πρωτεύοντες αγωγούς και αρχίζουν να γεμίζουν το μαστικό λίπος. Η ανάπτυξη του πόρου μειώνεται με την άφιξη της σεξουαλικής ωριμότητας και υπόκειται σε κύκλους οίστρου (προοίστρος, οίστρος, μήτεστρος και δίοιστρος). Ως αποτέλεσμα του κύκλου του οίστρου, ο μαστικός αδένας υφίσταται δυναμικές αλλαγές όπου τα κύτταρα πολλαπλασιάζονται και στη συνέχεια υποχωρούν με τάξη.[32]
Εγκυμοσύνη[Επεξεργασία | επεξεργασία κώδικα]
Κατά τη διάρκεια της εγκυμοσύνης, τα συστήματα του πόρου υφίστανται ταχύ πολλαπλασιασμό και σχηματίζουν κυψελιδικές δομές εντός των κλάδων που θα χρησιμοποιηθούν για την παραγωγή γάλακτος. Μετά τον τοκετό, η γαλουχία εμφανίζεται εντός του μαστικού αδένα. Η γαλουχία περιλαμβάνει την έκκριση γάλακτος από τα κύτταρα του αυλού των κυψελίδων. Η συστολή των μυοεπιθηλιακών κυττάρων που περιβάλλουν τις κυψελίδες προκαλεί την εξώθηση του γάλακτος μέσω των αγωγών στη θηλή για το βρέφος που θηλάζει. Με τον απογαλακτισμό του βρέφους, η γαλουχία σταματά και ο μαστικός αδένας υποστρέφει μόνος του, μια διαδικασία που ονομάζεται ενέλιξη. Αυτή η διαδικασία περιλαμβάνει την ελεγχόμενη κατάρρευση των μαστικών επιθηλιακών κυττάρων όπου τα κύτταρα αρχίζουν την απόπτωση με ελεγχόμενο τρόπο, επαναφέροντας τον μαστικό αδένα πίσω σε εφηβική κατάσταση.
Μετεμμηνοπαυσιακή[Επεξεργασία | επεξεργασία κώδικα]
Κατά τη μετεμμηνόπαυση, λόγω πολύ χαμηλότερων επιπέδων οιστρογόνων και λόγω χαμηλότερων επιπέδων GH και IGF-1, τα οποία μειώνονται με την ηλικία, ο ιστός του μαστικού αδένα ατροφεί και οι μαστικοί αδένες γίνονται μικρότεροι.
Φυσιολογία[Επεξεργασία | επεξεργασία κώδικα]
Ορμονικός έλεγχος[Επεξεργασία | επεξεργασία κώδικα]
Η ανάπτυξη του γαλακτοφόρου πόρου εμφανίζεται στα θηλυκά ως απόκριση στις ορμόνες που κυκλοφορούν. Η πρώτη ανάπτυξη παρατηρείται συχνά κατά τα προγεννητικά και μεταγεννητικά στάδια και αργότερα κατά την εφηβεία. Τα οιστρογόνα προάγουν τη διαφοροποίηση διακλάδωσης,[33] ενώ στους άνδρες η τεστοστερόνη την αναστέλλει. Ένα ώριμο δέντρο αγωγών που φτάνει στο όριο του λίπους του μαστικού αδένα δημιουργείται με διχασμό των τερματικών ακραίων οφθαλμών των αγωγών, δευτερευόντων κλαδιών που φυτρώνουν από πρωτεύοντες αγωγούς[4][34] και κατάλληλο σχηματισμό του αυλού. Αυτές οι διεργασίες ρυθμίζονται στενά από συστατικά της ECM του επιθηλίου του μαστού που αλληλεπιδρούν με συστηματικές ορμόνες και τοπικούς εκκριτικούς παράγοντες. Ωστόσο, για κάθε μηχανισμό η «κόγχη» των επιθηλιακών κυττάρων μπορεί να είναι λεπτεπίλεπτα μοναδική με διαφορετικά προφίλ υποδοχέα μεμβράνης και πάχος βασικής μεμβράνης από συγκεκριμένη περιοχή διακλάδωσης σε περιοχή, έτσι ώστε να ρυθμίζεται η κυτταρική ανάπτυξη ή διαφοροποίηση υποτοπικά.[35] Σημαντικοί παράγοντες περιλαμβάνουν τη βήτα-1 ιντεγκρίνη, τον υποδοχέα του επιδερμικού αυξητικού παράγοντα (EGFR), τη λαμινίνη-1/5, το κολλαγόνο-IV, τη μεταλλοπρωτεϊνάση μήτρας (MMPs), τις πρωτεογλυκάνες θειικής ηπαράνης και άλλα. Τα αυξημένα επίπεδα κυκλοφορούσας αυξητικής ορμόνης και οιστρογόνων φτάνουν στα πολυδύναμα κύτταρα στα άκρα των οφθαλμών μέσω ενός λεπτού στρώματος βασικής μεμβράνης με διαρροή. Αυτές οι ορμόνες προάγουν συγκεκριμένη γονιδιακή έκφραση. Ως εκ τούτου, τα κύτταρα μπορούν να διαφοροποιηθούν σε επιθηλιακά κύτταρα μυοεπιθηλίου και αυλού (αγωγού) και η αυξημένη ποσότητα ενεργοποιημένων MMPs μπορεί να υποβαθμίσει τη περιβάλλουσα ΕΚΜ βοηθώντας τους οφθαλμούς του αγωγού να φτάσουν περαιτέρω στα επιθέματα λίπους.[36][37] Από την άλλη πλευρά, η βασική μεμβράνη κατά μήκος των ώριμων μαστικών αγωγών είναι παχύτερη, με ισχυρή πρόσφυση στα επιθηλιακά κύτταρα μέσω δέσμευσης σε υποδοχείς ιντεγκρίνης και μη. Όταν αναπτύσσονται πλευρικοί κλάδοι, είναι μια πολύ πιο «ώθηση προς τα εμπρός» διαδικασία εργασίας που περιλαμβάνει την επέκταση μέσω των μυοεπιθηλιακών κυττάρων, την υποβάθμιση της βασικής μεμβράνης και στη συνέχεια την εισβολή σε ένα περιαγωγικό στρώμα ινώδους στρωματικού ιστού.[4] Τα υποβαθμισμένα θραύσματα βασικής μεμβράνης (λαμινίνη-5) παίζουν ρόλο στη μετανάστευση των μαστικών επιθηλιακών κυττάρων.[38] Ενώ, η λαμινίνη-1 αλληλεπιδρά με τη δυστρογλυκάνη του υποδοχέα μη ιντεγκρίνης ρυθμίζει αρνητικά αυτή τη διαδικασία πλευρικής διακλάδωσης σε περίπτωση καρκίνου.[39] Αυτές οι πολύπλοκες διαφωνίες εξισορρόπησης «Γιν-γιανγκ» μεταξύ της ΕΚΜ του μαστού και των επιθηλιακών κυττάρων «οδηγούν» την υγιή ανάπτυξη του μαστικού αδένα μέχρι την ενηλικίωση.
Εγκυμοσύνη[Επεξεργασία | επεξεργασία κώδικα]
Οι εκκριτικές κυψελίδες αναπτύσσονται κυρίως στην εγκυμοσύνη, όταν τα αυξημένα επίπεδα προλακτίνης, οιστρογόνων και προγεστερόνης προκαλούν περαιτέρω διακλάδωση, μαζί με αύξηση του λιπώδους ιστού και πλουσιότερη ροή αίματος. Κατά την κύηση, η προγεστερόνη του ορού παραμένει σε σταθερά υψηλή συγκέντρωση, έτσι η σηματοδότηση μέσω του υποδοχέα της ενεργοποιείται συνεχώς. Ως ένα από τα μεταγραφέντα γονίδια, τα Wnts που εκκρίνονται από τα επιθηλιακά κύτταρα του μαστού δρουν παρακρινικά για να επάγουν διακλάδωση περισσότερων γειτονικών κυττάρων.[40][41] Όταν το δέντρο του γαλακτοφόρου αγωγού είναι σχεδόν έτοιμο, οι κυψελίδες διαφοροποιούνται από τα επιθηλιακά κύτταρα του αυλού και προστίθενται στο τέλος κάθε κλάδου. Στο τέλος της εγκυμοσύνης και τις πρώτες μέρες μετά τον τοκετό, εκκρίνεται πρωτόγαλα. Η έκκριση γάλακτος (γαλουχία) ξεκινά λίγες μέρες αργότερα λόγω της μείωσης της κυκλοφορούσας προγεστερόνης και της παρουσίας μιας άλλης σημαντικής ορμόνης προλακτίνης, η οποία μεσολαβεί στην περαιτέρω κυψελογένεση, την παραγωγή πρωτεΐνης γάλακτος και ρυθμίζει την οσμωτική ισορροπία και τη λειτουργία σφιχτού συνδέσμου. Η λαμινίνη και το κολλαγόνο στη βασική μεμβράνη του μυοεπιθηλίου που αλληλεπιδρούν ξανά με τη βήτα-1 ιντεγκρίνη στην επιθηλιακή επιφάνεια είναι απαραίτητα σε αυτή τη διαδικασία.[42][43] Η σύνδεσή τους διασφαλίζει τη σωστή τοποθέτηση των υποδοχέων προλακτίνης στη βασική πλάγια πλευρά των κυψελιδικών κυττάρων και την κατευθυντική έκκριση γάλακτος στους γαλακτοφόρους αγωγούς.[42][43] Ο θηλασμός του μωρού προκαλεί απελευθέρωση της ορμόνης ωκυτοκίνης, η οποία διεγείρει τη συστολή των μυοεπιθηλιακών κυττάρων. Σε αυτόν τον συνδυασμένο έλεγχο από την ΕΚΤ και τις συστηματικές ορμόνες, η έκκριση γάλακτος μπορεί να ενισχυθεί αμοιβαία, ώστε να παρέχεται επαρκής διατροφή στο μωρό.
Απογαλακτισμός[Επεξεργασία | επεξεργασία κώδικα]
Κατά τον απογαλακτισμό, η μειωμένη προλακτίνη, η έλλειψη μηχανικής διέγερσης (θηλασμός του μωρού) και οι αλλαγές στην οσμωτική ισορροπία που προκαλούνται από τη στάση του γάλακτος και τη διαρροή των σφιχτών συνδέσμων προκαλούν διακοπή της παραγωγής γάλακτος. Είναι η (παθητική) διαδικασία ενός παιδιού ή ζώου που παύει να εξαρτάται από τη μητέρα για τροφή. Σε ορισμένα είδη υπάρχει πλήρης ή μερική υποστροφή των κυψελιδικών δομών μετά τον απογαλακτισμό, στους ανθρώπους υπάρχει μόνο μερική υποστροφή και το επίπεδο της υποστροφής στους ανθρώπους φαίνεται να είναι εξαιρετικά ατομικό. Οι αδένες του μαστού εκκρίνουν υγρό και σε μη θηλάζουσες γυναίκες.[44] Σε ορισμένα άλλα είδη (όπως οι αγελάδες), όλες οι δομές των κυψελίδων και του εκκριτικού πόρου καταρρέουν λόγω προγραμματισμένου κυτταρικού θανάτου (απόπτωση) και αυτοφαγίας λόγω έλλειψης παραγόντων που προωθούν την ανάπτυξη είτε από την ΕΚΜ είτε από τις κυκλοφορούσες ορμόνες.[45][46] Ταυτόχρονα, η απόπτωση των ενδοθηλιακών κυττάρων του τριχοειδούς αίματος επιταχύνει την παλινδρόμηση των πόρων της γαλουχίας. Η συρρίκνωση του δέντρου του μαστικού πόρου και η αναδιαμόρφωση της ΕΚΜ από διάφορες πρωτεϊνάσες είναι υπό τον έλεγχο της σωματοστατίνης και άλλων ορμονών αναστολής της ανάπτυξης και τοπικών παραγόντων.[47] Αυτή η σημαντική δομική αλλαγή οδηγεί τον χαλαρό λιπώδη ιστό να γεμίσει τον κενό χώρο στη συνέχεια. Αλλά ένα λειτουργικό δέντρο γαλακτοφόρου αγωγού μπορεί να σχηματιστεί ξανά όταν ένα θηλυκό είναι ξανά έγκυος.
Κλινική σημασία[Επεξεργασία | επεξεργασία κώδικα]
Η ογκογένεση στους μαστικούς αδένες μπορεί να προκληθεί βιοχημικά από μη φυσιολογικό επίπεδο έκφρασης των κυκλοφορούντων ορμονών ή τοπικών συστατικών της ΕΚΜ,[48] ή από μια μηχανική αλλαγή στην τάση του στρώματος του μαστού. Κάτω από οποιαδήποτε από τις δύο περιπτώσεις, τα επιθηλιακά κύτταρα του μαστού θα αναπτύσσονταν ανεξέλεγκτα και τελικά θα αναπτυχθεί καρκίνος. Σχεδόν όλες οι περιπτώσεις καρκίνου του μαστού προέρχονται από τους λοβούς ή τους πόρους των μαστικών αδένων.
Άλλα θηλαστικά[Επεξεργασία | επεξεργασία κώδικα]
Το στήθος των θηλυκών ανθρώπων διαφέρει από τα περισσότερα άλλα θηλαστικά που τείνουν να έχουν λιγότερο ευδιάκριτους μαστικούς αδένες. Ο αριθμός και η θέση των μαστικών αδένων ποικίλλει ευρέως στα διάφορα θηλαστικά. Οι προεξέχουσες θηλές και οι συνοδευτικοί αδένες μπορούν να βρίσκονται οπουδήποτε κατά μήκος των δύο γαλακτικών γραμμών. Γενικά, τα περισσότερα θηλαστικά αναπτύσσουν μαστικούς αδένες σε ζεύγη κατά μήκος αυτών των γραμμών, με έναν αριθμό που προσεγγίζει τον αριθμό των νεαρών που γεννιούνται συνήθως κάθε φορά. Ο αριθμός των θηλών ποικίλλει από 2 (στα περισσότερα πρωτεύοντα) έως 18 (στους χοίρους). Το οπόσουμ της Βιρτζίνια έχει 13, ένα από τα λίγα θηλαστικά με περιττό αριθμό.[49][50] Ο παρακάτω πίνακας παραθέτει τον αριθμό και τη θέση των θηλών και των αδένων που βρίσκονται σε μια σειρά από θηλαστικά:
| Είδος [51] | Πρόσθιοι (θωρακικοί) |
Ενδιάμεσοι (κοιλιακοί) | Οπίσθιοι (βουβωνική) | Σύνολο |
|---|---|---|---|---|
| Κατσίκα, πρόβατο, άλογο ινδικό χοιρίδιο |
0 | 0 | 2 | 2 |
| Βοοειδή | 0 | 0 | 4 | 4 |
| Γάτα | 2 | 2 | 4 | 8 |
| Σκύλος | 4 | 2 | 2 ή 4 | 8 ή 10 |
| Ποντίκι | 6 | 0 | 4 | 10 |
| Αρουραίος | 6 | 2 | 4 | 12 |
| Χοίρος | 6 | 6 | 6 | 18 |
| Προβοσκοειδή, πρωτεύοντα | 2 | 0 | 0 | 2 |
| Οπόσουμ της Βιρτζίνια[49][50] | 0 | 0 | 13 | 13 |
| Νότιο οπόσουμ με κόκκινη όψη[52] | 0 | 0 | 25 έως 27 | 25 έως 27 |
Τα αρσενικά θηλαστικά έχουν τυπικά υποτυπώδεις μαστικούς αδένες και θηλές, με λίγες εξαιρέσεις: τα αρσενικά ποντίκια δεν έχουν θηλές,[53] τα αρσενικά μαρσιποφόρα δεν έχουν μαστικούς αδένες[54] και τα αρσενικά άλογα δεν έχουν θηλές και μαστικούς αδένες. Η αρσενική νυχτερίδα φρούτων Dayak έχει γαλακτοφόρους μαστικούς αδένες.[55] Η αρσενική γαλουχία εμφανίζεται σπάνια σε ορισμένα είδη.[56]
Οι μαστικοί αδένες είναι πραγματικά εργοστάσια πρωτεϊνών[57] και αρκετά εργαστήρια έχουν κατασκευάσει διαγονιδιακά ζώα, κυρίως κατσίκες και αγελάδες, για να παράγουν πρωτεΐνες για φαρμακευτική χρήση.[58] Οι σύνθετες γλυκοπρωτεΐνες όπως τα μονοκλωνικά αντισώματα ή η αντιθρομβίνη δεν μπορούν να παραχθούν από γενετικά τροποποιημένα βακτήρια και η παραγωγή σε ζωντανά θηλαστικά είναι πολύ φθηνότερη από τη χρήση κυτταροκαλλιεργειών θηλαστικών.
Εξέλιξη[Επεξεργασία | επεξεργασία κώδικα]
Υπάρχουν πολλές θεωρίες για το πώς εξελίχθηκαν οι μαστικοί αδένες. Για παράδειγμα, πιστεύεται ότι ο μαστικός αδένας είναι ένας μεταμορφωμένος ιδρωτοποιός αδένας, που σχετίζεται στενότερα με τους αποκρινείς ιδρωτοποιούς αδένες.[59] Επειδή οι μαστικοί αδένες δεν απολιθώνονται καλά, η υποστήριξη τέτοιων θεωριών με απολιθώματα είναι δύσκολη. Πολλές από τις τρέχουσες θεωρίες βασίζονται σε συγκρίσεις μεταξύ ζώντων θηλαστικών- μονότρηματα, μαρσιποφόρα και ευθήρια. Μια θεωρία προτείνει ότι οι μαστικοί αδένες εξελίχθηκαν από αδένες που χρησιμοποιήθηκαν για να διατηρούν τα αυγά των πρώιμων θηλαστικών υγρά[60][61] και απαλλαγμένα από μόλυνση[62][63] (τα μονοτρήματα εξακολουθούν να γεννούν αυγά). Άλλες θεωρίες προτείνουν ότι οι πρώιμες εκκρίσεις χρησιμοποιήθηκαν απευθείας από εκκολαφθέντα μικρά[64] ή ότι οι εκκρίσεις χρησιμοποιήθηκαν από μικρά για να τους βοηθήσουν να προσανατολιστούν προς τις μητέρες τους.[65]
Εικόνες[Επεξεργασία | επεξεργασία κώδικα]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Newton, Michael; Newton, Niles Rumely (December 1948). «The let-down reflex in human lactation». The Journal of Pediatrics 33 (6): 698–704. doi:. PMID 18101061. https://archive.org/details/sim_journal-of-pediatrics_1948-12_33_6/page/698.
- ↑ Zucca-Matthes, Gustavo; Urban, Cícero; Vallejo, André (February 2016). «Anatomy of the nipple and breast ducts». Gland Surgery 5 (1): 32–36. doi:. ISSN 2227-684X. PMID 26855906.
- ↑ 3,0 3,1 3,2 Watson, C. J.; Khaled, W. T. (2008). «Mammary development in the embryo and adult: A journey of morphogenesis and commitment». Development 135 (6): 995–1003. doi:. PMID 18296651.
- ↑ 4,0 4,1 4,2 Wiseman, B. S.; Werb, Z. (2002). «Stromal Effects on Mammary Gland Development and Breast Cancer». Science 296 (5570): 1046–1049. doi:. PMID 12004111. Bibcode: 2002Sci...296.1046W.
- ↑ Pavlovich, A. L.; Manivannan, S.; Nelson, C. M. (2010). «Adipose Stroma Induces Branching Morphogenesis of Engineered Epithelial Tubules». Tissue Engineering Part A 16 (12): 3719–3726. doi:. PMID 20649458.
- ↑ 6,0 6,1 Ackerman (2005) ch.1 Apocrine Units Αρχειοθετήθηκε 21 April 2011 στο Wayback Machine.
- ↑ Moore (2010) ch.1 Thorax, p. 99
- ↑ Krstic, Radivoj V. (18 Μαρτίου 2004). Human Microscopic Anatomy: An Atlas for Students of Medicine and Biology. Springer. σελ. 466. ISBN 9783540536666.
- ↑ Wysolmerski, J. J.; Philbrick, W. M.; Dunbar, M. E.; Lanske, B.; Kronenberg, H.; Broadus, A. E. (1998). «Rescue of the parathyroid hormone-related protein knockout mouse demonstrates that parathyroid hormone-related protein is essential for mammary gland development». Development 125 (7): 1285–1294. doi:. PMID 9477327.
- ↑ Hens, J. R.; Wysolmerski, J. J. (2005). «Key stages of mammary gland development: Molecular mechanisms involved in the formation of the embryonic mammary gland». Breast Cancer Research 7 (5): 220–224. doi:. PMID 16168142.
- ↑ Montévil, Maël; Speroni, Lucia; Sonnenschein, Carlos; Soto, Ana M. (2016-10-01). «Modeling mammary organogenesis from biological first principles: Cells and their physical constraints». Progress in Biophysics and Molecular Biology. From the Century of the Genome to the Century of the Organism: New Theoretical Approaches 122 (1): 58–69. doi:. PMID 27544910.
- ↑ 12,0 12,1 Brisken; Malley (2 December 2010). «Hormone Action in the Mammary Gland». Cold Spring Harbor Perspectives in Biology 2 (12): a003178. doi:. PMID 20739412.
- ↑ 13,0 13,1 13,2 «Role of IGF-I in normal mammary development». Breast Cancer Res. Treat. 47 (3): 201–8. 1998. doi:. PMID 9516076. https://archive.org/details/sim_breast-cancer-research-and-treatment_1998-02_47_3/page/201.
- ↑ 14,0 14,1 14,2 «Early mammary development: growth hormone and IGF-1». J Mammary Gland Biol Neoplasia 2 (1): 49–57. 1997. doi:. PMID 10887519.
- ↑ 15,0 15,1 15,2 «Insulin-like growth factor I is essential for terminal end bud formation and ductal morphogenesis during mammary development». Endocrinology 140 (11): 5075–81. 1999. doi:. PMID 10537134.
- ↑ 16,0 16,1 16,2 16,3 16,4 «IGF-I: an essential factor in terminal end bud formation and ductal morphogenesis». J Mammary Gland Biol Neoplasia 5 (1): 7–17. 2000. doi:. PMID 10791764.
- ↑ «IGF-I, GH, and sex steroid effects in normal mammary gland development». J Mammary Gland Biol Neoplasia 13 (4): 353–60. 2008. doi:. PMID 19034633.
- ↑ «Mouse models of transforming growth factor beta impact in breast development and cancer». Endocr. Relat. Cancer 12 (4): 749–60. 2005. doi:. PMID 16322320.
- ↑ «Estrogen regulation of mammary gland development and breast cancer: amphiregulin takes center stage». Breast Cancer Res. 9 (4): 304. 2007. doi:. PMID 17659070.
- ↑ «Hepatocyte growth factor profile with breast cancer». Indian J Pathol Microbiol 54 (3): 509–13. 2011. doi:. PMID 21934211.
- ↑ Coad, Jane· Dunstall, Melvyn (2011). Anatomy and Physiology for Midwives. Elsevier Health Sciences. σελίδες 413–. ISBN 978-0-7020-3489-3.
- ↑ Hynes, N. E.; Watson, C. J. (2010). «Mammary Gland Growth Factors: Roles in Normal Development and in Cancer». Cold Spring Harbor Perspectives in Biology 2 (8): a003186. doi:. ISSN 1943-0264. PMID 20554705.
- ↑ Jay R. Harris· Marc E. Lippman (28 Μαρτίου 2012). Diseases of the Breast. Lippincott Williams & Wilkins. σελίδες 94–. ISBN 978-1-4511-4870-1.
- ↑ 24,0 24,1 24,2 «The potential clinical applications of insulin-like growth factor-1 ligand in human breast cancer». Anticancer Res. 27 (3B): 1617–24. 2007. PMID 17595785. http://ar.iiarjournals.org/cgi/pmidlookup?view=long&pmid=17595785.[νεκρός σύνδεσμος]
- ↑ Leonard R. Johnson (2003). Essential Medical Physiology. Academic Press. σελίδες 770–. ISBN 978-0-12-387584-6.
- ↑ 26,0 26,1 «Breast size in relation to endogenous hormone levels, body constitution, and oral contraceptive use in healthy nulligravid women aged 19–25 years». Am. J. Epidemiol. 145 (7): 571–80. 1997. doi:. PMID 9098173.
- ↑ «Testosterone inhibits estrogen-induced mammary epithelial proliferation and suppresses estrogen receptor expression». FASEB J. 14 (12): 1725–30. 2000. doi:. PMID 10973921. https://zenodo.org/record/1236080.
- ↑ «Gynecomastia in adolescent males». Semin Plast Surg 27 (1): 56–61. 2013. doi:. PMID 24872741.
- ↑ Sekhri, KK; Pitelka, DR; Deome, KB (Sep 1967). «Studies of mouse mammary glands. I. Cytomorphology of the normal mammary gland». J Natl Cancer Inst 39 (3): 459–90. PMID 6053715. https://archive.org/details/sim_journal-of-the-national-cancer-institute_1967-09_39_3/page/459.
- ↑ Tharmapalan, Pirashaanthy; Mahendralingam, Mathepan; Berman, Hal K; Khokha, Rama (2019-07-15). «Mammary stem cells and progenitors: targeting the roots of breast cancer for prevention». The EMBO Journal 38 (14): e100852. doi:. ISSN 0261-4189. PMID 31267556.
- ↑ Hens, JR; Wysolmerski JJ (10 August 2005). «Key stages of mammary gland development: molecular mechanisms involved in the formation of the embryonic mammary gland». Breast Cancer Res. 7 (5): 220–4. doi:. PMID 16168142.
- ↑ Daniel, CW; Smith, GH (January 1999). «The mammary gland: a model for development». Journal of Mammary Gland Biology and Neoplasia 4 (1): 3–8. doi:. PMID 10219902.
- ↑ Sternlicht, M. D. (2006). «Key stages in mammary gland development: The cues that regulate ductal branching morphogenesis». Breast Cancer Research 8 (1): 201–203. doi:. PMID 16524451.
- ↑ Sternlicht, M. D.; Kouros-Mehr, H.; Lu, P.; Werb, Z. (2006). «Hormonal and local control of mammary branching morphogenesis». Differentiation 74 (7): 365–381. doi:. PMID 16916375.
- ↑ Fata, J. E.; Werb, Z.; Bissell, M. J. (2003). «Regulation of mammary gland branching morphogenesis by the extracellular matrix and its remodeling enzymes». Breast Cancer Research 6 (1): 1–11. doi:. PMID 14680479.
- ↑ Wiseman, B. S.; Sternlicht, M. D.; Lund, L. R.; Alexander, C. M.; Mott, J.; Bissell, M. J.; Soloway, P.; Itohara, S. και άλλοι. (2003). «Site-specific inductive and inhibitory activities of MMP-2 and MMP-3 orchestrate mammary gland branching morphogenesis». The Journal of Cell Biology 162 (6): 1123–1133. doi:. PMID 12975354.
- ↑ Koshikawa, N.; Giannelli, G.; Cirulli, V.; Miyazaki, K.; Quaranta, V. (2000). «Role of cell surface metalloprotease MT1-MMP in epithelial cell migration over laminin-5». The Journal of Cell Biology 148 (3): 615–624. doi:. PMID 10662785.
- ↑ Dogic, D.; Rousselle, P.; Aumailley, M. (1998). «Cell adhesion to laminin 1 or 5 induces isoform-specific clustering of integrins and other focal adhesion components». Journal of Cell Science 111 (6): 793–802. doi:. PMID 9472007. http://jcs.biologists.org/content/111/6/793.full.pdf.
- ↑ Muschler, J.; Levy, D.; Boudreau, R.; Henry, M.; Campbell, K.; Bissell, M. J. (2002). «A role for dystroglycan in epithelial polarization: Loss of function in breast tumor cells». Cancer Research 62 (23): 7102–7109. PMID 12460932.
- ↑ Robinson, G. W.; Hennighausen, L.; Johnson, P. F. (2000). «Side-branching in the mammary gland: The progesterone-Wnt connection». Genes & Development 14 (8): 889–894. doi:. PMID 10783160.
- ↑ Brisken, C.; Heineman, A.; Chavarria, T.; Elenbaas, B.; Tan, J.; Dey, S. K.; McMahon, J. A.; McMahon, A. P. και άλλοι. (2000). «Essential function of Wnt-4 in mammary gland development downstream of progesterone signaling». Genes & Development 14 (6): 650–654. doi:. PMID 10733525.
- ↑ 42,0 42,1 Streuli, C. H.; Bailey, N.; Bissell, M. J. (1991). «Control of mammary epithelial differentiation: Basement membrane induces tissue-specific gene expression in the absence of cell-cell interaction and morphological polarity». The Journal of Cell Biology 115 (5): 1383–1395. doi:. PMID 1955479. PMC 2289247. https://archive.org/details/sim_journal-of-cell-biology_1991-12_115_5/page/1383.
- ↑ 43,0 43,1 Streuli, C. H.; Schmidhauser, C.; Bailey, N.; Yurchenco, P.; Skubitz, A. P.; Roskelley, C.; Bissell, M. J. (1995). «Laminin mediates tissue-specific gene expression in mammary epithelia». The Journal of Cell Biology 129 (3): 591–603. doi:. PMID 7730398. PMC 2120432. https://archive.org/details/sim_journal-of-cell-biology_1995-05_129_3/page/591.
- ↑ Nicholas L. Petrakis; Lynn Mason; Rose Lee; Barbara Sugimoto; Stella Pawson; Frank Catchpool (1975). «Association of Race, Age, Menopausal Status, and Cerumen Type With Breast Fluid Secretion in Nonlactating Women, as Determined by Nipple Aspiration». Journal of the National Cancer Institute 54: 829–834. doi:. PMID 1168727. https://archive.org/details/sim_journal-of-the-national-cancer-institute_1975-04_54_4/page/829.
- ↑ Zarzynska, J.; Motyl, T. (2008). «Apoptosis and autophagy in involuting bovine mammary gland». Journal of Physiology and Pharmacology 59 Suppl 9: 275–288. PMID 19261986.
- ↑ Fadok, V. A. (1999). «Clearance: The last and often forgotten stage of apoptosis». Journal of Mammary Gland Biology and Neoplasia 4 (2): 203–211. doi:. PMID 10426399.
- ↑ Motyl, T.; Gajkowska, B.; Zarzyńska, J.; Gajewska, M.; Lamparska-Przybysz, M. (2006). «Apoptosis and autophagy in mammary gland remodeling and breast cancer chemotherapy». Journal of Physiology and Pharmacology 57 Suppl 7: 17–32. PMID 17228094.
- ↑ Gudjonsson, T.; Rønnov-Jessen, L.; Villadsen, R.; Rank, F.; Bissell, M. J.; Petersen, O. W. (2002). «Normal and tumor-derived myoepithelial cells differ in their ability to interact with luminal breast epithelial cells for polarity and basement membrane deposition». Journal of Cell Science 115 (Pt 1): 39–50. doi:. PMID 11801722.
- ↑ 49,0 49,1 «With the Wild Things – Transcripts». Digitalcollections.fiu.edu. Αρχειοθετήθηκε από το πρωτότυπο στις 23 Μαρτίου 2013. Ανακτήθηκε στις 5 Απριλίου 2013.
- ↑ 50,0 50,1 Stockard, Mary (2005) Raising Orphaned Baby Opossums.
- ↑ Cunningham, Merle· LaTour, Mickey A. (2005). Animal Science and Industry. Pearson Prentice Hall. ISBN 978-0-13-046256-5.
- ↑ P Smith 2008 Red-Sided Short-Tailed Opossum.
- ↑ Julie Ann Mayer; John Foley; Damon De La Cruz; Cheng-Ming Chuong; Randall Widelitz (November 2008). «Conversion of the Nipple to Hair-Bearing Epithelia by Lowering Bone Morphogenetic Protein Pathway Activity at the Dermal-Epidermal Interface». Am J Pathol 173 (5): 1339–48. doi:. PMID 18832580.
- ↑ Patricia J. Armati· Chris R. Dickman (17 Αυγούστου 2006). Marsupials. Cambridge University Press. ISBN 978-1-139-45742-2.
- ↑ Francis, C. M.; Anthony, E. L. P.; Brunton, J. A.; Kunz, T. H. (1994). «Lactation in male fruit bats». Nature 367 (6465): 691–692. doi:. Bibcode: 1994Natur.367..691F. http://www.bu.edu/cecb/files/2009/08/lactationmale-fruit-bats.pdf.
- ↑ Kunz, T; Hosken, D (2009). «Male lactation: why, why not and is it care?». Trends in Ecology & Evolution 24 (2): 80–85. doi:. PMID 19100649.
- ↑ Li, Peng; Knabe, Darrell A.; Kim, Sung Woo; Lynch, Christopher J.; Hutson, Susan M.; Wu, Guoyao (2009-08-01). «Lactating Porcine Mammary Tissue Catabolizes Branched-Chain Amino Acids for Glutamine and Aspartate Synthesis» (στα αγγλικά). The Journal of Nutrition 139 (8): 1502–1509. doi:. ISSN 0022-3166. PMID 19549750. PMC 3151199. https://archive.org/details/sim_journal-of-nutrition_2009-08_139_8/page/1502.
- ↑ «BBC News – The goats with spider genes and silk in their milk». bbc.co.uk. 17 Ιανουαρίου 2012. Ανακτήθηκε στις 26 Απριλίου 2012.
- ↑ Oftedal, O. T. (2002). «The origin of lactation as a water source for parchment-shelled eggs». Journal of Mammary Gland Biology and Neoplasia 7 (3): 253–266. doi:. PMID 12751890.
- ↑ Lactating on Eggs.
- ↑ Oftedal, OT (2002). «The mammary gland and its origin during synapsid evolution». Journal of Mammary Gland Biology and Neoplasia 7 (3): 225–52. doi:. PMID 12751889.
- ↑ Breast beginnings. scienceblogs.com
- ↑ Vorbach, C.; Capecchi, M. R.; Penninger, J. M. (2006). «Evolution of the mammary gland from the innate immune system?». BioEssays 28 (6): 606–616. doi:. PMID 16700061.
- ↑ Lefèvre, C. M.; Sharp, J. A.; Nicholas, K. R. (2010). «Evolution of Lactation: Ancient Origin and Extreme Adaptations of the Lactation System». Annual Review of Genomics and Human Genetics 11: 219–238. doi:. PMID 20565255.
- ↑ Graves, B. M.; Duvall, D. (1983). «A Role for Aggregation Pheromones in the Evolution of Mammallike Reptile Lactation». The American Naturalist 122 (6): 835. doi:. https://archive.org/details/sim_american-naturalist_1983-12_122_6/page/835.
Βιβλιογραφία[Επεξεργασία | επεξεργασία κώδικα]
- Ackerman, A. Bernard· Almut Böer· Bruce Bennin· Geoffrey J. Gottlieb (2005). Histologic Diagnosis of Inflammatory Skin Diseases An Algorithmic Method Based on Pattern Analysis. ISBN 978-1-893357-25-9. Αρχειοθετήθηκε από το πρωτότυπο στις 21 Απριλίου 2011.
- Moore, Keith L. et al. (2010) Clinically Oriented Anatomy 6th Ed