Καταβύθιση

Καθίζηση ή καταβύθιση είναι η δημιουργία ενός στερεού σε ένα διάλυμα ή μέσα σε ένα άλλο στερεό κατά τη διάρκεια μιας χημικής αντίδρασης ή με διάχυση σε ένα στερεό. Όταν η αντίδραση συμβαίνει σε ένα υγρό διάλυμα, το σχηματιζόμενο στερεό λέγεται 'ίζημα'. Το χημικό που προκαλεί τον σχηματισμό στερεού λέγεται 'ιζηματοποιητής'. Χωρίς επαρκή δύναμη βαρύτητας (καθίζηση) για να οδηγήσει τα στερεά σωματίδια μαζί, το ίζημα παραμένει σε αιώρημα. Μετά την καταβύθιση, ειδικά όταν χρησιμοποιείται φυγοκέντριση για να συμπιεστεί σε συμπαγή μάζα, το ίζημα μπορεί να αναφέρεται ως 'συσσωμάτωμα'. Το υγρό ελεύθερο από ίζημα που παραμένει πάνω από το στερεό λέγεται υπερκείμενο. Οι σκόνες που παράγονται από καθίζηση είναι γνωστές επίσης ιστορικά ως 'άνθη'. Μερικές φορές ο σχηματισμός ενός ιζήματος δείχνει την ύπαρξη μιας χημικής αντίδρασης. Αν ένα διάλυμα νιτρικού αργύρου μεταγγιστεί σε ένα διάλυμα χλωριούχου νατρίου, συμβαίνει μια χημική αντίδραση σχηματισμού ενός λευκού ιζήματος του χλωριούχου αργύρου. Όταν ένα διάλυμα ιωδιούχου καλίου αντιδρά με διάλυμα νιτρικού μολύβδου, ένα κίτρινο ίζημα ιωδιούχου μολύβδου σχηματίζεται. Η καθίζηση μπορεί να συμβεί αν η συγκέντρωση μιας ένωσης υπερβεί τη διαλυτότητα της (όπως κατά την ανάμειξη διαλυτών ή αλλαγή της θερμοκρασίας τους). Η καθίζηση μπορεί να συμβεί γρήγορα από ένα υπερκορεσμένο διάλυμα.
Στα στερεά, η καθίζηση λαμβάνει χώρα αν η συγκέντρωση ενός στερεού είναι πάνω από το όριο διαλυτότητας, λόγω π.χ. της γρήγορης βαφής ή εμφύτευσης ιόντων και η θερμοκρασία είναι αρκετά ψηλή που η διάχυση μπορεί να οδηγήσει σε διχωρισμό σε ιζήματα. Η καθίζηση σε στερεά χρησιμοποιείται εκτενώς για τη σύνθεση νανοσωματιδίων.[1]
Ένα σημαντικό στάδιο της διεργασίας καθίζησης είναι η έναρξη της πυρήνωσης. Η δημιουργία ενός υποθετικού στερεού σωματιδίου περιλαμβάνει τον σχηματισμό μιας επιφάνειας συνεπαφής, που απαιτεί κάποια χημική ενέργεια με βάση τη σχετική επιφανειακή ενέργεια του στερεού και του διαλύματος. Αν αυτή η ενέργεια δεν είναι διαθέσιμη και δεν υπάρχει κατάλληλη επιφάνεια πυρήνωσης, συμβαίνει υπερκορεσμός.
Εφαρμογές[Επεξεργασία | επεξεργασία κώδικα]


Οι αντιδράσεις καθίζησης μπορούν να χρησιμοποιηθούν για τη δημιουργία χρωστικών ουσιών, αφαίρεση αλάτων από νερό σε επεξεργασία νερού και στην ποιοτική ανόργανη ανάλυση.
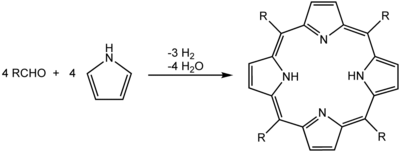
Η καθίζηση είναι επίσης χρήσιμη για απομόνωση των προϊόντων μιας αντίδρασης κατά τη διάρκεια μιας απομόνωσης και καθαρισμού. Ιδανικά, το προϊόν μιας αντίδρασης είναι αδιάλυτο στο διαλύτη της αντίδρασης. Συνεπώς, καθιζάνει καθώς σχηματίζεται, κατά προτίμηση με σχηματισμό καθαρών κρυστάλλων. Ένα παράδειγμα αυτού είναι η σύνθεση των πορφυρινών με αντιρροή προπανικού οξέος. Με ψύξη του μείγματος της αντίδρασης σε θερμοκρασία δωματίου, οι κρύσταλλοι της πορφυρίνης καθιζάνουν και συλλέγονται με διήθηση:[2]
Η καθίζηση μπορεί επίσης να συμβεί όταν προστίθεται ένας αντιδιαλύτης (ένας διαλύτης στον οποίο το προϊόν είναι αδιάλυτο), μειώνοντας δραστικά τη διαλυτότητα του επιθυμητού προϊόντος. Κατόπιν, το ίζημα μπορεί εύκολα να διαχωριστεί με διήθηση, απόχυση, ή φυγοκέντρηση). Ένα παράδειγμα είναι η σύνθεση της χλωριούχου χρωμικής τετραφαινυλοπορφυρίνης: προστίθεται νερό στο διάλυμα αντίδρασης DMF και το προϊόν καθιζάνει.[3] Η καθίζηση είναι επίσης χρήσιμη στον καθαρισμό προϊόντων: ακάθαρτο bmim-Cl αιθανονιτριλίου και προστίθεται σε αιθανικό αιθύλιο, όπου καθιζάνει.[4] Μια άλλη σημαντική εφαρμογή ενός αντιδιαλύτη είναι στην καθίζηση της αιθανόλης στο DNA.
Στην μεταλλουργία, η καθίζηση από ένα στερεό διάλυμα είναι επίσης ένας χρήσιμος τρόπος για να ενίσχυση κραμάτων· αυτή η διεργασία είναι γνωστή ως ισχυροποίηση στερεού διαλύματος.
Αναπαράσταση χρησιμοποιώντας χημικές εξισώσεις[Επεξεργασία | επεξεργασία κώδικα]
Ένα παράδειγμα αντίδρασης καθίζησης: Υδατικός νιτρικός άργυρος (AgNO3) προστίθεται σε διάλυμα που περιέχει χλωριούχο κάλιο (KCl), παρατηρείται η καθίζηση ενός λευκού στερεού χλωριούχου αργύρου (AgCl). (Zumdahl, 2005)
- AgNO3 (aq) + KCl (aq) → AgCl (s) + KNO3 (aq)
Ο χλωριούχος άργυρος (AgCl) έχει σχηματίσει ένα στερεό, που παρατηρείται ως ίζημα.
Αυτή η αντίδραση μπορεί να γραφτεί τονίζοντας τα διιστάμενα ιόντα σε ένα σύνθετο διάλυμα. Αυτό είναι γνωστό ως ιοντική εξίσωση.
- Ag+ (aq) + NO3− (aq) + K+ (aq) + Cl− (aq) → AgCl (s) + K+ (aq) + NO3− (aq)
Ένας άλλος τρόπος παρουσίασης μιας αντίδρασης καθίζησης είναι γνωστός ως καθαρή ιοντική αντίδραση. Σε αυτήν την περίπτωση, κάθε ιόν θεατής (αυτά που δεν συμμετέχουν στην αντίδραση) αφήνεται εκτός του τύπου πλήρως. Αυτό απλοποιεί τις παραπάνω εξισώσεις στην παρακάτω:
- Ag+ (aq) + Cl− (aq) → AgCl (s)
Χρώματα ιζημάτων[Επεξεργασία | επεξεργασία κώδικα]
Πολλές ενώσεις που περιέχουν μεταλλικά ιόντα παράγουν ιζήματα με ξεχωριστά χρώματα. Τα παρακάτω είναι τυπικά χρώματα για διάφορα μέταλλα. Όμως, πολλές από αυτές τις ενώσεις μπορούν να παραγάγουν χρώματα πολύ διαφορετικά από αυτά που αναφέρονται.
| Χρυσός | Πορτοκαλί |
| Χρώμιο | Βαθύ πράσινο, σκούρο πράσινο, πορτοκαλί, πορφυρό, κίτρινο, καφέ |
| Κοβάλτιο | Ροζ |
| Χαλκός | Γαλάζιο |
| Σίδηρος (II) | Πράσινο |
| Σίδηρος (III) | Κοκκινωπό καφετί |
| Μαγγάνιο | Ωχρό ροζ |
| Νικέλιο | Πράσινο |
Άλλες ενώσεις σχηματίζουν γενικά λευκά ιζήματα.
Ανάλυση ανιόντος/κατιόντος[Επεξεργασία | επεξεργασία κώδικα]
Ο σχηματισμός ιζήματος είναι χρήσιμος στην ανίχνευση του τύπου του κατιόντος σε ένα άλας. Για να γίνει αυτό, ένα άλκαλι αντιδρά πρώτα με το άγνωστο άλας για να παραγάγει ένα ίζημα που είναι το υδροξείδιο του άγνωστου άλατος. Για να ταυτοποιηθεί το κατιόν, σημειώνονται το χρώμα του ιζήματος και η διαλυτότητά του σε περίσσεια. Παρόμοιες διεργασίες χρησιμοποιούνται συχνά σε σειρά - π.χ., ένα διάλυμα νιτρικού βαρίου θα αντιδράσει με θειικά ιόντα για να σχηματίσει ένα στερεό ίζημα θειικού βαρίου, που δείχνει ότι είναι πιθανόν ότι τα θειικά ιόντα είναι παρόντα.
Χώνευση[Επεξεργασία | επεξεργασία κώδικα]
Χώνευση, ή πέψη ή γήρανση ιζήματος, συμβαίνει όταν ένα πρόσφατα δημιουργημένο ίζημα αφήνεται, συνήθως σε υψηλότερη θερμοκρασία, στο διάλυμα από το οποίο καταβυθίστηκε. Αυτό έχει ως αποτέλεσμα καθαρότερα και μεγαλύτερα σωματίδια. Η υποκείμενη φυσικοχημική διεργασία διεργασία χώνευσης λέγεται ωρίμανση Όστβαλντ.
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Dhara, S. (2007). «Formation, Dynamics, and Characterization of Nanostructures by Ion Beam Irradiation». Critical Reviews in Solid State and Materials Sciences 32 (1): 1–50. doi:.
- ↑ A. D. Adler; F. R. Longo; J. D. Finarelli; J. Goldmacher; J. Assour; L. Korsakoff (1967). «A simplified synthesis for meso-tetraphenylporphine». J. Org. Chem. 32 (2): 476–476. doi:.
- ↑ Alan D. Adler; Frederick R. Longo; Frank Kampas; Jean Kim (1970). «On the preparation of metalloporphyrins». Journal of Inorganic and Nuclear Chemistry 32 (7): 2443. doi:.
- ↑ Dupont, J., Consorti, C., Suarez, P., de Souza, R. (2004), «Preparation of 1-Butyl-3-methyl imidazolium-based Room Temperature Ionic Liquids», Org. Synth., http://www.orgsyn.org/orgsyn/orgsyn/prepContent.asp?prep=v79p0236; Coll. Vol. 10: 184
5. Precipitaion colours - From Chemistry For Wa Stage 2 Units 2a and 2b by Chris Lewis and Peter Lewis
Περαιτέρω μελέτη[Επεξεργασία | επεξεργασία κώδικα]
- Zumdahl, Steven S. (2005). Chemical Principles
 (5th έκδοση). New York: Houghton Mifflin. ISBN 0-618-37206-7.
(5th έκδοση). New York: Houghton Mifflin. ISBN 0-618-37206-7. - Smith, Mark (1993). Principles of Science.
Εξωτερικοί σύνδεσμοι[Επεξεργασία | επεξεργασία κώδικα]
- http://www.answers.com/supernatant
- Precipitation reactions of certain cations
- Digestion Instruments
- A Thesis on pattern formation in precipitation reactions
|