Ανόργανα βοράνια
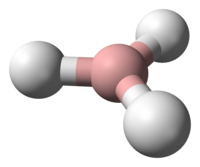


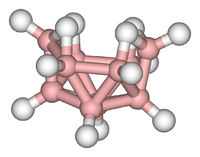

Τα «βοράνια» είναι μια σχετικά μεγάλη ομάδα χημικών ενώσεων με γενικό τύπο BxHy.[1] Καμμιά από αυτές τις ενώσεις δεν έχει βρεθεί στη φύση. Πολλά από τα βοράνια οξειδώνονται ταχύτατα όταν έρθουν σε επαφή με τον ατμοσφαιρικό αέρα, μερικά από τα οποία ακόμη και βίαια. Το πρώτο μέλος της σειράς, το βοράνιο, έχει απομονωθεί μόνο στην αέρια κατάσταση και διμερίζεται εύκολα σχηματίζοντας διβοράνιο(6). Τα μεγαλύτερου μοριακού βάρους βοράνια αποτελούνται από πολυατομικά επαναλαμβανόμενα συμπλέγματα που είναι πολυεδρικά και για μερικά μάλιστα υπάρχουν και ισομερή.
Τα πιο σημαντικά βοράνια είναι το διβοράνιο(6) (B2H6), το πενταβοράνιο (B5H9) και το δεκαβοράνιο (B10H14).
Η ανάπτυξη της χημείας των βορανίων οδήγησε σε νέες πειραματικές τεχνικές και θεωρίες. Έχουν μελετηθεί ως πιθανά μελλοντικά καύσιμα πυραύλων, αεροπλάνων και αυτοκινήτων.
Στα βοράνια περιλαμβάνονται εδώ και μερικές δεκαετίες και «ετεροβοράνια», δηλαδή ενώσεις που περιέχουν επίσης και άλλα (εκτός του βορίου και του υδρογόνου) χημικά στοιχεία, όπως μεταξύ άλλων ο άνθρακας (καρβοβοράνια) και διάφορα μέταλλα (μεταλλοβοράνια).
Ιστορία[Επεξεργασία | επεξεργασία κώδικα]
Η ανάπτυξη της χημείας των βορανίων έθεσε δυο προκλήσεις για τους χημικούς:
- Απαιτήθηκε η ανάπτυξη νέων εργαστηριακών τεχνικών για το χειρισμό τόσο δραστικών χημικών ενώαεων.
- Η διερεύνηση της δομής τους προκάλεσε τις υφιστάμενες θεωρίες για τους χημικούς δεσμούς.
Ο Γερμανός χημικός Alfred Stock πρώτος χαρακτήρησε τη σειρά των ενώσεων βορίου - υδρογόνου. Η ομάδα του ανέπτυξε τη γυάλινη γραμμή κενού και άλλες τεχνικές για το χειρισμό αυτών των ενώσεων. Ωστόσο, η έκθεση στον υδράργυρο (Hg) (που χρησιμοποίησε σε αντλίες διάχυσης και βαλβίδες επίπλευσης) προκάλεσε υδραργυρίαση (δηλητηρίαση από υδράργυρο) στον ίδιο το Stock, γεγονός που επιβεβαιώθηκε από τις σχετικές επιστημονικές του σημειώσεις. Η ερμηνεία των χημικών δεσμών των βορανίων και της δομής των συμπλεγμάτων τπυς ερευνήθηκε από τον Lipscomb και τους συνεργάτες του. Τελικά ο Lipscomb τιμήθηκε για το έργο του με το βραβείο Νόμπελ για τη Χημεία το 1976. Οι κανόνες Wades (PSEPT) μποεούν να χρησιμοποιοηθούν για να προβλέψουν τη δομή των βορανίων.
Το ενδιαφέρον για τα βοράνια αυξήθηκε κατά το Δεύτερο Παγκόσμιο Πόλεμο εξαιτίας της δυναμικής χρήσης του βοριοϋδριδίου του ουρανίου [U(BH4)4] για τον εμπλουτισμό των ισοτόπων του ουρανίου. Στις ΗΠΑ, μια ομάδα υπό την ηγεσία του Schlesinger ανέπτυξε τη βασική χημεία των βοριοϋδριδίων και των αντίστοιχων αργιλιοϋδριδίων. Παρόλο που τα βοριοϋδρίδια του ουτσνίου κρίθηκαν τελικά ανεπαρκή για τον ισοτοπικό διαχωρισμό, η δουλειά της ομάδας Schlesinger ώθησε τη χρήση αντιδραστηρίων βοριοϋδριδίων στην οργανική σύνθεση, που αναπτύχθηκε πολύ από τον Herbert C. Brown, που ήταν φοιτητής του Schlesinger. Αναπτύχθηκαν διάφορα βοριούχα αντιδραστήρια που χρησιμοποιήθηκαν ευρύτατα πλέον στην οργανική σύνθεση. Για παράδειγμα το βοριοϋδρίδιο του νατρίου (NaBH4) είναι ένα συνηθισμένο αντιδραστήριο για την αναγωγή αλδεϋδών και κετονών σε αλκοόλες. Ο Brown επιβραβεύθηκε για το έργο του με το βραβείο Νόμπελ για τη Χημεία το 1979.[2] Στη δεκαετία του '50 και στις αρχές εκέίνης του '60 και οι ΗΠΑ και η ΕΣΣΔ ερεύνησαν τη χρήση βοριοϋδριδίων και βορανίων ως καυσίμων υψηλής ενέργειας [κατέληξαν όμως περισσότερο στη χρήση οργανοβορανίων, όπως το αιθυλοβοράνιο (C2H5BH2)] για αεροσκάφη υψηλών ταχυτήτων, όπως το XB-70 Valkyrie. Η ανάπτυξη κατευθυνόμενων βλημάτων εδάφους-αέρος κατέστησε τα γρήγορα αεροσκάφη περιττά και τα σχετικά προγράμματα ανάπτυξης καυσίμων τερματίστηκαν. Παρ' όλα αυτά, αργότερα το τριαιθυλοβοράνιο [(C2H5)B] χρησιμοποιήθηκε για την ανάφλεξη στους κινητήρες του SR-71 Blackbird.[3]
Ονοματολογία ανόργανων βορανίων[Επεξεργασία | επεξεργασία κώδικα]
Η ονοματολογία των ουδέτερων ανόργανων βορανίων γίνεται ακολουθώντας τους ακόλουθους κανόνες:
- Το πρώτο τμήμα του κύριου ονόματος των ουδέτερων ανόργανων βορανίων αποτελείται από ένα ελληνικό αριθμητικό που δηλώνει τον αριθμό των ατόμων βορίου, αλλά για ένα άτομο, το πρόθεμα «μονο-» συνήθως δεν μπαίνει, αλλά εννοείται.
- Ακολουθεί η κατάληξη «-βοράνιο».
- Τέλος, μέσα σε παρένθεση τοποθετείται ο αριθμός των ατόμων υδρογόνου του βορανίου. Παραλήπεται αν εννοείται. Αν δεν μπει εννοείται το απλούστερο γνωστό βοράνιο.
Παραδείγματα:
- Β5H9: πενταβοράνιο(9).
- B6H12: εξαβοράνιο(12).
Η ονοματολογία των ανιόντων ανόργανων βορανίων γίνεται ακολουθώντας τους ακόλουθους κανόνες:
- Το πρώτο τμήμα του κύριου ονόματος των ανιόντων ανόργανων βορανίων αποτελείται από ένα ελληνικό αριθμητικό που δηλώνει τον αριθμό των ατόμων υδρογόνου του ανιόντος.
- Ακολουθεί η συλλαβή «-υδρο-».
- Μετά ακολουθεί ένα δεύτερο ελληνικό αριθμητικό που δηλώνει τον αριθμό των ατόμων βορίου, αλλά για ένα άτομο, το πρόθεμα «μονο-» συνήθως δεν μπαίνει, αλλά εννοείται.
- Ακολουθεί η κατάληξη «-βορανικό»
- Τέλος, μέσα σε παρένθεση τοποθετείται το φορτίο του ανιόντος.
Π.χ. [Β5H8]-: οκταϋδροπενταβορανικό(-1).
Σε μέρος της βιβλιογραφίας, ωστόσο, προστίθεται μπροστά από την παραπάνω αναφερόμενη ονομασία ένα πρόθεμα που δηλώνει σε ποια από τις υποκατηγορίες ανόργανων βορανίων ανήκει το βοράνιο στο οποίο αναφερόμαστε. Έχουν οριστεί οι ακόλουθες υποκατηγορίες:
- «κλοσο-» ή «closo-»: ΄Εχουν το γενικό τύπο: [BvHv]2- και υπάρχουν μόνο σε ανιόντα. Π.χ.: κλοσο-εξαϋδροεξαβορανικό(-2). Επίσης υπάρχουν παραδείγματα υποκατεστημενων βορανίων της σειράς «υπερκλοσο-» ή «hypercloso-»: Έχουν το γενικό τύπο BvXv, όπου X διάφοροι ανόργανοι ή οργανικοί υποκαταστάστες του υδρογόνου. Π.χ. B12(OCH2Ph)12 (υπερκλοσο-βενυλοξυδωδεκαβοράνιο(12)).
- «νιντο-» ή «nido-»: ΄Εχουν το γενικό τύπο: BvHv+4. Π.χ.: νιντο-πενταβοράνιο(9).
- «αραχνο-» ή «arachno-»: ΄Εχουν το γενικό τύπο: BvHv+6. Π.χ.: αραχνο-τετραβοράνιο(10).
- «υφο-» ή «hypho-»: ΄Εχουν το γενικό τύπο: BvHv+8. Μόνο σύμπλοκα αυτών των βορανίων είναι γνωστά.
Μοριακή δομή[Επεξεργασία | επεξεργασία κώδικα]
Μοριακή γεωμετρία[Επεξεργασία | επεξεργασία κώδικα]
Από τις αρχές της δεκαετίας του 1970 αποσαφηνήστηκε ότι η μοριακή γεωμετρία των βορανίων σχετίζεται με δελτάεδρα ακριβώς ή με δελτάεδρα από τα οποία λείπει μία ή περισσότερες κορυφές. Τα δελτάεδρα που έχουν βρεθεί στη μοριακή γεωμετρία των ανόργανων βορανίων είναι τα ακόλουθα:
| Όνομα δελταέδρου | Αριθμός κορυφών |
|---|---|
| τριγωνική διπυραμίδα | 5 |
| οκτάεδρο | 6 |
| πενταγωνική διπυραμίδα | 7 |
| δωδεκάεδρο | 8 |
| τρίκορφο τριγωνικό πρίσμα[4] | 9 |
| δίκορφο τετραγωνικό αντίπρισμα[5] | 10 |
| δεκαοκτάεδρο | 11 |
| εικοσάεδρο | 12 |
Ένα χαρακτηριστικό αυτών των δελτάεδρων είναι ότι τα άτομα βορίου στις κορυφές τους μπορεί να «συνέονται» με διαφορετικό αριθμό ατόμων βορίου σε σχέση με τα διπλανά τους. Για παράδειγμα, σε μια ομάδα βορανίου της οποίας τα άτομα βορίου σχηματίζουν τριγωνική διπυραμίδα, δύο (2) άτομα βορίου έχουν τρία (3) γειτονικά και τρία (3) έχουν τέσσερα (4) γειτονικά. Στην περίπτωση οκταέδρου και τα οκτώ (8) άτομα βορίου έχουν τέσσερα (4) γειτονικά.
Αυτές οι διαφοροποιήσεις μεταξύ ατόμων βορίου σε διαφορετικές θέσεις είναι σημαντικές για να ξεκαθαριστεί η δομή του μορίου τους, καθώς δείνουν διαφορετικές κορυφές στη φασματοσκοπία NMR 11B.
Το εξαβοράνιο(10) είναι ένα τυπικό παράδειγμα: Η γεωμετρία του είναι πενταγωνικής πυραμίδας, δηλαδή πενταγωνικής διπυραμίδας από την οποία λείπει η μια πυραμιδική κορυφή. Το κενό γεφυρώνεται με επιπλέον άτομα υδρογόνου που γεφυρώνονται γύρω από τον άδειο χώρο.
Οι δεσμοί στα βοράνια[Επεξεργασία | επεξεργασία κώδικα]
Αν επιχειρηθεί να ερμηνευτούν με συμβατικούς ομοιοπολικούς δεσμούς, τα μόρια των βορανίων, τίθεται ένα σημαντικό πρόβλημα: τα άτομα βορίου έχουν χάσμα οκτάδας. Στο βοράνιο (BH3), το μόριό του είναι ένα επίπεδο τριγωνικό (με μοριακή συμμετρία D3h). Το διβοράνιο(6) έχει μια δομή γέφυρας υδρογόνου. Η περιγραφή της δεσμολογίας των υπόλοιπων τυποποιήθηκε από τον William Lipscomb και περιλαμβάνει συνολικά τέσσερα (4) είδη δεσμών:
- Ομοιοπολικός δεσμός B-Η-B: Πρόκειται για ομοιοπολικό δεσμό «μπανάνα», τριών κέντρων και δύο ηλεκτρονίων.
- Ομοιοπολικός δεσμός B-B-B: Πρόκειται για ομοιοπολικό δεσμό «μπανάνα», τριών κέντρων και δύο ηλεκτρονίων.
- Ομοιοπολικός δεσμός Β-Β: Πρόκειται για συμβατικό ομοιοπολικό δεσμό σ 2sp2-2sp2, μήκους 164 pm.
- Ομοιοπολικός δεσμός Β-Η: Πρόκειται για συμβατικό ομοιοπολικό δεσμό σ 2sp2-1s, μήκους 114 pm και πολύ μικρής πόλωσης 0,8% B+-H-.
Υιοθετήθηκε ο «αριθμός styx», όπου s: ο αριθμός των δεσμών B-Η-B, t: ο αριθμός των δεσμών B-B-B, y: ο αριθμός των δεσμών Β-Β και x: ο αριθμός των ομάδων BH2.
Η μεθοδολογία του Lipscomb έχει σε μεγάλο βαθμό αντικατασταθεί από τη θεωρία των μοριακών τροχιακών, αλλά ωστόσο ακόμη εμπνέει. Τα ερευνητικά αποτελέσματα έχουν συγκεντρωθεί στον απλό αλλά ισχυρό κανόνα «PSEPT», που αποκαλείται συχνά με τον όρο «κανόνες του Wade», που προβλέπει τη δομική συμπεριφορά των μοριακών συμπλεγμάτων closo-, nido-, κ.τ.λ.. Η δύναμη αυτού του κανόνα είναι η ευκολία χρήσης και γενικής εφαρμογής σε πολλούς διαφορετικούς τύπους συμπλεγμάτων και εκτός των βορανίων. Υπάρχουν συνεχείς προσπάθειες από τους θεωρητικούς χημικούς για τη βελτίωση της εξήγησης της συγκόλλησης των συμπλεγμάτων στο συνολικό μόριο των πολύπλοκων βορανίων. Ένα παράδειγμα είναι η έννοια της επιφάνειας τανυστή Στόουν στην αρμονική ερμηνεία της συγκόλλησης συμπλέγματος. Μια πρόσφατη εξέλιξη είναι η εξήγηση με τη χρήση δεσμών τεσσάρων κέντρων και δύο ηλεκτρονίων των ατόμων - άκρων των συμπλεγμάτων που συγκολλούνται.
Ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Τα ανόργανα βοράνια είναι όλα άχρωμα και διαμαγνητικά. Είναι δραστικές ενώσεις και μάλιστα κάποια από αυτά είναι πυροφορικά. Η πλειοψηφία τους είναι πολύ δηλητηριώδη και χρειάζονται ειδική και προσεκτική μεταχείρηση.
Κλοσοβοράνια[Επεξεργασία | επεξεργασία κώδικα]
Δεν είναι γνωστά ουδέτερα κλοσοβοράνια. Είναι όμως γνωστά άλατα ανιόντων κλοσοβορανίων, με γενικό τύπο BvHv2-, που είναι σταθερά σε ουδέτερα υδατικά διαλύματα. Η σταθερότητά τους αυξάνεται με το μέγεθός τους, δηλαδή με τον αριθμό των ατόμων βορίου τους. Π.χ. το άλας K2B12H12 (ονομάζεται δωδεκαϋδροδωδεκαβορανικό(-2) κάλιο) είναι σταθερό μέχρι τους 700 °C.
Νιντοβοράνια[Επεξεργασία | επεξεργασία κώδικα]
Το εννεαβοράνιο(9) και το δεκαβοράνιο(14) είναι τα πιο σταθερά (γνωστά) νιντοβοράνια, σε αντίθεση με το οκταβοράνιο(12), που διασπάται σε θερμοκρασίες πάνω από -35 °C.
Αραχνοβοράνια[Επεξεργασία | επεξεργασία κώδικα]
Γενικά αυτά είναι ακόμη πιο δραστικά από τα νιντοβοράνια. Όπως και τα κλοσοβοράνια, τα μεγαλύτερα μέλη της σειράς είναι πιο σταθερά.
Παραγωγή και αντιδράσεις[Επεξεργασία | επεξεργασία κώδικα]
Το βοράνιο παράγεται με πυρόλυση του διβορανίου(6) και είναι ένα σημαντικό ενδιάμεσο για την παραγωγή ανώτερων (δηλαδή με μεγαλύτερο αριθμό ατόμων βορίου) βορανίων.
Το διβοράνιο(6) παράγεται βιομηχανικά με αναγωγή τριφθοριούχου βορίου και είναι η πρώτη ύλη για την παραγωγή όλων των άλλων βορανίων, ανόργανων και οργανικών.
Τυπικές κατηγορίες αντιδράσεων των βορανίων είναι οι ακόλουθες:
- Ηλεκτρονιόφιλη υποκατάσταση.
- Πυρηνόφιλη υποκατάσταση με βάσεις κατά Lewis.
- Αποπρωτονίωση από ισχυρές βάσεις.
- Σύνθεση ανώτερων ανόργανων βορανίων με «βοριοϋδρίδια», δηλαδή ενώσεις που περιέχουν το ανιόν BH4-, όπως π.χ. το βοριοϋδρίδιο του νατρίου (NaBH4).
- Προσθήκη νιντοβορανίων σε αλκένια ή αλκίνια για να δώσουν καρβοβοράνια.
- Παραγωγή ενώσεων συναρμογής. Κατά περίπτωση εμπλέκονται τόσο τα ίδια άτομα των βορανίων, όταν έχουν χάσμα οκτάδας, όσο και οι γέφυρες B-H-B, αν περιέχουν. Π.χ. το εξαβοράνιο(10) μπορεί να αντικαταστήσει το αιθάνιο στο άλας του Zeise για να παραγάγει το σύμπλοκο [Fe(η6-B6H10)(CO)4].
- Αντιδράσεις παραγωγής ετεροβορανίων, δηλαδή καρβοβορανίων ή μεταλλοβορανίων.
Παρατηρήσεις, υποσημειώσεις και αναφορές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Τα οργανικά βοράνια περιέχουν και μια τουλάχιστον οργανική ρίζα.
- ↑ Brown, H. C. “Organic Syntheses via Boranes” John Wiley & Sons, Inc. New York: 1975. ISBN 0-471-11280-1.
- ↑ http://incolor.inebraska.com/hwolfe/history/sr71.pdf
- ↑ Στο κέντρο καθεμιάς από τις τρεις παραλληλόγραμμες έδρες υπάρχει από μια επιπλέον υπερυψωμένη, σε σχέση με το επίπεδο της έδρας, κορυφή.
- ↑ Στο κέντρο καθεμιάς από τις δυο τετράγωνες έδρες υπάρχει από μια επιπλέον υπερυψωμένη, σε σχέση με το επίπεδο της έδρας, κορυφή.
|
