Φεμπουξοστάτη
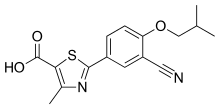 | |
| Ονομασία IUPAC | |
|---|---|
2-(3-cyano-4-isobutoxyphenyl)-4-methyl- 1,3-thiazole-5-carboxylic acid | |
| Κλινικά δεδομένα | |
| Εμπορικές ονομασίες | Uloric, Adenuric |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a609020 |
| Δεδομένα άδειας |
|
| Κατηγορία ασφαλείας κύησης | |
| Οδοί χορήγησης | By mouth |
| Κυκλοφορία | |
| Κυκλοφορία |
|
| Φαρμακοκινητική | |
| Βιοδιαθεσιμότητα | ≥84% absorbed |
| Πρωτεϊνική σύνδεση | 99.2% to albumin |
| Μεταβολισμός | via CYP1A1, 1A2, 2C8, 2C9, UGT1A1, 1A8, 1A9 |
| Βιολογικός χρόνος ημιζωής | ~5–8 hours |
| Απέκκριση | Urine (~49%, mostly as metabolites, 3% as unchanged drug); feces (~45%, mostly as metabolites, 12% as unchanged drug) |
| Κωδικοί | |
| Αριθμός CAS | 144060-53-7 |
| Κωδικός ATC | M04AA03 |
| PubChem | CID 134018 |
| IUPHAR/BPS | 6817 |
| DrugBank | DB04854 |
| ChemSpider | 118173 |
| UNII | 101V0R1N2E |
| KEGG | D01206 |
| ChEBI | CHEBI:31596 |
| ChEMBL | CHEMBL1164729 |
| Χημικά στοιχεία | |
| Χημικός τύπος | C16H16N2O3S |
| Μοριακή μάζα | 316,38 g·mol−1 |
N#Cc1c(OCC(C)C)ccc(c1)c2nc(c(s2)C(=O)O)C | |
InChI=1S/C16H16N2O3S/c1-9(2)8-21-13-5-4-11(6-12(13)7-17)15-18-10(3)14(22-15)16(19)20/h4-6,9H,8H2,1-3H3,(H,19,20) Key:BQSJTQLCZDPROO-UHFFFAOYSA-N | |
| | |
Η φεμπουξοστάτη, που πωλείται μεταξύ άλλων με τις εμπορικές ονομασίες Uloric και Adenuric, είναι νέας γενιάς φάρμακο που χρησιμοποιείται για τη θεραπεία της ουρικής αρθρίτιδας λόγω των υψηλών επιπέδων ουρικού οξέος.[3] Γενικά συνιστάται μόνο για άτομα που δεν μπορούν να φάρμακο με αλλοπουρινόλη.[4][5] Κατά την αρχική έναρξη, συχνά συνιστώνται φάρμακα όπως τα ΜΣΑΦ για την πρόληψη των εξάρσεων της ουρικής αρθρίτιδας.[3][5] Η φεμπουξοστάτη λαμβάνεται από το στόμα.[3]
Οι συχνές ανεπιθύμητες ενέργειες περιλαμβάνουν ηπατικά προβλήματα, ναυτία, πόνο στις αρθρώσεις και εξάνθημα.[3] Οι σοβαρές ανεπιθύμητες ενέργειες περιλαμβάνουν αυξημένο κίνδυνο θανάτου σε σύγκριση με την αλλοπουρινόλη, το σύνδρομο Stevens-Johnson και την αναφυλαξία.[5][4]
Δεν συνιστάται η χρήση της κατά τη διάρκεια της εγκυμοσύνης ή του θηλασμού.[5] Αναστέλλει την οξειδάση της ξανθίνης, μειώνοντας έτσι την παραγωγή ουρικού οξέος στο σώμα.[3]
Εγκρίθηκε για ιατρική χρήση στην Ευρωπαϊκή Ένωση το 2008 και στις Ηνωμένες Πολιτείες το 2009.[6][3] Μια γενική έκδοση αυτού του φαρμάκου εγκρίθηκε το 2019.[7][8]
Χρησιμοποιείται για τη θεραπεία της χρόνιας ουρικής αρθρίτιδας και της υπερουριχαιμίας.[9] Η φεμπουξοστάτη συνήθως συνιστάται μόνο σε άτομα που δεν μπορούν να ανεχθούν την αλλοπουρινόλη.[10] Το Εθνικό Ινστιτούτο Υγείας και Κλινικής Αριστείας κατέληξε στο συμπέρασμα ότι η φεμπουξοστάτη είναι πιο αποτελεσματική από τις τυπικές δόσεις αλλοπουρινόλης, αλλά όχι πιο αποτελεσματική από τις υψηλότερες δόσεις αλλοπουρινόλης.[9]
Παρενέργειες
[Επεξεργασία | επεξεργασία κώδικα]Οι ανεπιθύμητες ενέργειες -που σχετίζονται με τη θεραπεία με φεμπουξοστάτη- περιλαμβάνουν ναυτία, διάρροια, αρθραλγία, πονοκέφαλο, αυξημένα επίπεδα ηπατικών ενζύμων στον ορό και εξάνθημα.[11][12]
Αλληλεπιδράσεις
[Επεξεργασία | επεξεργασία κώδικα]Η φεμπουξοστάτη αντενδείκνυται με ταυτόχρονη χρήση θεοφυλλίνης και χημειοθεραπευτικών παραγόντων, συγκεκριμένα της αζαθειοπρίνης και της 6-μερκαπτοπουρίνης, επειδή θα μπορούσε να αυξήσει τις συγκεντρώσεις αυτών των φαρμάκων στο πλάσμα του αίματος και συνεπώς την τοξικότητά τους.[11][13]
Φαρμακολογία
[Επεξεργασία | επεξεργασία κώδικα]Η φεμπουξοστάτη είναι ένας μη εκλεκτικός αναστολέας της οξειδάσης της ξανθίνης.[11] Λειτουργεί αναστέλλοντας μη ανταγωνιστικά το κέντρο της πτερίνης του μολυβδαινίου, το οποίο είναι η ενεργή θέση της οξειδάσης της ξανθίνης.
Η οξειδάση της ξανθίνης απαιτείται για την διαδοχική οξείδωση της υποξανθίνης και της ξανθίνης σε ουρικό οξύ. Έτσι, η φεμπουξοστάτη αναστέλλει την οξειδάση της ξανθίνης, μειώνοντας έτσι την παραγωγή ουρικού οξέος. Η φεμπουξοστάτη αναστέλλει τόσο την οξειδωμένη όσο και την ανηγμένη μορφή της οξειδάσης της ξανθίνης λόγω της στενής δέσμευσής της στη θέση της πτερίνης του μολυβδαινίου.[12]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ «Febuxostat (Uloric) Use During Pregnancy». Drugs.com. 22 Φεβρουαρίου 2019. Ανακτήθηκε στις 17 Μαΐου 2020.
- ↑ «Prescription medicines: registration of new chemical entities in Australia, 2014». Therapeutic Goods Administration (TGA). 21 Ιουνίου 2022. Αρχειοθετήθηκε από το πρωτότυπο στις 10 Απριλίου 2023. Ανακτήθηκε στις 10 Απριλίου 2023.
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 «Febuxostat Monograph for Professionals». Drugs.com. American Society of Health-System Pharmacists. Ανακτήθηκε στις 26 Φεβρουαρίου 2019.
- ↑ 4,0 4,1 «Drug Safety and Availability - FDA adds Boxed Warning for increased risk of death with gout medicine Uloric (febuxostat)». FDA. 21 Φεβρουαρίου 2019. Ανακτήθηκε στις 26 Φεβρουαρίου 2019.
- ↑ 5,0 5,1 5,2 5,3 British national formulary : BNF 76 (76 έκδοση). Pharmaceutical Press. 2018. σελ. 1087. ISBN 9780857113382.
- ↑ «Adenuric». European Medicines Agency - Commission. 17 Σεπτεμβρίου 2018. Ανακτήθηκε στις 26 Φεβρουαρίου 2019.
- ↑ «Generic Uloric Availability». Drugs.com. Ανακτήθηκε στις 1 Αυγούστου 2019.
- ↑ «Febuxostat Generic Uloric». Ανακτήθηκε στις 15 Απριλίου 2020.
- ↑ 9,0 9,1 Febuxostat for the management of hyperuricaemia in people with gout (TA164) Chapter 4.
- ↑ «Febuxostat for the management of hyperuricaemia in people with gout Guidance and guidelines». www.nice.org.uk. 17 Δεκεμβρίου 2008. Αρχειοθετήθηκε από το πρωτότυπο στις 28 Μαρτίου 2017. Ανακτήθηκε στις 28 Μαρτίου 2017.
- ↑ 11,0 11,1 11,2 Uloric label Updated February, 2009.
- ↑ 12,0 12,1 «Urate-lowering therapy for gout: focus on febuxostat». Pharmacotherapy 30 (6): 594–608. 2010. doi:. PMID 20500048. https://archive.org/details/sim_pharmacotherapy_2010-06_30_6/page/594.
- ↑ Ashraf Mozayani· Lionel Raymon (2011). Handbook of Drug Interactions: A Clinical and Forensic Guide. Springer Science+Business Media.
Εξωτερικοί σύνδεσμοι
[Επεξεργασία | επεξεργασία κώδικα] Πολυμέσα σχετικά με το θέμα Febuxostat στο Wikimedia Commons
Πολυμέσα σχετικά με το θέμα Febuxostat στο Wikimedia Commons
