Λοσαρτάνη
 | |
 | |
| Ονομασία IUPAC | |
|---|---|
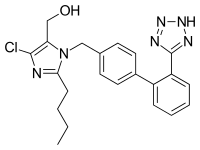
(2-butyl-4-chloro-1-{[2'-(2H-tetrazol-5-yl)biphenyl-4-yl]methyl}-1H-imidazol-5-yl)methanol | |
| Κλινικά δεδομένα | |
| Εμπορικές ονομασίες | Cozaar, αλλες |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a695008 |
| Δεδομένα άδειας | |
| Κατηγορία ασφαλείας κύησης | |
| Οδοί χορήγησης | Από το στόμα |
| Κυκλοφορία | |
| Κυκλοφορία |
|
| Φαρμακοκινητική | |
| Βιοδιαθεσιμότητα | 25–35% |
| Πρωτεϊνική σύνδεση | 99.7% (κυρίως αλβουμίνη) |
| Μεταβολισμός | Ηπατικός (CYP2C9, CYP3A4) |
| Βιολογικός χρόνος ημιζωής | 1.5–2 ώρες |
| Απέκκριση | Νεφρά 13–25%, χολή 50–60% |
| Κωδικοί | |
| Αριθμός CAS | 114798-26-4 |
| Κωδικός ATC | C09CA01 |
| PubChem | CID 3961 |
| IUPHAR/BPS | 590 |
| DrugBank | DB00678 |
| ChemSpider | 3824 |
| UNII | JMS50MPO89 |
| KEGG | D08146 |
| ChEBI | CHEBI:6541 |
| ChEMBL | CHEMBL191 |
| Χημικά στοιχεία | |
| Χημικός τύπος | C22H23ClN6O |
| Μοριακή μάζα | 422,92 g·mol−1 |
O=C(O)[C@H](C(C)C)N(Cc1ccc(cc1)c1ccccc1c1n[NH]nn1)C(=O)CCCC | |
InChI=1S/C22H23ClN6O/c1-2-3-8-20-24-21(23)19(14-30)29(20)13-15-9-11-16(12-10-15)17-6-4-5-7-18(17)22-25-27-28-26-22/h4-7,9-12,30H,2-3,8,13-14H2,1H3,(H,25,26,27,28) Key:PSIFNNKUMBGKDQ-UHFFFAOYSA-N | |
| (verify) | |
Η λοσαρτάνη, που πωλείται με την εμπορική ονομασία Cozaar μεταξύ άλλων, είναι φάρμακο που χρησιμοποιείται κυρίως για τη θεραπεία της υψηλής αρτηριακής πίεσης.[2] Χρησιμοποιείται επίσης για διαβητική νεφρική νόσο, καρδιακή ανεπάρκεια και διόγκωση της αριστερής κοιλίας. Λαμβάνεται από το στόμα. Μπορεί να χρησιμοποιηθεί μόνο του ή μαζί με άλλα φάρμακα για την αρτηριακή πίεση. Ενδέχεται να απαιτούνται έως και έξι εβδομάδες για να εμφανιστεί η πλήρης δράση.[2]
Συχνές ανεπιθύμητες ενέργειες περιλαμβάνουν μυϊκές κράμπες, βουλωμένη μύτη, βήχα, υψηλό κάλιο στο αίμα και αναιμία.[2] Σοβαρές ανεπιθύμητες ενέργειες μπορεί να περιλαμβάνουν αγγειοοίδημα, χαμηλή αρτηριακή πίεση και προβλήματα στα νεφρά. Η χρήση κατά τη διάρκεια της εγκυμοσύνης μπορεί να προκαλέσει βλάβη στο μωρό. Η χρήση δεν συνιστάται κατά τη διάρκεια του θηλασμού.[1] Είναι στην οικογένεια φαρμάκων που δεσμεύει τον υποδοχέα της αγγειοτενσίνης. Δρα αναστέλλοντας την αγγειοτενσίνη II.[2]
Η λοσαρτάνη κατοχυρώθηκε με δίπλωμα ευρεσιτεχνίας το 1986 και εγκρίθηκε για ιατρική χρήση στις Ηνωμένες Πολιτείες το 1995.[2][3] Είναι στον κατάλογο των βασικών φαρμάκων του Παγκόσμιου Οργανισμού Υγείας.[4] Διατίθεται ως γενικό φάρμακο.[5] Το 2017, ήταν το ένατο πιο συχνά συνταγογραφούμενο φάρμακο στις Ηνωμένες Πολιτείες, με περισσότερες από 51 εκατομμύρια συνταγές.[6][7] Διατίθεται μια έκδοση σε συνδυασμό με την υδροχλωροθειαζίδη και, το 2017, ήταν η 67η πιο συχνά συνταγογραφούμενη φαρμακευτική αγωγή στις Ηνωμένες Πολιτείες, με περισσότερες από έντεκα εκατομμύρια συνταγές.[8]
Ιατρικές χρήσεις[Επεξεργασία | επεξεργασία κώδικα]
Η λοσαρτάνη χρησιμοποιείται για την υπέρταση, συμπεριλαμβανομένων ατόμων με υπερτροφία της αριστερής κοιλίας (διευρυμένος καρδιακός μυς) και νεφρική δυσλειτουργία σε ασθενείς με διαβήτη τύπου II.[9] Μπορεί επίσης να καθυστερήσει την πρόοδο της διαβητικής νεφροπάθειας. Είναι κατάλληλος φαρμακολογικός παράγοντας για τη μείωση της εξέλιξης της νεφρικής νόσου σε ασθενείς με διαβήτη τύπου 2, υπέρταση και μικρολευκωματινουρία (> 30 mg / 24 ώρες) ή πρωτεϊνουρία (> 900 mg / 24 ώρες).[10]
Παρενέργειες[Επεξεργασία | επεξεργασία κώδικα]
Οι πιο συχνές παρενέργειες της λοσαρτάνης σε ενήλικες είναι λοιμώξεις του ανώτερου αναπνευστικού, ζάλη και πόνος στην πλάτη.[9] Τα άτομα με διαβήτη τύπου 2 και νεφρική νόσο μπορεί να παρουσιάσουν διάρροια, κόπωση, χαμηλή αρτηριακή πίεση, χαμηλή γλυκόζη στο αίμα, αυξημένο κάλιο, πόνο στο στήθος ή αλλεργική αντίδραση. Η λοσαρτάνη δεν πρέπει να λαμβάνεται από άτομα που είναι διαβητικά και λαμβάνουν αλισκιρένη. Μπορεί να εμφανιστεί αναιμία, λόγω αναστολής του συστήματος ρενίνης-αγγειοτενσίνης. Όπως και με άλλους αναστολείς των υποδοχέων της αγγειοτασίνης, η λοσαρτάνη μπορεί να βλάψει το ήπαρ, αν και αυτό το φαινόμενο φαίνεται να είναι σπάνιο.[11] Μπορεί να εμφανιστούν ανισορροπίες ηλεκτρολυτών σε άτομα με νεφρικά προβλήματα που λαμβάνουν λοσαρτάνη. Οι ανεπιθύμητες ενέργειες δεν διαφέρουν ανάλογα με το φύλο, την ηλικία ή τη φυλή.
Εγκυμοσύνη[Επεξεργασία | επεξεργασία κώδικα]
Τον Οκτώβριο του 2014, η Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων (FDA) εξέδωσε προειδοποίηση ότι η λοσαρτάνη μπορεί να προκαλέσει εμβρυϊκή τοξικότητα και θα πρέπει να διακοπεί μόλις εντοπιστεί εγκυμοσύνη.[12][9] Η χρήση λοσαρτάνης κατά τη διάρκεια της εγκυμοσύνης μπορεί να οδηγήσει σε εμβρυϊκό τραυματισμό ή θάνατο.
Υπερβολική δόση[Επεξεργασία | επεξεργασία κώδικα]
Η υπερδοσολογία πιθανότατα θα είχε ως αποτέλεσμα τη μείωση της αρτηριακής πίεσης, η οποία θα μπορούσε να εκδηλωθεί ως αυξημένος καρδιακός ρυθμός, ζάλη, αίσθημα ελαφριάς κεφαλής ή απώλεια συνείδησης. Μελέτες ποντικών έδειξαν ότι η θνησιμότητα εμφανίστηκε σε δόσεις περίπου 44 έως 170 φορές μεγαλύτερες από τη μέγιστη συνιστώμενη δόση μετά την προσαρμογή του βάρους των ποντικών.[9]
Αλληλεπιδράσεις[Επεξεργασία | επεξεργασία κώδικα]
Η λοσαρτάνη μπορεί να έχει ανεπιθύμητες αλληλεπιδράσεις με τη φαινοβαρβιτάλη, τη ριφαμπίνη ή τη φλουκοναζόλη, πιθανόν αναστέλλοντας τη δράση της στη μείωση της αρτηριακής πίεσης.[9]
Μηχανισμός δράσης[Επεξεργασία | επεξεργασία κώδικα]
Η λοσαρτάνη είναι ένας επιλεκτικός, ανταγωνιστικός ανταγωνιστής υποδοχέα αγγειοτασίνης II τύπου 1 (ΑΤ1), μειώνοντας τις αποκρίσεις των τελικών οργάνων στην αγγειοτασίνη II. Η χορήγηση της λοσαρτάνης οδηγεί σε μείωση της συνολικής περιφερειακής αντίστασης (μεταφορτίο) και της καρδιακής φλεβικής επιστροφής (προφορτίο). Όλες οι φυσιολογικές επιδράσεις της αγγειοτασίνης II, συμπεριλαμβανομένης της απελευθέρωσης αλδοστερόνης, ανταγωνίζονται παρουσία λοσαρτάνης. Η μείωση της αρτηριακής πίεσης συμβαίνει ανεξάρτητα από την κατάσταση του συστήματος ρενίνης-αγγειοτασίνης. Ως αποτέλεσμα της χορήγησης λοσαρτάνης, η δραστηριότητα της ρενίνης στο πλάσμα αυξάνεται λόγω της αφαίρεσης της ανατροφοδότησης της αγγειοτασίνης II. Η ρενίνη απελευθερώνεται από τα νεφρά όταν υπάρχει μειωμένη νεφρική αρτηριακή πίεση, συμπαθητική ενεργοποίηση ή αυξημένη παροχή νατρίου στο απομακρυσμένο νεφρικό σωληνάριο.[13] Η ρενίνη δρα στη συνέχεια μετατρέποντας το αγγειοτασινογόνο σε αγγειοτασίνη Ι. Το ένζυμο μετατροπής αγγειοτασίνης (ACE) μετατρέπει την αγγειοτασίνη I σε αγγειοτασίνη II. Η αγγειοτασίνη II προκαλεί αγγειοσυστολή και απελευθέρωση αλδοστερόνης. Η αλδοστερόνη χρησιμεύει για τη συγκράτηση νατρίου από το περιφερικό νεφρικό σωληνάριο. Η κατακράτηση νατρίου οδηγεί τελικά σε αυξημένη αρτηριακή πίεση.[14] Επομένως, η χρήση ανταγωνιστών του υποδοχέα της αγγειοτασίνης II όπως η λοσαρτάνη έχει ως αποτέλεσμα τον αποκλεισμό της κατάντη επίδρασης της ρενίνης, της αγγειοτασίνης II και τελικά τη μείωση της αρτηριακής πίεσης.
Οι ανταγωνιστές του υποδοχέα της αγγειοτασίνης II περιλαμβάνουν τις λοσαρτάνη, βαλσαρτάνη, αζιλσαρτάνη, καντεσαρτάνη, επροσαρτάνη, ιρβεσαρτάνη, ολμεσαρτάνη και τελμισαρτάνη. Όλοι έχουν τον ίδιο μηχανισμό δράσης και δυνητικά αναστέλλουν τις δράσεις της αγγειοτασίνης καλύτερα από τους αναστολείς ΜΕΑ, όπως η λισινοπρίλη, επειδή υπάρχουν άλλα ένζυμα εκτός του ACE που έχουν την ικανότητα παραγωγής αγγειοτασίνης II.[13]
Η λοσαρτάνη είναι ουρικοσουρικό. Ως ειδικός αναστολέας του μεταφορέα ουρικών 1 (SLC22A12, URAT1), η λοσαρτάνη εμποδίζει την πρόσληψη ουρικού οξέος στα κύτταρα, αφήνοντας έτσι περισσότερο διαθέσιμο στην κυκλοφορία του αίματος να φιλτραριστεί και να εκκρίνεται από τα νεφρά.[15] Επειδή η λοσαρτάνη μπορεί να προκαλέσει υπερκαλιαιμία, τα άτομα δεν πρέπει να χρησιμοποιούν συμπληρώματα καλίου ή υποκατάστατα αλατιού που περιέχουν κάλιο χωρίς κατάλληλη παρακολούθηση από γιατρό.[16]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 1,2 «Losartan (Cozaar) Use During Pregnancy». Drugs.com. Ανακτήθηκε στις 10 Δεκεμβρίου 2017.
- ↑ 2,0 2,1 2,2 2,3 2,4 «Losartan Potassium». The American Society of Health-System Pharmacists. Ανακτήθηκε στις 8 Δεκεμβρίου 2017.
- ↑ Fischer, Jnos· Ganellin, C. Robin (2006). Analogue-based Drug Discovery. John Wiley & Sons. σελ. 470. ISBN 9783527607495.
- ↑ World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. 2019. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ↑ British national formulary : BNF 69 (69 έκδοση). British Medical Association. 2015. σελ. 127. ISBN 9780857111562.
- ↑ «The Top 300 of 2020». ClinCalc. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ «Losartan Potassium - Drug Usage Statistics». ClinCalc. 23 Δεκεμβρίου 2019. Αρχειοθετήθηκε από το πρωτότυπο στις 11 Απριλίου 2020. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ «Hydrochlorothiazide; Losartan Potassium - Drug Usage Statistics». ClinCalc. 23 Δεκεμβρίου 2019. Αρχειοθετήθηκε από το πρωτότυπο στις 11 Απριλίου 2020. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ 9,0 9,1 9,2 9,3 9,4 «Cozaar- losartan potassium tablet, film coated». DailyMed. 14 Νοεμβρίου 2019. Ανακτήθηκε στις 20 Μαρτίου 2020.
- ↑ «Pharmacoeconomics of angiotensin II antagonists in type 2 diabetic patients with nephropathy: implications for decision making». PharmacoEconomics 24 (6): 523–35. 2006. doi:. PMID 16761901.
- ↑ «Losartan-induced severe hepatic injury: A case report and literature review». Cureus 11 (5): e4769. May 2019. doi:. PMID 31363450.
- ↑ «Cozaar (losartan potassium) 25 mg, 50 mg, and 100 mg Tablets». U.S. Food and Drug Administration (FDA). 16 Οκτωβρίου 2014. Αρχειοθετήθηκε από το πρωτότυπο στις 12 Ιανουαρίου 2017. Ανακτήθηκε στις 21 Ιουλίου 2015.
- ↑ 13,0 13,1 Katzung, Bertram G., editor (30 Νοεμβρίου 2017). Basic & clinical pharmacology. ISBN 9781259641152.
- ↑ Graudal, Niels A.; Hubeck-Graudal, Thorbjørn; Jürgens, Gesche (January 2012). «Effects of low-sodium diet vs. high-sodium diet on blood pressure, renin, aldosterone, catecholamines, cholesterol, and triglyceride (Cochrane Review)». American Journal of Hypertension 25 (1): 1–15. doi:. ISSN 1941-7225. PMID 22068710.
- ↑ «Uricosuric action of losartan via the inhibition of urate transporter 1 (URAT 1) in hypertensive patients». American Journal of Hypertension 21 (10): 1157–1162. 1 October 2008. doi:. PMID 18670416. https://archive.org/details/sim_american-journal-of-hypertension_2008-10_21_10/page/1157.
- ↑ RxList. The Internet Drug Index. Clinical pharmacology of Cozaar. Retrieved January 6, 2014.
