Ακρυλονιτρίλιο
| Ακρυλονιτρίλιο | |||
|---|---|---|---|

| |||

| |||
| |||

| |||
| Γενικά | |||
| Όνομα IUPAC | 2-προπενονιτρίλιο, προπ-2-ενονιτρίλιο | ||
| Άλλες ονομασίες | κυανοαιθένιο βινυλοκυανίδιο (VCN) κυανοαιθυλένιο[1] προπενονιτρίλιο[1] | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C3H3N | ||
| Μοριακή μάζα | 53,06 g·mol−1 | ||
| Αριθμός CAS | 107-13-1 | ||
| SMILES | C=CC#N | ||
| InChI | NLHHRLWOUZZQLW-UHFFFAOYAG | ||
| Αριθμός UN | MP1U0D42PE | ||
| PubChem CID | 7855 | ||
| ChemSpider ID | 7567 | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -84°C | ||
| Σημείο βρασμού | 77°C | ||
| Πυκνότητα | 0,81 g/cm3 | ||
| Διαλυτότητα στο νερό |
70 g/L | ||
| Διαλυτότητα σε άλλους διαλύτες |
αιθανόλη, διαιθυλαιθέρας, χλωροφόρμιο | ||
| Τάση ατμών | 83 mmHg[1] | ||
| Εμφάνιση | Άχρωμο υγρό | ||
| Χημικές ιδιότητες | |||
| Ελάχιστη θερμοκρασία ανάφλεξης |
−1 °C; 30 °F; 272 K | ||
| Σημείο αυτανάφλεξης | 471 °C (880 °F; 744 K) | ||
| Επικινδυνότητα | |||
 
| |||
| Κίνδυνοι κατά NFPA 704 |
|||
| Άλλοι κίνδυνοι | Δυνητικά καρκινογόνο | ||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
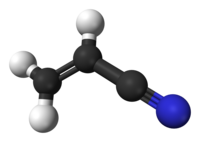
Το ακρυλονιτρίλιο είναι μια χημική ένωση με τον χημικό τύπο C3H3N. Αυτό το άχρωμο υγρό συχνά εμφανίζεται ως κίτρινο λόγω των προσμίξεων. Είναι ένα σημαντικό μονομερές για την κατασκευή χρήσιμων πλαστικών όπως το πολυακριλονιτρίλιο. Από πλευράς μοριακής δομής, αποτελείται από μια βινυλομάδα συνδεμένη με ένα νιτρίλιο.
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
Το περισσότερο βιομηχανικό ακρυλονιτρίλιο παράγεται με καταλυτική αμμωνιοξείδωση του προπενίου, γνωστή επίσης ως διεργασία σόχιο (Sohio). Το 2002, η παγκόσμια παραγωγή εκτιμήθηκε σε 5 εκατομμύρια τόνους τον χρόνο.[2][3] Το ακετονιτρίλιο και το υδροκυάνιο είναι σημαντικά παραπροϊόντα που ανακτώνται προς πώληση.[2] Στην πραγματικότητα, η έλλειψη ακετονιτριλίου του 2008-2009 προκλήθηκε από τη μείωση της ζήτησης για ακρυλονιτρίλιο.[4]
Στη διεργασία Sohio, το προπένιο, η αμμωνία, και ο αέρας (οξειδωτικό) διέρχονται μέσα από ένα αντιδραστήρα ρευστοποιημένης κλίνης που περιέχει τον καταλύτη στους 400–510 °C και 50–200 kPag. Τα αντιδρώντα περνάνε από τον αντιδραστήρα μόνο μια φορά, πριν να εμβαπτιστούν σε υδατικό θειικό οξύ. Η περίσσεια προπυλενίου, μονοξειδίου του άνθρακα, διοξειδίου του άνθρακα και διαζώτου που δεν διαλύονται διοχετεύονται άμεσα στην ατμόσφαιρα, ή αποτεφρώνονται. Το υδατικό διάλυμα αποτελείται από ακρυλονιτρίλιο, ακετονιτρίλιο, υδροκυανικό οξύ, και θειικό αμμώνιο (από την περίσσεια της αμμωνίας). Μια στήλη ανάκτησης αφαιρεί το χύμα νερό και τα ακρυλονιτρίλιο και ακετονιτρίλιο διαχωρίζονται με απόσταξη. Ιστορικά, ένας από τους πρώτους πετυχημένους καταλύτες ήταν το φωσφορομολυβδαινικό βισμούθιο σε διοξείδιο του πυριτίου ως ετερογενής καταλύτης. Από τότε, έχουν γίνει και άλλες βελτιώσεις.[2]
Χρήσεις[Επεξεργασία | επεξεργασία κώδικα]
Το ακρυλονιτρίλιο χρησιμοποιείται κυρίως ως ένα μονομερές στην παρασκευή του πολυακρυλονιτριλίου, ενός ομοπολυμερούς, ή για πολλά σημαντικά συμπολυμερή, όπως τα στυρένιο-ακρυλονιτρίλιο (styrene-acrylonitrile) (SAN), ακρυλονιτρίλιο-βουταδιένιο-στυρένιο (acrylonitrile butadiene styrene) (ABS), ακρυλονιτρίλιο-ακρυλικό στυρένιο (acrylonitrile styrene acrylate) (ASA) και άλλα συνθετικά ελαστικά όπως τα ελαστικά νιτριλίου (NBR). Ο διμερισμός του ακρυλονιτριλίου δίνει αδιπονιτρίλιο, που χρησιμοποιείται στη σύνθεση συγκεκριμένων πολυαμιδίων. Μικρές ποσότητες χρησιμοποιούνται επίσης ως εντομοκτόνα. Το ακρυλονιτρίλιο και τα παράγωγα, όπως το 2-χλωρο-ακρυλονιτρίλιο, είναι διενόφιλα στις αντιδράσεις Ντίλς-Άλντερ. Το ακρυλονιτρίλιο είναι επίσης πρόδρομη ένωση στη βιομηχανική παρασκευή του ακρυλαμιδίου και του προπενικού οξέος.[2]
Επιπτώσεις στην υγεία[Επεξεργασία | επεξεργασία κώδικα]
Το ακρυλονιτρίλιο είνα πολύ εύφλεκτο και τοξικό. Υφίσταται εκρηκτικό πολυμερισμό. Το καιόμενο υλικό απελευθερώνει ατμούς υδροκυανίου και οξείδια του αζώτου. Ταξινομείται ως ένα πιθανό καρκινογόνο από τον Διεθνή Οργανισμό Ερευνών για τον Καρκίνο (IARC),[5] και οι εργαζόμενοι που εκτίθενται σε υψηλά επίπεδα αιωρούμενου ακρυλονιτριλίου διαγιγνώσκονται πιο συχνά με καρκίνο του πνεύμονα από τον υπόλοιπο πληθυσμό.[6]
Το ακρυλονιτρίλιο αυξάνει τον καρκίνο σε δοκιμές υψηλών δόσεων σε αρσενικούς και θηλυκούς επιμύες και ποντίκια. [7]
Οι τρόποι έκθεσης για τους ανθρώπους περιλαμβάνουν εκπομπή, αυτόματη εξάτμιση και κάπνισμα τσιγάρου, που μπορούν να εκθέσουν τον άνθρωπο άμεσα με την αναπνοή ή το κάπνισμα. Οι οδοί έκθεσης περιλαμβάνουν εισπνοή, από το στόμα και σε κάποια έκταση δερματική πρόσληψη (έχει δοκιμαστεί σε εθελοντές ανθρώπους και σε μελέτες με ποντίκια).[8]
Υπάρχουν δύο κύριες διεργασίες αποβολής του ακρυλονιτριλίου. Η κύρια μέθοδος είναι αποβολή στα ούρα όταν μεταβολίζεται το ακρυλονιτρίλιο όντας ενωμένο άμεσα με την γλουταθειόνη. Η άλλη μέθοδος είναι όταν το ακρυλονιτρίλιο μεταβολίζεται με το οξείδιο του 2-κυανοαιθυλενίου για να παραγάγει κυανιούχα τελικά προϊόντα που σχηματίζουν θειοκυανικά, που αποβάλλονται μέσω των ούρων, ή διοξείδιο του άνθρακα και εξουδετερώνονται στα πνευμόνια.[8]
Το ακρυλονιτρίλιο επάγει απόπτωση των μεσεγχυματικών βλαστικών κυττάρων στον ανθρώπινο ομφάλιο λώρο[9]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 1,2 "NIOSH Pocket Guide to Chemical Hazards #0014", National Institute for Occupational Safety and Health (NIOSH)
- ↑ 2,0 2,1 2,2 2,3 Πρότυπο:Ullmann
- ↑ «The Sohio Acrylonitrile Process». American Chemical Society National Historic Chemical Landmarks. Αρχειοθετήθηκε από το πρωτότυπο στις 23 Φεβρουαρίου 2013. Ανακτήθηκε στις 13 Μαΐου 2013.
- ↑ A. Tullo. «A Solvent Dries Up». Chemical & Engineering News 86: 27. doi:.
- ↑ IARC evaluation of Acrylonitrile
- ↑ EPA:OPPT Chemical Fact Sheets
- ↑ «Animal Test Result on Acrylonitrile in the Carcinogenic Potency Database». Αρχειοθετήθηκε από το πρωτότυπο στις 2 Μαρτίου 2012. Ανακτήθηκε στις 5 Μαΐου 2015.
- ↑ 8,0 8,1 Acrylonitrile Fact Sheet: Support Document (CAS No. 107-13-1)
- ↑ Sun X (Jan 2014). «Cytotoxic effects of acrylonitrile on human umbilical cord mesenchymal stem cells in vitro.». J Mol Med Rep 9 (1): 97–102. doi:. PMID 24248151. http://www.spandidos-publications.com/mmr/9/1/97.
Εξωτερικοί σύνδεσμοι[Επεξεργασία | επεξεργασία κώδικα]
- National Pollutant Inventory - Acrylonitrile
- Comparing Possible Cancer Hazards from Human Exposures to Rodent Carcinogens Αρχειοθετήθηκε 2012-09-03 στο Wayback Machine.
- Acrylonitrile – Integrated Risk Information System, U.S. Environmental Protection Agency
- CDC - NIOSH Pocket Guide to Chemical Hazards - Acrylonitrile
- OSHA Table Z-1 for Air Contaminants
|

