Πρωτοταγής δομή πρωτεΐνης
Η πρωτοταγής δομή της πρωτεΐνης είναι η γραμμική αλληλουχία των αμινοξέων σε πεπτίδιο ή πρωτεΐνη.[1] Κατά συνθήκη, η πρωτοταγής δομή μιας πρωτεΐνης αναφέρεται ξεκινώντας από το αμινο - τερματικό άκρο (Ν) προς το καρβοξυλο - τερματικό άκρο (C). Η πρωτεϊνική βιοσύνθεση εκτελείται συνήθως από τα ριβοσώματα στα κύτταρα. Τα πεπτίδια μπορούν επίσης να συντίθεται στο εργαστήριο. Οι πρωτοταγείς δομές των πρωτεϊνών μπορεί να αλληλουχούνται άμεσα, ή να συνάγονται από αλληλουχίες DNA.
Σχηματισμός[Επεξεργασία | επεξεργασία κώδικα]
Βιολογικός[Επεξεργασία | επεξεργασία κώδικα]
Τα αμινοξέα πολυμερίζονται μέσω πεπτιδικών δεσμών για να σχηματίσουν μια μακρά αλυσίδα, με τις διαφορετικές πλευρικές αλυσίδες αμινοξέων να προεξέχουν κατά μήκος αυτής. Στα βιολογικά συστήματα, οι πρωτεΐνες παράγονται κατά τη διάρκεια της μετάφρασης από τα ριβοσώματα κυττάρου. Μερικοί οργανισμοί μπορούν επίσης να παράγουν μικρά πεπτίδια με σύνθεση μη ριβοσωμικών πεπτιδίων, τα οποία συχνά χρησιμοποιούν αμινοξέα διαφορετικά από τα τυπικά 20 και μπορεί να είναι κυκλοποιημένα, τροποποιημένα και διασυνδεδεμένα.
Χημικός[Επεξεργασία | επεξεργασία κώδικα]
Τα πεπτίδια μπορούν να είναι συντίθεται χημικά μέσω μιας σειράς εργαστηριακών μεθόδων. Οι χημικές μέθοδοι συνθέτουν συνήθως πεπτίδια με την αντίθετη σειρά (ξεκινώντας από το άκρο C) από ό,τι η σύνθεση βιολογικής πρωτεΐνης (ξεκινώντας από το άκρο N).
Σημειογραφία[Επεξεργασία | επεξεργασία κώδικα]
Η πρωτεϊνική αλληλουχία σημειώνεται συνήθως ως μια σειρά από γράμματα, παραθέτοντας τα αμινοξέα που ξεκινούν από το αμινο - τερματικό άκρο προς το καρβοξυλο - τερματικό άκρο. Μπορεί να χρησιμοποιηθεί κωδικός τριών γραμμάτων ή κωδικός ενός γράμματος για να αντιπροσωπεύσει τα 20 φυσικά απαντώμενα αμινοξέα, καθώς και μίγματα ή διφορούμενα αμινοξέα (παρόμοια με τη σημειογραφία των νουκλεϊκών οξέων)[1][2][3]
Τα πεπτίδια μπορεί να αλληλουχούνται άμεσα ή να συνάγονται από αλληλουχίες DNA. Υπάρχουν μεγάλες βάσεις δεδομένων αλληλουχιών που συνδυάζουν γνωστές αλληλουχίες πρωτεϊνών.
| Αμινοξύ | 3-Γράμματα[4] | 1-Γράμμα[4] |
|---|---|---|
| Αλανίνη | Ala | A |
| Αργινίνη | Arg | R |
| Ασπαραγίνη | Asn | N |
| Ασπαραγινικό οξύ | Asp | D |
| Κυστεΐνη | Cys | C |
| Γλουταμινικό οξύ | Glu | E |
| Γλουταμίνη | Gln | Q |
| Γλυκίνη | Gly | G |
| Ιστιδίνη | His | H |
| Ισολευκίνη | Ile | I |
| Λευκίνη | Leu | L |
| Λυσίνη | Lys | K |
| Μεθειονίνη | Met | M |
| Φαινυλαλανίνη | Phe | F |
| Προλίνη | Pro | P |
| Σερίνη | Ser | S |
| Θρεονίνη | Thr | T |
| Τρυπτοφάνη | Trp | W |
| Τυροσίνη | Tyr | Y |
| Βαλίνη | Val | V |
| Σύμβολο | Περιγραφή | Εμφανιζόμενα υπολείμματα |
|---|---|---|
| X | Οποιοδήποτε αμινοξύ, ή άγνωστο | All |
| B | Ασπαργανικό, ή ασπαραγίνη | D, N |
| Z | Γλουταμινικό, ή γλουταμίνη | E, Q |
| J | Λευκίνη ή ισολευκίνη | I, L |
| Φ | Υδρόφοβο | V, I, L, F, W, M |
| Ω | Αρωματικό | F, W, Y, H |
| Ψ | Αλειφατικό | V, I, L, M |
| π | Μικρό | P, G, A, S |
| ζ | Υδρόφιλο | S, T, H, N, Q, E, D, K, R, Y |
| + | Θετικά φορτισμένο | K, R, H |
| - | Αρνητικά φορτισμένο | D, E |
Τροποποίηση[Επεξεργασία | επεξεργασία κώδικα]
Γενικά, τα πολυπεπτίδια είναι μη διακλαδισμένα πολυμερή, επομένως η πρωτοταγής δομή τους μπορεί συχνά να προσδιοριστεί από την αλληλουχία των αμινοξέων κατά μήκος του κορμού τους. Ωστόσο, οι πρωτεΐνες μπορούν να γίνουν διασταυρωμένες, συνήθως από δισουλφιδικούς δεσμούς και η πρωτοταγής δομή απαιτεί επίσης τον προσδιορισμό των διασταυρούμενων ατόμων, π.χ., τον καθορισμό των κυστεϊνών που εμπλέκονται στους δισουλφιδικούς δεσμούς της πρωτεΐνης. Άλλοι διασταυρώσεις περιλαμβάνουν τη δεσμοσίνη.
Ισομερίωση[Επεξεργασία | επεξεργασία κώδικα]
Τα χειρόμορφα κέντρα μιας πολυπεπτιδικής αλυσίδας μπορούν να υποστούν ρακεμοποίηση. Αν και δεν αλλάζει την αλληλουχία, επηρεάζει τις χημικές ιδιότητες της αλληλουχίας. Ειδικότερα, τα L -αμινοξέα που βρίσκονται συνήθως σε πρωτεΐνες μπορούν να ισομεριστούν αυθόρμητα στο άτομο για να σχηματίσουν D-αμινοξέα, τα οποία δεν μπορούν να διασπαστούν από τις περισσότερες πρωτεάσες. Επιπρόσθετα, η προλίνη μπορεί να σχηματίσει σταθερά trans-ισομερή στον πεπτιδικό δεσμό.
Μετα-μεταφραστική τροποποίηση[Επεξεργασία | επεξεργασία κώδικα]
Τέλος, η πρωτεΐνη μπορεί να υποβληθεί σε μια ποικιλία μετα-μεταφραστικών τροποποιήσεων, οι οποίες συνοψίζονται εν συντομία εδώ.
Η Ν-τερματική αμινομάδα ενός πολυπεπτιδίου μπορεί να τροποποιηθεί ομοιοπολικά, π.χ.
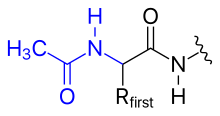
- ακετυλίωση
- Το θετικό φορτίο στην Ν-τερματική αμινομάδα μπορεί να εξαλειφθεί αλλάζοντας το σε ακετυλομάδα (Ν-τερματικός αποκλεισμός).
- φορμυλίωση
- Η Ν-τελική μεθειονίνη που βρίσκεται συνήθως μετά τη μετάφραση έχει ένα Ν-άκρο μπλοκαρισμένο με μια φορμυλική ομάδα. Αυτή η ομάδα φορμυλίου (και μερικές φορές το ίδιο το υπόλειμμα της μεθειονίνης, εάν ακολουθείται από Gly ή Ser) απομακρύνεται από το ένζυμο αποφορμυλάση.
- "'πυρογλουταμικό"'
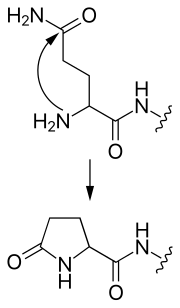
- Μια Ν-τερματική γλουταμίνη μπορεί να προσβάλει τον εαυτό της, σχηματίζοντας μια κυκλική ομάδα πυρογλουταμικού.
- μυριστοϋλίωση (myristoylation)
- Παρόμοιa με την ακετυλίωση. Αντί για μια απλή ομάδα μεθυλίου, η ομάδα μυριστοϋλίου έχει ουρά 14 υδρόφοβων ανθράκων, οι οποίες την καθιστούν ιδανική για την αγκύρωση πρωτεϊνών σε κυτταρικές μεμβράνες.
Η C-τερματική καρβοξυλική ομάδα ενός πολυπεπτιδίου μπορεί επίσης να τροποποιηθεί, π.χ.
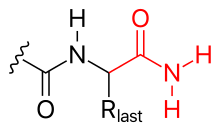
- αμίνωση (βλέπε σχήμα)
- Το C-τερματικό μπορεί επίσης να μπλοκαριστεί (εξουδετερώνοντας, έτσι, το αρνητικό του φορτίο) με αμίνωση.
- προσκόλληση γλυκοζυλοφωσφατιδυλινοσιτόλης (GPI)
- Η γλυκοζυλοφωσφατιδυλινοσιτόλη (GPI) είναι μια μεγάλη, υδρόφοβη φωσφολιπιδική προσθετική ομάδα που προσδένεται πρωτεΐνες στις κυτταρικές μεμβράνες. Συνδέεται στο C-άκρο του πολυπεπτιδίου μέσω ενός αμιδικού δεσμού που στη συνέχεια συνδέεται με αιθανολαμίνη, από εκεί σε διάφορα σάκχαρα και τέλος με τη μονάδα λιπιδίου φωσφατιδυλοσινοτόλης.
Τέλος, οι πλευρικές αλυσίδες μπορεί επίσης να τροποποιηθούν ομοιοπολικά, π.χ.
- φωσφορυλίωση
- Εκτός από τη διάσπαση, η φωσφορυλίωση είναι ίσως η πιο σημαντική χημική τροποποίηση των πρωτεϊνών. Μια φωσφορική ομάδα μπορεί να προσκολληθεί στην ομάδα υδροξυλίου της πλευρικής αλυσίδας των υπολειμμάτων σερίνης, θρεονίνης και τυροσίνης, προσθέτοντας αρνητικό φορτίο σε αυτήν τη θέση και παράγοντας ένα αφύσικο αμινοξύ. Τέτοιες αντιδράσεις καταλύονται από κινάσες και η αντίστροφη αντίδραση καταλύεται από φωσφατάσες. Οι φωσφορυλιωμένες τυροσίνες χρησιμοποιούνται συχνά ως "λαβές" με τις οποίες οι πρωτεΐνες μπορούν να συνδεθούν μεταξύ τους, ενώ η φωσφορυλίωση της Ser/Thr προκαλεί συχνά διαμορφωτικές αλλαγές, πιθανώς λόγω του εισαγόμενου αρνητικού φορτίου. Οι επιδράσεις της φωσφορυλίωσης των Ser/Thr μπορεί μερικές φορές να προσομοιωθούν μεταλλάσσοντας το υπόλειμμα Ser/Thr σε γλουταμινικό.
- γλυκοσυλίωση
- Ένα γενικό όνομα για ένα σύνολο πολύ κοινών και πολύ ετερογενών χημικών τροποποιήσεων. Τα τμήματα σακχάρου μπορούν να προσκολληθούν στις υδοξυλομάδες της πλευρικής αλυσίδας των Ser/Thr ή στις αμιδομάδες της πλευρικής αλυσίδας του Asn. Τέτοιες προσκολλήσεις μπορούν να εξυπηρετούν πολλές λειτουργίες, από την αύξηση της διαλυτότητας έως την πολύπλοκη αναγνώριση. Όλη η γλυκοσυλίωση μπορεί να αποκλειστεί με ορισμένους αναστολείς, όπως η τινικαμυκίνη.
- απαμίδωση (σχηματισμός ηλεκτριμιδίου)
- Σε αυτήν την τροποποίηση, μια πλευρική αλυσίδα ασπαραγίνης ή ασπαρτικού προσβάλλει τον ακόλουθο πεπτιδικό δεσμό, σχηματίζοντας ένα συμμετρικό ενδιάμεσο ηλεκτριμίδιο. Η υδρόλυση του ενδιαμέσου παράγει είτε ασπαρτικό είτε β-αμινοξύ, ισο(Asp). Για την ασπαραγίνη, οποιοδήποτε από τα δύο προϊόντα έχει ως αποτέλεσμα την απώλεια της αμιδικής ομάδας, εξ ου και η απαμίδωση.
- υδροξυλίωση
- Τα υπολείμματα προλίνης μπορεί να είναι υδροξυλικά σε οποιοδήποτε από τα δύο άτομα, όπως μπορεί και λυσίνη (σε ένα άτομο). Η υδροξυπρολίνη είναι ένα κρίσιμο συστατικό του κολλαγόνου, το οποίο καθίσταται ασταθές μετά την απώλεια της. Η αντίδραση υδροξυλίωσης καταλύεται από ένα ένζυμο που απαιτεί βιταμίνη C (ασκορβικό οξύ), ανεπάρκεια του οποίου οδηγεί σε πολλές ασθένειες του συνδετικού ιστού όπως σκορβούτο.
- μεθυλίωση
- Αρκετά υπολείμματα πρωτεϊνών μπορούν να μεθυλιωθούν, κυρίως οι θετικές ομάδες της λυσίνης και της αργινίνης. Τα υπολείμματα αργινίνης αλληλεπιδρούν με τον φωσφορικό σκελετό του νουκλεϊκού οξέος και συνήθως σχηματίζουν δεσμούς υδρογόνου με τα υπολείμματα βάσης, ιδιαίτερα με τη γουανίνη, σε σύμπλοκα πρωτεΐνης-DNA. Τα υπολείμματα λυσίνης μπορούν να μεθυλιωθούν μεμονωμένα, διπλά και ακόμη και τριπλά. Ωστόσο, η μεθυλίωση δεν αλλάζει το θετικό φορτίο στην πλευρική αλυσίδα.
- ακετυλίωση
- Η ακετυλίωση των αμινομάδων λυσίνης είναι χημικά ανάλογη με την ακετυλίωση του Ν-άκρου. Λειτουργικά, ωστόσο, η ακετυλίωση υπολειμμάτων λυσίνης χρησιμοποιείται για ρύθμιση της δέσμευσης πρωτεϊνών με νουκλεϊκά οξέα. Η ακύρωση του θετικού φορτίου στη λυσίνη αποδυναμώνει την ηλεκτροστατική έλξη για τα (αρνητικά φορτισμένα) νουκλεϊκά οξέα.
- θείωση
- Οι τυροσίνες ενδέχεται να θειωθούν στο άτομο τους. Κάπως ασυνήθιστα, αυτή η τροποποίηση συμβαίνει στο σωμάτιο Golgi και όχι στο ενδοπλασματικό δίκτυο. Παρόμοια με τις φωσφορυλιωμένες τυροσίνες, οι θειωμένες τυροσίνες χρησιμοποιούνται για ειδική αναγνώριση, π.χ., σε υποδοχείς χημειοκίνης στην κυτταρική επιφάνεια. Όπως με τη φωσφορυλίωση, η θείωση προσθέτει ένα αρνητικό φορτίο σε μια προηγουμένως ουδέτερη θέση.
- πρενυλίωση και παλμιτοϋλίωση
- Οι υδρόφοβες ομάδες ισοπρενίου (π.χ. ομάδες φαρνεζυλίου, γερανίου και γερανυλγερανυλίου) και παλμιτοϋλίου μπορούν να προστεθούν στο άτομο των υπολειμμάτων κυστεΐνης για να προσδέσουν τις πρωτεΐνες στις κυτταρικές μεμβράνες. Σε αντίθεση με τις προσδέσεις γλυκοσυλφωσφατιδυλινοσιτόλη (GPI) και μυριτοϋλίου, αυτές οι ομάδες δεν προστίθενται απαραίτητα στα άκρα.
- καρβοξυλίωση
- Μια σχετικά σπάνια τροποποίηση που προσθέτει μια επιπλέον καρβοξυλική ομάδα (και, ως εκ τούτου, ένα διπλό αρνητικό φορτίο) σε μια πλευρική αλυσίδα γλουταμινικού, παράγοντας ένα υπόλειμμα Gla. Αυτό χρησιμοποιείται για την ενίσχυση της δέσμευσης στα σκληρά μεταλλικά ιόντα όπως το ασβέστιο.
- ADP-ριβοσυλίωση
- Η μεγάλη ομάδα ADP-ριβοσυλίου μπορεί να μεταφερθεί σε διάφορους τύπους πλευρικών αλυσίδων εντός πρωτεϊνών, με ετερογενή αποτελέσματα. Αυτή η τροποποίηση είναι στόχος για τις ισχυρές τοξίνες ανόμοιων βακτηρίων, π.χ. "Vibrio cholerae", "Corynebacterium diphtheriae" και "Bordetella pertussis".
- ADP-ribosylation
- Ουμπικουιτινοποίηση και SUMOποίηση (SUMO = Small Ubiquitin-like Modifier)
- Διάφορες, πλήρους μήκους, διπλωμένες πρωτεΐνες μπορούν να προσκολληθούν στα C-άκρα τους στις ομάδες αμμωνίου πλευρικής αλυσίδας λυσινών άλλων πρωτεϊνών. Η ουμπικιτίνη είναι η πιο κοινή από αυτές και συνήθως σηματοδοτεί ότι η πρωτεΐνη με επισημασμένη ουμπικιτίνη πρέπει να αποικοδομηθεί.
Οι περισσότερες από τις τροποποιήσεις του πολυπεπτιδίου που αναφέρονται παραπάνω εμφανίζονται μετά την μετάφραση, δηλαδή, αφού η πρωτεΐνη έχει συντεθεί στο ριβόσωμα, που συμβαίνει συνήθως στο ενδοπλασματικό δίκτυο, ένα υποκυτταρικό οργανίδιο του ευκαρυωτικού κυττάρου.
Πολλές άλλες χημικές αντιδράσεις (π.χ. κυανυλίωση) έχουν εφαρμοστεί σε πρωτεΐνες από χημικούς, αν και δεν βρίσκονται σε βιολογικά συστήματα.
Διάσπαση και συνένωση[Επεξεργασία | επεξεργασία κώδικα]
Εκτός από αυτά που αναφέρονται παραπάνω, η πιο σημαντική τροποποίηση της πρωτοταγούς δομής είναι η διάσπαση του πεπτιδίου (με χημική υδρόλυση ή από ππρωτεάσες. Οι πρωτεΐνες συχνά συντίθενται σε ανενεργή πρόδρομη μορφή. Συνήθως, ένα Ν-τερματικό ή C-τερματικό τμήμα μπλοκάρει την ενεργή θέση της πρωτεΐνης, αναστέλλοντας τη λειτουργία της. Η πρωτεΐνη ενεργοποιείται διασπώντας το ανασταλτικό πεπτίδιο.
Ορισμένες πρωτεΐνες έχουν ακόμη τη δύναμη να διασπαστούν οι ίδιες. Συνήθως, η υδροξυλομάδα μιας σερίνης (σπάνια, θρεονίνης) ή η ομάδα θειόλης ενός υπολείμματος κυστεΐνης θα προσβάλει τον καρβονυλάνθρακα του προηγούμενου πεπτιδικού δεσμού, σχηματίζοντας ένα τετραεδρικά ενωμένο ενδιάμεσο [ταξινομημένο ως ενδιάμεσο υδροξυοξαζολιδίνη (Ser / Thr) ή υδροξυθειαζολιδίνη ( Cys)]. Αυτό το ενδιάμεσο τείνει να επανέλθει στη μορφή αμιδίου, εκδιώκοντας την επιθετική ομάδα, αφού η μορφή αμιδίου προτιμάται συνήθως από την ελεύθερη ενέργεια (πιθανώς λόγω της ισχυρής σταθεροποίησης συντονισμού της πεπτιδικής ομάδας). Ωστόσο, επιπρόσθετες μοριακές αλληλεπιδράσεις μπορεί να καταστήσουν τη μορφή αμιδίου λιγότερο σταθερή. η αμινομάδα αποβάλλεται αντ 'αυτής, με αποτέλεσμα έναν δεσμό εστέρα (Ser / Thr) ή θειοεστέρα (Cys) στη θέση του πεπτιδικού δεσμού. Ο δεσμός εστέρα/θειοεστέρα μπορεί να διασπαστεί με διάφορους τρόπους:
- Η απλή υδρόλυση θα χωρίσει την πολυπεπτιδική αλυσίδα, όπου η εκτοπισμένη αμινομάδα γίνεται το νέο Ν-άκρο. Αυτό φαίνεται στην ωρίμανση της γλυκοζυλοασπαραργινάσης.
- Μια αντίδραση β-απομάκρυνσης χωρίζει επίσης την αλυσίδα, αλλά οδηγεί σε μια ομάδα πυρουβοϋλίου στο νέο Ν-άκρο. Αυτή η πυρουβοϋλομάδα μπορεί να χρησιμοποιηθεί ως ένας ομοιοπολικώς συνδεδεμένος καταλυτικός συμπαράγοντας σε ορισμένα ένζυμα, ειδικά σε αποκαρβοξυλάσες όπως η S-αδενοσυλμεθειονική αποκαρβοξυλάση (S-adenosylmethionine decarboxylase ή SAMDC) που εκμεταλλεύονται την ισχύ ως δέκτη ηλεκτρονίων της πυρουβοϋλικής (pyruvoyl) ομάδας.
- Ενδομοριακή διεστεροποίηση, με αποτέλεσμα ένα "διακλαδισμένο" πολυπεπτίδιο. Σε ιντεΐνες (inteins), ο νέος εστερικός δεσμός διασπάται από μια ενδομοριακή επίθεση από την επικείμενη C-τερματική ασπαραγίνη.
- Η διαμοριακή διεστεροποίηση μπορεί να μεταφέρει ένα ολόκληρο τμήμα από το ένα πολυπεπτίδιο στο άλλο, όπως φαίνεται στην αυτοεπεξεργασία της πρωτεΐνης Hedgehog
Συμπίεση αλληλουχίας[Επεξεργασία | επεξεργασία κώδικα]
Η συμπίεση των αλληλουχιών αμινοξέων είναι ένα σχετικά δύσκολο έργο. Οι υπάρχοντες εξειδικευμένοι συμπιεστές αλληλουχίας αμινοξέων είναι χαμηλοί σε σύγκριση με εκείνους των συμπιεστών αλληλουχίας DNA, κυρίως λόγω των χαρακτηριστικών των δεδομένων. Για παράδειγμα, οι αντιστροφές μοντέλων είναι δυσκολότερες λόγω της αντίστροφης απώλειας πληροφοριών (από τα αμινοξέα προς την αλληλουχία DNA). Ο τρέχων συμπιεστής δεδομένων χωρίς απώλειες που παρέχει υψηλότερη συμπίεση είναι ο AC2. .[5] Ο AC2 συνδυάζει διάφορα μοντέλα περιβάλλοντος χρησιμοποιώντας νευρωνικά δίκτυα και κωδικοποιεί τα δεδομένα χρησιμοποιώντας αριθμητική κωδικοποίηση.
Ιστορικό[Επεξεργασία | επεξεργασία κώδικα]
Η πρόταση ότι οι πρωτεΐνες ήταν γραμμικές αλυσίδες α-αμινοξέων έγινε σχεδόν ταυτόχρονα από δύο επιστήμονες στο ίδιο συνέδριο το 1902, την 74η συνάντηση της Εταιρείας Γερμανών Επιστημόνων και Ιατρών, που πραγματοποιήθηκε στο Καρλσμπάντ. Ο Franz Hofmeister υπέβαλε την πρόταση το πρωί, με βάση τις παρατηρήσεις του σχετικά με την αντίδραση διουρίας στις πρωτεΐνες. Ο Χοφμάιστερ (Hofmeister) ακολούθησε λίγες ώρες αργότερα από τον Εμίλ Φίσερ, ο οποίος είχε συγκεντρώσει πληθώρα χημικών λεπτομερειών που υποστήριζαν το μοντέλο πεπτιδικού δεσμού. Για πληρότητα, η πρόταση ότι οι πρωτεΐνες περιείχαν αμιδικούς δεσμούς υποβλήθηκε ήδη από το 1882 από τον Γάλλο χημικό E. Grimaux. [6]
Παρά αυτά τα δεδομένα και τις μεταγενέστερες ενδείξεις ότι οι πρωτεολυτικά χωνευμένες πρωτεΐνες απέδωσαν μόνο ολιγοπεπτίδια, η ιδέα ότι οι πρωτεΐνες ήταν γραμμικά, μη διακλαδισμένα πολυμερή αμινοξέων δεν έγινε αποδεκτή αμέσως. Μερικοί αξιοσέβαστοι επιστήμονες όπως ο William Astbury αμφισβήτησαν ότι οι ομοιοπολικοί δεσμοί ήταν αρκετά ισχυροί για να συγκρατούν μαζί τόσο μακριά μόρια. Φοβόντουσαν ότι οι θερμικές αναταράξεις θα δονούσαν τόσο μακριά μόρια. Ο Χέρμαν Στάουντινγκερ αντιμετώπισε παρόμοιες προκαταλήψεις τη δεκαετία του 1920 όταν υποστήριξε ότι το καουτσούκ αποτελούταν από μακρομόρια. [6]
Έτσι, προέκυψαν διάφορες εναλλακτικές υποθέσεις. Η υπόθεση της κολλοειδούς πρωτεΐνης δήλωνε ότι οι πρωτεΐνες ήταν κολλοειδή συγκροτήματα μικρότερων μορίων. Αυτή η υπόθεση αποδείχθηκε τη δεκαετία του 1920 με μετρήσεις υπερφυγοκέντρησης από τον Theodor Svedberg που έδειξαν ότι οι πρωτεΐνες είχαν ένα καλά καθορισμένο, αναπαραγώγιμο μοριακό βάρος και με ηλεκτροφορητικές μετρήσεις από τον Arne Tiselius που έδειξαν ότι οι πρωτεΐνες ήταν μεμονωμένα μόρια. Μια δεύτερη υπόθεση, η υπόθεση κυκλόλης που προχώρησε από τον Dorothy Wrinch, πρότεινε ότι το γραμμικό πολυπεπτίδιο υποβλήθηκε σε χημική αναδιάταξη κυκλόλης C = O + HN C(OH)-N που διασύνδεσε τις αμιδικές ομάδες του κορμού, σχηματίζοντας ένα δισδιάστατο "ύφασμα". Άλλες πρωτοταγείς δομές πρωτεϊνών προτάθηκαν από διάφορους ερευνητές, όπως το πρότυπο δικετοπιπεραζίνης (diketopiperazine) του Emil Abderhalden και το πρότυπο πυρρολ/πιπεριδίνης του Troensegaard το 1942. Αν και ποτέ δεν τους αποδόθηκε ιδιαίτερη αξιοπιστία, αυτά τα εναλλακτικά πρότυπα τελικά απορρίφθηκαν όταν Φρέντερικ Σάνγκερ αλληλούχισε με επιτυχία την ινσουλίνη και με τον κρυσταλλογραφικό προσδιορισμό της μυοσφαιρίνης και της αιμοσφαιρίνης από τους Max Perutz και John Kendrew.
Κύρια δομή σε άλλα μόρια[Επεξεργασία | επεξεργασία κώδικα]
Οποιοδήποτε ετεροπολυμερές γραμμικής αλυσίδας μπορεί να θεωρηθεί ότι έχει πρωτογενή δομή κατ 'αναλογία με τη χρήση του όρου για πρωτεΐνες, αλλά αυτή η χρήση είναι σπάνια σε σύγκριση με την εξαιρετικά κοινή χρήση σε σχέση με πρωτεΐνες. Στο RNA, το οποίο έχει επίσης εκτεταμένη δευτεροταγή δομή, η γραμμική αλυσίδα των βάσεων αναφέρεται γενικά ως η αλληλουχία όπως είναι στο DNA (η οποία συνήθως σχηματίζει μια γραμμική διπλή έλικα με μικρή δευτεροταγή δομή). Άλλα βιολογικά πολυμερή όπως πολυσακχαρίτες μπορούν επίσης να θεωρηθούν ότι έχουν μια πρωτοταγή δομή, αν και η χρήση δεν είναι πρότυπη.
Σχέση με τη δευτεροταγή και τριτοταγή δομή[Επεξεργασία | επεξεργασία κώδικα]
Η κύρια δομή ενός βιολογικού πολυμερούς καθορίζει σε μεγάλο βαθμό το τρισδιάστατο σχήμα (τριτοταγής δομή). Η αλληλουχία πρωτεϊνών μπορεί να χρησιμοποιηθεί για πρόβλεψη τοπικών χαρακτηριστικών, όπως τμήματα δευτεροταγούς δομής ή περιοχές trans-μεμβράνης. Ωστόσο, η πολυπλοκότητα της αναδίπλωσης της πρωτεΐνης προς το παρόν απαγορεύει την πρόβλεψη της τριτοταγούς δομής μιας πρωτεΐνης μόνο από την αλληλουχία της. Γνωρίζοντας τη δομή μιας παρόμοιας ομόλογης αλληλουχίας (για παράδειγμα ένα μέλος της ίδιας οικογένειας πρωτεΐνης) επιτρέπει πολύ ακριβή πρόβλεψη της τριτοταγούς δομής από προτυποποίηση ομολογίας. Εάν είναι διαθέσιμη η αλληλουχία πρωτεΐνης πλήρους μήκους, είναι δυνατόν να εκτιμηθούν οι γενικές βιοφυσικές της ιδιότητες, όπως το ισοηλεκτρικό σημείο της.
Οι οικογένειες αλληλουχιών καθορίζονται συχνά από ομαδοποίηση αλληλουχίας και δομική γονιδιωματική και στοχεύουν στην παραγωγή ενός συνόλου αντιπροσωπευτικών δομών για την κάλυψη του χώρου αλληλουχίας των πιθανών μη περιττών αλληλουχιών.
Δείτε επίσης[Επεξεργασία | επεξεργασία κώδικα]
Σημειώσεις και παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 SANGER F (1952). «The arrangement of amino acids in proteins». Στο: M.L. Anson· Kenneth Bailey· John T. Edsall. Advances in Protein Chemistry. 7. σελίδες 1–67. doi:10.1016/S0065-3233(08)60017-0. ISBN 9780120342075. PMID 14933251.
- ↑ Aasland, Rein; Abrams, Charles; Ampe, Christophe; Ball, Linda J.; Bedford, Mark T.; Cesareni, Gianni; Gimona, Mario; Hurley, James H. και άλλοι. (2002-02-20). «Normalization of nomenclature for peptide motifs as ligands of modular protein domains». FEBS Letters 513 (1): 141–144. doi:. ISSN 1873-3468.
- ↑ «A One-Letter Notation for Amino Acid Sequences*». European Journal of Biochemistry 5 (2): 151–153. 1968-07-01. doi:. ISSN 1432-1033. PMID 11911894.
- ↑ 4,0 4,1 Hausman, Robert E.· Cooper, Geoffrey M. (2004). The cell: a molecular approach. Washington, D.C: ASM Press. σελ. 51. ISBN 978-0-87893-214-6.
- ↑ Silva M, Pratas D, Pinho AJ (April 2021). «AC2: An Efficient Protein Sequence Compression Tool Using Artificial Neural Networks and Cache-Hash Models». Entropy 23: 530. doi:.
- ↑ 6,0 6,1 Fruton JS (May 1979). «Early theories of protein structure». Ann. N. Y. Acad. Sci. 325: xiv, 1–18. doi:. PMID 378063.








