Μελοξικάμη
 | |
 | |
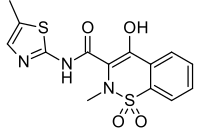
| Ονομασία IUPAC | |
|---|---|
4-υδροξυλο-2-μεθυλο-N-(5-μεθυλο-2-θιαζολύλη)-2H-1,2-βενζοθειαζίνη-3-καρβοξαμίδη-1,1-διοξείδιο | |
| Κλινικά δεδομένα | |
| Εμπορικές ονομασίες | Mobic, Metacam, Anjeso, others |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a601242 |
| Δεδομένα άδειας | |
| Κατηγορία ασφαλείας κύησης | |
| Οδοί χορήγησης | Μέσω στόματος, IV |
| Κυκλοφορία | |
| Κυκλοφορία |
|
| Φαρμακοκινητική | |
| Βιοδιαθεσιμότητα | 89%[2] |
| Πρωτεϊνική σύνδεση | 99.4%[2] |
| Μεταβολισμός | Συκώτι (μεσολαβούν τα ένζυμα CYP2C9 και 3A4)[2] |
| Βιολογικός χρόνος ημιζωής | 20 ώρες[2] |
| Απέκκριση | Σε ισοδύναμες ποσότητες στα περιττώματα και τα ούρα[2] |
| Κωδικοί | |
| Αριθμός CAS | 71125-38-7 |
| Κωδικός ATC | M01AC06 M01AC56, QM01AC06 (WHO), QM01AC56 (WHO) |
| PubChem | CID 5281106 |
| IUPHAR/BPS | 7220 |
| DrugBank | DB00814 |
| ChemSpider | 10442740 |
| UNII | VG2QF83CGL |
| KEGG | D00969 |
| ChEBI | CHEBI:6741 |
| ChEMBL | CHEMBL599 |
| PDB ID | MXM (PDBe, RCSB PDB) |
| Χημικά στοιχεία | |
| Χημικός τύπος | C14H13N3O4S2 |
| Μοριακή μάζα | 351,40 g·mol−1 |
Cc1cnc(s1)NC(=O)C\3=C(/O)c2ccccc2S(=O)(=O)N/3C | |
InChI=1S/C14H13N3O4S2/c1-8-7-15-14(22-8)16-13(19)11-12(18)9-5-3-4-6-10(9)23(20,21)17(11)2/h3-7,18H,1-2H3,(H,15,16,19) Key:ZRVUJXDFFKFLMG-UHFFFAOYSA-N | |
| (verify) | |
Η μελοξικάμη (εμπορική ονομασία: Mobic και άλλες) είναι ένα μη στεροειδές αντιφλεγμονώδες φάρμακο (ΜΣΑΦ) το οποίο χρησιμοποιείται για τη θεραπεία του πόνου και της φλεγμονής σε άτομα που πάσχουν από ρευματικές παθήσεις ή από οστεοαρθρίτιδα.[3] Μπορεί να ληφθεί είτε με κατάποση από το στόμα ή με ενδοφλέβια ένεση.[4] Συνιστάται να χρησιμοποιείται όσο το δυνατόν λιγότερες ημέρες και σε χαμηλή ποσότητα.
Οι κοινές παρενέργειες από τη χρήση μελοξικάμης συμπεριλαμβάνουν το κοιλιακό άλγος, τη ζάλη, το οίδημα, τη κεφαλαλγία και το εξάνθημα.[4] Οι σοβαρές παρενέργειες από τη χρήση μελοξικάμης περιλαμβάνουν: καρδιακή νόσο, εγκεφαλικό επεισόδιο, προβλήματα στα νεφρά καθώς και στομαχικό έλκος. Για τις γυναίκες που διανύουν το τρίτο τρίμηνο της εγκυμοσύνης, συνίσταται να μην την χρησιμοποιούν. Αναστέλλει την λειτουργία της κυκλοοξυγεννάσης-2 (COX-2) περισσότερο απ'όσο αναστέλλει την κυκλοοξυγεννάση-1 (COX-1). Ανήκει στην ομάδα χημικών ενώσεων των οξικαμών και συνδέεται στενά με την πιροξικάμη.
Το δίπλωμα ευρεσιτεχνίας της μελοξικάμης καταχωρήθηκε το 1977. Στις Ηνωμένες Πολιτείες, η χρήση της για ιατρικούς σκοπούς εγκρίθηκε το 2000.[4][5] Αναπτύχθηκε από την Boehringer Ingelheim. Είναι διαθέσιμο και ως γενόσημο φάρμακο. Το 2017, ήταν το 38ο πιο συνταγογραφημένο φάρμακο στις Ηνωμένες Πολιτείες με πάνω από 19 εκατομμύρια συνταγογραφήσεις.[6][7]
Δυσμενείς επιπτώσεις
[Επεξεργασία | επεξεργασία κώδικα]Η χρήση μελοξικάμης μπορεί να προκαλέσει γαστρεντερική τοξικότητα και αιμορραγία, πονοκεφάλους, εξανθήματα, καθώς και έκκριση κοπράνων με πολύ σκούρο ή μαύρο χρώμα (η έκκριση τέτοιου είδους κοπράνων είναι σημάδι εντερικής αιμορραγίας). Όπως και άλλα ΜΣΑΦ, η χρήση μελοξικάμης αυξάνει το κίνδυνο εκδήλωσης καρδιαγγειακών επιπλοκών, στα οποία συμπεριλαμβάνονται η καρδιακή προσβολή και το εγκεφαλικό επεισόδιο.[8] Έχει λιγότερες γαστρεντερικές παρενέργειες από τη δικλοφενάκη, τη πιροξικάμη,[9] τη ναπροξένη,[10] και ίσως απ'όλα τα υπόλοιπα ΜΣΑΦ, τα οποία δεν είναι επιλεκτικά στην κυκλοοξυγενάση-2.[11] Αν και η μελοξικάμη αναστέλλει το σχηματισμό της θρομβοξάνης Α, φαίνεται ότι δεν το κάνει σε επίπεδα που θα μπορούσαν να επηρεάσουν την λειτουργία των αιμοπεταλίων.
Μια συγκεντρωτική ανάλυση τυχαιοποιημένων, ελεγχόμενων μελετών όπου οι εξεταζόμενοι ασθενείς χρησιμοποιούσαν την μελοξικάμη για θεραπεία για 60 ημέρες διαπίστωσε ότι η χρήση μελοξικάμης συνδεόταν με σημαντικά χαμηλότερη πιθανότητα εκδήλωσης θρομβοεμβολικών επιπλοκών σε σύγκριση με ένα άλλο ΜΣΑΦ, τη δικλοφενάκη (η πιθανότητα με χρήση μελοξικάμης έφτανε το 0.2%, ενώ με δικλοφενάκη έφτανε το 0.8%). Ωστόσο η πιθανότητα εμφάνισης θρομβοεμβολικών επιπλοκών σε ασθενείς που χρησιμοποιούν μελοξικάμη είναι παρόμοια με αυτούς που χρησιμοποιούν ναπροξένη ή πιροξικάμη.[12]
Καρδιαγγειακές επιπλοκές
[Επεξεργασία | επεξεργασία κώδικα]Τα άτομα με υπέρταση, υψηλά νούμερα χοληστερόλης ή διαβήτη έχουν πιθανότητα εκδήλωσης καρδιαγγειακών επιπλοκών από τη χρήση μελοξικάμης. Τα άτομα με οικογενειακό ιστορικό εμφάνισης καρδιακής νόσου, καρδιακής προσβολής ή εγκεφαλικού επεισοδίου πρέπει να ενημερώσουν τον θεράποντα ιατρό τους, καθώς υπάρχει σημαντική πιθανότητα εκδήλωσης σοβαρών καρδιαγγειακών επιπλοκών.[13][14]
Γαστρεντερικές επιπλοκές
[Επεξεργασία | επεξεργασία κώδικα]Η κατανάλωση ΜΣΑΦ προκαλεί και αυξάνει την πιθανότητα εμφάνισης σοβαρών γαστρεντερικών ανεπιθύμητων επιπλοκών (συμπεριλαμβανομένης της αιμορραγίας, της εξέλκωσης και της διάτρησης του στομάχου ή των εντέρων), οι οποίες μπορούν να οδηγήσουν ακόμη και σε θάνατο. Οι ηλικιωμένοι ασθενείς διατρέχουν μεγαλύτερο κίνδυνο για σοβαρές γαστρεντερικές εκδηλώσεις.[15]
Επιπλοκές στο στόμα
[Επεξεργασία | επεξεργασία κώδικα]Για όσους πρόκειται να υποβληθούν σε χειρουργεία ή σε οδοντιατρικές επεμβάσεις, συνιστάται να σταματήσουν την χρήση μελοξικάμης για τέσσερις με έξι ημιζωές. Υπάρχει αυξημένη πιθανότητα εμφάνισης γευστικής διαστροφής, ελκώδους στοματίτιδας και ξηροστομίας.
Μηχανισμός δράσης
[Επεξεργασία | επεξεργασία κώδικα]Η μελοξικάμη αναστέλλει την κυκλοοξυγενάση (COX), το ένζυμο που ευθύνεται για τη μετατροπή του αραχιδονικού οξέος σε προσταγλανδίνη H2. Η εν λόγω μετατροπή είναι το πρώτο βήμα για την σύνθεση προσταγλανδινών, οι οποίες είναι μεσολαβητές της φλεγμονής. Έχει αποδειχθεί, ότι ειδικά αν ο θεραπευόμενος ασθενείς λαμβάνει μελοξικάμη σε χαμηλές θεραπευτικές δόσεις, αναστέλλει περισσότερο την κυκλοοξυγενάση-2 απ'ότι την κυκλοοξυγενάση-1.[2]
Οι συγκεντρώσεις μελοξικάμης στο αρθρικό υγρό αντιστοιχούν στο 40% με 50% των αντιστοίχων συγκεντρώσεων στο πλάσματο. Το ελεύθερο κλάσμα στο αρθρικό υγρό είναι 2.5 φορές υψηλότερο σε σχέση με το πλάσμα, επειδή οι συγκεντρώσεις λευκωματίνης στο αρθρικό υγρό είναι μικρότερες σε σύγκριση με το πλάσμα. Η σημασία αυτής της διείσδυσης είναι άγνωστη,[15] αλλά μπορεί να ευθύνεται για το γεγονός ότι αποδίδει εξαιρετικά καλά στην θεραπεία της αρθρίτιδας σε ζώα.[16]
Φαρμακοκινητικές ιδιότητες της μελοξικάμης
[Επεξεργασία | επεξεργασία κώδικα]Απορρόφηση
[Επεξεργασία | επεξεργασία κώδικα]Η βιοδιαθεσιμότητα της μελοξικάμης μειώνεται όταν χορηγείται από το στόμα. Η χορήγηση της μελοξικάμης από το στόμα μετά από κατανάλωση πρωινού με υψηλή περιεκτικότητα σε λιπαρά αυξάνει τα μέγιστα επίπεδα κορυφής των φαρμάκων κατά περίπου 22%. Ωστόσο, ο κατασκευαστής του φαρμάκου δεν κάνει κάποια ιδιαίτερη διατροφική σύσταση. Επιπλέον, η χρήση αντιόξινων δεν δείχνουν φαρμακοκινητικές αλληλεπιδράσεις.[17]
Διανομή
[Επεξεργασία | επεξεργασία κώδικα]Ο μέσος όγκος διανομής της μελοξικάμης είναι περίπου 10 λίτρα. Έχει υψηλή περιεκτικότητα σε πρωτεΐνες, κυρίως λευκωματίνη.
Μεταβολισμός
[Επεξεργασία | επεξεργασία κώδικα]Η μελοξικάμη μεταβολίζεται εκτενώς στο ήπαρ από τα ένζυμα CYP2C9 και το CYP3A4 (ήσσονος σημασίας) σε τέσσερις ανενεργούς μεταβολίτες. Πιστεύεται ότι η δραστηριότητα της υπεροξειδάσης οφείλεται για τις δραστηριότητες των δύο υπόλοιπων μεταβολιτών.[17][18]
Απέκκριση
[Επεξεργασία | επεξεργασία κώδικα]Η μελοξικάμη απεκκρίνεται κυρίως με τη μορφή των μεταβολιτών. Από τα ούρα και τα περιττώματα αποβάλλονται οι ίδιες ποσότητες μελοξικάμης. Στα ούρα και τα περιττώματα βρίσκονται ίχνη αμετάβλητης μελοξικάμης. Η μέση ημιπερίοδος ζωής της μελοξικάμης κυμαίνεται στις 15 με 20 ώρες.[17]
Οδηγίες για συγκεκριμένες πληθυσμιακές ομάδες
[Επεξεργασία | επεξεργασία κώδικα]Γηριατρική
[Επεξεργασία | επεξεργασία κώδικα]Συνιστάται η μη χρήση μελοξικάμης σε άτομα με πεπτικό έλκος ή αυξημένο κίνδυνο για την εκδήλωση γαστρεντερικής αιμορραγίας. Το ίδιο συνιστάται και για άτομα άνω των 75 ετών και σε όσους λαμβάνουν φάρμακα που σχετίζονται με τον κίνδυνο αιμορραγίας.[19] Έχει διαπιστωθεί ότι οι ανεπιθύμητες παρενέργειες είναι δοσοεξαρτώμενες και σχετίζονται με την διάρκεια της θεραπείας.[17]
Κτηνιατρική χρήση
[Επεξεργασία | επεξεργασία κώδικα]Η μελοξικάμη χρησιμοποιείται ως κτηνιατρικό φάρμακο, κυρίως σε σκύλους και γάτες. Ωστόσο, χρησιμοποιείται και σε άλλα είδη ζώων που δεν αναφέρονται στη συσκευασία, συμπεριλαμβανομένων των βοοειδών.
Οι παρενέργειες από χρήση μελοξικάμης σε ζώα είναι παρόμοιες με αυτές που εμφανίζουν οι άνθρωποι. Η κύρια παρενέργεια είναι ο γαστρεντερικός ερεθισμός (εμετός, διάρροια και εξέλκωση). Στις σπάνιες αλλά σοβαρές ανεπιθύμητες παρενέργειες συμπεριλαμβάνεται η ηπατική και νεφρική τοξικότητα.
Σε υγιείς σκύλους στους οποίους χορηγήθηκε μελοξικάμη, δεν βρέθηκαν περιεγχειρητικές δυσμενείς επιδράσεις στο καρδιαγγειακό σύστημα όταν τους χορηγήθηκαν οι συνιστώμενες δοσολογίες.[20] Στις γάτες, η περιεγχειρητική χορήγηση μελοξικάμης δεν επηρέασε τη μετεγχειρητική αναπνευστική συχνότητα, ούτε τον καρδιακό ρυθμό.[21]
Η Βασιλική Εταιρεία για την Προστασία των Πτηνών έχει εξετάσει την μελοξικάμη ως εναλλακτική για την δικλοφενάκη, για την αποτροπή των θανάτων των γυπών.[22]
Η χρήση Μελοξικάμης σε Γάτες
[Επεξεργασία | επεξεργασία κώδικα]Το ζήτημα της χρήσης μελοξικάμης σε γάτες περιλαμβάνει αντικρουόμενες οδηγίες, διαφορετικές νομοθεσίες και ένα περιορισμένο θεραπευτικό εύρος ασφαλείας που μπορεί εύκολα να μετατρέψει το φάρμακο από ίαμα σε δηλητήριο. Συγκεκριμένα:
Η FDA (Food & Drug Administration) των ΗΠΑ εγκρίνει τη χρήση της μελοξικάμης σε γάτες μόνο σε ενέσιμη μορφή και μόνο για μία και μοναδική ένεση πριν από επέμβαση.[23][24] Δεν εγκρίνει το πόσιμο εναιώρημα μελοξικάμης για γάτες και δεν εγκρίνει το σπρέι μελοξικάμης για γάτες καθώς μετά από εξέταση πολυάριθμων αναφορών παρενεργειών της μελοξικάμης σε γάτες, εντόπισε πολλές περιπτώσεις οξείας νεφρικής ανεπάρκειας και θανάτου και έχει προσθέσει στα προϊόντα το εξής προειδοποιητικό μήνυμα σε πλαίσιο: "Η επαναλαμβανόμενη χρήση μελοξικάμης σε γάτες έχει συσχετιστεί με οξεία νεφρική ανεπάρκεια και θάνατο. Μη χορηγείτε πρόσθετη ενέσιμη ή από του στόματος μελοξικάμη σε γάτες. Δείτε τις Αντενδείξεις, Προειδοποιήσεις και Προφυλάξεις για λεπτομερείς πληροφορίες."[25] Αντίθετα όμως στην Ευρωπαϊκή Ένωση και σε άλλες ηπείρους ή χώρες επιτρέπεται κανονικά η χρήση του φαρμάκου σε γάτες χωρίς καμία αντίστοιχη προειδοποίηση.[26][27]
Άλλη αντικρουόμενη οδηγία αφορά συγκεκριμένο προϊόν πόσιμου εναιωρήματος μελοξικάμης για γάτες. Στο φύλλο οδηγιών του αναγράφεται ότι: "Τυπικές ανεπιθύμητες ενέργειες των ΜΣΑΦ, όπως απώλεια της όρεξης, έµετος, διάρροια, ίχνη αίµατος στα κόπρανα, απάθεια και νεφρική ανεπάρκεια έχουν αναφερθεί σποραδικά. Αυτές οι ανεπιθύµητες ενέργειες είναι, στις περισσότερες περιπτώσεις, παροδικές και παρέρχονται µετά τη διακοπή της θεραπείας, αλλά σε σπάνιες περιπτώσεις µπορεί να είναι σοβαρές ή θανατηφόρες."[28] Η κεντρική σελίδα όμως της επίσημης ιστοσελίδας του ίδιου προϊόντος μελοξικάμης αναφέρει: "Σημαντικές πληροφορίες για την ασφάλεια: ΜΗ ΧΡΗΣΙΜΟΠΟΙΕΙΤΕ ΤΟ ΠΟΣΙΜΟ ΕΝΑΙΩΡΗΜΑ ΣΕ ΓΑΤΕΣ. Η οξεία νεφρική ανεπάρκεια και ο θάνατος έχουν συσχετιστεί με τη χρήση της μελοξικάμης σε γάτες."[29]
Στα φύλλα οδηγιών των προϊόντων μελοξικάμης για γάτες αναφέρεται ακόμη ότι: "Η μελοξικάμη έχει περιορισμένο θεραπευτικό εύρος ασφαλείας στις γάτες και μπορούν να παρατηρηθούν κλινικά συμπτώματα υπερδοσολογίας μετά από σχετικά μικρά επίπεδα υπερδοσίας."[28] Η πολιτική δοσολογίας προϊόντων μελοξικάμης για γάτες όπως περιγράφεται στα φύλλα οδηγιών ορίζει τη χορηγούμενη ποσότητα ως ανάλογη του σωματικού βάρους. Για τις υπέρβαρες ή παχύσαρκες γάτες δεν υπάρχει ξεχωριστή οδηγία δοσολογίας. Αυτό είναι άξιο αναφοράς αφενός επειδή στο άρθρο Δοσολογία φαρμάκων σε παχύσαρκους ενήλικες[30] πρεσβεύεται ότι η χρήση του συνολικού σωματικού βάρους παχύσαρκων ενηλίκων μπορεί να οδηγήσει σε τοξικότητα του φαρμάκου και προτείνεται εξατομικευμένη δοσολογία με βάση το ιδανικό και όχι το πραγματικό σωματικό βάρος του ασθενούς, και αφετέρου, ακριβώς επειδή το εύρος ασφαλείας της μελοξικάμης για γάτες είναι τόσο περιορισμένο. Αντίστοιχα, στο φύλλο οδηγιών δεν υπάρχει ξεχωριστή οδηγία δοσολογίας ούτε για τις ηλικιωμένες γάτες.
Κάποια πρόσθετα στοιχεία σχετικά με τη χορήγηση μελοξικάμης σε γάτες από ερευνητές είναι τα εξής: Ένα επιστημονικό περιοδικό, αναθεωρούμενο από ομότιμους επιστήμονες, αναφέρει ότι τα ΜΣΑΦ, συμπεριλαμβανομένης της μελοξικάμης, προκαλούν γαστρεντερικές ενοχλήσεις. Αν χορηγηθεί μεγάλη ποσότητα του φαρμάκου σε γάτες προκαλείται ζημιά στο νευρικό σύστημα και παρενέργειες στο κεντρικό νευρικό σύστημα όπως επιληπτικές κρίσεις και κώμα. Προσθέτει ότι οι γάτες παρουσιάζουν μικρή ανοχή στα ΜΣΑΦ.[31][32] Επίσης, σε άλλο επιστημονικό περιοδικό γίνεται λόγος για έρευνα σύμφωνα με την οποία οι γάτες στις οποίες χορηγήθηκε μελοξικάμη είχαν μεγαλύτερη πρωτεϊνουρία σε διάστημα 6 μηνών, σε σύγκριση με τις γάτες στις οποίες χορηγήθηκε το εικονικό φάρμακο (πλασέμπο). Το συμπέρασμα ήταν ότι η μελοξικάμη πρέπει να χορηγείται με προσοχή σε γάτες που πάσχουν από χρόνια νεφρική νόσο.[33]
Προϊόντα μελοξικάμης για γάτες που κυκλοφορούν και πωλούνται στην ελληνική αγορά είναι: Loxicom, Metacam, Meloxidyl, Melosus, Meloxoral.
Φαρμακοκινητική
[Επεξεργασία | επεξεργασία κώδικα]Στους σκύλους, η απορρόφηση της μελοξικάμης από το στομάχι δεν επηρεάζεται από την παρουσία τροφής.[34] Η μέγιστη συγκέντρωση (C max) της μελοξικάμης στο σκύλο καταγράφεται στο αίμα 7-8 ώρες μετά την χορήγηση της. Η ημιπερίοδος ζωής της μελοξικάμης στους σκύλους είναι περίπου 24 ώρες.
Το κοάλα (Phascolarctos cinereus) απορροφά μια πολύ χαμηλή ποσότητα μελοξικάμης στο αίμα αφού του χορηγηθεί μελοξικάμη από το στόμα (δηλαδή έχει χαμηλή βιοδιαθεσιμότητα).[35]
Νομικό καθεστώς
[Επεξεργασία | επεξεργασία κώδικα]Ηνωμένες Πολιτείες
[Επεξεργασία | επεξεργασία κώδικα]Το 2003 οι αρχές των ΗΠΑ ενέκριναν την χρήση της μελοξικάμης σε σκύλους για τη διαχείριση του πόνου και της φλεγμονής που σχετίζεται με τη οστεοαρθρίτιδα, χορηγούμενη από το στόμα.[36] Τον Ιανουάριο του 2005 εισήχθη μια προειδοποίηση με έντονα γράμματα που έγραφε το εξής: "Μην το χρησιμοποιείτε σε γάτες."[37] Τον Νοέμβριο του 2003 η αμερικάνικη Υπηρεσία Τροφίμων και Φαρμάκων ενέκρινε την διάθεση ενός ενέσιμου σκευάσματος για σκύλους.[38]
Τον Οκτώβριο του 2004 εγκρίθηκε η χρήση ενός σκευάσματος, του οποίου επιτρεπόταν η χρήση μόνο πριν μια χειρουργική επέμβαση.[39] Αυτό το σκεύασμα είναι ενέσιμο, το οποίο πρέπει να χορηγηθεί μόνο μια φορά. Υπάρχουν συγκεκριμένες και επαναλαμβανόμενες προειδοποιήσεις να μην χορηγηθεί δεύτερη δόση του σκευάσματος.
Το 2005, η αμερικάνικη Υπηρεσία Τροφίμων και Φαρμάκων (FDA) έστειλε μια έγγραφη προειδοποίηση παράβασης στον κατασκευαστή του σκευάσματος λόγω του τρόπου της προώθησης του, η οποία περιλάμβανε προώθηση για χρήση του σκευάσματος και για ζωικούς οργανισμούς.[40]
Τον Φεβρουάριο του 2020 εγκρίθηκε η χρήση ενός ενέσιμου σκευάσματος μελοξικάμης στις Ηνωμένες Πολιτείες. Η Υπηρεσία Τροφίμων και Φαρμάκων ενέκρινε τη χρήση του σκευάσματος Anjeso της Baudax Bio.[41][42]
Ευρωπαϊκή Ένωση
[Επεξεργασία | επεξεργασία κώδικα]Στην Ευρώπη το προϊόν διατίθεται από τις αρχές της δεκαετίας του 1990. Έχει αδειοδοτηθεί η χρήση του για αντιφλεγμονώδεις σκοπούς, όπως η ανακούφιση από οξείς και χρόνιους πόνους σε σκύλους. Τον Ιούνιο του 2007 εγκρίθηκε η πώληση ενός σκευάσματος μελοξικάμης για την ανακούφιση του πόνου στις γάτες, το οποίο λαμβανόταν από το στόμα.[43] Επιτρέπεται η χρήση της μελοξικάμης σε άλογα, για να ανακουφίσει τον πόνο που σχετίζεται με μυοσκελετικές διαταραχές.[44]
Η μελοξικάμη εγκρίθηκε για χρήση σε βοοειδή σε όλη την Ευρωπαϊκή Ένωση, τον Ιανουάριο του 1998, μέσω μιας κεντρικής άδειας κυκλοφορίας.[45] Το πρώτο γενόσημο προϊόν μελοξικάμης εγκρίθηκε το 2006.
Άλλες χώρες
[Επεξεργασία | επεξεργασία κώδικα]Τον Ιούνιο του 2008, η μελοξικάμη έχει εγγραφθεί για μακροπρόθεσμη χρήση σε γάτες στην Αυστραλία, τη Νέα Ζηλανδία και τον Καναδά.[43]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ 1,0 1,1 Use During Pregnancy and Breastfeeding
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 «Meloxicam». Drugs 51 (3): 424–30; discussion 431–32. March 1996. doi:. PMID 8882380.
- ↑ British national formulary : BNF 76 (76 έκδοση). Pharmaceutical Press. 2018. σελίδες 1112–1113. ISBN 9780857113382.
- ↑ 4,0 4,1 4,2 «Meloxicam Monograph for Professionals». Drugs.com. AHFS. Αρχειοθετήθηκε από το πρωτότυπο στις 23 Δεκεμβρίου 2018. Ανακτήθηκε στις 23 Δεκεμβρίου 2018.
- ↑ Fischer, Jnos· Ganellin, C. Robin (2006). Analogue-based Drug Discovery. John Wiley & Sons. σελ. 519. ISBN 9783527607495. Ανακτήθηκε στις 30 Ιουνίου 2020.
- ↑ «The Top 300 of 2020». ClinCalc. Αρχειοθετήθηκε από το πρωτότυπο στις 18 Μαρτίου 2020. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ «Meloxicam Drug Usage Statistics». ClinCalc. 23 Δεκεμβρίου 2019. Αρχειοθετήθηκε από το πρωτότυπο στις 12 Απριλίου 2020. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ «Development of a special electrode for continuous subcutaneous pH measurement in the infant scalp». American Journal of Obstetrics and Gynecology 124 (2): 193–5. January 1976. doi:. PMID 2012.
- ↑ «Improvement in gastrointestinal tolerability of the selective cyclooxygenase (COX)-2 inhibitor, meloxicam, compared with piroxicam: results of the Safety and Efficacy Large-scale Evaluation of COX-inhibiting Therapies (SELECT) trial in osteoarthritis». British Journal of Rheumatology 37 (9): 946–51. September 1998. doi:. PMID 9783758.
- ↑ «A six-month double-blind trial to compare the efficacy and safety of meloxicam 7.5 mg daily and naproxen 750 mg daily in patients with rheumatoid arthritis». British Journal of Rheumatology 35 Suppl 1: 22–8. April 1996. doi:. PMID 8630632.
- ↑ «Gastrointestinal tolerability of meloxicam compared to diclofenac in osteoarthritis patients. International MELISSA Study Group. Meloxicam Large-scale International Study Safety Assessment». British Journal of Rheumatology 37 (9): 937–45. September 1998. doi:. PMID 9783757.
- ↑ «Risk of serious upper gastrointestinal and cardiovascular thromboembolic complications with meloxicam». The American Journal of Medicine 117 (2): 100–6. July 2004. doi:. PMID 15234645.
- ↑ «Meloxicam». MedlinePlus. Αρχειοθετήθηκε από το πρωτότυπο στις 29 Νοεμβρίου 2014. Ανακτήθηκε στις 15 Νοεμβρίου 2014.
- ↑ «Meloxicam». Drugs.com. Αρχειοθετήθηκε από το πρωτότυπο στις 16 Νοεμβρίου 2014. Ανακτήθηκε στις 15 Νοεμβρίου 2014.
- ↑ 15,0 15,1 «Meloxicam official FDA information, side effects, and uses». Drugs.com. Μαρτίου 2010. Αρχειοθετήθηκε από το πρωτότυπο στις 16 Μαρτίου 2010. Ανακτήθηκε στις 17 Μαρτίου 2010.
- ↑ «Anti-inflammatory, analgesic, antipyretic and related properties of meloxicam, a new non-steroidal anti-inflammatory agent with favourable gastrointestinal tolerance». Inflammation Research 44 (10): 423–33. October 1995. doi:. PMID 8564518. https://archive.org/details/sim_inflammation-research_1995-10_44_10/page/423.
- ↑ 17,0 17,1 17,2 17,3 «Mobic- meloxicam tablet label». DailyMed. 11 Οκτωβρίου 2018. Αρχειοθετήθηκε από το πρωτότυπο στις 1 Σεπτεμβρίου 2020. Ανακτήθηκε στις 2 Αυγούστου 2019.
- ↑ «Meloxicam (Professional Patient Advice)». Drugs.com. Αρχειοθετήθηκε από το πρωτότυπο στις 6 Αυγούστου 2019. Ανακτήθηκε στις 6 Αυγούστου 2019.
- ↑ «American Geriatrics Society 2019 Updated AGS Beers Criteria® for Potentially Inappropriate Medication Use in Older Adults». Journal of the American Geriatrics Society 67 (4): 674–694. April 2019. doi:. PMID 30693946.
- ↑ «Effects of meloxicam on renal function in dogs with hypotension during anaesthesia». Veterinary Anaesthesia and Analgesia 33 (1): 62–9. January 2006. doi:. PMID 16412133.
- ↑ «Effect of non-steroidal anti-inflammatory drugs on postoperative respiratory and heart rate in cats subjected to ovariohysterectomy». Journal of Feline Medicine and Surgery 20 (10): 980–984. October 2018. doi:. PMID 29165006.
- ↑ «Removing the threat of diclofenac to critically endangered Asian vultures». PLOS Biology 4 (3): e66. March 2006. doi:. PMID 16435886.
- ↑ Medicine, Center for Veterinary (Thu, 09/29/2022 - 06:27). «Get the Facts about Pain Relievers for Pets» (στα αγγλικά). FDA. https://www.fda.gov/animal-veterinary/animal-health-literacy/get-facts-about-pain-relievers-pets.
- ↑ Medicine, Center for Veterinary (Tue, 08/15/2023 - 14:24). «What Veterinarians Should Advise Clients About Pain Control and Nonsteroidal Anti-Inflammatory Drugs (NSAIDs) in Dogs and Cats» (στα αγγλικά). FDA. https://www.fda.gov/animal-veterinary/resources-you/what-veterinarians-should-advise-clients-about-pain-control-and-nonsteroidal-anti-inflammatory-drugs.
- ↑ Medicine, Center for Veterinary (Mon, 08/14/2023 - 13:20). «Information about the Boxed Warning on Meloxicam Labels regarding Safety Risks in Cats» (στα αγγλικά). FDA. https://www.fda.gov/animal-veterinary/product-safety-information/information-about-boxed-warning-meloxicam-labels-regarding-safety-risks-cats.
- ↑ «Metacam | European Medicines Agency». www.ema.europa.eu. Ανακτήθηκε στις 28 Μαρτίου 2024.
- ↑ [https://questions-statements.parliament.uk/written-questions/detail/2021-05-11/HL10/ «Cats: Meloxicam Question for Department for Environment, Food and Rural Affairs»]. UK Parliament Written questions, answers and statements. https://questions-statements.parliament.uk/written-questions/detail/2021-05-11/HL10/.
- ↑ 28,0 28,1 «Meloxidyl oral cat / Λίστα προϊόντων / Προϊόντα / Ceva Greece». Ceva Greece. Ανακτήθηκε στις 28 Μαρτίου 2024.
- ↑ «Meloxidyl® from Ceva Animal Health» (στα Αγγλικά). Ανακτήθηκε στις 28 Μαρτίου 2024.
- ↑ Barras, Michael; Legg, Amy (3 October 2017). Drug dosing in obese adults. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5662437/.
- ↑ «Toxicology Brief: The 10 most common toxicoses in cats». Dvm360. 2006-06-01. Αρχειοθετήθηκε από το πρωτότυπο στις 29 August 2018. https://web.archive.org/web/20180829212043/http://veterinarymedicine.dvm360.com/toxicology-brief-10-most-common-toxicoses-cats?id=&sk=&date=&pageID=3. Ανακτήθηκε στις 2018-09-16.
- ↑ «The 10 most common toxicoses in cats». Veterinary Medicine: 340–342. June 2006. Αρχειοθετήθηκε από το πρωτότυπο στις 9 August 2019. https://web.archive.org/web/20190809040133/https://www.aspcapro.org/sites/default/files/zl-vetm0606_339-342.pdf. Ανακτήθηκε στις 9 August 2019.
- ↑ KuKanich, Kate; George, Christopher; Roush, James K; Sharp, Sherry; Farace, Giosi; Yerramilli, Murthy; Peterson, Sarah; Grauer, Gregory F (29 June 2020). «Effects of low-dose meloxicam in cats with chronic kidney disease». Journal of Feline Medicine and Surgery: 1098612X2093575. doi:. PMID 32594827.
- ↑ «Toxicology of frequently encountered nonsteroidal anti-inflammatory drugs in dogs and cats». The Veterinary Clinics of North America. Small Animal Practice 42 (2): 289–306, vi-vii. March 2012. doi:. PMID 22381180.
- ↑ «Pharmacokinetics of meloxicam in koalas (Phascolarctos cinereus) after intravenous, subcutaneous and oral administration». Journal of Veterinary Pharmacology and Therapeutics 36 (5): 486–93. October 2013. doi:. PMID 23406022.
- ↑ «NADA 141-213: New Animal Drug Application Approval (for Metacam (meloxicam) 0.5 mg/mL and 1.5 mg/mL Oral Suspension)» (PDF). Food and Drug Administration (FDA). 15 Απριλίου 2003. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 6 Απριλίου 2017. Ανακτήθηκε στις 24 Ιουλίου 2010.
- ↑ «Client Information Sheet For Metacam (meloxicam) 1.5 mg/mL Oral Suspension» (PDF). Food and Drug Administration (FDA). Ιανουαρίου 2005. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 15 Νοεμβρίου 2017.
Metacam is a prescription non-steroidal anti-inflammatory drug (NSAID) that is used to control pain and inflammation (soreness) due to osteoarthritis in dogs. Osteoarthritis (OA) is a painful condition caused by “wear and tear” of cartilage and other parts of the joints that may result in the following changes or signs in your dog: Limping or lameness, decreased activity or exercise (reluctance to stand, climb stairs, jump or run, or difficulty in performing these activities), stiffness or decreased movement of joints. Metacam is given to dogs by mouth. Do not use Metacam Oral Suspension in cats. Acute kidney injury and death have been associated with the use of meloxicam in cats.
- ↑ «NADA 141-219: Metacam (meloxicam) 5 mg/mL Solution for Injection» (PDF). U.S. Food and Drug Administration (FDA). 12 Νοεμβρίου 2003. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 15 Νοεμβρίου 2017. Ανακτήθηκε στις 8 Αυγούστου 2019.
- ↑ «Metacam 5 mg/mL Solution for Injection, Supplemental Approval» (PDF). U.S. Food and Drug Administration (FDA). 28 Οκτωβρίου 2004. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 15 Νοεμβρίου 2017. Ανακτήθηκε στις 8 Αυγούστου 2019.
- ↑ «Notice of Violation» (PDF). U.S. Food and Drug Administration (FDA). 19 Απριλίου 2005. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 13 Ιανουαρίου 2017. Ανακτήθηκε στις 8 Αυγούστου 2019.
- ↑ (20 February 2020). Baudax Bio Announces FDA Approval of Anjeso for the Management of Moderate to Severe Pain. Δελτίο τύπου. Αρχειοθετήθηκε 2020-02-21 στο Wayback Machine.
- ↑ «Anjeso (meloxicam) injection, for intravenous use» (PDF). U.S. Food and Drug Administration (FDA). Φεβρουαρίου 2020. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 22 Φεβρουαρίου 2020. Ανακτήθηκε στις 21 Φεβρουαρίου 2020.
- ↑ 43,0 43,1 Gaschen, Frederic P., επιμ. (2016). «Recent NSAID developments». Clinical medicine of the dog and cat (3rd έκδοση). CRC Press. ISBN 9781482226065.
Η παράμετρος |access-date=χρειάζεται|url=(βοήθεια) - ↑ «Meloxicam». Small animal clinical pharmacology (2nd έκδοση). Edinburgh: Saunders/Elsevier. 2008. σελίδες 301–302. ISBN 9780702028588.
- ↑ Wright, Elizabethann (March 2007). «Generic and biosimilar medicinal products in the European Union». Chemistry Today 25 (2): 4–6. Αρχειοθετήθηκε από το πρωτότυπο στις 28 January 2020. https://web.archive.org/web/20200128032019/https://www.hoganlovells.com/~/media/hogan-lovells/pdf/publication/chemistrytodayapr07_pdf.pdf. Ανακτήθηκε στις 28 January 2020.
Εξωτερικοί σύνδεσμοι
[Επεξεργασία | επεξεργασία κώδικα]- «Meloxicam». Drug Information Portal. U.S. National Library of Medicine.
