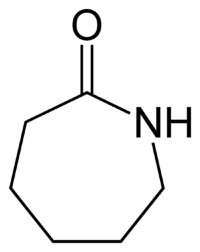
Καπρολακτάμη
| Καπρολακτάμη | |||
|---|---|---|---|
| |||

| |||
| Γενικά | |||
| Άλλες ονομασίες | ε-καπρολακτάμη, 6-εξανολακτάμη | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C6H11NO | ||
| Αριθμός CAS | 105-60-2 | ||
| SMILES | O=C1NCCCCC1 | ||
| InChI | 1S/C6H11NO/c8-6-4-2-1-3-5-7-6/h1-5H2,(H,7,8) | ||
| Αριθμός EINECS | 203-313-2 | ||
| PubChem CID | 7768 | ||
| ChemSpider ID | 7480 | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | 69,2 | ||
| Σημείο βρασμού | 270,8 στα 1013,25 hPa | ||
| Πυκνότητα | 1,01 g/cm3 | ||
| Διαλυτότητα στο νερό |
866,89 g/L (22 °C) | ||
| Τάση ατμών | 0,00000008 mmHg (20° C)[1] | ||
| Εμφάνιση | Λευκό στερεό | ||
| Χημικές ιδιότητες | |||
| Ελάχιστη θερμοκρασία ανάφλεξης |
125 | ||
| Επικινδυνότητα | |||
| Φράσεις κινδύνου | R20, R22, R36/37/38 | ||
| Άλλοι κίνδυνοι | Όρια έκρηξης = 1,4%-8,0%[1] | ||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Η καπρολακτάμη (CPL) είναι μια οργανική ένωση με τον χημικό τύπο (CH2)5C(O)NH. Αυτό το άχρωμο στερεό είναι μια λακτάμη ή ένα κυκλικό αμίδιο του εξανικού οξέος. Περίπου 4,5 δισεκατομμύρια χιλιόγραμμα παράγονται ετησίως. Η καπρολακτάμη είναι η πρόδρομη ένωση για το νάιλον-6, ένα πλατιά χρησιμοποιούμενο συνθετικό πολυμερές.[2]
Σύνθεση και παραγωγή
[Επεξεργασία | επεξεργασία κώδικα]Η καπρολακτάμη πρωτοπεριγράφτηκε όταν παρασκευάστηκε από την κυκλοποίηση του ε-αμινοκαπροϊκού οξέος, το προϊόν της υδρόλυσης της καπρολακτάμης. Με δεδομένη την εμπορική σημασία του νάιλον-6, έχουν αναπτυχθεί πολλές μέθοδοι για την παραγωγή της καπρολακτάμης. Το μεγαλύτερο ποσοστό της καπρολακτάμης συντίθεται από κυκλοεξανόνη (1), που πρώτα μετατρέπεται στην οξίμη της (2). Η επεξεργασία αυτής της οξίμης με οξύ προκαλεί την αναδιάταξη Μπέκμαν (Beckmann rearrangement) για να δώσει καπρολακτάμη (3):
Το ενδιάμεσο προϊόν της επαγόμενης από οξύ αναδιάταξης είναι το διθειικό άλας της καπρολακτάμης. Αυτό το άλας εξουδετερώνεται με αμμωνία για να απελευθερώσει την ελεύθερη λακτάμη και να συμπαράξει θειικό αμμώνιο. Στη βελτιστοποίηση των βιομηχανικών πρακτικών, δίνεται πολλή προσοχή στην ελαχιστοποίηση της παραγωγής των αμμωνιακών αλάτων.
Η άλλη κύρια βιομηχανική οδός περιλαμβάνει τον σχηματισμό της οξίμης από κυκλοεξάνιο χρησιμοποιώντας χλωριούχο νιτροσύλιο. Το πλεονέκτημα αυτής της μεθόδου είναι ότι το κυκλοεξάνιο είναι πιο φθηνό από την κυκοεξανόνη. Στην αρχή, η καπρολακτάμη παρασκευαζόταν από την επεξεργασία της καπρολακτόνης με αμμωνία.[2]
Χρήσεις
[Επεξεργασία | επεξεργασία κώδικα]Σχεδόν όλη η παραγόμενη καπρολακτάμη πηγαίνει για την κατασκευή του νάιλον-6. Η μετατροπή συνεπάγεται τον πολυμερισμό διάνοιξης δακτυλίου (ring-opening polymerization):
- n (CH2)5C(O)NH → [(CH2)5C(O)NH]n
Το νάιλον-6 χρησιμοποιείται πλατιά στις ίνες και τα πλαστικά.
Ο επιτόπιος ανιονικός πολυμερισμός χρησιμοποιείται για παραγωγή χυτού νάιλον, ενώ η μετατροπή από ε-καπρολακτάμη σε νάιλον-6 λαμβάνει χώρα μέσα σε μια μήτρα. Σε συνδυασμό με την συνεχή επεξεργασία ίνας χρησιμοποιείται συχνά ο όρος μορφοποίηση με μεταφορά θερμοπλαστικής ρητίνης (thermoplastic resin transfer molding) (T-RTM).
Ασφάλεια
[Επεξεργασία | επεξεργασία κώδικα]Η καπρολακτάμη είναι ερεθιστική και ήπια τοξική, με μια LD50 1,1 g/kg (επίμυς, από το στόμα). Το 1991, συμπεριελήφθη στον κατάλογο των επικίνδυνων ρυπαντών του αέρα από τις ΗΠΑ (Clean Air Act of 1990). Στη συνέχεια, αφαιρέθηκε από τον κατάλογο το 1996.[3] Στο νερό, η καπρολακτάμη υδρολύεται σε αμινοκαπροϊκό οξύ, που χρησιμοποιείται ιατρικά.
Από το 2014 η καπρολακτάμη έχει την ασυνήθιστη κατάσταση να είναι η μοναδική χημική ουσία στην χαμηλότερη κατηγορία κινδύνου της ομάδας 4 "προφανώς μη καρκινογόνος για ανθρώπους" του Διεθνούς Οργανισμού Ερευνών για τον Καρκίνο, .[4]
Προς το παρόν, δεν υπάρχει κανένα επίσημο επιτρεπτό όριο έκθεσης που να έχει οριστεί για τους εργαζόμενους που χειρίζονται την καπρολακτάμη στις ΗΠΑ. Το συνιστώμενο όριο έκθεσης έχει οριστεί σε 1 mg/m3 για μια οκτάωρη εργασία για τους ατμούς και τις σκόνες της καπρολακτάμης. Το όριο βραχυχρόνιας έκθεσης έχει οριστεί σε 3 mg/m3 για τις σκόνες και τους ατμούς της καπρολακτάμης.[5]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ 1,0 1,1 Πρότυπο:PGCH
- ↑ 2,0 2,1 Josef Ritz; Hugo Fuchs; Heinz Kieczka; William C. Moran. «Ullmann's Encyclopedia of Industrial Chemistry». Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:. ISBN 978-3527306732.
- ↑ EPA - Modifications To The 112(b)1 Hazardous Air Pollutants
- ↑ Agents Classified by the IARC Monographs, Volumes 1–102, WHO, http://monographs.iarc.fr/ENG/Classification/ClassificationsGroupOrder.pdf, ανακτήθηκε στις July 15, 2011
- ↑ NIOSH Pocket Guide to Chemical Hazards, CDC, http://www.cdc.gov/niosh/npg/npgd0097.html, ανακτήθηκε στις November 8, 2013

