Ακεσουλφάμη καλίου
| |

| |
| Names | |
|---|---|
| IUPAC name
Potassium 6-methyl-2,2-dioxo-2H-1,2λ6,3-oxathiazin-4-olate
| |
| Other names
Acesulfame K; Ace K
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.054.269 |
| EC Number | 259-715-3 |
| E number | E950 (glazing agents, ...) |
PubChem <abbr title="<nowiki>Compound ID</nowiki>">CID
|
|
| UNII |
|
| |
| |
| Properties | |
| C4H4KNO4S | |
| Molar mass | 201.242 |
| Appearance | white crystalline powder |
| Density | 1.81 g/cm3 |
| Melting point | 225 °C (437 °F; 498 K) |
| 270 g/L at 20 °C | |
| Hazards | |
| NFPA 704 | |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |
| Infobox<span typeof="mw:Entity"> </span>references | |
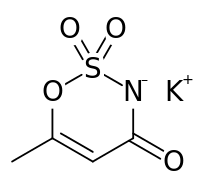
Η ακεσουλφάμη καλίου ( AY-see-SUL-faym [1] ), επίσης γνωστή ως ακεσουλφάμη Κ (Κ είναι το σύμβολο για το κάλιο ) ή Ace Κ, είναι ένα ολιγοθερμιδικό υποκατάστατο ζάχαρης (τεχνητό γλυκαντικό ) που διατίθεται συχνά στο εμπόριο με τα εμπορικά ονόματα Sunett και Sweet One . Στην Ευρωπαϊκή Ένωση, είναι γνωστή με τον αριθμό Ε (κωδικός πρόσθετου) E950 . [2] Ανακαλύφθηκε τυχαία το 1967 από τον Γερμανό χημικό Καρλ Κλάους στη Hoechst AG (τώρα Nutrinova ). [3] Ως χημική δομή, η ακεσουλφάμη καλίου είναι το άλας καλίου του 2,2-διοξειδίου του 6-μεθυλ-1,2,3-οξαθειαζινο-4 ( 3Η ) -όνης. Πρόκειται για μια λευκή κρυσταλλική σκόνη με μοριακό τύπο C4H4KNO4S και μοριακό βάρος 201,24 g / mol. [4]
Ιδιότητες
[Επεξεργασία | επεξεργασία κώδικα]Η ακεσουλφάμη K είναι 200 φορές πιο γλυκιά από τη ζάχαρη, το ίδιο γλυκιά όπως η ασπαρτάμη, περίπου κατά τα δύο τρίτα γλυκιά όσο η σακχαρίνη και κατά το ένα τρίτο γλυκιά όσο η σουκραλόζη . Όπως και η σακχαρίνη, έχει μια ελαφρώς πικρή επίγευση, ειδικά σε υψηλές συγκεντρώσεις. Η Kraft Foods κατοχύρωσε με δίπλωμα ευρεσιτεχνίας τη χρήση φερουλιούχου νατρίου για να καλύψει την επίγευση της ακεσουλφάμης. [5] Η ακεσουλφάμη Κ αναμιγνύεται συχνά με άλλα γλυκαντικά (συνήθως σουκραλόζη ή ασπαρτάμη). Αυτά τα μίγματα παρασκευάζονται για να δώσουν μια γεύση κοντά σε αυτή της ζάχαρης, όπου κάθε γλυκαντικό καλύπτει την επίγευση του άλλου ή παρουσιάζει ένα συνεργατικό αποτέλεσμα με το οποίο το μείγμα είναι πιο γλυκό από τα συστατικά του. [6] Η ακεσουλφάμη καλίου έχει μικρότερο μέγεθος σωματιδίων από τη σακχαρόζη, επιτρέποντας τα μίγματα της με άλλα γλυκαντικά να είναι πιο ομοιόμορφα. [7]
Σε αντίθεση με την ασπαρτάμη, η ακεσουλφάμη K είναι σταθερή υπό θερμότητα, ακόμη και υπό μετρίως όξινες ή βασικές συνθήκες, ως εκ τούτου μπορεί να χρησιμοποιείται ως πρόσθετο τροφίμων στο ψήσιμο ή σε προϊόντα που απαιτούν μεγάλη διάρκεια ζωής. Αν και η ακεσουλφάμη καλίου έχει σταθερή διάρκεια ζωής, μπορεί τελικά να αποικοδομείται σε ακετοακεταμίδιο, το οποίο είναι τοξικό σε υψηλές δόσεις. [8] Στα αεριούχα ποτά, χρησιμοποιείται σχεδόν πάντοτε σε συνδυασμό με άλλα γλυκαντικά, όπως η ασπαρτάμη ή η σουκραλόζη. Χρησιμοποιείται επίσης ως γλυκαντικό σε πρωτεϊνικά ροφήματα και φαρμακευτικά προϊόντα, [9] ειδικά μασώμενα και υγρά φάρμακα, όπου μπορεί να καταστήσει τα ενεργά συστατικά περισσότερο εύγευστα. Η αποδεκτή ημερήσια πρόσληψη ακεσουλφάμης καλίου αναφέρεται ως 15 mg / kg / ημέρα. [10]
Το ακεσουλφαμικό κάλιο καθώς και άλλοι υποκαταστάτες ζάχαρης παρεμβάλλονται σε μερικούς πολυεστέρους ξενιστές διπλής υδροξείδωσης (LDH) με ανταλλαγή ιόντων. Οι δοκιμές χαρακτηρισμού έχουν δείξει ότι υπάρχει πλήρης παρεμβολή των ανιόντων στους ξενιστές LDH. Στην ακεσουλφάμη K, η απορρόφηση στο 1290 cm -1 βρίσκεται στο παρεμβαλλόμενο προϊόν στο 1314 cm- 1 . [11] Επειδή αυτή η απορρόφηση αντιστοιχεί στον διπλό δεσμό SO, αυτό σημαίνει ότι οι δεσμοί αλληλεπιδρούν έντονα με τις στιβάδες υδροξειδίου του μετάλλου και έτσι είναι δυνατός ο προσανατολισμός των παρεμβαλλόμενων μορίων. [11]
Η ακεσουλφάμη καλίου χρησιμοποιείται ευρέως στην ανθρώπινη διατροφή και αποβάλλεται από τα νεφρά. Χρησιμοποιήθηκε έτσι από τους ερευνητές ως δείκτης για να εκτιμηθεί σε ποιο βαθμό οι πισίνες μολύνονται με ούρα. [12]
Άλλες ονομασίες για την ακεσουλφάμη K είναι ακεσουλφάμη καλίου, το άλας καλίου του 6-μεθυλο-1,2,3-οξοθειαζινο-4 (3Η) -όνη-2,3-διοξειδίου και 6-μεθυλο- 1,2,3- οξαθειαζίνη -4 (3Η) -ονο-3-α-2,2-διοξείδιο.
Αποτελεσματικότητα ως προς τη μείωση του βάρους
[Επεξεργασία | επεξεργασία κώδικα]Το ακεσουλφαμικό κάλιο παρέχει γλυκιά γεύση χωρίς να επηρεάζει τις γλυκαιμικές αποκρίσεις και χωρίς την υψηλή περιεκτικότητα σε θερμιδικά σάκχαρα. Ορισμένες μελέτες, ωστόσο, ανακάλυψαν ότι η κατανάλωση μη θρεπτικών γλυκαντικών έχει οδηγήσει σε αύξηση του σωματικού βάρους, επειδή οι άνθρωποι ως αντιστάθμισμα καταναλώνουν υπερβολικές θερμίδες, αυξάνοντας έτσι τον κίνδυνο διαβήτη τύπου 2 . [13]
Μια συστηματική ανασκόπηση των δημοσιευμένων μελετών σχετικά με τις επιπτώσεις τεχνητών γλυκαντικών ποτών σε βάρος κατέληξε ότι οι μελέτες με τη βοήθεια τεχνητών γλυκαντικών ουσιών ήταν πολύ πιο πιθανό να έχουν ευνοϊκά αποτελέσματα από τις μελέτες που δεν χορηγούνται από τη βιομηχανία και ότι όλες οι δημοσιευμένες μελέτες που χρηματοδοτήθηκαν από ανταγωνιστικές βιομηχανίες παρήγαγαν δυσμενή συμπεράσματα. [14]
Ανακάλυψη
[Επεξεργασία | επεξεργασία κώδικα]Το ακεσουλφαμικό κάλιο αναπτύχθηκε μετά την τυχαία ανακάλυψη μιας παρόμοιας ένωσης (2,2,6-διμεθυλο-1,2,3-οξαθειαζιν-4 (3Η) -όνη 2,2-διοξείδιο) το 1967 από τους Καρλ Κλάους (Karl Clauss) και Χάραλντ Τζένσεν (Harald Jensen) στη Hoechst AG . [15] [16] Ο Κλάους είναι είναι εγγεγραμμένος ως εφευρέτης με δίπλωμα ευρεσιτεχνίας των Ηνωμένων Πολιτειών που εκδόθηκε το 1975 στον εκδοχέα Hoechst Aktiengesellschaft για τη διαδικασία κατασκευής ακεσουλφάμης καλίου. [17] Μεταγενέστερη έρευνα έδειξε ότι διάφορες ενώσεις με την ίδια δομή βασικού δακτυλίου είχαν διαφορετικά επίπεδα γλυκύτητας. Το 6-μεθυλο-1,2,3-οξαθιαζινο-4 (3Η) -όνη 2,2-διοξείδιο είχε ιδιαίτερα ευνοϊκά χαρακτηριστικά γεύσης και ήταν σχετικά εύκολο να συντεθεί, έτσι επισημάνθηκε για περαιτέρω έρευνα και έλαβε το γενικό του όνομα ακεσουλφάμη καλίου από την Παγκόσμια Οργάνωση Υγείας το 1978. [15] Το ακεσουλφαμικό κάλιο έλαβε την πρώτη έγκριση για χρήση επιτραπέζιου πιάτου στις Ηνωμένες Πολιτείες το 1988. [10]
Ασφάλεια
[Επεξεργασία | επεξεργασία κώδικα]Όπως συμβαίνει με άλλα τεχνητά γλυκαντικά, υπάρχει ανησυχία για την ασφάλεια της ακεσουλφάμης καλίου. Ωστόσο, η Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων (FDA) ενέκρινε τη γενική χρήση της. Οι ενάντιοι ως προς τη χρήση της, λένε ότι η ακεσουλφάμη καλίου δεν έχει μελετηθεί επαρκώς και μπορεί να είναι καρκινογόνος [18] παρόλο που οι ισχυρισμοί αυτοί απορρίφθηκαν από την Ευρωπαϊκή Αρχή για την Ασφάλεια των Τροφίμων [19] και τον FDA. [20]
Ο καναδικός κυβερνητικός οργανισμός Environment Canada ανέλυσε δείγματα νερού που λήφθηκαν από τον ποταμό Grand River σε 23 τοποθεσίες μεταξύ των πηγών του και εκεί που ρέει, στη λίμνη Ήρι (Erie). Τα αποτελέσματα έδειξαν ότι η ακεσουλφάμη καλίου εμφανιζόταν σε πολύ υψηλότερες συγκεντρώσεις από τη σακχαρίνη ή τη σουκραλόζη στις διάφορες θέσεις δοκιμών. [21]
Συμπληρωματική κατάσταση
[Επεξεργασία | επεξεργασία κώδικα]- Βρετανική Φαρμακοποιία [22]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ «acesulfame–K». Merriam-Webster. Merriam-Webster. Ανακτήθηκε στις 31 Ιανουαρίου 2017.
- ↑ «Current EU approved additives and their E Numbers». UK: Food Standards Agency. 14 Μαρτίου 2012.
- ↑ Clauss, K.; Jensen, H. (1973). «Oxathiazinone Dioxides - A New Group of Sweetening Agents». Angewandte Chemie International Edition 12 (11): 869–876. doi:.
- ↑ Ager, D. J.; Pantaleone, D. P.; Henderson, S. A.; Katritzky, A. R.; Prakash, I.; Walters, D. E. (1998). «Commercial, Synthetic Nonnutritive Sweeteners». Angewandte Chemie International Edition 37 (13–14): 1802–1817. doi:. Αρχειοθετήθηκε από το πρωτότυπο στις 2008-09-10. https://web.archive.org/web/20080910124009/http://ufark12.chem.ufl.edu/Published_Papers/PDF/728.pdf.
- ↑ Ηνωμένο δίπλωμα ευρεσιτεχνίας 5.336.513 (έληξε το 2006)
- ↑ Deis RC (Νοεμβρίου 2006). «Customizing Sweetness Profiles» (PDF). Food Product Design. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 11 Αυγούστου 2014. Ανακτήθηκε στις 16 Μαΐου 2018.
- ↑ Mullarney, Μ .; Hancock, Β .; Carlson, Ο .; Ladipo, D .; Langdon, Β. Η ροή σκόνης και οι συμπαγείς μηχανικές ιδιότητες της σακχαρόζης και τριών γλυκαντικών υψηλής έντασης που χρησιμοποιούνται σε μασώμενα δισκία. Int. J. Pharm. 2003, 257, 227-236.
- ↑ Findikli, Ζ .; Zeynep, F .; Sifa, Τ. Προσδιορισμός των επιδράσεων ορισμένων τεχνητών γλυκαντικών σε ανθρώπινα περιφερικά λεμφοκύτταρα χρησιμοποιώντας τη δοκιμασία κομήτη. Εφημερίδα των τοξικολογικών και περιβαλλοντικών επιστημών υγείας 2014, 6, 147-153.
- ↑ «Home - WHO - Prequalification of Medicines Programme». Ανακτήθηκε στις 2 Μαρτίου 2017.
- ↑ 10,0 10,1 Whitehouse, C .; Boullata, J .; McCauley, L. Η πιθανή τοξικότητα των τεχνητών γλυκαντικών. AAOHN J. 2008, 56, 251-9 κουίζ 260.
- ↑ 11,0 11,1 Markland, Charles; Williams, Gareth R.; O'Hare, Dermot (2011). «The intercalation of flavouring compounds into layered double hydroxides». Journal of Materials Chemistry 21 (44): 17896. doi:.
- ↑ Erika Engelhaupt (March 1, 2017). «Just How Much Pee Is In That Pool?». NPR. https://www.npr.org/sections/health-shots/2017/03/01/517785902/just-how-much-pee-is-in-that-pool. Ανακτήθηκε στις March 2, 2017.
- ↑ Dewinter, Louise; Casteels, Kristina; Corthouts, Karen. Van de Kerckhove, Kristel. Van der Vaerent, Katrien. Vanmeerbeeck, Kelly; Μάθιους, Κρίστοφερ. Διατροφική πρόσληψη μη θρεπτικών γλυκαντικών σε παιδιά τύπου 1 διαβήτη Παιδιά προσμείξεις προσμείξεων. Μέρος Α. Χημεία, ανάλυση, έλεγχος, εκτίμηση κινδύνου έκθεσης, 2015, 33, 1, 1-8, Taylor Francis, ENGLAND
- ↑ Mandrioli, Daniele; Kearns, Cristin E.; Bero, Lisa A. (2016-09-08). «Relationship between Research Outcomes and Risk of Bias, Study Sponsorship, and Author Financial Conflicts of Interest in Reviews of the Effects of Artificially Sweetened Beverages on Weight Outcomes: A Systematic Review of Reviews» (στα αγγλικά). PLOS ONE 11 (9): e0162198. doi:. ISSN 1932-6203. PMID 27606602. Bibcode: 2016PLoSO..1162198M.
- ↑ 15,0 15,1 O'Brien-Nabors, L. (2001). Alternative Sweeteners. New York, NY: Marcel Dekker. σελ. 13. ISBN 978-0-8247-0437-7.
- ↑ Williams, R. J.· Goldberg, I. (1991). Biotechnology and Food Ingredients. New York: Van Nostrand Reinhold. ISBN 978-0-442-00272-5.
- ↑ Clauss, Κ. Μέθοδος παρασκευής 6-μεθυλο-3,4-διυδρο-1,2,3-οξαθειαζινο-4-ονο-2,2-διοξειδίου. US Patent 3917589, 1975.
- ↑ Karstadt, M. L. (2006). «Testing Needed for Acesulfame Potassium, an Artificial Sweetener». Environmental Health Perspectives 114 (9): A516; author reply A516–7. doi:. PMID 16966071.
- ↑ Scientific Committee on Food (2000). «Opinion - Re-evaluation of acesulfame K with reference to the previous SCF opinion of 1991» (PDF). SCF/CS/ADD/EDUL/194 final. EU Commission. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 10 Σεπτεμβρίου 2008. Ανακτήθηκε στις 4 Οκτωβρίου 2007.
- ↑ Kroger, M.; Meister, K.; Kava, R. (2006). «Low-Calorie Sweeteners and Other Sugar Substitutes: A Review of the Safety Issues». Comprehensive Reviews in Food Science and Food Safety 5 (2): 35–47. doi:.
- ↑ «Major Canadian river contains artificial sweeteners». Waterloo News (University of Waterloo). December 13, 2013. https://uwaterloo.ca/news/news/major-canadian-river-contains-artificial-sweeteners.
- ↑ British Pharmacopoeia Commission Secretariat (2009). «Index, BP 2009» (PDF). Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 11 Απριλίου 2009.
Εξωτερικοί σύνδεσμοι
[Επεξεργασία | επεξεργασία κώδικα]- Joint FAO/WHO Expert Committee on Food Additives evaluation monograph of Acesulfame Potassium Αρχειοθετήθηκε 2011-09-16 στο Wayback Machine. (αγγλικά)
- FDA approval of Acesulfame Potassium (αγγλικά)
- FDA approval of Acesulfame Potassium as a General Purpose Sweetener in Food (αγγλικά)
- Elmhurst College, Illinois Virtual ChemBook Acesulfame K (αγγλικά)
- Discovery News Sweeteners Linger in Groundwater (αγγλικά)


