Ερυθρόζη
| Ερυθρόζη | |
|---|---|

| |

| |
| |
| Γενικά | |
| Όνομα IUPAC | 2R,3R,4-τριυδροξυβουτανάλη (D) 2S,3S,4-τριυδροξυβουτανάλη (L) |
| Άλλες ονομασίες | Ερυθρόζη |
| Χημικά αναγνωριστικά | |
| Χημικός τύπος | C4H8O4 |
| Μοριακή μάζα | 120,042259 amu |
| Σύντομος συντακτικός τύπος |
HOCH2CH(OH)CH(OH)CHO |
| Αριθμός CAS | 583-50-6 (D) 533-49-3 (L) |
| SMILES | OC[C@@H](O)[C@@H](O)C=Ο (D) OC[C@H](O)[C@H](O)C=Ο (L) |
| PubChem CID | 94176 (D) |
| ChemSpider ID | 84990 (D) |
| Ισομέρεια | |
| Ισομερή θέσης | 16 (σταθερά) |
| Οπτικά ισομερή | 4 |
| Φυσικές ιδιότητες | |
| Εμφάνιση | σιρόπι |
| Χημικές ιδιότητες | |
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |
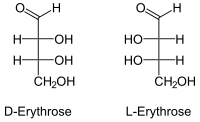
Η ερυθρόζη (σε δύο (2) οπτικά ισομερή) αντιπροσωπεύει τα δύο (2) από τα τέσσερα (4) συνολικά στερεοϊσομερή της 2,3,4-τριυδροξυβουτανάλης και είναι μια αλδόζη με τέσσερα (4) άτομα άνθρακα, δηλαδή μια τετρόζη. Για την ακρίβεια, μόνο το D-ισομερές της, δηλαδή η 2R,3R,4-τριυδροξυβουτανάλη, είναι φυσικό.
Βιοχημικός ρόλος[Επεξεργασία | επεξεργασία κώδικα]
Η ερυθρόζη αντιδρά αργά με το υδροχλωρικό οξύ, σχηματίζοντας γαλακτικό οξύ. Στο μεταβολισμό των σακχάρων η 4-φωσφοερυθρόζη είναι ένα ενδιάμεσο μόριο-κλειδί[1]. Σχηματίζεται στη μεταβολική οδό της φωσφοπεντόζης μετά τη δράση του ενζύμου τρανσαλδολάση, από 7-φωσφοσεδοεπτουλόζη και 3-φωσφογλυκεριναλδεΰδη, μαζί με 6-φωσφοφρουκτόζη. Τα φυτά και πολλοί μικροοργανισμοί μπορούν να χρησιμοποιήσουν την 4-φωσφοερυθρόζη μαζί με το φωσφενολοπυροσταφυλικό οξύ (PEP) για τη σύνθεση των τριών (3) αρωματικών αμινοξέων, δηλαδή της τρυπτοφάνης, της τυροσίνης και της φαινυλαλανίνης[2]. Επιπλέον η 4-φωσφοερυθρόζη μπορεί να χρησιμοποιηθεί από φυτά, βακτήρια και άλγη για τη σύνθεση της πυριδοξίνης (που είναι η βιταμίνη B6).
Παραπομπές και σημειώσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ H. P. T. Ammon: Hunnius pharmazeutisches Worterbuch, Walter de Gruyter, 2004, ISBN 3-11-017475-8.
- ↑ J. M. Berg, J. L. Tymoczko, L. Stryer: Biochemie. 6. Auflage. Spektrum Akademischer Verlag, Elsevier GmbH, München 2007; S. 644f, 773–775; ISBN 978-3-8274-1800-5.
Πηγές[Επεξεργασία | επεξεργασία κώδικα]
- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
- Δημήτριου Ν. Νικολαΐδη: Ειδικά μαθήματα Οργανικής Χημείας, Θεσσαλονίκη 1983.
| ||||||||||||||||||||||||||||||||||||
