Χρήστης:Dmtrs32/πρόχειρο: Διαφορά μεταξύ των αναθεωρήσεων
| Γραμμή 20: | Γραμμή 20: | ||
Χρειάζονται ι[[Ιόν|όντα]] [[Μαγνήσιο|μαγνησίου]] (Mg<sup>2+</sup>) για την ενζυματική δραστηριότητα. Η σωστή τοποθέτηση των Mg<sup>2+</sup> στην ενεργή θέση του ενζύμου περιλαμβάνει την προσθήκη ενός "ενεργοποιητικού" μορίου [[Διοξείδιο του άνθρακα|διοξειδίου του άνθρακα]] στην ενεργή θέση μίας [[λυσίνη]] (σχηματίζοντας ένα καρβαμικό).<ref>[https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=mcb.figgrp.4496 Molecular Cell Biology], 4th edition, by Harvey Lodish, Arnold Berk, S. Lawrence Zipursky, Paul Matsudaira, David Baltimore and James E. Darnell. Published by W. H. Freeman & Co. (2000) New York. Online textbook. Figure 16-48 shows a structural model of the active site, including the involvement of magnesium. The Protein Data Bank feature article on RuBisCO also includes a model of [http://nist.rcsb.org/pdb/molecules/pdb11_3.html magnesium at the active site] {{Webarchive|url=https://web.archive.org/web/20060109143747/http://nist.rcsb.org/pdb/molecules/pdb11_3.html |date=2006-01-09 }}.</ref> Το Mg <sup> 2+ </sup> λειτουργεί οδηγώντας στην αποπρωτονίωση του υπολείμματος Lys210, με αποτέλεσμα το υπόλειμμα Lys να περιστρέφεται κατά 120 μοίρες προς το διαμορφομερές «trans», μειώνοντας την απόσταση μεταξύ του αζώτου της Lys και του άνθρακα του CO<sub>2</sub>. Η εγγύτητα επιτρέπει τον σχηματισμό ενός ομοιοπολικού δεσμού, με αποτέλεσμα το καρβαμιδικό. |
Χρειάζονται ι[[Ιόν|όντα]] [[Μαγνήσιο|μαγνησίου]] (Mg<sup>2+</sup>) για την ενζυματική δραστηριότητα. Η σωστή τοποθέτηση των Mg<sup>2+</sup> στην ενεργή θέση του ενζύμου περιλαμβάνει την προσθήκη ενός "ενεργοποιητικού" μορίου [[Διοξείδιο του άνθρακα|διοξειδίου του άνθρακα]] στην ενεργή θέση μίας [[λυσίνη]] (σχηματίζοντας ένα καρβαμικό).<ref>[https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=mcb.figgrp.4496 Molecular Cell Biology], 4th edition, by Harvey Lodish, Arnold Berk, S. Lawrence Zipursky, Paul Matsudaira, David Baltimore and James E. Darnell. Published by W. H. Freeman & Co. (2000) New York. Online textbook. Figure 16-48 shows a structural model of the active site, including the involvement of magnesium. The Protein Data Bank feature article on RuBisCO also includes a model of [http://nist.rcsb.org/pdb/molecules/pdb11_3.html magnesium at the active site] {{Webarchive|url=https://web.archive.org/web/20060109143747/http://nist.rcsb.org/pdb/molecules/pdb11_3.html |date=2006-01-09 }}.</ref> Το Mg <sup> 2+ </sup> λειτουργεί οδηγώντας στην αποπρωτονίωση του υπολείμματος Lys210, με αποτέλεσμα το υπόλειμμα Lys να περιστρέφεται κατά 120 μοίρες προς το διαμορφομερές «trans», μειώνοντας την απόσταση μεταξύ του αζώτου της Lys και του άνθρακα του CO<sub>2</sub>. Η εγγύτητα επιτρέπει τον σχηματισμό ενός ομοιοπολικού δεσμού, με αποτέλεσμα το καρβαμιδικό. |
||
<ref name=":2">{{cite journal | vauthors = Stec B | title = Structural mechanism of RuBisCO activation by carbamylation of the active site lysine | journal = Proceedings of the National Academy of Sciences of the United States of America | volume = 109 | issue = 46 | pages = 18785–90 | date = November 2012 | pmid = 23112176 | pmc = 3503183 | doi = 10.1073/pnas.1210754109 | bibcode = 2012PNAS..10918785S }}</ref> Το Mg<sup>2+</sup> ενεργοποιείται πρώτα για να συνδεθεί με την ενεργή θέση από την περιστροφή του His335 σε μια εναλλακτική διαμόρφωση. Το Mg<sup>2+</sup> στη συνέχεια συντονίζεται από τα υπολείμματα His της ενεργής θέσης (His300, His302, His335) και εξουδετερώνεται εν μέρει από το συντονισμό των τριών μορίων νερού και τη μετατροπή τους σε <sup>-</sup>OH.<ref name=":2" /> Αυτός ο συντονισμός καταλήγει σε ένα ασταθές σύμπλεγμα, αλλά παράγει ένα ευνοϊκό περιβάλλον για τη δέσμευση του Mg<sup>2+ </sup>. Ο σχηματισμός του καρβαμικού ευνοείται από ένα [[αλκαλικότητα | αλκαλικό]] [[pH]]. Το pH και η [[συγκέντρωση]] ιόντων μαγνησίου στο διαμέρισμα ρευστού (στα φυτά, στο στρώμα του χλωροπλάστη<ref>The [https://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=books&doptcmdl=GenBookHL&term=RuBisCO+AND+mcb%5Bbook%5D+AND+106599%5Buid%5D&rid=mcb.section.4493#4494 Lodish textbook] describes the localization of RuBisCO to the stromal space of chloroplasts. [https://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=books&doptcmdl=GenBookHL&term=RuBisCO+stroma+AND+106623%5Buid%5D&rid=mcb.figgrp.4715 Figure 17-7] illustrates how RuBisCO small subunits move into the chloroplast stroma and assemble with the large subunits.</ref>) αυξάνεται στο φως. Ο ρόλος της αλλαγής των επιπέδων ιόντων pH και μαγνησίου στη ρύθμιση της δραστηκότητας του ενζύμου RuBisCO συζητείται [[#Regulation of the enzymatic activity | παρακάτω]]. Μόλις σχηματιστεί το καρβαμικό, το His335 ολοκληρώνει την ενεργοποίηση επιστρέφοντας στην αρχική του θέση μέσω θερμικής διακύμανσης.<ref name=":2" /> |
<ref name=":2">{{cite journal | vauthors = Stec B | title = Structural mechanism of RuBisCO activation by carbamylation of the active site lysine | journal = Proceedings of the National Academy of Sciences of the United States of America | volume = 109 | issue = 46 | pages = 18785–90 | date = November 2012 | pmid = 23112176 | pmc = 3503183 | doi = 10.1073/pnas.1210754109 | bibcode = 2012PNAS..10918785S }}</ref> Το Mg<sup>2+</sup> ενεργοποιείται πρώτα για να συνδεθεί με την ενεργή θέση από την περιστροφή του His335 σε μια εναλλακτική διαμόρφωση. Το Mg<sup>2+</sup> στη συνέχεια συντονίζεται από τα υπολείμματα His της ενεργής θέσης (His300, His302, His335) και εξουδετερώνεται εν μέρει από το συντονισμό των τριών μορίων νερού και τη μετατροπή τους σε <sup>-</sup>OH.<ref name=":2" /> Αυτός ο συντονισμός καταλήγει σε ένα ασταθές σύμπλεγμα, αλλά παράγει ένα ευνοϊκό περιβάλλον για τη δέσμευση του Mg<sup>2+ </sup>. Ο σχηματισμός του καρβαμικού ευνοείται από ένα [[αλκαλικότητα | αλκαλικό]] [[pH]]. Το pH και η [[συγκέντρωση]] ιόντων μαγνησίου στο διαμέρισμα ρευστού (στα φυτά, στο στρώμα του χλωροπλάστη<ref>The [https://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=books&doptcmdl=GenBookHL&term=RuBisCO+AND+mcb%5Bbook%5D+AND+106599%5Buid%5D&rid=mcb.section.4493#4494 Lodish textbook] describes the localization of RuBisCO to the stromal space of chloroplasts. [https://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=books&doptcmdl=GenBookHL&term=RuBisCO+stroma+AND+106623%5Buid%5D&rid=mcb.figgrp.4715 Figure 17-7] illustrates how RuBisCO small subunits move into the chloroplast stroma and assemble with the large subunits.</ref>) αυξάνεται στο φως. Ο ρόλος της αλλαγής των επιπέδων ιόντων pH και μαγνησίου στη ρύθμιση της δραστηκότητας του ενζύμου RuBisCO συζητείται [[#Regulation of the enzymatic activity | παρακάτω]]. Μόλις σχηματιστεί το καρβαμικό, το His335 ολοκληρώνει την ενεργοποίηση επιστρέφοντας στην αρχική του θέση μέσω θερμικής διακύμανσης.<ref name=":2" /> |
||
{| |
|||
|- valign=top |
|||
|{{Infobox protein family |
|||
| Symbol = RuBisCO_large |
|||
| Name = RuBisCO large chain,<br />catalytic domain |
|||
| image = |
|||
| width = |
|||
| caption = |
|||
| Pfam = PF00016 |
|||
| InterPro = IPR000685 |
|||
| SMART = |
|||
| PROSITE = PDOC00142 |
|||
| SCOP = 3rub |
|||
| TCDB = |
|||
| OPM family = |
|||
| OPM protein = |
|||
| CDD = cd08148 |
|||
| PDB = {{PDB2|1aa1}}, {{PDB2|1aus}}, {{PDB2|1bwv}}, {{PDB2|1bxn}}, {{PDB2|1ej7}}, {{PDB2|1geh}}, {{PDB2|1gk8}}, {{PDB2|1ir1}}, {{PDB2|1ir2}}, {{PDB2|1iwa}}, {{PDB2|1rba}}, {{PDB2|1rbl}}, {{PDB2|1rbo}}, {{PDB2|1rco}}, {{PDB2|1rcx}}, {{PDB2|1rld}}, {{PDB2|1rsc}}, {{PDB2|1rus}}, {{PDB2|1rxo}}, {{PDB2|1svd}}, {{PDB2|1tel}}, {{PDB2|1upm}}, {{PDB2|1upp}}, {{PDB2|1uw9}}, {{PDB2|1uwa}}, {{PDB2|1uzd}}, {{PDB2|1uzh}}, {{PDB2|1wdd}}, {{PDB2|1ykw}}, {{PDB2|2cwx}}, {{PDB2|2cxe}}, {{PDB2|2d69}}, {{PDB2|2qyg}}, {{PDB2|2rus}}, {{PDB2|2v63}}, {{PDB2|2v67}}, {{PDB2|2v68}}, {{PDB2|2v69}}, {{PDB2|2v6a}}, {{PDB2|3rub}}, {{PDB2|4rub}}, {{PDB2|5rub}}, {{PDB2|8ruc}}, {{PDB2|9rub}} |
|||
}} |
|||
|{{Infobox protein family |
|||
| Symbol = RuBisCO_large_N |
|||
| Name = RuBisCO, N-terminal domain |
|||
| image = |
|||
| width = |
|||
| caption = |
|||
| Pfam = PF02788 |
|||
| InterPro = IPR017444 |
|||
| SMART = |
|||
| PROSITE = |
|||
| SCOP = 3rub |
|||
| TCDB = |
|||
| OPM family = |
|||
| OPM protein = |
|||
| PDB = {{PDB2|1aa1}}, {{PDB2|1aus}}, {{PDB2|1bwv}}, {{PDB2|1bxn}}, {{PDB2|1ej7}}, {{PDB2|1geh}}, {{PDB2|1gk8}}, {{PDB2|1ir1}}, {{PDB2|1ir2}}, {{PDB2|1iwa}}, {{PDB2|1rba}}, {{PDB2|1rbl}}, {{PDB2|1rbo}}, {{PDB2|1rco}}, {{PDB2|1rcx}}, {{PDB2|1rld}}, {{PDB2|1rsc}}, {{PDB2|1rus}}, {{PDB2|1rxo}}, {{PDB2|1svd}}, {{PDB2|1tel}}, {{PDB2|1upm}}, {{PDB2|1upp}}, {{PDB2|1uw9}}, {{PDB2|1uwa}}, {{PDB2|1uzd}}, {{PDB2|1uzh}}, {{PDB2|1wdd}}, {{PDB2|1ykw}}, {{PDB2|2cwx}}, {{PDB2|2cxe}}, {{PDB2|2d69}}, {{PDB2|2qyg}}, {{PDB2|2rus}}, {{PDB2|2v63}}, {{PDB2|2v67}}, {{PDB2|2v68}}, {{PDB2|2v69}}, {{PDB2|2v6a}}, {{PDB2|3rub}}, {{PDB2|4rub}}, {{PDB2|5rub}}, {{PDB2|8ruc}}, {{PDB2|9rub}} |
|||
}} |
|||
|{{Infobox protein family |
|||
| Symbol = RuBisCO_small |
|||
| Name = RuBisCO, small chain |
|||
| image = |
|||
| width = |
|||
| caption = |
|||
| Pfam = PF00101 |
|||
| InterPro = IPR000894 |
|||
| SMART = |
|||
| PROSITE = |
|||
| SCOP = 3rub |
|||
| TCDB = |
|||
| OPM family = |
|||
| OPM protein = |
|||
| CDD = cd03527 |
|||
| PDB = {{PDB2|1aa1}}, {{PDB2|1aus}}, {{PDB2|1bwv}}, {{PDB2|1bxn}}, {{PDB2|1ej7}}, {{PDB2|1gk8}}, {{PDB2|1ir1}}, {{PDB2|1ir2}}, {{PDB2|1iwa}}, {{PDB2|1rbl}}, {{PDB2|1rbo}}, {{PDB2|1rco}}, {{PDB2|1rcx}}, {{PDB2|1rlc}}, {{PDB2|1rld}}, {{PDB2|1rsc}}, {{PDB2|1rxo}}, {{PDB2|1svd}}, {{PDB2|1upm}}, {{PDB2|1upp}}, {{PDB2|1uw9}}, {{PDB2|1uwa}}, {{PDB2|1uzd}}, {{PDB2|1uzh}}, {{PDB2|1wdd}}, {{PDB2|2v63}}, {{PDB2|2v67}}, {{PDB2|2v68}}, {{PDB2|2v69}}, {{PDB2|2v6a}}, {{PDB2|3rub}}, {{PDB2|4rub}}, {{PDB2|8ruc}} |
|||
}} |
|||
|} |
|||
==Ενζυματική δραστηριότητα== |
==Ενζυματική δραστηριότητα== |
||
[[File:RuBisCO reaction CO2 or O2.svg|center|thumb|upright=2|Δύο κύριες αντιδράσεις του RuBisCo: CO<sub>2</sub> σταθεροποίηση και οξυγόνωση. |
[[File:RuBisCO reaction CO2 or O2.svg|center|thumb|upright=2|Δύο κύριες αντιδράσεις του RuBisCo: CO<sub>2</sub> σταθεροποίηση και οξυγόνωση.]] |
||
| ⚫ | Η RuBisCO είναι ένα από τα πολλά ένζυμα στον [[Κύκλος του Κάλβιν|κύκλο του Κάλβιν]]. Όταν η Rubisco διευκολύνει την επίθεση του CO<sub>2 </sub> στον άνθρακα C2 του RuBP και την επακόλουθη διάσπαση δεσμών μεταξύ του άνθρακα C3 και C2, σχηματίζονται 2 μόρια 3-φωσφορικού γλυκερικού. Η μετατροπή περιλαμβάνει αυτά τα στάδια: ενολοποίηση, [[καρβοξυλίωση]], ενυδάτωση, διάσπαση δεσμού C-C και [[πρωτονίωση]].<ref name="catalysis">{{cite journal | vauthors = Andersson I | title = Catalysis and regulation in Rubisco | journal = Journal of Experimental Botany | volume = 59 | issue = 7 | pages = 1555–68 | date = May 2008 | pmid = 18417482 | doi = 10.1093/jxb/ern091 | doi-access = free }}</ref><ref>{{cite journal | vauthors = Erb TJ, Zarzycki J | title = A short history of RubisCO: the rise and fall (?) of Nature's predominant CO<sub>2</sub> fixing enzyme | journal = Current Opinion in Biotechnology | volume = 49 | pages = 100–107 | date = February 2018 | pmid = 28843191 | doi = 10.1016/j.copbio.2017.07.017 | pmc = 7610757 | doi-access = free }}</ref><ref>{{cite journal | vauthors = Lundqvist T, Schneider G | title = Crystal structure of activated ribulose-1,5-bisphosphate carboxylase complexed with its substrate, ribulose-1,5-bisphosphate | journal = The Journal of Biological Chemistry | volume = 266 | issue = 19 | pages = 12604–11 | date = July 1991 | pmid = 1905726 | doi = 10.1016/S0021-9258(18)98942-8 | doi-access = free }}</ref> |
||
Two main reactions of RuBisCo: CO<sub>2</sub> fixation and oxygenation.]] |
|||
Το RuBisCO είναι ένα από τα πολλά ένζυμα στον [[κύκλο Calvin]]. Όταν το Rubisco διευκολύνει την επίθεση του CO <sub> 2 </sub> στον άνθρακα C2 του RuBP και την επακόλουθη διάσπαση δεσμών μεταξύ του άνθρακα C3 και C2, σχηματίζονται 2 μόρια γλυκερικού-3-φωσφορικού. Η μετατροπή περιλαμβάνει αυτά τα στάδια: [[Τατομερισμός κετο-ενόλης | ενοποίηση]], [[καρβοξυλίωση]], [[Αντίδραση ενυδάτωσης | ενυδάτωση]], διάσπαση δεσμού C-C και [[πρωτονίωση]]. |
|||
| ⚫ | RuBisCO |
||
κκκ |
|||
=== Υποστρώματα === |
=== Υποστρώματα === |
||
[[Υπόστρωμα (χημεία) | Υποστρώματα]] για τη RuBisCO είναι η 1,5-διφωσφορική ριβουλόζη και το [[διοξείδιο του άνθρακα]] (διακριτά από το "ενεργοποιητικό" διοξείδιο του άνθρακα).<ref>The [https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=stryer.section.2785#2790 chemical reactions] catalyzed by RuBisCO are described in the online [https://www.ncbi.nlm.nih.gov/books/bv.fcgi?call=bv.View..ShowTOC&rid=stryer.TOC&depth=2 Biochemistry] textbook by Stryer et al.</ref> Η RuBisCO καταλύει επίσης μια αντίδραση 1,5-διφωσφορικής ριβουλόζης και μοριακού [[Οξυγόνο|οξυγόνου]] ({{Chem | O | 2}}) αντί του διοξειδίου του άνθρακα. Η διάκριση μεταξύ των υποστρωμάτων CO<sub>2 </sub> και O<sub>2 </sub> αποδίδεται στις διαφορετικές αλληλεπιδράσεις των τετραπολικών ροπών του υποστρώματος και μιας υψηλής βαθμίδας [[Ηλεκτρικό πεδίο|ηλεκτροστατικού πεδίου]].<ref name=":2" /> Αυτή η βαθμίδα καθορίζεται από τη διμερή μορφή της ελάχιστα ενεργής RuBisCO, η οποία με τα δύο συστατικά της παρέχει έναν συνδυασμό αντίθετα φορτισμένων τομέων που απαιτούνται για την αλληλεπίδραση του ενζύμου με το O<sub>2 </sub> και το CO<sub>2</sub>. Αυτές οι συνθήκες βοηθούν στην εξήγηση του χαμηλού ποσοστού αντικατάστασης που βρέθηκε στη RuBisCO: Για να αυξηθεί η ισχύς του [[Ηλεκτρικό πεδίο|ηλεκτρικού πεδίου]] που απαιτείται για επαρκή αλληλεπίδραση με τις τετραπολικές ροπές των υποστρωμάτων, τα τερματικά τμήματα C και N του ενζύμου πρέπει να κλείσουν, επιτρέποντας την απομόνωση της δραστικής θέσης από τον διαλύτη και μειώνοντας τη [[διηλεκτρική σταθερά]].<ref>{{cite journal | vauthors = Satagopan S, Spreitzer RJ | title = Plant-like substitutions in the large-subunit carboxy terminus of Chlamydomonas Rubisco increase CO2/O2 specificity | journal = BMC Plant Biology | volume = 8 | pages = 85 | date = July 2008 | pmid = 18664299 | pmc = 2527014 | doi = 10.1186/1471-2229-8-85 }}</ref> Αυτή η απομόνωση έχει σημαντικό[[Εντροπία | εντροπικό]] κόστος και έχει ως αποτέλεσμα το χαμηλό ποσοστό αντικατάστασης. |
|||
[[Υπόστρωμα (χημεία) | Υπόστρωμα]] για το RuBisCO είναι [[ριβουλόζη-1,5-διφωσφορική]] και [[διοξείδιο του άνθρακα]] (διακριτά από το "ενεργοποιητικό" διοξείδιο του άνθρακα). |
|||
[[Substrate (chemistry)|Substrate]]s for RuBisCO are [[ribulose-1,5-bisphosphate]] and [[carbon dioxide]] (distinct from the "activating" carbon dioxide).<ref>The [https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=stryer.section.2785#2790 chemical reactions] catalyzed by RuBisCO are described in the online [https://www.ncbi.nlm.nih.gov/books/bv.fcgi?call=bv.View..ShowTOC&rid=stryer.TOC&depth=2 Biochemistry] textbook by Stryer et al.</ref> Το RuBisCO καταλύει επίσης μια αντίδραση ριβουλόζης-1,5-διφωσφορικής και [[οξυγόνου | μοριακό οξυγόνο]] ({{Chem | O | 2}}) αντί του διοξειδίου του άνθρακα ({{CO2}}). |
|||
Η διάκριση μεταξύ των υποστρωμάτων CO <sub> 2 </sub> και O <sub> 2 </sub> αποδίδεται στις διαφορετικές αλληλεπιδράσεις των [[τετραπολικών στιγμών]] του υποστρώματος και ενός υψηλού [[ηλεκτροστατικού πεδίου]] [[ βαθμίδα]]. |
|||
RuBisCO also catalyses a reaction of ribulose-1,5-bisphosphate and [[oxygen|molecular oxygen]] ({{Chem|O|2}}) instead of carbon dioxide ({{CO2}}). |
|||
Discriminating between the substrates CO<sub>2</sub> and O<sub>2</sub> is attributed to the differing interactions of the substrate's [[quadrupole moment]]s and a high [[electrostatic field]] [[gradient]].<ref name=":2" /> Αυτή η κλίση καθορίζεται από τη μορφή [[Dimer (chemistry) | dimer]] του ελάχιστα ενεργού RuBisCO, το οποίο με τα δύο συστατικά του παρέχει έναν συνδυασμό αντίθετα φορτισμένων τομέων που απαιτούνται για την αλληλεπίδραση του ενζύμου με το O <sub> 2 </sub> και {{CO2}}. Αυτές οι συνθήκες βοηθούν στην εξήγηση του χαμηλού ποσοστού κύκλου εργασιών που βρέθηκε στο RuBisCO: Για να αυξηθεί η ισχύς του [[ηλεκτρικού πεδίου]] που απαιτείται για επαρκή αλληλεπίδραση με τα [[τετράπολα στιγμή]] των υποστρωμάτων, τα τερματικά C και N το ένζυμο πρέπει να κλείσει, επιτρέποντας την απομόνωση της δραστικής θέσης από τον διαλύτη και μείωση της [[διηλεκτρικής σταθεράς]]. |
|||
This gradient is established by the [[Dimer (chemistry)|dimer]] form of the minimally active RuBisCO, which with its two components provides a combination of oppositely charged domains required for the enzyme's interaction with O<sub>2</sub> and {{CO2}}. These conditions help explain the low turnover rate found in RuBisCO: In order to increase the strength of the [[electric field]] necessary for sufficient interaction with the substrates’ [[quadrupole moment]]s, the C- and N- terminal segments of the enzyme must be closed off, allowing the active site to be isolated from the solvent and lowering the [[dielectric constant]].<ref>{{cite journal | vauthors = Satagopan S, Spreitzer RJ | title = Plant-like substitutions in the large-subunit carboxy terminus of Chlamydomonas Rubisco increase CO2/O2 specificity | journal = BMC Plant Biology | volume = 8 | pages = 85 | date = July 2008 | pmid = 18664299 | pmc = 2527014 | doi = 10.1186/1471-2229-8-85 }}</ref> Αυτή η απομόνωση έχει σημαντικό κόστος [[Εντροπία | εντροπική]] και έχει ως αποτέλεσμα το χαμηλό ποσοστό κύκλου εργασιών. |
|||
This isolation has a significant [[Entropy|entropic]] cost, and results in the poor turnover rate. |
|||
κκκ |
|||
==== Δέσιμο RuBP Binding RuBP ==== |
==== Δέσιμο RuBP Binding RuBP ==== |
||
Η καρβαμυλίωση της ε-αμινο ομάδας του Lys201 σταθεροποιείται με συντονισμό με το Mg <sup> 2+ </sup>. |
Η καρβαμυλίωση της ε-αμινο ομάδας του Lys201 σταθεροποιείται με συντονισμό με το Mg <sup> 2+ </sup>. |
||
Έκδοση από την 18:22, 24 Δεκεμβρίου 2021
| Καρβοξυλάση/οξυγονάση της 1,5-διφωσφορικής ριβουλόζης | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Μια τρισδιάστατη απεικόνιση του ενεργοποιημένου RuBisCO από σπανάκι σε ανοιχτή μορφή με προσβάσιμη ενεργή τοποθεσία. Τα υπολείμματα της ενεργού θέσης Lys175 σημειώνονται με ροζ χρώμα και παρέχεται ένα κοντινό πλάνο του υπολείμματος στα δεξιά για ένα από τα μονομερή που συνθέτουν το ένζυμο. | |||||||||
| Ταυτοποιητές | |||||||||
| Αρ. EC | 4.1.1.39 | ||||||||
| Αρ. CAS | 9027-23-0 | ||||||||
| Βάσεις δεδομένων | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | metabolic pathway | ||||||||
| PRIAM | profile | ||||||||
| Δομές PDB | RCSB PDB PDBe PDBsum | ||||||||
| Γονιδιακή οντολογία | AmiGO / QuickGO | ||||||||
| |||||||||
H καρβοξυλάση-οξυγονάση της 1,5-διφωσφορική ριβουλόζης (Ribulose-1,5-bisphosphate carboxylase-oxygenase), κοινώς γνωστή με τις συντομογραφίες RuBisCo, rubisco[1], RuBPCase, ή RuBPco, είναι ένα ένζυμο που εμπλέκεται στο πρώτο σημαντικό βήμα της δέσμευσης του άνθρακα, μιας διαδικασίας με την οποία το ατμοσφαιρικό διοξείδιο του άνθρακα μετατρέπεται από φυτά και άλλους φωτοσυνθετικούς οργανισμούς σε πλούσια σε ενέργεια μόρια όπως γλυκόζη. Από χημική άποψη, καταλύει την καρβοξυλίωση της 1,5-διφωσφορικής ριβουλόζης (επίσης γνωστής ως RuBP). Είναι ίσως το πιο άφθονο ένζυμο στη Γη.[2][3][4]
Εναλλακτικές διαδρομές δέσμευσης του άνθρακα
Η RuBisCO είναι σημαντική βιολογικά επειδή καταλύει την κύρια χημική αντίδραση με την οποία ο ανόργανος άνθρακας εισέρχεται στη βιόσφαιρα. Ενώ πολλά αυτότροφα βακτήρια και αρχαία διορθώνουν τον άνθρακα μέσω της αναγωγικής οδού του ακετυλοσυνένζυμου Α, του 3-υδροξυπροπιονικού κύκλου, ή του αντίστροφου κύκλου Krebs, αυτά τα μονοπάτια είναι σχετικά μικροί συντελεστές στη γενική δέσμευση άνθρακα σε σύγκριση με αυτούς που καταλύονται από τη RuBisCO. Η φωσφοενολοπυροσταφυλική καρβοξυλάση, σε αντίθεση με το RuBisCO, διορθώνει μόνο προσωρινά τον άνθρακα. Αντικατοπτρίζοντας τη σημασία του, η RuBisCO είναι η πιο άφθονη πρωτεΐνη στα φύλλα, που αντιπροσωπεύει το 50% της διαλυτής πρωτεΐνης φύλλων στην αφομοίωση του C3 (20-30% του συνολικού αζώτου των φύλλων) και 30% της διαλυτής πρωτεΐνης φύλλων σε δέσμευση C4 (5-9% του συνολικού αζώτου των φύλλων).[4] Δεδομένου του σημαντικού ρόλου του στη βιόσφαιρα, η γενετική μηχανική της RuBisCO στις καλλιέργειες έχει συνεχές ενδιαφέρον (βλ. παρακάτω).
Δομή

Η ενεργή θέση της RuBisCO της Galdieria sulphuraria με CO2: Τα υπολείμματα που εμπλέκονται τόσο στη δραστική θέση όσο και στο σταθεροποιητικό CO2 για την κατάλυση ενζύμων εμφανίζονται με χρώμα και επισημαίνονται. Οι αποστάσεις των αλληλεπιδράσεων των δεσμών υδρογόνου φαίνονται σε angstroms. Το ιόν Mg2+ (πράσινη σφαίρα) εμφανίζεται συντονισμένο με το CO2 και ακολουθείται από τρία μόρια νερού (κόκκινες σφαίρες). Όλα τα άλλα υπολείμματα τοποθετούνται σε κλίμακα του γκρι.

Στα φυτά, στα άλγη, στα κυανοβακτήρια και στα φωτοτροφικά και χημειοαυτοτροφικά πρωτεοβακτήρια το ένζυμο αποτελείται συνήθως από δύο τύπους υπομονάδας πρωτεΐνης, που ονομάζονται η μεγάλη αλυσίδα (L, περίπου 55.000 Da) και η μικρή αλυσίδα (S, περίπου 13.000 Da). Το γονίδιο της μεγάλης αλυσίδας ( rbcL ) κωδικοποιείται από το χλωροπλάστη DNA στα φυτά.[5] Τυπικά υπάρχουν αρκετά γονίδια σχετικά μικρής αλυσίδας στον πυρήνα των φυτικών κυττάρων και οι μικρές αλυσίδες εισάγονται στο διαμέρισμα στρωματικών χλωροπλαστών από το κυτταρόλυμα διασχίζοντας την εξωτερική μεμβράνη των χλωροπλαστών.[6][7] Οι ενζυματικά ενεργές θέσεις δέσμευσης του υποστρώματος (1,5-διφωσφορική ριβουλόζη ) βρίσκονται στις μεγάλες αλυσίδες που σχηματίζονται διμερή στα οποία τααμινοξέα από κάθε μεγάλη αλυσίδα συνεισφέρουν στις θέσεις σύνδεσης. Συνολικά οκτώ μεγάλες αλυσίδες (= 4 διμερή) και οκτώ μικρές αλυσίδες σχηματίζουν ένα μεγαλύτερο συγκρότημα περίπου 540.000 Da.[8] Σε ορισμένα πρωτεοβακτήρια και δυνοφύκη, έχουν βρεθεί ένζυμα που αποτελούνται μόνο από μεγάλες υπομονάδες.[9] Χρειάζονται ιόντα μαγνησίου (Mg2+) για την ενζυματική δραστηριότητα. Η σωστή τοποθέτηση των Mg2+ στην ενεργή θέση του ενζύμου περιλαμβάνει την προσθήκη ενός "ενεργοποιητικού" μορίου διοξειδίου του άνθρακα στην ενεργή θέση μίας λυσίνη (σχηματίζοντας ένα καρβαμικό).[10] Το Mg 2+ λειτουργεί οδηγώντας στην αποπρωτονίωση του υπολείμματος Lys210, με αποτέλεσμα το υπόλειμμα Lys να περιστρέφεται κατά 120 μοίρες προς το διαμορφομερές «trans», μειώνοντας την απόσταση μεταξύ του αζώτου της Lys και του άνθρακα του CO2. Η εγγύτητα επιτρέπει τον σχηματισμό ενός ομοιοπολικού δεσμού, με αποτέλεσμα το καρβαμιδικό. [11] Το Mg2+ ενεργοποιείται πρώτα για να συνδεθεί με την ενεργή θέση από την περιστροφή του His335 σε μια εναλλακτική διαμόρφωση. Το Mg2+ στη συνέχεια συντονίζεται από τα υπολείμματα His της ενεργής θέσης (His300, His302, His335) και εξουδετερώνεται εν μέρει από το συντονισμό των τριών μορίων νερού και τη μετατροπή τους σε -OH.[11] Αυτός ο συντονισμός καταλήγει σε ένα ασταθές σύμπλεγμα, αλλά παράγει ένα ευνοϊκό περιβάλλον για τη δέσμευση του Mg2+ . Ο σχηματισμός του καρβαμικού ευνοείται από ένα αλκαλικό pH. Το pH και η συγκέντρωση ιόντων μαγνησίου στο διαμέρισμα ρευστού (στα φυτά, στο στρώμα του χλωροπλάστη[12]) αυξάνεται στο φως. Ο ρόλος της αλλαγής των επιπέδων ιόντων pH και μαγνησίου στη ρύθμιση της δραστηκότητας του ενζύμου RuBisCO συζητείται παρακάτω. Μόλις σχηματιστεί το καρβαμικό, το His335 ολοκληρώνει την ενεργοποίηση επιστρέφοντας στην αρχική του θέση μέσω θερμικής διακύμανσης.[11]
Ενζυματική δραστηριότητα

Η RuBisCO είναι ένα από τα πολλά ένζυμα στον κύκλο του Κάλβιν. Όταν η Rubisco διευκολύνει την επίθεση του CO2 στον άνθρακα C2 του RuBP και την επακόλουθη διάσπαση δεσμών μεταξύ του άνθρακα C3 και C2, σχηματίζονται 2 μόρια 3-φωσφορικού γλυκερικού. Η μετατροπή περιλαμβάνει αυτά τα στάδια: ενολοποίηση, καρβοξυλίωση, ενυδάτωση, διάσπαση δεσμού C-C και πρωτονίωση.[13][14][15]
Υποστρώματα
Υποστρώματα για τη RuBisCO είναι η 1,5-διφωσφορική ριβουλόζη και το διοξείδιο του άνθρακα (διακριτά από το "ενεργοποιητικό" διοξείδιο του άνθρακα).[16] Η RuBisCO καταλύει επίσης μια αντίδραση 1,5-διφωσφορικής ριβουλόζης και μοριακού οξυγόνου (O 2) αντί του διοξειδίου του άνθρακα. Η διάκριση μεταξύ των υποστρωμάτων CO2 και O2 αποδίδεται στις διαφορετικές αλληλεπιδράσεις των τετραπολικών ροπών του υποστρώματος και μιας υψηλής βαθμίδας ηλεκτροστατικού πεδίου.[11] Αυτή η βαθμίδα καθορίζεται από τη διμερή μορφή της ελάχιστα ενεργής RuBisCO, η οποία με τα δύο συστατικά της παρέχει έναν συνδυασμό αντίθετα φορτισμένων τομέων που απαιτούνται για την αλληλεπίδραση του ενζύμου με το O2 και το CO2. Αυτές οι συνθήκες βοηθούν στην εξήγηση του χαμηλού ποσοστού αντικατάστασης που βρέθηκε στη RuBisCO: Για να αυξηθεί η ισχύς του ηλεκτρικού πεδίου που απαιτείται για επαρκή αλληλεπίδραση με τις τετραπολικές ροπές των υποστρωμάτων, τα τερματικά τμήματα C και N του ενζύμου πρέπει να κλείσουν, επιτρέποντας την απομόνωση της δραστικής θέσης από τον διαλύτη και μειώνοντας τη διηλεκτρική σταθερά.[17] Αυτή η απομόνωση έχει σημαντικό εντροπικό κόστος και έχει ως αποτέλεσμα το χαμηλό ποσοστό αντικατάστασης.
Δέσιμο RuBP Binding RuBP
Η καρβαμυλίωση της ε-αμινο ομάδας του Lys201 σταθεροποιείται με συντονισμό με το Mg 2+ . Carbamylation of the ε-amino group of Lys201 is stabilized by coordination with the Mg2+.[18] Αυτή η αντίδραση περιλαμβάνει σύνδεση των καρβοξυλικών άκρων του Asp203 και Glu204 στο ιόν Mg 2+ . Το υπόστρωμα RuBP δεσμεύει το Mg 2+ μετατοπίζοντας δύο από τους τρεις υδατοσυνδέτες. This reaction involves binding of the carboxylate termini of Asp203 and Glu204 to the Mg2+ ion. The substrate RuBP binds Mg2+ displacing two of the three aquo ligands.[13][19][20] κκκ
Ενοποίηση Enolisation
Η ενοποίηση του RuBP είναι η μετατροπή του κετοταυτομερούς του RuBP σε μια ενδιόλη (ate). Ενοποίηση ξεκινά με αποπρωτονίωση στο C3. Η ενζυμική βάση σε αυτό το βήμα έχει συζητηθεί, Enolisation of RuBP is the conversion of the keto tautomer of RuBP to an enediol(ate). Enolisation is initiated by deprotonation at C3. The enzyme base in this step has been debated,[19][21] αλλά οι στερικοί περιορισμοί που παρατηρούνται στις κρυσταλλικές δομές έχουν κάνει το Lys201 τον πιο πιθανό υποψήφιο. but the steric constraints observed in crystal structures have made Lys201 the most likely candidate.[13] Συγκεκριμένα, το καρβαμικό οξυγόνο στο Lys201 που δεν συντονίζεται με το ιόν Mg αποπρωτονώνει τον άνθρακα C3 του RuBP για να σχηματίσει ένα 2,3-ενδιοδιόλιο. Specifically, the carbamate oxygen on Lys201 that is not coordinated with the Mg ion deprotonates the C3 carbon of RuBP to form a 2,3-enediolate.[19][20] κκκ
Carboxylation

Η καρβοξυλίωση του 2,3-ενδιοδιόλης έχει ως αποτέλεσμα την ενδιάμεση 3-κετο-2′-καρβοξυαραβινιτόλη-1,5-διφωσφορική και το Lys334 να διευκολύνει την προσθήκη του υποστρώματος CO 2 καθώς αντικαθιστά το τρίτο Mg 2+ συντονισμένο μόριο νερού και προσθέστε απευθείας στην εενδιόλη. Σε αυτή τη διαδικασία δεν σχηματίζεται σύμπλεγμα Michaelis. Carboxylation of the 2,3-enediolate results in the intermediate 3-keto-2′-carboxyarabinitol-1,5-bisphosphate and Lys334 is positioned to facilitate the addition of the CO2 substrate as it replaces the third Mg2+-coordinated water molecule and add directly to the enediol. No Michaelis complex is formed in this process.[13][21] Η ενυδάτωση αυτής της κετόνης οδηγεί σε μια πρόσθετη ομάδα υδροξέων στο C3, σχηματίζοντας ένα ενδιάμεσο προϊόν γεμ-διόλης. Hydration of this ketone results in an additional hydroxy group on C3, forming a gem-diol intermediate.[19][22] Η καρβοξυλίωση και η ενυδάτωση έχουν προταθεί είτε ως ένα μόνο συντονισμένο βήμα Carboxylation and hydration have been proposed as either a single concerted step[19] ή ως δύο διαδοχικά βήματα. or as two sequential steps.[22] Ο συντονισμένος μηχανισμός υποστηρίζεται από την εγγύτητα του μορίου νερού στο C3 του RuBP σε πολλαπλές κρυσταλλικές δομές. Μέσα στη δομή του σπανακιού, άλλα υπολείμματα είναι καλά τοποθετημένα για να βοηθήσουν στο βήμα ενυδάτωσης καθώς βρίσκονται σε απόσταση σύνδεσης υδρογόνου από το μόριο του νερού. Concerted mechanism is supported by the proximity of the water molecule to C3 of RuBP in multiple crystal structures. Within the spinach structure, other residues are well placed to aid in the hydration step as they are within hydrogen bonding distance of the water molecule.[13] κκκ
Διάσπαση δεσμού C-C C-C bond cleavage
Το ενδιάμεσο προϊόν πολύ-διόλης διασπάται στο δεσμό C2-C3 για να σχηματίσει ένα μόριο γλυκερικού-3-φωσφορικού και ένα αρνητικά φορτισμένο καρβοξυλικό. The gem-diol intermediate cleaves at the C2-C3 bond to form one molecule of glycerate-3-phosphate and a negatively charge carboxylate.[13] Η στερεοφωνική πρωτονίωση του C2 αυτού του καρβανίου έχει ως αποτέλεσμα ένα άλλο μόριο γλυκερικού-3-φωσφορικού. Αυτό το βήμα πιστεύεται ότι διευκολύνεται από το Lys175 ή πιθανώς το καρβαμυλιωμένο Lys201. Stereo specific protonation of C2 of this carbanion results in another molecule of glycerate-3-phosphate. This step is thought to be facilitated by Lys175 or potentially the carbamylated Lys201.[13] κκκ
Προϊόντα
Όταν το διοξείδιο του άνθρακα είναι το υπόστρωμα, το προϊόν της αντίδρασης καρβοξυλάσης είναι ένα ασταθές φωσφορυλιωμένο ενδιάμεσο έξι άνθρακα γνωστό ως 3-κετο-2-καρβοξυαραβινιτόλη-1,5-διφωσφορικό, το οποίο διασπάται γρήγορα σε δύο μόρια γλυκερικού-3-φωσφορικού. Το 3-φωσφογλυκερικό άλας μπορεί να χρησιμοποιηθεί για την παραγωγή μεγαλύτερων μορίων όπως γλυκόζη. When carbon dioxide is the substrate, the product of the carboxylase reaction is an unstable six-carbon phosphorylated intermediate known as 3-keto-2-carboxyarabinitol-1,5-bisphosphate, which decays rapidly into two molecules of glycerate-3-phosphate. The 3-phosphoglycerate can be used to produce larger molecules such as glucose. κκκ Το Rubisco παράπλευρες δραστηριότητες μπορεί να οδηγήσει σε άχρηστα ή ανασταλτικά υποπροϊόντα. ένα τέτοιο προϊόν είναι η ξυλουλόζη-1,5-διφωσφορική, η οποία αναστέλλει τη δραστηριότητα Rubisco. Rubisco side activities can lead to useless or inhibitory by-products; one such product is xylulose-1,5-bisphosphate, which inhibits Rubisco activity.[23] κκκ Όταν το μοριακό οξυγόνο είναι το υπόστρωμα, τα προϊόντα της αντίδρασης οξυγονάσης είναι φωσφογλυκολικό και 3-φωσφογλυκερικό. Το φωσφογλυκολικό ανακυκλώνεται μέσω μιας αλληλουχίας αντιδράσεων που ονομάζεται φωτοαναπνοή, η οποία περιλαμβάνει ένζυμα και κυτοχρώματα που βρίσκονται στα μιτοχόνδρια και υπεροξυσώματα (πρόκειται για επισκευή μεταβολιτών). Σε αυτή τη διαδικασία, δύο μόρια φωσφογλυκολικού μετατρέπονται σε ένα μόριο διοξειδίου του άνθρακα και ένα μόριο 3-φωσφογλυκερικού, το οποίο μπορεί να επανεισαχθεί στον κύκλο Calvin. Μερικά από τα φωσφογλυκολικά που εισέρχονται σε αυτό το μονοπάτι μπορούν να συγκρατηθούν από τα φυτά για να παράγουν άλλα μόρια όπως γλυκίνη. Σε επίπεδα περιβάλλοντος διοξειδίου του άνθρακα και οξυγόνου, η αναλογία των αντιδράσεων είναι περίπου 4 προς 1, πράγμα που οδηγεί σε καθαρή σταθεροποίηση διοξειδίου του άνθρακα μόνο 3,5. Έτσι, η αδυναμία του ενζύμου να αποτρέψει την αντίδραση με οξυγόνο μειώνει σημαντικά τη φωτοσυνθετική ικανότητα πολλών φυτών. Ορισμένα φυτά, πολλά φύκια και φωτοσυνθετικά βακτήρια έχουν ξεπεράσει αυτόν τον περιορισμό επινοώντας μέσα για την αύξηση της συγκέντρωσης διοξειδίου του άνθρακα γύρω από το ένζυμο, συμπεριλαμβανομένων των [[C4 carbon fixation | Πρότυπο:C4 στερέωση άνθρακα]], [[μεταβολισμός οξέος του χαλκού] ], και τη χρήση του πυρενοειδούς. When molecular oxygen is the substrate, the products of the oxygenase reaction are phosphoglycolate and 3-phosphoglycerate. Phosphoglycolate is recycled through a sequence of reactions called photorespiration, which involves enzymes and cytochromes located in the mitochondria and peroxisomes (this is a case of metabolite repair). In this process, two molecules of phosphoglycolate are converted to one molecule of carbon dioxide and one molecule of 3-phosphoglycerate, which can reenter the Calvin cycle. Some of the phosphoglycolate entering this pathway can be retained by plants to produce other molecules such as glycine. At ambient levels of carbon dioxide and oxygen, the ratio of the reactions is about 4 to 1, which results in a net carbon dioxide fixation of only 3.5. Thus, the inability of the enzyme to prevent the reaction with oxygen greatly reduces the photosynthetic capacity of many plants. Some plants, many algae, and photosynthetic bacteria have overcome this limitation by devising means to increase the concentration of carbon dioxide around the enzyme, including [[C4 carbon fixation|Πρότυπο:C4 carbon fixation]], crassulacean acid metabolism, and the use of pyrenoid. κκκ
Ποσοστό ενζυματικής δραστηριότητας Rate of enzymatic activity
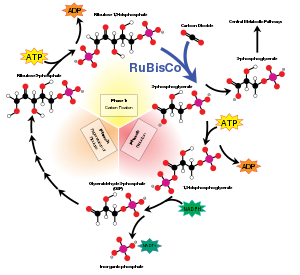
κκκ Ορισμένα ένζυμα μπορούν να πραγματοποιήσουν χιλιάδες χημικές αντιδράσεις κάθε δευτερόλεπτο. Ωστόσο, το RuBisCO είναι αργό, καθορίζοντας μόνο 3-10 μόρια διοξειδίου του άνθρακα κάθε δευτερόλεπτο ανά μόριο ενζύμου. Some enzymes can carry out thousands of chemical reactions each second. However, RuBisCO is slow, fixing only 3-10 carbon dioxide molecules each second per molecule of enzyme.[24] Η αντίδραση που καταλύεται από το RuBisCO είναι, επομένως, ο πρωταρχικός παράγοντας περιορισμού της ταχύτητας του κύκλου Calvin κατά τη διάρκεια της ημέρας. Ωστόσο, υπό τις περισσότερες συνθήκες και όταν το φως δεν περιορίζει διαφορετικά τη φωτοσύνθεση, η ταχύτητα του RuBisCO ανταποκρίνεται θετικά στην αύξηση της συγκέντρωσης διοξειδίου του άνθρακα. The reaction catalyzed by RuBisCO is, thus, the primary rate-limiting factor of the Calvin cycle during the day. Nevertheless, under most conditions, and when light is not otherwise limiting photosynthesis, the speed of RuBisCO responds positively to increasing carbon dioxide concentration. κκκ Το RuBisCO είναι συνήθως ενεργό μόνο κατά τη διάρκεια της ημέρας, καθώς η 1,5-διφωσφορική ριβουλόζη δεν αναγεννάται στο σκοτάδι. Αυτό οφείλεται στη ρύθμιση αρκετών άλλων ενζύμων στον κύκλο του Calvin. Επιπλέον, η δραστηριότητα του RuBisCO συντονίζεται με εκείνη των άλλων ενζύμων του κύκλου Calvin με διάφορους άλλους τρόπους: RuBisCO is usually only active during the day, as ribulose 1,5-bisphosphate is not regenerated in the dark. This is due to the regulation of several other enzymes in the Calvin cycle. In addition, the activity of RuBisCO is coordinated with that of the other enzymes of the Calvin cycle in several other ways: κκκ
Κατά ιόντα By ions
Κατά το φωτισμό των χλωροπλαστών, το pH του στρώματος αυξάνεται από 7.0 σε 8.0 λόγω της κλίσης του πρωτονίου (ιόν υδρογόνου, H +) που δημιουργείται τη μεμβράνη θυλακοειδούς. Η κίνηση των πρωτονίων στα θυλακοειδή είναι οδηγείται από το φως και είναι θεμελιώδης για σύνθεση ATP στους χλωροπλάστες »(Περαιτέρω ανάγνωση: [[Κέντρο φωτοσυνθετικής αντίδρασης] ]; Αντιδράσεις εξαρτώμενες από το φως) . Για την εξισορρόπηση του δυναμικού ιόντων στη μεμβράνη, τα ιόντα μαγνησίου (Mg 2+) μετακινούνται έξω από τα θυλακοειδή ως απάντηση, αυξάνοντας τη συγκέντρωση μαγνησίου στο στρώμα των χλωροπλαστών. Το RuBisCO έχει υψηλό βέλτιστο ρΗ (μπορεί να είναι> 9,0, ανάλογα με τη συγκέντρωση ιόντων μαγνησίου) και, επομένως, "ενεργοποιείται" με την εισαγωγή διοξειδίου του άνθρακα και μαγνησίου στις ενεργές θέσεις όπως περιγράφηκε παραπάνω. Upon illumination of the chloroplasts, the pH of the stroma rises from 7.0 to 8.0 because of the proton (hydrogen ion, H+) gradient created across the thylakoid membrane. The movement of protons into thylakoids is driven by light and is fundamental to ATP synthesis in chloroplasts (Further reading: Photosynthetic reaction centre; Light-dependent reactions). To balance ion potential across the membrane, magnesium ions (Mg2+) move out of the thylakoids in response, increasing the concentration of magnesium in the stroma of the chloroplasts. RuBisCO has a high optimal pH (can be >9.0, depending on the magnesium ion concentration) and, thus, becomes "activated" by the introduction of carbon dioxide and magnesium to the active sites as described above. κκκ
Από την ενεργοποίηση RuBisCO By RuBisCO activase
Σε φυτά και ορισμένα φύκια, ένα άλλο ένζυμο, 'RuBisCO activase' (Rca, Πρότυπο:GO, Πρότυπο:UniProt), απαιτείται για να επιτραπεί ο γρήγορος σχηματισμός του κρίσιμου [ [καρβαμικό]] στην ενεργή τοποθεσία του RuBisCO. In plants and some algae, another enzyme, RuBisCO activase (Rca, Πρότυπο:GO, Πρότυπο:UniProt), is required to allow the rapid formation of the critical carbamate in the active site of RuBisCO.[25][26] Αυτό απαιτείται επειδή 1,5-διφωσφορική ριβουλόζη (RuBP) συνδέεται πιο έντονα με τις ενεργές θέσεις του RuBisCO όταν υπάρχει περίσσεια καρβαμιδικού, εμποδίζοντας τη διαδικασία που προχωράει προς τα εμπρός. Υπό το φως, η ακτιβάση RuBisCO προωθεί την απελευθέρωση του ανασταλτικού (ή - σε ορισμένες απόψεις - αποθήκευσης) RuBP από τις καταλυτικές θέσεις του RuBisCO. Η ακτιβάση απαιτείται επίσης σε ορισμένα φυτά (π.χ. καπνό και πολλά φασόλια) επειδή, στο σκοτάδι, το RuBisCO αναστέλλεται (ή προστατεύεται από την υδρόλυση) από έναν ανταγωνιστικό αναστολέα που συντίθεται από αυτά τα φυτά, ένα αναλογικό υπόστρωμα 2-καρβοξυ-Δ-αραβιτινόλη 1-φωσφορικό (CA1P). This is required because ribulose 1,5-bisphosphate (RuBP) binds more strongly to the active sites of RuBisCO when excess carbamate is present, preventing processes form moving forward. In the light, RuBisCO activase promotes the release of the inhibitory (or — in some views — storage) RuBP from the catalytic sites of RuBisCO. Activase is also required in some plants (e.g., tobacco and many beans) because, in darkness, RuBisCO is inhibited (or protected from hydrolysis) by a competitive inhibitor synthesized by these plants, a substrate analog 2-Carboxy-D-arabitinol 1-phosphate (CA1P).[27] Το CA1P συνδέεται στενά με τη δραστική θέση του καρβαμυλιωμένου RuBisCO και αναστέλλει την καταλυτική δραστηριότητα σε ακόμη μεγαλύτερο βαθμό. Το CA1P έχει επίσης αποδειχθεί ότι διατηρεί το RuBisCO σε διαμόρφωση που προστατεύεται από πρωτεόλυση. CA1P binds tightly to the active site of carbamylated RuBisCO and inhibits catalytic activity to an even greater extent. CA1P has also been shown to keep RuBisCO in a conformation that is protected from proteolysis.[28] Υπό το φως, η ακτιβάση RuBisCO προωθεί επίσης την απελευθέρωση του CA1P από τις καταλυτικές θέσεις. Μετά την απελευθέρωση του CA1P από το RuBisCO, μετατρέπεται γρήγορα σε μη ανασταλτική μορφή από μια ενεργοποιημένη από το φως CA1P-φωσφατάση. Ακόμη και χωρίς αυτούς τους ισχυρούς αναστολείς, μία φορά κάθε αρκετές εκατοντάδες αντιδράσεις, οι κανονικές αντιδράσεις με διοξείδιο του άνθρακα ή οξυγόνο δεν ολοκληρώνονται. άλλα ανασταλτικά ανάλογα υποστρώματος εξακολουθούν να σχηματίζονται στην ενεργή θέση. Για άλλη μια φορά, η ακτιβάση RuBisCO μπορεί να προωθήσει την απελευθέρωση αυτών των αναλόγων από τις καταλυτικές θέσεις και να διατηρήσει το ένζυμο σε καταλυτικά ενεργή μορφή. Ωστόσο, σε υψηλές θερμοκρασίες, η RuBisCO ενεργοποιείται και δεν μπορεί πλέον να ενεργοποιήσει το RuBisCO. Αυτό συμβάλλει στη μειωμένη ικανότητα καρβοξυλίωσης που παρατηρείται κατά τη θερμική καταπόνηση. In the light, RuBisCO activase also promotes the release of CA1P from the catalytic sites. After the CA1P is released from RuBisCO, it is rapidly converted to a non-inhibitory form by a light-activated CA1P-phosphatase. Even without these strong inhibitors, once every several hundred reactions, the normal reactions with carbon dioxide or oxygen are not completed; other inhibitory substrate analogs are still formed in the active site. Once again, RuBisCO activase can promote the release of these analogs from the catalytic sites and maintain the enzyme in a catalytically active form. However, at high temperatures, RuBisCO activase aggregates and can no longer activate RuBisCO. This contributes to the decreased carboxylating capacity observed during heat stress.[29][30] κκκ
Με ATP/ADP και κατάσταση στρωματικής αναγωγής/οξείδωσης μέσω της ακτινάσης By ATP/ADP and stromal reduction/oxidation state through the activase
Η απομάκρυνση του ανασταλτικού RuBP, CA1P και των άλλων ανασταλτικών αναλόγων υποστρώματος με ακτιβάση απαιτεί την κατανάλωση ATP. Αυτή η αντίδραση αναστέλλεται από την παρουσία ADP, και, συνεπώς, η δραστηριότητα της ακτινάσης εξαρτάται από την αναλογία αυτών των ενώσεων στο στρώμα του χλωροπλάστη. Επιπλέον, στα περισσότερα φυτά, η ευαισθησία της ακτιβάσης προς την αναλογία ATP/ADP τροποποιείται από την κατάσταση της στρωματικής αναγωγής/οξείδωσης (οξειδοαναγωγή) μέσω μιας άλλης μικρής ρυθμιστικής πρωτεΐνης, θειορεδοξίνη. Με αυτόν τον τρόπο, η δραστηριότητα της ακτινάσης και η κατάσταση ενεργοποίησης του RuBisCO μπορούν να ρυθμιστούν ως απόκριση της έντασης του φωτός και, επομένως, του ρυθμού σχηματισμού του υποστρώματος 1,5-διφωσφορικής ριβουλόζης. The removal of the inhibitory RuBP, CA1P, and the other inhibitory substrate analogs by activase requires the consumption of ATP. This reaction is inhibited by the presence of ADP, and, thus, activase activity depends on the ratio of these compounds in the chloroplast stroma. Furthermore, in most plants, the sensitivity of activase to the ratio of ATP/ADP is modified by the stromal reduction/oxidation (redox) state through another small regulatory protein, thioredoxin. In this manner, the activity of activase and the activation state of RuBisCO can be modulated in response to light intensity and, thus, the rate of formation of the ribulose 1,5-bisphosphate substrate.[31] κκκ
Με φωσφορικά By phosphate
Στα κυανοβακτήρια, το ανόργανο φωσφορικό (P i ) συμμετέχει επίσης στη συντονισμένη ρύθμιση της φωτοσύνθεσης: Το P i συνδέεται με την ενεργό τοποθεσία RuBisCO και σε άλλη τοποθεσία στη μεγάλη αλυσίδα όπου μπορεί να επηρεάσει τις μεταβάσεις μεταξύ ενεργοποιημένων και λιγότερο ενεργών διαμορφώσεων του ενζύμου. Με αυτόν τον τρόπο, η ενεργοποίηση του βακτηριακού RuBisCO μπορεί να είναι ιδιαίτερα ευαίσθητη στα επίπεδα P i , γεγονός που θα μπορούσε να τον αναγκάσει να ενεργήσει με παρόμοιο τρόπο με τον τρόπο λειτουργίας της RuBisCO activase σε υψηλότερα φυτά. In cyanobacteria, inorganic phosphate (Pi) also participates in the co-ordinated regulation of photosynthesis: Pi binds to the RuBisCO active site and to another site on the large chain where it can influence transitions between activated and less active conformations of the enzyme. In this way, activation of bacterial RuBisCO might be particularly sensitive to Pi levels, which might cause it to act in a similar way to how RuBisCO activase functions in higher plants.[32] κκκ
Με διοξείδιο του άνθρακα By carbon dioxide
Δεδομένου ότι το διοξείδιο του άνθρακα και το οξυγόνο ανταγωνίζονται στο ενεργό σημείο του RuBisCO, η στερέωση άνθρακα από το RuBisCO μπορεί να ενισχυθεί αυξάνοντας το επίπεδο διοξειδίου του άνθρακα στο διαμέρισμα που περιέχει RuBisCO (στρώμα χλωροπλάστης). Αρκετές φορές κατά τη διάρκεια της εξέλιξης των φυτών, έχουν αναπτυχθεί μηχανισμοί για την αύξηση του επιπέδου διοξειδίου του άνθρακα στο στρώμα (βλέπε [[C4 στερέωση άνθρακα | Πρότυπο:C4 στερέωση άνθρακα]]). Η χρήση οξυγόνου ως υπόστρωμα φαίνεται να είναι μια περίεργη διαδικασία, καθώς φαίνεται να πετάει τη δεσμευμένη ενέργεια. Ωστόσο, μπορεί να είναι ένας μηχανισμός για την πρόληψη της υπερφόρτωσης υδατανθράκων σε περιόδους υψηλής ροής φωτός. Αυτή η αδυναμία στο ένζυμο είναι η αιτία της φωτοαναπνοή, έτσι ώστε τα υγιή φύλλα σε έντονο φως ενδέχεται να έχουν μηδενική καθαρή στερέωση άνθρακα όταν ο λόγος O 2 προς CO2 είναι διαθέσιμος στο RuBisCO μετατοπίζεται πολύ προς το οξυγόνο. Αυτό το φαινόμενο εξαρτάται κυρίως από τη θερμοκρασία: Οι υψηλές θερμοκρασίες μπορούν να μειώσουν τη συγκέντρωση του CO2 που διαλύεται στην υγρασία των ιστών των φύλλων. Αυτό το φαινόμενο σχετίζεται επίσης με το καταπόνηση νερού: Δεδομένου ότι τα φύλλα των φυτών ψύχονται με εξάτμιση, το περιορισμένο νερό προκαλεί υψηλές θερμοκρασίες στα φύλλα. [[Φυτά C4 | Πρότυπο:C4 φυτά]] χρησιμοποιήστε αρχικά το ένζυμο καρβοξυλάση PEP, το οποίο έχει μεγαλύτερη συγγένεια με το CO2. Η διαδικασία δημιουργεί πρώτα μια ενδιάμεση ένωση 4 άνθρακα, η οποία μεταφέρεται σε μια περιοχή με [[φυτά C3 | Πρότυπο:C3 φωτοσύνθεση]] και στη συνέχεια απο-καρβοξυλιώνεται, απελευθερώνοντας CO2 για να αυξήσει τη συγκέντρωση του CO2, εξ ου και το όνομα Πρότυπο:C4 φυτά. Since carbon dioxide and oxygen compete at the active site of RuBisCO, carbon fixation by RuBisCO can be enhanced by increasing the carbon dioxide level in the compartment containing RuBisCO (chloroplast stroma). Several times during the evolution of plants, mechanisms have evolved for increasing the level of carbon dioxide in the stroma (see [[C4 carbon fixation|Πρότυπο:C4 carbon fixation]]). The use of oxygen as a substrate appears to be a puzzling process, since it seems to throw away captured energy. However, it may be a mechanism for preventing carbohydrate overload during periods of high light flux. This weakness in the enzyme is the cause of photorespiration, such that healthy leaves in bright light may have zero net carbon fixation when the ratio of O2 to CO2 available to RuBisCO shifts too far towards oxygen. This phenomenon is primarily temperature-dependent: High temperatures can decrease the concentration of CO2 dissolved in the moisture of leaf tissues. This phenomenon is also related to water stress: Since plant leaves are evaporatively cooled, limited water causes high leaf temperatures. [[C4 plants|Πρότυπο:C4 plants]] use the enzyme PEP carboxylase initially, which has a higher affinity for CO2. The process first makes a 4-carbon intermediate compound, which is shuttled into a site of [[C3 plants|Πρότυπο:C3 photosynthesis]] then de-carboxylated, releasing CO2 to boost the concentration of CO2, hence the name Πρότυπο:C4 plants. κκκ Τα φυτά μεταβολισμός οξέος Crassulacean (CAM) διατηρούν το στόμα τους κλειστό κατά τη διάρκεια της ημέρας, το οποίο εξοικονομεί νερό, αλλά εμποδίζει τις αντιδράσεις ανεξάρτητες από το φως (γνωστός και ως κύκλος Calvin), καθώς αυτές Οι αντιδράσεις απαιτούν CO2 να περάσουν από την ανταλλαγή αερίου μέσω αυτών των ανοιγμάτων. Η εξάτμιση μέσω της άνω πλευράς ενός φύλλου εμποδίζεται από ένα στρώμα κερί. Crassulacean acid metabolism (CAM) plants keep their stomata closed during the day, which conserves water but prevents the light-independent reactions (a.k.a. the Calvin Cycle) from taking place, since these reactions require CO2 to pass by gas exchange through these openings. Evaporation through the upper side of a leaf is prevented by a layer of wax. κκκ
Γενετική μηχανική
κκκ Δεδομένου ότι το RuBisCO είναι συχνά περιοριστικό για τη φωτοσύνθεση στα φυτά, μπορεί να είναι δυνατή η βελτίωση της φωτοσυνθετικής απόδοσης τροποποιώντας τα γονίδια RuBisCO στα φυτά για να αυξηθεί η καταλυτική δραστηριότητα και/ή να μειωθούν τα ποσοστά οξυγόνωσης. Since RuBisCO is often rate-limiting for photosynthesis in plants, it may be possible to improve photosynthetic efficiency by modifying RuBisCO genes in plants to increase catalytic activity and/or decrease oxygenation rates.[33][34][35][36] Αυτό θα μπορούσε να βελτιώσει την βιοανάκριση του CO2 και να είναι ταυτόχρονα μια σημαντική κλιματική αλλαγή στρατηγική και μια στρατηγική για την αύξηση των αποδόσεων των καλλιεργειών. This could improve biosequestration of CO2 and be both an important climate change strategy and a strategy to increase crop yields.[37] Οι προσεγγίσεις που διερευνώνται περιλαμβάνουν τη μεταφορά γονιδίων RuBisCO από έναν οργανισμό σε άλλο οργανισμό, την κατασκευή της Rubisco activase από θερμόφιλα κυανοβακτήρια σε φυτά ευαίσθητα στη θερμοκρασία, αυξάνοντας το επίπεδο έκφρασης των υπομονάδων RuBisCO, εκφράζοντας τις μικρές αλυσίδες RuBisCO από το χλωροπλαστικό DNA και μεταβάλλοντας τα γονίδια RuBisCO για να αυξήσουμε την εξειδίκευση για το διοξείδιο του άνθρακα ή με άλλο τρόπο να αυξήσουμε τον ρυθμό στερέωσης του άνθρακα. Approaches under investigation include transferring RuBisCO genes from one organism into another organism, engineering Rubisco activase from thermophilic cyanobacteria into temperature sensitive plants, increasing the level of expression of RuBisCO subunits, expressing RuBisCO small chains from the chloroplast DNA, and altering RuBisCO genes to increase specificity for carbon dioxide or otherwise increase the rate of carbon fixation.[38][39] κκκ
Mutagenesis in plants
Γενικά, μεταλλαξογένεση που κατευθύνεται στον ιστότοπο του RuBisCO ήταν ως επί το πλείστον ανεπιτυχές, In general, site-directed mutagenesis of RuBisCO has been mostly unsuccessful,[37] αν και έχουν επιτευχθεί μεταλλαγμένες μορφές της πρωτεΐνης σε φυτά καπνού με είδη υπομονάδας C 4 , though mutated forms of the protein have been achieved in tobacco plants with subunit C4 species,[40] και ένα RuBisCO με περισσότερα C 4 κινητικά χαρακτηριστικά έχουν επιτευχθεί στο ρύζι μέσω πυρηνικού μετασχηματισμού. and a RuBisCO with more C4-like kinetic characteristics have been attained in rice via nuclear transformation.[41] Ισχυρή και αξιόπιστη μηχανική για απόδοση RuBisCO και άλλων ενζύμων στον κύκλο C 3 αποδείχθηκε ότι είναι δυνατή, Robust and reliable engineering for yield of RuBisCO and other enzymes in the C3 cycle was shown to be possible,[42] και επιτεύχθηκε για πρώτη φορά το 2019 μέσω μιας προσέγγισης συνθετικής βιολογίας. and it was first achieved in 2019 through a synthetic biology approach.[43] κκκ Ένας τρόπος είναι να εισαχθούν παραλλαγές RuBisCO με φυσιολογικά υψηλές τιμές εξειδίκευσης, όπως αυτές από το κόκκινο άλγος 'Galdieria partita' 'στα φυτά. Αυτό μπορεί να βελτιώσει τη φωτοσυνθετική απόδοση των φυτών, αν και οι πιθανές αρνητικές επιπτώσεις δεν έχουν ακόμη μελετηθεί. One avenue is to introduce RuBisCO variants with naturally high specificity values such as the ones from the red alga Galdieria partita into plants. This may improve the photosynthetic efficiency of crop plants, although possible negative impacts have yet to be studied.[44] Οι εξελίξεις σε αυτόν τον τομέα περιλαμβάνουν την αντικατάσταση του ενζύμου καπνού με εκείνο του πορφυρού φωτοσυνθετικού βακτηρίου [[[Rhodospirillum rubrum]] . Advances in this area include the replacement of the tobacco enzyme with that of the purple photosynthetic bacterium Rhodospirillum rubrum.[45] Το 2014, δημιουργήθηκαν δύο γραμμές μεταπλαστωτικού καπνού με λειτουργικό RuBisCO από το cyanobacterium Synechococcus elongatus PCC7942 (Se7942) αντικαθιστώντας το RuBisCO με τα μεγάλα και μικρά γονίδια υπομονάδας του ενζύμου Se7942, σε συνδυασμός είτε με το αντίστοιχο chaperone συγκρότησης Se7942, RbcX, είτε με εσωτερική καρβοξυσωματική πρωτεΐνη, CcmM35. Και οι δύο μεταλλάξεις είχαν αυξημένα ποσοστά σταθεροποίησης CO2 όταν μετρήθηκαν ως μόρια άνθρακα ανά RuBisCO. Ωστόσο, τα μεταλλαγμένα φυτά αναπτύχθηκαν πιο αργά από ό, τι άγριου τύπου. In 2014, two transplastomic tobacco lines with functional RuBisCO from the cyanobacterium Synechococcus elongatus PCC7942 (Se7942) were created by replacing the RuBisCO with the large and small subunit genes of the Se7942 enzyme, in combination with either the corresponding Se7942 assembly chaperone, RbcX, or an internal carboxysomal protein, CcmM35. Both mutants had increased CO2 fixation rates when measured as carbon molecules per RuBisCO. However, the mutant plants grew more slowly than wild-type.[46] κκκ Μια πρόσφατη θεωρία διερευνά την αντιστάθμιση μεταξύ της σχετικής ιδιαιτερότητας (δηλαδή, την ικανότητα να ευνοείται η CO2 σταθεροποίηση έναντι της O 2 ενσωμάτωσης, η οποία οδηγεί στην ενεργειακά σπατάλη της διαδικασίας φωτοαναπνοής ) και ο ρυθμός με τον οποίο σχηματίζεται το προϊόν. Οι συγγραφείς καταλήγουν στο συμπέρασμα ότι το RuBisCO μπορεί πράγματι να έχει εξελιχθεί για να φτάσει σε ένα σημείο «σχεδόν τελειότητας» σε πολλά φυτά (με ευρέως ποικίλες διαθεσιμότητες υποστρώματος και περιβαλλοντικές συνθήκες), επιτυγχάνοντας συμβιβασμό μεταξύ της ειδικότητας και του ρυθμού αντίδρασης. A recent theory explores the trade-off between the relative specificity (i.e., ability to favour CO2 fixation over O2 incorporation, which leads to the energy-wasteful process of photorespiration) and the rate at which product is formed. The authors conclude that RuBisCO may actually have evolved to reach a point of 'near-perfection' in many plants (with widely varying substrate availabilities and environmental conditions), reaching a compromise between specificity and reaction rate.[47] Έχει επίσης προταθεί ότι η αντίδραση οξυγονάσης του RuBisCO εμποδίζει την εξάντληση του CO 2 κοντά στις ενεργές θέσεις του και παρέχει τη διατήρηση της οξειδοαναγωγικής κατάστασης των χλωροπλαστών. It has been also suggested that the oxygenase reaction of RuBisCO prevents CO2 depletion near its active sites and provides the maintenance of the chloroplast redox state.[48] κκκ Δεδομένου ότι η φωτοσύνθεση είναι ο πιο αποτελεσματικός φυσικός ρυθμιστής του διοξειδίου του άνθρακα στην ατμόσφαιρα της Γης, Since photosynthesis is the single most effective natural regulator of carbon dioxide in the Earth's atmosphere,[49] ένα βιοχημικό μοντέλο αντίδρασης RuBisCO χρησιμοποιείται ως βασική μονάδα μοντέλων κλιματικής αλλαγής. Έτσι, ένα σωστό μοντέλο αυτής της αντίδρασης είναι απαραίτητο για τη βασική κατανόηση των σχέσεων και των αλληλεπιδράσεων των περιβαλλοντικών μοντέλων. a biochemical model of RuBisCO reaction is used as the core module of climate change models. Thus, a correct model of this reaction is essential to the basic understanding of the relations and interactions of environmental models. κκκ
Έκφραση σε βακτηριακούς ξενιστές
Υπάρχουν επί του παρόντος πολύ λίγες αποτελεσματικές μέθοδοι για την έκφραση του λειτουργικού φυτού Rubisco σε βακτηριακούς ξενιστές για μελέτες γενετικής χειραγώγησης. Αυτό οφείλεται σε μεγάλο βαθμό στην απαίτηση του Rubisco για πολύπλοκα κυτταρικά μηχανήματα για τη βιογένεση και τη μεταβολική του συντήρηση, συμπεριλαμβανομένων των πυρηνικών κωδικοποιημένων υπομονάδων RbcS, οι οποίες εισάγονται συνήθως σε χλωροπλάστες ως ξεδιπλωμένες πρωτεΐνες. There currently are very few effective methods for expressing functional plant Rubisco in bacterial hosts for genetic manipulation studies. This is largely due to Rubisco's requirement of complex cellular machinery for its biogenesis and metabolic maintenance including the nuclear-encoded RbcS subunits, which are typically imported into chloroplasts as unfolded proteins.[50][51] Επιπλέον, η επαρκής έκφραση και αλληλεπίδραση με τη Rubisco activase αποτελούν επίσης μεγάλες προκλήσεις. Furthermore, sufficient expression and interaction with Rubisco activase are major challenges as well.[52] Μια επιτυχημένη μέθοδος έκφρασης του Rubisco στο E. coli περιλαμβάνει τη συν-έκφραση πολλαπλών χλωροπλαστικών καπερόνων, αν και αυτό έχει αποδειχθεί μόνο για το Arabidopsis thaliana Rubisco. One successful method for expression of Rubisco in E. coli involves the co-expression of multiple chloroplast chaperones, though this has only been shown for Arabidopsis thaliana Rubisco.[53] κκκ
Εξάντληση σε πρωτεομικές μελέτες Depletion in proteomic studies
Λόγω της μεγάλης αφθονίας του στα φυτά (γενικά το 40% της συνολικής περιεκτικότητας σε πρωτεΐνες), το RuBisCO συχνά εμποδίζει την ανάλυση σημαντικών πρωτεϊνών σηματοδότησης όπως παράγοντας μεταγραφής s, κινάσης και ρυθμιστικών πρωτεϊνών που βρίσκονται σε χαμηλότερη αφθονία (10-100 μόρια ανά κύτταρο) εντός των φυτών. Due to its high abundance in plants (generally 40% of the total protein content), RuBisCO often impedes analysis of important signaling proteins such as transcription factors, kinases, and regulatory proteins found in lower abundance (10-100 molecules per cell) within plants.[54] Για παράδειγμα, η χρήση φασματομετρία μάζας σε μείγματα φυτικών πρωτεϊνών θα είχε ως αποτέλεσμα πολλαπλές έντονες κορυφές υπομονάδας RuBisCO που παρεμβαίνουν και αποκρύπτουν εκείνες άλλων πρωτεϊνών. For example, using mass spectrometry on plant protein mixtures would result in multiple intense RuBisCO subunit peaks that interfere and hide those of other proteins. κκκ Πρόσφατα, μία αποτελεσματική μέθοδος για την καθίζηση του RuBisCO περιλαμβάνει τη χρήση διαλύματος [θειικής πρωτεμίνης]. Recently, one efficient method for precipitating out RuBisCO involves the usage of protamine sulfate solution.[55] Άλλες υπάρχουσες μέθοδοι εξάντλησης του RuBisCO και μελέτης πρωτεϊνών χαμηλότερης αφθονίας περιλαμβάνουν τεχνικές κλασματοποίησης με ασβέστιο και φυτικό άλας, Other existing methods for depleting RuBisCO and studying lower abundance proteins include fractionation techniques with calcium and phytate,[56] ηλεκτροφόρηση γέλης με πολυαιθυλενογλυκόλη, gel electrophoresis with polyethylene glycol,[57][58] affinity chromatography,[59][60] και συσσωμάτωση χρησιμοποιώντας DTT, and aggregation using DTT,[61] αν και αυτές οι μέθοδοι είναι πιο χρονοβόρες και λιγότερο αποτελεσματικές σε σύγκριση με την καθίζηση θειικής πρωτεμίνης. though these methods are more time-consuming and less efficient when compared to protamine sulfate precipitation.[54] κκκ
Φυλογενετικές μελέτες
Το γονίδιο χλωροπλάστη "rbcL, το οποίο κωδικοποιεί τη μεγάλη υπομονάδα του RuBisCO έχει χρησιμοποιηθεί ευρέως ως κατάλληλο [[τόπος (γενετική] | τόπος]] για ανάλυση φυλογενετικής στην ταξινόμηση φυτών Ε The chloroplast gene rbcL, which codes for the large subunit of RuBisCO has been widely used as an appropriate locus for analysis of phylogenetics in plant taxonomy.[62] κκκ
Εξέλιξη του RuBisCO
Με την εξέλιξη του μονοπατιού στερέωσης C 4 σε ορισμένα είδη φυτών, το C 3 RuBisCO εξελίχθηκε για να έχει ταχύτερο κύκλο εργασιών CO2 με αντάλλαγμα χαμηλότερη εξειδίκευση ως αποτέλεσμα του μεγαλύτερου εντοπισμού CO2 από το κύτταρο μεσοφύλλης s στα κύτταρα θήκης δέσμης. With the evolution of the C4-fixation pathway in certain species of plants, C3 RuBisCO evolved to have faster turnover of CO2 in exchange for lower specificity as a result of the greater localization of CO2 from the mesophyll cells into the bundle sheath cells.[63] Αυτό επιτεύχθηκε μέσω της ενίσχυσης της διαμορφωτικής ευελιξίας της μετάβασης «ανοικτού-κλειστού» στον Κύκλο Calvin. Εργαστηριακές φυλογενετικές μελέτες έχουν δείξει ότι αυτή η εξέλιξη περιορίστηκε από την αντιστάθμιση μεταξύ σταθερότητας και δραστηριότητας που προκλήθηκε από τη σειρά απαραίτητων μετάλλαξης για το C 4 RuBisCO. This was achieved through enhancement of conformational flexibility of the “open-closed” transition in the Calvin Cycle. Laboratory-based phylogenetic studies have shown that this evolution was constrained by the trade-off between stability and activity brought about by the series of necessary mutations for C4 RuBisCO.[64] Επιπλέον, για να διατηρηθούν οι αποσταθεροποιητικές μεταλλάξεις, προηγήθηκε η εξέλιξη στο C 4 RuBisCO από μια περίοδο κατά την οποία οι μεταλλάξεις έδωσαν στο ένζυμο αυξημένη σταθερότητα, δημιουργώντας ένα ρυθμιστικό για τη διατήρηση και διατήρηση των μεταλλάξεων που απαιτούνται για C < sub> 4 RuBisCO. Για να βοηθήσει με αυτή τη ρυθμιστική διαδικασία, το νεοεξελιγμένο ένζυμο βρέθηκε να έχει αναπτύξει περαιτέρω μια σειρά σταθεροποιητικών μεταλλάξεων. Ενώ το RuBisCO συσσωρεύει πάντα νέες μεταλλάξεις, οι περισσότερες από αυτές τις μεταλλάξεις που έχουν επιβιώσει δεν είχαν σημαντικές επιπτώσεις στη σταθερότητα της πρωτεΐνης. Οι αποσταθεροποιητικές μεταλλάξεις C 4 στο RuBisCO υποστηρίχθηκαν από περιβαλλοντικές πιέσεις όπως χαμηλές συγκεντρώσεις CO2, απαιτώντας θυσία σταθερότητας για νέες προσαρμοστικές λειτουργίες. Moreover, in order to sustain the destabilizing mutations, the evolution to C4 RuBisCO was preceded by a period in which mutations granted the enzyme increased stability, establishing a buffer to sustain and maintain the mutations required for C4 RuBisCO. To assist with this buffering process, the newly-evolved enzyme was found to have further developed a series of stabilizing mutations. While RuBisCO has always been accumulating new mutations, most of these mutations that have survived have not had significant effects on protein stability. The destabilizing C4 mutations on RuBisCO has been sustained by environmental pressures such as low CO2 concentrations, requiring a sacrifice of stability for new adaptive functions.[64] κκκ
Ιστορικό του όρου
Ο όρος "RuBisCO" επινοήθηκε χιουμοριστικά το 1979, από τον David Eisenberg σε ένα σεμινάριο που τιμούσε τη συνταξιοδότηση του πρώιμου, εξέχοντος ερευνητή του RuBisCO, Sam Wildman, και υπαινίχθηκε επίσης την εμπορική ονομασία σνακ »[[ [Nabisco]] "σε σχέση με τις προσπάθειες του Wildman να δημιουργήσει ένα βρώσιμο συμπλήρωμα πρωτεΐνης από φύλλα καπνού. The term "RuBisCO" was coined humorously in 1979, by David Eisenberg at a seminar honouring the retirement of the early, prominent RuBisCO researcher, Sam Wildman, and also alluded to the snack food trade name "Nabisco" in reference to Wildman's attempts to create an edible protein supplement from tobacco leaves.[65][66] κκκ Η κεφαλαιοποίηση του ονόματος έχει συζητηθεί εδώ και πολύ καιρό. Μπορεί να κεφαλαιοποιηθεί για κάθε γράμμα με το πλήρες όνομα ( 'R' ib 'u' lose-1,5 'bis' phosphate 'c' arboxylase/' o 'ξυγενάση), αλλά έχει επίσης υποστηριχθεί ότι πρέπει να είναι όλα με πεζά γράμματα (rubisco), παρόμοια με άλλους όρους όπως το scuba ή το laser. The capitalization of the name has been long debated. It can be capitalized for each letter of the full name (Ribulose-1,5 bisphosphate carboxylase/oxygenase), but it has also been argued that is should all be in lower case (rubisco), similar to other terms like scuba or laser.[67] κκκ
Παραπομπές
- ↑ «Discovery of the canonical Calvin-Benson cycle». Photosynth Res 53 (2): 835–18. 2019. doi:. PMID 30374727.
- ↑ Cooper, Geoffrey M. (2000). «10.The Chloroplast Genome». The Cell: A Molecular Approach
 (2nd έκδοση). Washington, D.C: ASM Press. ISBN 978-0-87893-106-4.
(2nd έκδοση). Washington, D.C: ASM Press. ISBN 978-0-87893-106-4. , one of the subunits of ribulose bisphosphate carboxylase (rubisco) is encoded by chloroplast DNA. Rubisco is the critical enzyme that catalyzes the addition of CO2 to ribulose-1,5-bisphosphate during the Calvin cycle. It is also thought to be the single most abundant protein on Earth, so it is noteworthy that one of its subunits is encoded by the chloroplast genome.
- ↑ «Enhanced translation of a chloroplast-expressed RbcS gene restores small subunit levels and photosynthesis in nuclear RbcS antisense plants». Proceedings of the National Academy of Sciences of the United States of America 101 (16): 6315–20. April 2004. doi:. PMID 15067115. Bibcode: 2004PNAS..101.6315D. «(Rubisco) is the most prevalent enzyme on this planet, accounting for 30–50% of total soluble protein in the chloroplast;».
- ↑ 4,0 4,1 «Rubiscolytics: fate of Rubisco after its enzymatic function in a cell is terminated». Journal of Experimental Botany 59 (7): 1615–24. 2008. doi:. PMID 17975207. http://doc.rero.ch/record/290465/files/erm242.pdf.
- ↑ (Entrez GeneID: )
- ↑ «Enhanced translation of a chloroplast-expressed RbcS gene restores small subunit levels and photosynthesis in nuclear RbcS antisense plants». Proceedings of the National Academy of Sciences of the United States of America 101 (16): 6315–20. April 2004. doi:. PMID 15067115. Bibcode: 2004PNAS..101.6315D.
- ↑ Arabidopsis thaliana has four RuBisCO small chain genes.
«Determination of the relative expression levels of rubisco small subunit genes in Arabidopsis by rapid amplification of cDNA ends». Analytical Biochemistry 291 (2): 237–44. April 2001. doi:. PMID 11401297. - ↑ Stryer, Lubert· Berg, Jeremy Mark· Tymoczko, John L. (2002). «20. The Calvin Cycle and the Pentose Phosphate Pathway». Biochemistry
 (5th έκδοση). San Francisco: W.H. Freeman. ISBN 978-0-7167-3051-4.
(5th έκδοση). San Francisco: W.H. Freeman. ISBN 978-0-7167-3051-4. Figure 20.3. Structure of Rubisco. (Color-coded ribbon diagram)
- ↑ The structure of RuBisCO from the photosynthetic bacterium Rhodospirillum rubrum has been determined by X-ray crystallography, see: Πρότυπο:Protein Data Bank. A comparison of the structures of eukaryotic and bacterial RuBisCO is shown in the Protein Data Bank feature article on Rubisco.
- ↑ Molecular Cell Biology, 4th edition, by Harvey Lodish, Arnold Berk, S. Lawrence Zipursky, Paul Matsudaira, David Baltimore and James E. Darnell. Published by W. H. Freeman & Co. (2000) New York. Online textbook. Figure 16-48 shows a structural model of the active site, including the involvement of magnesium. The Protein Data Bank feature article on RuBisCO also includes a model of magnesium at the active site Αρχειοθετήθηκε 2006-01-09 στο Wayback Machine..
- ↑ 11,0 11,1 11,2 11,3 «Structural mechanism of RuBisCO activation by carbamylation of the active site lysine». Proceedings of the National Academy of Sciences of the United States of America 109 (46): 18785–90. November 2012. doi:. PMID 23112176. Bibcode: 2012PNAS..10918785S.
- ↑ The Lodish textbook describes the localization of RuBisCO to the stromal space of chloroplasts. Figure 17-7 illustrates how RuBisCO small subunits move into the chloroplast stroma and assemble with the large subunits.
- ↑ 13,0 13,1 13,2 13,3 13,4 13,5 13,6 «Catalysis and regulation in Rubisco». Journal of Experimental Botany 59 (7): 1555–68. May 2008. doi:. PMID 18417482.
- ↑ «A short history of RubisCO: the rise and fall (?) of Nature's predominant CO2 fixing enzyme». Current Opinion in Biotechnology 49: 100–107. February 2018. doi:. PMID 28843191.
- ↑ «Crystal structure of activated ribulose-1,5-bisphosphate carboxylase complexed with its substrate, ribulose-1,5-bisphosphate». The Journal of Biological Chemistry 266 (19): 12604–11. July 1991. doi:. PMID 1905726.
- ↑ The chemical reactions catalyzed by RuBisCO are described in the online Biochemistry textbook by Stryer et al.
- ↑ «Plant-like substitutions in the large-subunit carboxy terminus of Chlamydomonas Rubisco increase CO2/O2 specificity». BMC Plant Biology 8: 85. July 2008. doi:. PMID 18664299.
- ↑ «Carbamate formation on the epsilon-amino group of a lysyl residue as the basis for the activation of ribulosebisphosphate carboxylase by CO2 and Mg2+». Biochemistry 19 (23): 5321–8. November 1980. doi:. PMID 6778504.
- ↑ 19,0 19,1 19,2 19,3 19,4 «Mechanism of Rubisco: The Carbamate as General Base». Chemical Reviews 98 (2): 549–562. April 1998. doi:. PMID 11848907.
- ↑ 20,0 20,1 «Crystal structure of the active site of ribulose-bisphosphate carboxylase». Nature 337 (6204): 229–234. 1989. doi:. Bibcode: 1989Natur.337..229A.
- ↑ 21,0 21,1 «Structure, function, regulation, and assembly of D-ribulose-1,5-bisphosphate carboxylase/oxygenase». Annual Review of Biochemistry 63: 197–234. 1994. doi:. PMID 7979237.
- ↑ 22,0 22,1 «The structure of the complex between rubisco and its natural substrate ribulose 1,5-bisphosphate». Journal of Molecular Biology 265 (4): 432–44. January 1997. doi:. PMID 9034362.
- ↑ «Catalytic by-product formation and ligand binding by ribulose bisphosphate carboxylases from different phylogenies». The Biochemical Journal 399 (3): 525–34. November 2006. doi:. PMID 16822231.
- ↑ «Biochemistry: Tackling unintelligent design». Nature 463 (7278): 164–5. January 2010. doi:. PMID 20075906. Bibcode: 2010Natur.463..164E.
- ↑ «Rubisco activase - Rubisco's catalytic chaperone». Photosynthesis Research 75 (1): 11–27. 2003. doi:. PMID 16245090.
- ↑ «Characteristics of photosynthesis in rice plants transformed with an antisense Rubisco activase gene». Journal of Zhejiang University Science 5 (8): 897–9. August 2004. doi:. PMID 15236471. https://semanticscholar.org/paper/9f8af66ec94a48a27feab9f05b5cb8b59fbe7634.
- ↑ «Incorporation of carbon from photosynthetic products into 2-carboxyarabinitol-1-phosphate and 2-carboxyarabinitol». The Biochemical Journal 304 (3): 781–6. December 1994. doi:. PMID 7818481.
- ↑ «2'-carboxy-D-arabitinol 1-phosphate protects ribulose 1, 5-bisphosphate carboxylase/oxygenase against proteolytic breakdown». European Journal of Biochemistry 266 (3): 840–7. December 1999. doi:. PMID 10583377. https://repository.rothamsted.ac.uk/download/2d5eca8f4b497d9d14914da64f7f56163817c6e91d61ed28df023b9ff7a39a4a/521895/Khan-1999--carboxy-d-arabitinol--phosphate-pr.pdf.
- ↑ «Exceptional sensitivity of Rubisco activase to thermal denaturation in vitro and in vivo». Plant Physiology 127 (3): 1053–64. November 2001. doi:. PMID 11706186.
- ↑ «Rubisco activase constrains the photosynthetic potential of leaves at high temperature and CO2». Proceedings of the National Academy of Sciences of the United States of America 97 (24): 13430–5. November 2000. doi:. PMID 11069297. Bibcode: 2000PNAS...9713430C.
- ↑ «Light modulation of Rubisco in Arabidopsis requires a capacity for redox regulation of the larger Rubisco activase isoform». Proceedings of the National Academy of Sciences of the United States of America 99 (5): 3330–4. March 2002. doi:. PMID 11854454. Bibcode: 2002PNAS...99.3330Z.
- ↑ «Activation of cyanobacterial RuBP-carboxylase/oxygenase is facilitated by inorganic phosphate via two independent mechanisms». European Journal of Biochemistry 267 (19): 5995–6003. October 2000. doi:. PMID 10998060.
- ↑ «Rubisco: structure, regulatory interactions, and possibilities for a better enzyme». Annual Review of Plant Biology 53: 449–75. 2002. doi:. PMID 12221984. https://semanticscholar.org/paper/437c9700bdb4b82bee7c40f78b7619a1bda377d1.
- ↑ Timmer J (7 Δεκεμβρίου 2017). «We may now be able to engineer the most important lousy enzyme on the planet». Ars Technica. Ανακτήθηκε στις 5 Ιανουαρίου 2019. Unknown parameter
|name-list-style=ignored (βοήθεια) - ↑ Timmer J (3 Ιανουαρίου 2019). «Fixing photosynthesis by engineering it to recycle a toxic mistake». Ars Technica. Ανακτήθηκε στις 5 Ιανουαρίου 2019. Unknown parameter
|name-list-style=ignored (βοήθεια) - ↑ «Synthetic glycolate metabolism pathways stimulate crop growth and productivity in the field». Science 363 (6422): eaat9077. January 2019. doi:. PMID 30606819.
- ↑ 37,0 37,1 «Improving photosynthesis and yield potential in cereal crops by targeted genetic manipulation: Prospects, progress and challenges». Field Crops Research 182: 19–29. 2015. doi:.
- ↑ «Manipulation of Rubisco: the amount, activity, function and regulation». Journal of Experimental Botany 54 (386): 1321–33. May 2003. doi:. PMID 12709478.
- ↑ «Engineering Rubisco activase from thermophilic cyanobacteria into high-temperature sensitive plants». Critical Reviews in Biotechnology 38 (4): 559–572. June 2018. doi:. PMID 28937283.
- ↑ «Isoleucine 309 acts as a C4 catalytic switch that increases ribulose-1,5-bisphosphate carboxylase/oxygenase (rubisco) carboxylation rate in Flaveria». Proceedings of the National Academy of Sciences of the United States of America 108 (35): 14688–93. August 2011. doi:. PMID 21849620. Bibcode: 2011PNAS..10814688W.
- ↑ «Functional incorporation of sorghum small subunit increases the catalytic turnover rate of Rubisco in transgenic rice». Plant Physiology 156 (3): 1603–11. July 2011. doi:. PMID 21562335.
- ↑ «Analysis and Optimization of C3 Photosynthetic Carbon Metabolism». 2010 IEEE International Conference on BioInformatics and BioEngineering (Philadelphia, PA, USA: IEEE): 44–51. 2010. doi:. ISBN 978-1-4244-7494-3. https://ieeexplore.ieee.org/document/5521713.
- ↑ «Synthetic glycolate metabolism pathways stimulate crop growth and productivity in the field». Science 363 (6422): eaat9077. January 2019. doi:. PMID 30606819.
- ↑ «Plastome-encoded bacterial ribulose-1,5-bisphosphate carboxylase/oxygenase (RubisCO) supports photosynthesis and growth in tobacco». Proceedings of the National Academy of Sciences of the United States of America 98 (25): 14738–43. December 2001. doi:. PMID 11724961. Bibcode: 2001PNAS...9814738W.
- ↑ «Manipulating ribulose bisphosphate carboxylase/oxygenase in the chloroplasts of higher plants». Archives of Biochemistry and Biophysics 414 (2): 159–69. June 2003. doi:. PMID 12781767.
- ↑ «A faster Rubisco with potential to increase photosynthesis in crops». Nature 513 (7519): 547–50. September 2014. doi:. PMID 25231869. Bibcode: 2014Natur.513..547L.
- ↑ «Despite slow catalysis and confused substrate specificity, all ribulose bisphosphate carboxylases may be nearly perfectly optimized». Proceedings of the National Academy of Sciences of the United States of America 103 (19): 7246–51. May 2006. doi:. PMID 16641091. Bibcode: 2006PNAS..103.7246T.
- ↑ «Control of Rubisco function via homeostatic equilibration of CO2 supply». Frontiers in Plant Science 6: 106. 2015. doi:. PMID 25767475.
- ↑ «Land plants equilibrate O2 and CO2 concentrations in the atmosphere». Photosynthesis Research 87 (2): 177–94. February 2006. doi:. PMID 16432665.
- ↑ «Biogenesis and Metabolic Maintenance of Rubisco». Annual Review of Plant Biology 68: 29–60. April 2017. doi:. PMID 28125284.
- ↑ «Import of Soluble Proteins into Chloroplasts and Potential Regulatory Mechanisms» (στα English). Frontiers in Plant Science 8: 168. 2017. doi:. PMID 28228773.
- ↑ «Manipulation of Rubisco: the amount, activity, function and regulation» (στα αγγλικά). Journal of Experimental Botany 54 (386): 1321–1333. 2003-05-01. doi:. ISSN 0022-0957. PMID 12709478.
- ↑ «E. coli with five chloroplast chaperones including BSD2». Science 358 (6368): 1272–1278. December 2017. doi:. PMID 29217567. Bibcode: 2017Sci...358.1272A. https://www.dora.lib4ri.ch/psi/islandora/object/psi%3A3608/datastream/PDF/view.
- ↑ 54,0 54,1 Heazlewood J (2012). Proteomic applications in biology. New York: InTech Manhattan. ISBN 978-953-307-613-3.
- ↑ Gupta R, Kim ST (2015). «Depletion of RuBisCO protein using the protamine sulfate precipitation method». Proteomic Profiling. Methods in Molecular Biology. 1295. New York, NY: Humana Press. σελίδες 225–33. doi:10.1007/978-1-4939-2550-6_17. ISBN 978-1-4939-2549-0. PMID 25820725.
- ↑ «A rapid method for depletion of Rubisco from soybean (Glycine max) leaf for proteomic analysis of lower abundance proteins». Phytochemistry 70 (17–18): 1958–64. December 2009. doi:. PMID 19766275.
- ↑ «Two-dimensional electrophoretic analysis of rice proteins by polyethylene glycol fractionation for protein arrays». Electrophoresis 22 (10): 2103–9. June 2001. doi:. PMID 11465512.
- ↑ «Polyethylene glycol fractionation improved detection of low-abundant proteins by two-dimensional electrophoresis analysis of plant proteome». Phytochemistry 67 (21): 2341–8. November 2006. doi:. PMID 16973185.
- ↑ «Cross species applicability of abundant protein depletion columns for ribulose-1,5-bisphosphate carboxylase/oxygenase». Journal of Chromatography B 861 (1): 29–39. January 2008. doi:. PMID 18063427.
- ↑ «Rice proteomics: ending phase I and the beginning of phase II». Proteomics 9 (4): 935–63. February 2009. doi:. PMID 19212951.
- ↑ «The effect of DTT in protein preparations for proteomic analysis: Removal of a highly abundant plant enzyme, ribulose bisphosphate carboxylase/oxygenase» (στα αγγλικά). Journal of Plant Biology 51 (4): 297–301. July 2008. doi:. ISSN 1226-9239.
- ↑ Chase et al 1993.
- ↑ «Photorespiration and the evolution of C4 photosynthesis». Annual Review of Plant Biology 63: 19–47. 2012. doi:. PMID 22404472. https://semanticscholar.org/paper/6bcf761b5c2d9d09d21ea03722215c4be077e734.
- ↑ 64,0 64,1 «Stability-activity tradeoffs constrain the adaptive evolution of RubisCO». Proceedings of the National Academy of Sciences of the United States of America 111 (6): 2223–8. February 2014. doi:. PMID 24469821. Bibcode: 2014PNAS..111.2223S.
- ↑ «Along the trail from Fraction I protein to Rubisco (ribulose bisphosphate carboxylase-oxygenase)». Photosynthesis Research 73 (1–3): 243–50. 2002. doi:. PMID 16245127.
- ↑ «Discoveries in Rubisco (Ribulose 1,5-bisphosphate carboxylase/oxygenase): a historical perspective». Photosynthesis Research 94 (1): 121–43. October 2007. doi:. PMID 17665149.
- ↑ «Discovery of the canonical Calvin-Benson cycle». Photosynthesis Research 140 (2): 235–252. May 2019. doi:. PMID 30374727.
κκκ

κκκ
Βιβλιογραφία
- «Phylogenetics of Seed Plants: An Analysis of Nucleotide Sequences from the Plastid Gene rbcL». Annals of the Missouri Botanical Garden 80 (3): 528–580. 1993. doi:. https://spectrum.library.concordia.ca/6741/1/Dayanandan_AnnalsMissouriBotanicalGardens_1993.pdf.
- «Crystal structure of carboxylase reaction-oriented ribulose 1, 5-bisphosphate carboxylase/oxygenase from a thermophilic red alga, Galdieria partita». The Journal of Biological Chemistry 274 (22): 15655–61. May 1999. doi:. PMID 10336462.
- «Discoveries in Rubisco (Ribulose 1,5-bisphosphate carboxylase/oxygenase): a historical perspective». Photosynthesis Research 94 (1): 121–43. October 2007. doi:. PMID 17665149.
- «Was photosynthetic RuBisCO recruited by acquisitive evolution from RuBisCO-like proteins involved in sulfur metabolism?». Research in Microbiology 156 (5–6): 611–8. 2005. doi:. PMID 15950120.
- «Mutagenesis at two distinct phosphate-binding sites unravels their differential roles in regulation of Rubisco activation and catalysis». Journal of Bacteriology 187 (12): 4222–8. June 2005. doi:. PMID 15937184.
κκκ
