Ατομική ακτίνα
| Το λήμμα δεν περιέχει πηγές ή αυτές που περιέχει δεν επαρκούν. |
Ατομική ακτίνα (r) ορίζεται ως το μισό της απόστασης μεταξύ των πυρήνων δύο γειτονικών ατόμων, όπως αυτά διατάσσονται στο κρυσταλλικό πλέγμα του χημικού στοιχείου.
Η ατομική ακτίνα καθορίζει το μέγεθος του ατόμου. Αν θεωρήσουμε το άτομο ως σφαίρα, τότε η ατομική ακτίνα είναι η μέση απόσταση των ηλεκτρονίων της εξωτερικής στιβάδας από το κέντρο του πυρήνα. Επειδή όμως τα όρια των ηλεκτρονιακών νεφών δεν είναι σαφή (πιθανότητα εύρεσης του ηλεκτρονίου),είναι αδύνατον να προσδιοριστεί με ακρίβεια η ατομική ακτίνα.
Παραδείγματα
[Επεξεργασία | επεξεργασία κώδικα]- Na: Η ατομική ακτίνα είναι το 1/2 της απόστασης μεταξύ δύο γειτονικών ατόμων Na στο μεταλλικό πλέγμα (μεταλλική ακτίνα).
- Cl: Η ατομική ακτίνα είναι το 1/2 της απόστασης των πυρήνων δύο ατόμων Cl που ενώνονται με απλό ομοιοπολικό δεσμό (ομοιοπολική ακτίνα). Έτσι, το μήκος του δεσμού Cl-Cl είναι 198pm, οπότε η ομοιοπολική ακτίνα του Cl είναι 99pm.
- Xe: Η ατομική ακτίνα είναι το 1/2 της απόστασης δύο ατόμων Xe τα οποία βρίσκονται σε επαφή μεταξύ τους χωρίς να συνδέονται με ομοιοπολικό δεσμό (ακτίνα van de Waals).
Η ατομική ακτίνα παίζει σημαντικό ρόλο στη συμπεριφορά ενός χημικού στοιχείου, γιατί καθορίζει την ελκτική δύναμη που ασκεί ο θετικά φορτισμένος πυρήνας στα ηλεκτρόνια της εξωτερικής στιβάδας του ατόμου.
Από ποιους παράγοντες εξαρτάται η ατομική ακτίνα;
[Επεξεργασία | επεξεργασία κώδικα]Οι παράγοντες από τους οποίους εξαρτάται η ατομική ακτίνα είναι οι εξής:
- Ο κύριος κβαντικός αριθμός (n) των ηλεκτρονίων της εξωτερικής στιβάδας.
Αύξηση του κύριου κβαντικού αριθμού n των ηλεκτρονίων της εξωτερικής στιβάδας (nεξ.) σημαίνει προσθήκη νέων ηλεκτρονιακών στιβάδων και επομένως αύξηση της ατομικής ακτίνας.
- Το δραστικό πυρηνικό φορτίο (Z*).
Όσο αυξάνεται το δραστικό πυρηνικό φορτίο Ζ*, τόσο αυξάνεται η εκλκτική δύναμη του πυρήνα στα ηλεκτρόνια της εξωτερικής στιβάδας, άρα ελαττώνεται η ατομική ακτίνα.
Από τους δύο παράγοντες (n και Ζ*) μεγαλύτερη επίδραση στην ατομική ακτίνα έχει ο κύριος κβαντικός αριθμός των ηλεκτρονίων της εξωτερικής στιβάδας (nεξ.).
Πώς μεταβάλλεται η ατομική ακτίνα των χημικών στοιχείων σε σχέση με τη θέση τους στον Περιοδικό Πινακα
[Επεξεργασία | επεξεργασία κώδικα]Η ατομική ακτίνα είναι μία ομαλά μεταβαλλόμενη περιοδική ιδιότητα των χημικών στοιχείων.
Σε μία ομάδα του Π.Π. η ατομική ακτίνα αυξάνεται από πάνω προς τα κάτω. Τα χημικά στοιχεία μίας ομάδας του Π.Π. έχουν περίπου το ίδιο δραστικό πυρηνικό φορτίο (Ζ*). Καθώς προχωράμε από πάνω προς τα κάτω σε μία ομάδα του Π.Π., αυξάνεται ο κύριος κβαντικός αριθμός των ηλεκτρονίων της εξωτερικής στιβάδας (nεξ.), δηλαδή προστίθενται νέες ηλεκτρονιακές στιβάδες. Έτσι, αυξάνεται η μέση απόσταση των ηλεκτρονίων της εξωτερικής στιβάδας από τον πυρήνα, οπότε ελαττώνεται η ελκτική δύναμη του πυρήνα στα ηλεκτρόνια της εξωτερικής στιβάδας, με αποτέλεσμα η ατομική ακτίνα να αυξάνεται.
Παραδείγματα
[Επεξεργασία | επεξεργασία κώδικα]- Τα άτομα των αλκαλίων (IA ομάδα) έχουν εξωτερική ηλεκτρονιακή δομή ns1 και περίπου ίδια τιμή Z*. Οι ατομικές ακτίνες τους αυξάνονται σύμφωνα με τη σειρά
3Li < 11Na < 19K < 37Rb < 55Cs
nεξ.=2 nεξ.=3 nεξ.=4 nεξ.=5 nεξ.=6
- Τα άτομα των αλογόνων (VIIA ομάδα) έχουν εξωτερική ηλεκτρονιακή δομή ns2np5 και περίπου ίδια τιμή Ζ*. Οι ατομικές ακτίνες τους αυξάνονται σύμφωνα με τη σειρά:
nεξ.=2 nεξ.=3 nεξ.=4 nεξ.=5
Κατά μήκος μίας περιόδου του Π.Π. η ατομική ακτίνα ελαττώνεται από αριστερά προς τα δεξιά.
Τα χημικά στοιχεία μίας περιόδου του Π.Π. έχουν τον ίδιο κύριο κβαντικό αριθμό n για τα ηλεκτρόνια της εξωτερικής στιβάδας (έχουν τον ίδιο αριθμό στιβάδων).
Καθώς προχωράμε από αριστερά προς τα δεξιά σε μία περίοδο του Π.Π., αυξάνεται ο ατομικός αριθμός Ζ των χημικών στοιχείων, άρα αυξάνεται και το δραστικό πυρηνικό φορτίο Ζ* των ατόμων. Έτσι, προς την κατεύθυνση αυτή αυξάνεται η ελκτική δύναμη του πυρήνα στα ηλεκτρόνια της εξωτερικής στιβάδας, με αποτέλεσμα η ατομική ακτίνα να ελαττώνεται.
Τα στοιχεία μετάπτωσης παρουσιάζουν μικρές αποκλίσεις κατά τη μεταβολή της ατομικής τους ακτίνας. Αυτό συμβαίνει γιατί σε μία σειρά στοιχείων μετάπτωσης (χημικά στοιχεία που ανήκουν στην ίδια περίοδο), καθώς προχωράμε προς τα δεξιά, τα επιπλέον ηλεκτρόνια προστίθενται στην εσωτερική (n-1)d υποστιβάδα, οπότε επηρεάζεται ελάχιστα η ατομική ακτίνα.
Στην αρχή μίας σειράς στοιχείων μετάπτωσης η αύξηση του Ζ συνοδεύεται με μικρή ελάττωση της ατομικής ακτίνας (π.χ. Sc > Ti > V), ενώ προς το τέλος της κάθε σειράς παρατηρείται μικρή αύξηση των ατομικών ακτίνων (π.χ. Ni < Cu < Zn).
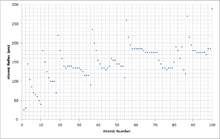
Η ατομική ακτίνα μεταβάλλεται περιοδικά σε συνάρτηση με τον ατομικό αριθμό (Ζ). Όπως προκύπτει από το διάγραμμα, όταν αλλάζει περίοδος, η ατομική ακτίνα αυξάνεται απότομα, επειδή αυξάνεται η τιμή του nεξ. (προστίθεται μία νέα στιβάδα) και το Ζ* ελαττώνεται απότομα.
