Φλουοξετίνη
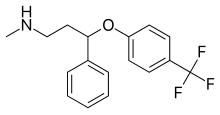 | |
 Φλουοξετίνη (πάνω), (R)-φλουοξετίνη (αριστερά), (S)-φλουοξετίνη (δεξιά) | |
| Ονομασία IUPAC | |
|---|---|
N-methyl-3-phenyl-3-[4-(trifluoromethyl)phenoxy]propan-1-amine | |
| Κλινικά δεδομένα | |
| Εμπορικές ονομασίες | Prozac, Sarafem, Ladose, άλλα |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a689006 |
| Δεδομένα άδειας |
|
| Κατηγορία ασφαλείας κύησης | |
| Πιθανότητα εθισμού | Καμία[1] |
| Οδοί χορήγησης | Από το στόμα |
| Κυκλοφορία | |
| Κυκλοφορία |
|
| Φαρμακοκινητική | |
| Βιοδιαθεσιμότητα | 60–80%[2] |
| Πρωτεϊνική σύνδεση | 94–95%[3] |
| Μεταβολισμός | Ήπαρ (κυρίως μέσω του CYP2D6)[4] |
| Μεταβολίτες | νορφλουοξετίνη, δεσμεθυφλουοξετίνη |
| Βιολογικός χρόνος ημιζωής | 1–3 ημέρες (οξεία) 4–6 ημέρες (χρόνια)[4][5] |
| Απέκκριση | Ούρα (80%), κόπρανα (15%)[4][5] |
| Κωδικοί | |
| Αριθμός CAS | 54910-89-3 |
| Κωδικός ATC | N06AB03 |
| PubChem | CID 3386 |
| IUPHAR/BPS | 203 |
| DrugBank | DB00472 |
| ChemSpider | 3269 |
| UNII | 01K63SUP8D |
| KEGG | D00326 |
| ChEBI | CHEBI:5118 |
| ChEMBL | CHEMBL41 |
| Χημικά στοιχεία | |
| Χημικός τύπος | C17H18F3NO |
| Μοριακή μάζα | 309,33 g·mol−1 |
CNCCC(c1ccccc1)Oc2ccc(cc2)C(F)(F)F | |
InChI=1S/C17H18F3NO/c1-21-12-11-16(13-5-3-2-4-6-13)22-15-9-7-14(8-10-15)17(18,19)20/h2-10,16,21H,11-12H2,1H3 Key:RTHCYVBBDHJXIQ-UHFFFAOYSA-N | |
| Φυσικά στοιχεία | |
| Σημείο τήξης | 179 to 182 °C (354 to 360 °F) |
| Σημείο βρασμού | 395 °C (743 °F) |
| Υδροδιαλυτότητα | 14 mg/mL (20 °C) |
| (verify) | |
Η φλουοξετίνη, που πωλείται με τις επωνυμίες Prozac και Ladose, μεταξύ άλλων, είναι αντικαταθλιπτικό της κατηγορίας εκλεκτικών αναστολέων επαναπρόσληψης σεροτονίνης (SSRI).[2] Χρησιμοποιείται για τη θεραπεία της μείζονος καταθλιπτικής διαταραχής, της ιδεοψυχαναγκαστικής διαταραχής (OCD), της νευρικής βουλιμίας, της διαταραχής πανικού και της προεμμηνορροϊκής δυσφορικής διαταραχής.[2] Μπορεί να μειώσει τον κίνδυνο αυτοκτονίας σε άτομα άνω των 65 ετών. Έχει επίσης χρησιμοποιηθεί για τη θεραπεία της πρόωρης εκσπερμάτωσης. Η φλουοξετίνη λαμβάνεται από το στόμα.[2]
Συχνές ανεπιθύμητες ενέργειες περιλαμβάνουν δυσπεψία, δυσκολία στον ύπνο, σεξουαλική δυσλειτουργία, απώλεια όρεξης, ξηροστομία, εξάνθημα και ανώμαλα όνειρα.[2] Σοβαρές παρενέργειες περιλαμβάνουν σύνδρομο σεροτονίνης, μανία, επιληπτικές κρίσεις, αυξημένο κίνδυνο αυτοκτονικής συμπεριφοράς σε άτομα κάτω των 25 ετών και αυξημένο κίνδυνο αιμορραγίας. Εάν σταματήσει ξαφνικά, μπορεί να εμφανιστεί σύνδρομο στέρησης με άγχος, ζάλη και αλλαγές στην αίσθηση. Δεν είναι σαφές εάν είναι ασφαλές κατά την εγκυμοσύνη. Εάν λαμβάνεται ήδη, μπορεί να είναι λογικό να συνεχίσει κατά τη διάρκεια του θηλασμού.[6] Ο μηχανισμός δράσης του δεν είναι απολύτως σαφής αλλά πιστεύεται ότι σχετίζεται με την αύξηση της δραστηριότητας της σεροτονίνης στον εγκέφαλο.[2]
Η φλουοξετίνη ανακαλύφθηκε από την Eli Lilly and Company το 1972 και εγκρίθηκε για ιατρική χρήση το 1986.[7] Είναι στον κατάλογο των βασικών φαρμάκων του Παγκόσμιου Οργανισμού Υγείας.[8] Διατίθεται ως γενόσημο φάρμακο.[2] Το 2017, ήταν η 31η πιο συχνά συνταγογραφούμενη φαρμακευτική αγωγή στις Ηνωμένες Πολιτείες, με περισσότερες από 21 εκατομμύρια συνταγές.[9][10]
Ιατρικές χρήσεις
[Επεξεργασία | επεξεργασία κώδικα]
Η φλουοξετίνη χρησιμοποιείται συχνά για τη θεραπεία μείζονος καταθλιπτικής διαταραχής, ιδεοψυχαναγκαστικής διαταραχής (OCD), διαταραχής μετατραυματικού στρες (PTSD), νευρικής βουλιμίας, διαταραχής πανικού, προεμμηνορροϊκής δυσφορικής διαταραχής και τριχοτιλομανίας.[11][12][13][14] Έχει επίσης χρησιμοποιηθεί για καταπληξία, παχυσαρκία και εξάρτηση από το αλκοόλ,[15] καθώς και για την αδηφαγική διαταραχή.[16] Η φλουοξετίνη φαίνεται να είναι αναποτελεσματική για τη διαταραχή κοινωνικού άγχους.[17] Οι μελέτες υποδεικνύουν όφελος σε παιδιά με αυτισμό, αν και υπάρχουν μόνο προσωρινές ενδείξεις για το όφελος του στον αυτισμό των ενηλίκων.[18][19][20][21]
Κατάθλιψη
[Επεξεργασία | επεξεργασία κώδικα]Η αποτελεσματικότητα της φλουοξετίνης και άλλων αντικαταθλιπτικών στη θεραπεία της ήπιας έως μέτριας κατάθλιψης είναι αμφιλεγόμενη. Μια ανασκόπηση της συγκριτικής αποτελεσματικότητας 21 αντικαταθλιπτικών φαρμάκων διαπίστωσε ότι η φλουοξετίνη ήταν αποτελεσματική για τη θεραπεία της κατάθλιψης, αν και άλλα SSRIs ήταν πιο αποτελεσματικά.[22] Μια μετα-ανάλυση που δημοσιεύθηκε από τον Κιρς το 2008 υποδηλώνει ότι σε άτομα με ήπια ή μέτρια συμπτώματα, η αποτελεσματικότητα της φλουοξετίνης και άλλων SSRIs είναι κλινικά ασήμαντη.[23] Μια μετα-ανάλυση του 2009 από τον Φουρνιέ, η οποία αξιολόγησε δεδομένα σε επίπεδο ασθενούς από έξι δοκιμές της SSRI παροξετίνης και της μη-SSRI αντικαταθλιπτικής ιμιπραμίνης έχει αναφερθεί περαιτέρω ως απόδειξη ότι τα αντικαταθλιπτικά εμφανίζουν ελάχιστη αποτελεσματικότητα σε ήπια έως μέτρια κατάθλιψη.[24] Μια μετα-ανάλυση του 2012 χρησιμοποιώντας δεδομένα επιπέδου μεμονωμένου ασθενούς για τη θεραπεία της κατάθλιψης κατέληξε στο συμπέρασμα ότιπαρατηρήθηκε στατιστικά και κλινικά σημαντικό όφελος ανεξάρτητα από τη σοβαρότητα της κατάθλιψης κατά την έναρξη και δεν βρέθηκε σημαντική επίδραση στη σοβαρότητα κατά την έναρξη στην παρατηρούμενη αποτελεσματικότητα.[25] Συνολικά δεν υπάρχουν στοιχεία από τυχαιοποιημένες ελεγχόμενες δοκιμές ότι η φλουοξετίνη ή άλλα SSRI μειώνουν τον κίνδυνο αυτοκτονίας.[26] Υπάρχουν προσωρινές ενδείξεις που υποδηλώνουν ότι μπορεί να μειώσει τον κίνδυνο αυτοκτονίας σε άτομα άνω των 65 ετών.[2]
Μια συστηματική ανασκόπηση του 2009 από το Εθνικό Ινστιτούτο Φροντίδας και Κλινικής Αριστείας (NICE) (το οποίο έλαβε υπόψιν τον Κιρς, αλλά όχι τις μεταγενέστερες μετα-αναλύσεις) κατέληξε στο συμπέρασμα ότι υπήρχαν ισχυρά στοιχεία για την αποτελεσματικότητα των SSRI στη θεραπεία της μέτριας και σοβαρής κατάθλιψης, με ορισμένα στοιχεία για την αποτελεσματικότητά τους στη θεραπεία της ήπιας κατάθλιψης.[27] Τόσο οι αναλύσεις του NICE όσο και του Φουρνιέ κατέληξαν στο συμπέρασμα ότι παρατηρούνται μεγαλύτερες ενδείξεις για την αποτελεσματικότητα των αντικαταθλιπτικών στη θεραπεία της χρόνιας ήπιας κατάθλιψης (δυσθυμίας) από ό, τι στην ήπια κατάθλιψη πρόσφατης έναρξης.
Ιδεοψυχαναγκαστική διαταραχή
[Επεξεργασία | επεξεργασία κώδικα]Η αποδοτικότητα της φλουοξετίνης στη θεραπεία της ιδεοψυχαναγκαστικής διαταραχής (OCD) υποδείχθηκαν σε δύο τυχαιοποιημένες πολυκεντρικές κλινικές δοκιμές φάσεις 3. Τα αποτελέσματα αυτών των δοκιμών έδειξαν ότι το 47% των συμμετεχόντων που ολοκλήρωσαν τις δοκιμές με τη μεγαλύτερη δόση είχαν «βελτιωθεί πολύ» ή «πάρα πολύ» μετά από 13 εβδομάδες θεραπείας, σε σχέση με το 11% όσων είχαν λάβει εικονικό φάρμακο.[3] Η Αμερικανική Ακαδημία Ψυχιατρικής Παιδιών και Εφήβων δήλωσε ότι τα SSRI, συμπεριλαμβανομένης της φλουοξετίνης, θα πρέπει να είναι θεραπεία πρώτης γραμμής στα παιδιά, μαζί με τη γνωσιακή συμπεριφορική αγωγή, για τη θεραπεία μετρίου προς σοβαρού OCD.[28]
Διαταραχή πανικού
[Επεξεργασία | επεξεργασία κώδικα]Η αποτελεσματικότητα της φλουοξετίνης στη θεραπεία της διαταραχής πανικού αποδείχθηκε σε δύο πολυκεντρικές τυχαιοποιημένες κλινικές δοκιμές φάσης ΙΙΙ διάρκειας 12 εβδομάδων στις οποίες συμμετείχαν ασθενείς που είχαν διαγνωστεί με διαταραχή πανικού, με ή χωρίς αγοραφοβία. Στην πρώτη δοκιμή, το 42% των ατόμων στο σκέλος που έλαβε φλουοξετίνη ήταν απαλλαγμένα από κρίσεις πανικού στο τέλος της μελέτης, έναντι 28% στο σκέλος του εικονικού φαρμάκου. Στη δεύτερη δοκιμή, το 62% των ασθενών που έλαβαν φλουοξετίνη ήταν απαλλαγμένα από κρίσεις πανικού στο τέλος της μελέτης, έναντι 44% στο σκέλος του εικονικού φαρμάκου.[3]
Νευρογενής βουλιμία
[Επεξεργασία | επεξεργασία κώδικα]Μια συστηματική ανασκόπηση του 2011 συζήτησε επτά δοκιμές που συνέκριναν τη φλουοξετίνη με ένα εικονικό φάρμακο στη θεραπεία της νευρικής βουλιμίας, έξι από τις οποίες βρήκαν στατιστικά σημαντική μείωση των συμπτωμάτων όπως ο εμετός και η υπερβολική κατανάλωση.[29] Ωστόσο, δεν παρατηρήθηκε διαφορά μεταξύ των σκελών θεραπείας όταν η φλουοξετίνη και η ψυχοθεραπεία συγκρίθηκαν μόνο με την ψυχοθεραπεία.
Ειδικοί πληθυσμοί
[Επεξεργασία | επεξεργασία κώδικα]Σε παιδιά και εφήβους, η φλουοξετίνη είναι το αντικαταθλιπτικό επιλογής, λόγω των προσωρινών ενδείξεων που ευνοούν την αποτελεσματικότητα και την ανεκτικότητά της.[30][31] Κατά την εγκυμοσύνη, η φλουοξετίνη θεωρείται φάρμακο κατηγορίας C από την Υπηρεσία Τροφίμων και Φαρμάκων των ΗΠΑ (FDA). Τα στοιχεία που υποστηρίζουν αυξημένο κίνδυνο σοβαρών εμβρυϊκών δυσπλασιών που προκύπτουν από την έκθεση στη φλουοξετίνη είναι περιορισμένα, αν και η Ρυθμιστική Υπηρεσία των Φαρμάκων και Υγείας του Ηνωμένου Βασιλείου έχει προειδοποιήσει τους ιατρούς και τους ασθενείς ότι σε περίπτωση έκθεσης σε φλουοξετίνη κατά το πρώτο τρίμηνο (κατά τη διάρκεια της οργανογένεσης, του σχηματισμού των εμβρυϊκών οργάνων) μπορεί να οδηγήσει σε ελαφρά αύξηση του κινδύνου συγγενών καρδιακών δυσπλασιών στο νεογέννητο.[32][33][34] Επιπλέον, σε μια μελέτη παρατηρήθηκε συσχέτιση μεταξύ της χρήσης φλουοξετίνης κατά το πρώτο τρίμηνο και αυξημένου κινδύνου μικρών εμβρυϊκών δυσπλασιών.
Σύμφωνα με τη FDA, τα βρέφη που εκτίθενται σε SSRI στα τέλη της εγκυμοσύνης μπορεί να έχουν αυξημένο κίνδυνο για επίμονη πνευμονική υπέρταση του νεογέννητου. Περιορισμένα δεδομένα υποστηρίζουν αυτόν τον κίνδυνο, αλλά η FDA συνιστά στους γιατρούς να εξετάσουν τη μείωση των SSRI όπως η φλουοξετίνη κατά το τρίτο τρίμηνο.[3] Μια μελέτη του 2009 αποθάρρυνε τη χρήση της φλουοξετίνης ως SSRI πρώτης γραμμής κατά τη γαλουχία, δηλώνοντας ότι «η φλουοξετίνη θα πρέπει να θεωρείται ως λιγότερο προτιμώμενο SSRI για θηλάζουσες μητέρες, ειδικά με νεογέννητα βρέφη και σε εκείνες τις μητέρες που κατανάλωναν φλουοξετίνη κατά τη διάρκεια της κύησης.»[35] Η σερτραλίνη είναι συχνά το προτιμώμενο SSRI κατά τη διάρκεια της εγκυμοσύνης λόγω της σχετικά ελάχιστης έκθεσης που παρατηρείται στο έμβρυο και του προφίλ ασφάλειας κατά το θηλασμό.[36]
Παρενέργειες
[Επεξεργασία | επεξεργασία κώδικα]Οι παρενέργειες που παρατηρήθηκαν σε άτομα που έλαβαν φλουοξετίνη σε κλινικές δοκιμές με συχνότητα > 5% και τουλάχιστον δύο φορές συχνότερα σε άτομα που έλαβαν φλουοξετίνη σε σύγκριση με εκείνα που έλαβαν χάπι εικονικού φαρμάκου περιλαμβάνουν ανώμαλα όνειρα, ανώμαλη εκσπερμάτωση, ανορεξία, άγχος, ασθένεια, διάρροια, ξηροστομία, δυσπεψία, γριπώδη συνδρομή, ανικανότητα, αϋπνία, μειωμένη λίμπιντο, ναυτία, νευρικότητα, φαρυγγίτιδα, εξάνθημα, ιγμορίτιδα, υπνηλία, εφίδρωση, τρόμος, αγγειοδιαστολή και χασμουρητό.[37] Η φλουοξετίνη θεωρείται η πιο διεγερτική από τα SSRI (δηλαδή, είναι πιο επιρρεπής στην πρόκληση αϋπνίας και διέγερσης).[38] Φαίνεται επίσης ότι είναι το πιο επιρρεπές SSRI στην εκδήλωση δερματολογικών αντιδράσεων (π.χ. κνίδωση, εξάνθημα, φαγούρα κ.λπ. ).[33]
Σεξουαλική δυσλειτουργία
[Επεξεργασία | επεξεργασία κώδικα]Η σεξουαλική δυσλειτουργία, συμπεριλαμβανομένης της απώλειας λίμπιντο, της ανοργασμίας, της έλλειψης κολπικής λίπανσης και της στυτικής δυσλειτουργίας, είναι μερικές από τις πιο συχνά εμφανιζόμενες ανεπιθύμητες ενέργειες της θεραπείας με φλουοξετίνη και άλλα SSRI. Ενώ οι πρώτες κλινικές δοκιμές πρότειναν σχετικά χαμηλό ποσοστό σεξουαλικής δυσλειτουργίας, πιο πρόσφατες μελέτες στις οποίες ο ερευνητής αναζήτησε ενεργά σεξουαλικά προβλήματα υποδηλώνουν ότι η συχνότητα είναι >70%.[39] Τα συμπτώματα της σεξουαλικής δυσλειτουργίας έχουν αναφερθεί ότι παραμένουν μετά τη διακοπή των SSRI, αν και πιστεύεται ότι είναι περιστασιακά.[3][40][41]
Σύνδρομο διακοπής
[Επεξεργασία | επεξεργασία κώδικα]Το σύνδρομο διακοπής αντικαταθληπτικών μπορεί να εμφανιστεί εντός ημερών ή εβδομάδων από τη διακοπή ενός αντικαταθλιπτικού. Τα συμπτώματα μπορεί να περιλαμβάνουν ζάλη, διαταραχή της ισορροπίας, πονοκέφαλο, ναυτία, αϋπνία, έντονα όνειρα, αίσθημα μυρμηγκιάσματος ή μούδιασμα, ευερεθιστότητα, ψευδαισθήσεις, κόπωση, συμπτώματα κατάθλιψης και αυτοκτονία. Το σύνδρομο διακοπής αντικαταθλιπτικών συχνά εκλαμβάνεται ως υποτροπιάζουσα κατάθλιψη, προκαλώντας την επαναχορήγηση του φαρμάκου. Το σύνδρομο διακοπής αντικαταθληπτικών μπορεί να μειωθεί ή να προληφθεί με τη μείωση της δόσης του φαρμάκου επί αρκετές εβδομάδες ή μήνες.[42][43] Ο μακρύτερος χρόνος ημιζωής της φλουοξετίνης καθιστά λιγότερο συχνή την εμφάνιση συνδρόμου διακοπής μετά τη διακοπή της θεραπείας, ειδικά σε σύγκριση με τα αντικαταθλιπτικά με μικρότερο χρόνο ημιζωής όπως η παροξετίνη.[44][45] Αν και συνιστάται σταδιακή μείωση της δόσης σε αντικαταθλιπτικά με μικρότερο χρόνο ημιζωής, μπορεί να μην είναι απαραίτητη η μείωση στην περίπτωση της φλουοξετίνης.[46]
Αυτοκτονία
[Επεξεργασία | επεξεργασία κώδικα]Το 2007, η FDA ζήτησε από όλα τα αντικαταθλιπτικά να φέρουν προειδοποίηση μαύρου κουτιού που να δηλώνει ότι τα αντικαταθλιπτικά μπορεί να αυξήσουν τον κίνδυνο αυτοκτονίας σε άτομα κάτω των 25 ετών. Αυτή η προειδοποίηση βασίζεται σε στατιστικές αναλύσεις που διεξήχθησαν από δύο ανεξάρτητες ομάδες εμπειρογνωμόνων της FDA, οι οποίες διαπίστωσαν διπλάσια αύξηση του αυτοκτονικού ιδεασμού και συμπεριφοράς σε παιδιά και εφήβους, και 1,5 φορές αύξηση της αυτοκτονίας στην ηλικιακή ομάδα 18-24. Η αυτοκτονία μειώθηκε ελαφρώς για όσους ήταν άνω των 24 ετών, και ήταν στατιστικά σημαντικά χαμηλότερη στην ομάδα των 65 και άνω.[47][48][49] Αυτή η ανάλυση επικρίθηκε από τον Ντόναλντ Κλάιν, ο οποίος σημείωσε ότι η αυτοκτονία, δηλαδή ο αυτοκτονικός ιδεασμός και συμπεριφορά, δεν είναι απαραίτητα ένας καλός υποκατάστατος για ολοκληρωμένη αυτοκτονία και είναι ακόμα πιθανό τα αντικαταθλιπτικά να αποτρέψουν την πραγματική αυτοκτονία αυξάνοντας ταυτόχρονα την αυτοκτονικότητα.[50]
Υπάρχουν λιγότερα δεδομένα για τη φλουοξετίνη από ό, τι για τα αντικαταθλιπτικά στο σύνολό τους. Για την παραπάνω ανάλυση σχετικά με το επίπεδο αντικαταθλιπτικών, η FDA έπρεπε να συνδυάσει τα αποτελέσματα 295 δοκιμών 11 αντικαταθλιπτικών για ψυχιατρικές ενδείξεις για να λάβει στατιστικά σημαντικά αποτελέσματα. Θεωρείται χωριστά, η χρήση φλουοξετίνης στα παιδιά αύξησε τις πιθανότητες αυτοκτονίας κατά 50%,[51] και σε ενήλικες μείωσε τις πιθανότητες αυτοκτονίας κατά περίπου 30%.[48][49] Ομοίως, η ανάλυση που πραγματοποιήθηκε από το Ηνωμένο Βασίλειο MHRA διαπίστωσε αύξηση κατά 50% των πιθανών συμβάντων που σχετίζονται με αυτοκτονία, χωρίς να φθάνει σε στατιστική σημασία, στα παιδιά και τους εφήβους που λαμβάνουν φλουοξετίνη σε σύγκριση με αυτά του εικονικού φαρμάκου. Σύμφωνα με τα δεδομένα MHRA, για τους ενήλικες η φλουοξετίνη δεν άλλαξε το ποσοστό αυτοτραυματισμού και μείωσε στατιστικά σημαντικά τον αυτοκτονικό ιδεασμό κατά 50%.[52][53]
Παράταση QT
[Επεξεργασία | επεξεργασία κώδικα]Η φλουοξετίνη μπορεί να επηρεάσει τα ηλεκτρικά ρεύματα που χρησιμοποιούν τα καρδιακά μυϊκά κύτταρα για να συντονίσουν τη συστολή τους, ειδικά τα ρεύματα καλίου I έως και I Ks που επαναπολώνουν το δυναμικό καρδιακής δράσης.[54] Υπό ορισμένες συνθήκες, αυτό μπορεί να οδηγήσει σε παράταση του διαστήματος QT, μια μέτρηση που γίνεται σε ένα ηλεκτροκαρδιογράφημα που αντικατοπτρίζει πόσο καιρό χρειάζεται για την καρδιά να επαναφορτιστεί ηλεκτρικά μετά από κάθε καρδιακό παλμό. Όταν η φλουοξετίνη λαμβάνεται μαζί με άλλα φάρμακα που παρατείνουν το διάστημα QT ή από άτομα με ευαισθησία στο σύνδρομο μακρού QT, υπάρχει μικρός κίνδυνος δυνητικά θανατηφόρων μη φυσιολογικών καρδιακών ρυθμών όπως η πολύμορφη κοιλιακή ταχυκαρδία.[55] Από το 2019, ο ιστότοπος αναφοράς για τα φάρμακα CredibleMeds χαρακτηρίζει τη φλουοξετίνη ως αιτία αύξησης του κινδύνου αρρυθμιών.[56]
Υπερδοσολογία
[Επεξεργασία | επεξεργασία κώδικα]Σε υπερβολική δόση, οι συχνότερες ανεπιθύμητες ενέργειες περιλαμβάνουν:[57]
|
Νευρολικές
|
Γαστρεντερικές |
Άλλες |
Αλληλεπιδράσεις
[Επεξεργασία | επεξεργασία κώδικα]Οι αντενδείξεις περιλαμβάνουν προηγούμενη θεραπεία (εντός των τελευταίων 5-6 εβδομάδων, ανάλογα με τη δόση)[58][59] με αναστολείς ΜΑΟ όπως η φαινελζίνη και η τρανυλκυπρομίνη, λόγω της πιθανότητας για σύνδρομο σεροτονίνης. Η χρήση του πρέπει επίσης να αποφεύγεται σε άτομα με γνωστές υπερευαισθησίες στη φλουοξετίνη ή σε οποιοδήποτε άλλο από τα συστατικά της συνταγοποίησης που χρησιμοποιείται. Δεν συνιστάται επίσης η χρήση του σε αυτούς που λαμβάνουν ταυτόχρονα πιμοζίδη ή θειοριδαζίνη.
Οι ασθενείς που λαμβάνουν αντιπηκτικά ή ΜΣΑΦ πρέπει να είναι προσεκτικοί όταν λαμβάνουν φλουοξετίνη ή άλλα SSRI, καθώς μερικές φορές μπορούν να αυξήσουν τις επιδράσεις αυτών των φαρμάκων στην αραίωση του αίματος.[60]
Η χρήση της θα πρέπει επίσης να αποφεύγεται σε όσους λαμβάνουν άλλα σεροτονινεργικά φάρμακα όπως αναστολείς μονοαμινοξειδάσης, τρικυκλικά αντικαταθλιπτικά, μεθαμφεταμίνη, αμφεταμίνη, MDMA, τριπτάνες, βουσπιρόνη, αναστολείς επαναπρόσληψης σεροτονίνης-νορεπινεφρίνης και άλλα SSRI λόγω της πιθανότητας εκδήλωσης σεροτονινεργικού συνδρόμου ως αποτέλεσμα.
Φαρμακολογία
[Επεξεργασία | επεξεργασία κώδικα]Φαρμακοδυναμική
[Επεξεργασία | επεξεργασία κώδικα]Η φλουοξετίνη είναι ένας εκλεκτικός αναστολέας επαναπρόσληψης σεροτονίνης (SSRI) και δεν αναστέλλει σημαντικά την επαναπρόσληψη νορεπινεφρίνης και ντοπαμίνης σε θεραπευτικές δόσεις. Ωστόσο, καθυστερεί την επαναπρόσληψη της σεροτονίνης, με αποτέλεσμα η σεροτονίνη να παραμένει περισσότερο όταν απελευθερώνεται. Μεγάλες δόσεις σε αρουραίους έχει αποδειχθεί ότι προκαλούν σημαντική αύξηση της συναπτικής νορεπινεφρίνης και της ντοπαμίνης.[61][62][63][64] Έτσι, η ντοπαμίνη και η νορεπινεφρίνη μπορεί να συμβάλλουν στην αντικαταθλιπτική δράση της φλουοξετίνης στον άνθρωπο σε υπερθεραπευτικές δόσεις (60-80 mg).[65] Αυτό το αποτέλεσμα μπορεί να προκαλείται από τους υποδοχείς 5ΗΤ 2C, οι οποίοι αναστέλλονται από υψηλότερες συγκεντρώσεις φλουοξετίνης.[66]
Η φλουοξετίνη αυξάνει τη συγκέντρωση της κυκλοφορούσας αλλοπρεγνανολόνης, ενός ισχυρού θετικού αλλοστερικού ρυθμιστή του στον υποδοχέα GABAA, στον εγκέφαλο.[64][67] Η νορφλουοξετίνη, ένας πρωταρχικός ενεργός μεταβολίτης της φλουοξετίνης, παράγει παρόμοια επίδραση στα επίπεδα αλλοπρεγνανολόνης στους εγκεφάλους των ποντικών. Επιπρόσθετα, τόσο η φλουοξετίνη όσο και η νορφλουοξετίνη είναι τέτοιοι ρυθμιστές οι ίδιες, δράση που μπορεί να είναι κλινικά σχετική.[68]
Επιπλέον, η φλουοξετίνη έχει βρεθεί ότι δρα ως αγωνιστής του σ1-υποδοχέα, με ισχύ μεγαλύτερη από αυτήν της σιταλοπράμης αλλά μικρότερη από εκείνη της φλουβοξαμίνης. Ωστόσο, η σημασία αυτού του ευρύματος δεν είναι απολύτως σαφής.[69][70] Η φλουοξετίνη λειτουργεί επίσης ως αποκλειστής διαύλων της ανοκταμίνης 1, ενός διαύλου χλωρίου που ενεργοποιηείται από ασβέστιο.[71][72] Ένας αριθμός άλλων διαύλων ιόντων, συμπεριλαμβανομένων των νικοτινικών υποδοχέων ακετυλοχολίνης και των υποδοχέων 5-ΗΤ3, είναι επίσης γνωστό ότι αναστέλλονται σε παρόμοιες συγκεντρώσεις.[68]
Φαρμακοκινητική
[Επεξεργασία | επεξεργασία κώδικα]
Η βιοδιαθεσιμότητα της φλουοξετίνης είναι σχετικά υψηλή (72%) και οι μέγιστες συγκεντρώσεις στο πλάσμα επιτυγχάνονται εντός 6-8 ωρών. Συνδέεται σε μεγάλο βαθμό με πρωτείνες του πλάσματος, κυρίως την αλβουμίνη και την α1-γλυκοπρωτείνη. Η φλουοξετίνη μεταβολίζεται κυρίως στο ήπαρ από τα ισοένζυμα του κυτοχρώματος P450, συμπεριλαμβανομένου του CYP2D6.[73] Ο ρόλος του CYP2D6 στον μεταβολισμό της φλουοξετίνης μπορεί να είναι κλινικά σημαντικός, καθώς παρουσιάζει μεγάλη γενετική ποικιλία στη λειτουργικότητα σε διαφορετικά άτομα. Το CYP2D6 είναι υπεύθυνο για τη μετατροπή της φλουοξετίνης στον μόνο ενεργό μεταβολίτη της, τη νορφλουοξετίνη.[74] Και τα δύο φάρμακα είναι ισχυροί αναστολείς του CYP2D6.[75]
Η εξαιρετικά αργή αποβολή της φλουοξετίνης και του ενεργού μεταβολίτη της νορφλουοξετίνης από το σώμα τη διακρίνει από άλλα αντικαταθλιπτικά. Με την πάροδο του χρόνου, η φλουοξετίνη και η νορφλουοξετίνη αναστέλλουν τον δικό τους μεταβολισμό, οπότε ο χρόνος ημιζωής αποβολής της φλουοξετίνης αλλάζει από 1 σε 3 ημέρες, μετά από μία εφάπαξ δόση, σε 4 έως 6 ημέρες, μετά από μακροχρόνια χρήση. Ομοίως, ο χρόνος ημιζωής της νορφλουοξετίνης είναι μεγαλύτερος (16 ημέρες) μετά από μακροχρόνια χρήση.[73][76][77] Επομένως, η συγκέντρωση του φαρμάκου και του ενεργού μεταβολίτη του στο αίμα συνεχίζει να αυξάνεται κατά τις πρώτες εβδομάδες θεραπείας και η σταθερή συγκέντρωσή τους στο αίμα επιτυγχάνεται μόνο μετά από τέσσερις εβδομάδες.[78][79] Επιπλέον, η συγκέντρωση της φλουοξετίνης και των μεταβολιτών της στον εγκέφαλο αυξάνεται συνεχώς τουλάχιστον κατά τις πρώτες πέντε εβδομάδες θεραπείας.[80] Αυτό σημαίνει ότι τα πλήρη οφέλη της τρέχουσας δόσης που λαμβάνει ένας ασθενής δεν εμφανίζονται για τουλάχιστον ένα μήνα από την έναρξή του. Για παράδειγμα, σε μια μελέτη 6 εβδομάδων, ο διάμεσος χρόνος για την επίτευξη σταθερής απόκρισης ήταν 29 μέρες.[78] Ομοίως, η πλήρης απέκκριση του φαρμάκου μπορεί να χρειαστεί αρκετές εβδομάδες. Κατά τη διάρκεια της πρώτης εβδομάδας μετά τη διακοπή της θεραπείας, η συγκέντρωση της φλουοξετίνης στον εγκέφαλο μειώνεται μόνο κατά 50%.[80] Τα επίπεδα της νορφλουοξετίνης στο αίμα 4 εβδομάδες μετά τη διακοπή της θεραπείας είναι περίπου το 80% των επιπέδων που καταγράφηκαν μέχρι το τέλος της πρώτης εβδομάδας θεραπείας και 7 εβδομάδες μετά τη διακοπή η νορφλουοξετίνη είναι ακόμη ανιχνεύσιμη στο αίμα.[76]
Ιστορία
[Επεξεργασία | επεξεργασία κώδικα]Η εργασία που τελικά οδήγησε στην ανακάλυψη της φλουοξετίνης ξεκίνησε στην Eli Lilly and Company το 1970 ως συνεργασία των Μπράιαν Μολόι και Ρόμπερτ Ράτμπαν. Ήταν γνωστό τότε ότι το αντισταμινικό διφαινυδραμίνη παρουσίαζε κάποιες αντικαταθλιπτικές ιδιότητες. Η 3-φαινοξυ-3-φαινυλοπροπυλαμίνη, μια ουσία δομικά όμοια με τη διφαινυδραμίνη χρησιμοποιήθηκε ως εναρκτήριο σημείο, και ο Μολόι συνέθεσε δεκάδες παράγωγά του.[81] Ελπίζοντας να βρουν ένα παράγωγο που να εμπόδιζε την επαναπρόσληψη μόνο της σεροτονίνης, ο Ντέιβιντ Γουόνγκ πρότεινε να επανεξετάση τη σειρά για in vitro επαναπρόσληψη σεροτονίνης, νορεπινεφρίνης και ντοπαμίνης. Αυτή η μελέτη διεξήχθη από τον Γιονγκ-Σιρ Χορνγκ το Μάιο του 1972, και έδειξε ότι η ουσία που ονομάστηκε αργότερα φλουοξετίνη ήταν ο πιο ισχυρός και εκλεκτικός αναστολέας επαναπρόσληψης της σειράς.[82] Ο Γουόνγκ δημοσίευσε το πρώτο άρθρο για τη φλουοξετίνη το 1974. Ένα χρόνο αργότερα έλαβε το επίσημο χημικό όνομα φλουοξετίνη και η Eli Lilly and Company της έδωσε το εμπορικό όνομα Prozac. Το Φεβρουάριο του 1977, η Dista Products Company, θυγατρική της Eli Lilly & Company, υπέβαλε αίτημα εξέτασης χρήσεων της φλουοξετίνης στην FDA.[83]
Η φλουοξετίνη εμφανίστηκε στη βελγική αγορά το 1986.[84] Στις ΗΠΑ, η FDA έδωσε την τελική έγκρισή της τον Δεκέμβριο του 1987,[85] και ένα μήνα αργότερα η Eli Lilly άρχισε να εμπορεύεται το Prozac. Οι ετήσιες πωλήσεις στις ΗΠΑ έφτασαν τα 350 εκατομμύρια δολάρια εντός ενός έτους.[83] Οι παγκόσμιες πωλήσεις τελικά έφθασαν τα 2,6 δισεκατομμύρια δολάρια το χρόνο.[86]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Hubbard JR, Martin PR (2001). Substance Abuse in the Mentally and Physically Disabled (στα Αγγλικά). CRC Press. σελ. 26. ISBN 9780824744977.
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 2,7 «Fluoxetine Hydrochloride». The American Society of Health-System Pharmacists. Αρχειοθετήθηκε από το πρωτότυπο στις 8 Δεκεμβρίου 2015. Ανακτήθηκε στις 2 Δεκεμβρίου 2015.
- ↑ 3,0 3,1 3,2 3,3 3,4 «Prozac Label» (PDF). FDA. 2014. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 4 Μαρτίου 2016. Ανακτήθηκε στις 5 Απριλίου 2016.
- ↑ 4,0 4,1 4,2 «PROZAC® Fluoxetine Hydrochloride» (PDF). TGA eBusiness Services. Eli Lilly Australia Pty. Limited. 9 Οκτωβρίου 2013. Αρχειοθετήθηκε από το πρωτότυπο στις 25 Απριλίου 2017. Ανακτήθηκε στις 23 Νοεμβρίου 2013.
- ↑ 5,0 5,1 «Clinical pharmacokinetics of fluoxetine». Clinical Pharmacokinetics 26 (3): 201–14. March 1994. doi:. PMID 8194283.
- ↑ «Fluoxetine Pregnancy and Breastfeeding Warnings». Αρχειοθετήθηκε από το πρωτότυπο στις 31 Αυγούστου 2017. Ανακτήθηκε στις 2 Δεκεμβρίου 2015.
- ↑ Myers, Richard L. (2007). The 100 most important chemical compounds: a reference guide (1st έκδοση). Westport, Conn.: Greenwood Press. σελ. 128. ISBN 978-0-313-33758-1.
- ↑ World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. 2019. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ↑ «The Top 300 of 2020». ClinCalc. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ «Fluoxetine Hydrochloride - Drug Usage Statistics». ClinCalc. 23 Δεκεμβρίου 2019. Αρχειοθετήθηκε από το πρωτότυπο στις 11 Απριλίου 2020. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ Hagerman, Randi Jenssen (16 Σεπτεμβρίου 1999). Neurodevelopmental Disorders: Diagnosis and Treatment. Oxford University Press. ISBN 978-0-19-512314-2.
Dech and Budow (1991) were among the first to report the anecdotal use of fluoxetine in a case of PWS to control behavior problems, appetite, and trichotillomania.
- ↑ Truven Health Analytics, Inc. DrugPoint® System (Internet) [cited 2013 Oct 4]. Greenwood Village, CO: Thomsen Healthcare; 2013.
- ↑ Australian Medicines Handbook 2013. The Australian Medicines Handbook Unit Trust; 2013.
- ↑ British National Formulary (BNF) 65. Pharmaceutical Pr; 2013.
- ↑ «Fluoxetine Hydrochloride». The American Society of Health-System Pharmacists. Αρχειοθετήθηκε από το πρωτότυπο στις 11 Απριλίου 2011. Ανακτήθηκε στις 3 Απριλίου 2011.
- ↑ «NIMH•Eating Disorders». The National Institute of Mental Health. National Institute of Health. 2011. Αρχειοθετήθηκε από το πρωτότυπο στις 19 Αυγούστου 2011. Ανακτήθηκε στις 25 Νοεμβρίου 2013.
- ↑ Publishing, Harvard Health. «Treating social anxiety disorder». Harvard Health. Αρχειοθετήθηκε από το πρωτότυπο στις 23 Σεπτεμβρίου 2020. Ανακτήθηκε στις 15 Μαΐου 2019.
- ↑ «Selective serotonin reuptake inhibitors (SSRIs) for autism spectrum disorders (ASD)». The Cochrane Database of Systematic Reviews 8 (8): CD004677. August 2013. doi:. PMID 23959778.
- ↑ «The status of pharmacotherapy for autism spectrum disorders». Expert Opinion on Pharmacotherapy 8 (11): 1579–603. August 2007. doi:. PMID 17685878.
- ↑ «Pharmacotherapy to control behavioral symptoms in children with autism». Expert Opinion on Pharmacotherapy 13 (11): 1615–29. August 2012. doi:. PMID 22550944.
- ↑ «Pharmacotherapy of autism spectrum disorders». Brain & Development 35 (2): 119–27. February 2013. doi:. PMID 22541665.
- ↑ «Comparative efficacy and acceptability of 21 antidepressant drugs for the acute treatment of adults with major depressive disorder: a systematic review and network meta-analysis». Lancet 391 (10128): 1357–1366. April 2018. doi:. PMID 29477251.
- ↑ «Initial severity and antidepressant benefits: a meta-analysis of data submitted to the Food and Drug Administration». PLOS Medicine 5 (2): e45. February 2008. doi:. PMID 18303940.
- ↑ «Antidepressant drug effects and depression severity: a patient-level meta-analysis». JAMA 303 (1): 47–53. January 2010. doi:. PMID 20051569.
- ↑ «Benefits from antidepressants: synthesis of 6-week patient-level outcomes from double-blind placebo-controlled randomized trials of fluoxetine and venlafaxine». Archives of General Psychiatry 69 (6): 572–9. June 2012. doi:. PMID 22393205.
- ↑ «Selective serotonin reuptake inhibitors versus placebo in patients with major depressive disorder. A systematic review with meta-analysis and Trial Sequential Analysis». BMC Psychiatry 17 (1): 58. February 2017. doi:. PMID 28178949.
- ↑ «CG90 Depression in adults: full guidance». National Institute for Health and Care Excellence. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 9 Ιανουαρίου 2014.
- ↑ «Practice parameter for the assessment and treatment of children and adolescents with obsessive-compulsive disorder». Journal of the American Academy of Child and Adolescent Psychiatry 51 (1): 98–113. January 2012. doi:. PMID 22176943.
- ↑ «World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for the pharmacological treatment of eating disorders». The World Journal of Biological Psychiatry 12 (6): 400–43. September 2011. doi:. ISSN 1814-1412. PMID 21961502. Αρχειοθετήθηκε από το πρωτότυπο στις 1 August 2014. https://web.archive.org/web/20140801032832/http://www.wfsbp.org/fileadmin/user_upload/Treatment_Guidelines/Aigner_WFSBP_guidelines_eating_disorder_World_J_Biol_Psychia_11.pdf.
- ↑ «Pharmacotherapy in depressed children and adolescents». The World Journal of Biological Psychiatry 12 Suppl 1 (Suppl 1): 11–5. September 2011. doi:. PMID 21905988.
- ↑ «Should the use of selective serotonin reuptake inhibitors in child and adolescent depression be banned?». Psychotherapy and Psychosomatics 76 (1): 5–14. 2007. doi:. PMID 17170559.
- ↑ «Fluoxetine during pregnancy: impact on fetal development». Reproduction, Fertility, and Development 17 (6): 641–50. March 2005. doi:. PMID 16263070.
- ↑ 33,0 33,1 Brayfield, A, επιμ. (13 Αυγούστου 2013). Fluoxetine Hydrochloride. London, UK: Pharmaceutical Press. Ανακτήθηκε στις 24 Νοεμβρίου 2013.(απαιτείται συνδρομή)
- ↑ «Fluoxetine in pregnancy: slight risk of heart defects in unborn child» (PDF). MHRA. Medicines and Healthcare products Regulatory Agency. 10 Σεπτεμβρίου 2011. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 2 Δεκεμβρίου 2013. Ανακτήθηκε στις 23 Νοεμβρίου 2013.
- ↑ «The use of antidepressants in pregnant and breastfeeding women: a review of recent studies». Journal of Human Lactation 26 (2): 187–95. May 2010. doi:. PMID 19652194.
- ↑ The Maudsley prescribing guidelines in psychiatry. West Sussex: Wiley-Blackwell. 2012. ISBN 978-0-470-97948-8.
- ↑ «Rapid infusion of sodium bicarbonate and albumin into high-risk premature infants soon after birth: a controlled, prospective trial». American Journal of Obstetrics and Gynecology 124 (3): 263–7. February 1976. doi:. PMID 2013.
- ↑ Applied therapeutics: the clinical use of drugs (10th έκδοση). Baltimore: Wolters Kluwer Health/Lippincott Williams & Wilkins. 2012. ISBN 978-1609137137.
- ↑ «Clinical inquiry: How do antidepressants affect sexual function?». The Journal of Family Practice 62 (11): 660–1. November 2013. PMID 24288712. https://archive.org/details/sim_journal-of-family-practice_2013-11_62_11/page/660.
- ↑ «Persistent sexual dysfunction after discontinuation of selective serotonin reuptake inhibitors». The Journal of Sexual Medicine 5 (1): 227–33. January 2008. doi:. PMID 18173768.
- ↑ «Persistent sexual side effects after SSRI discontinuation». Psychotherapy and Psychosomatics 75 (3): 187–8. 2006. doi:. PMID 16636635. https://www.researchgate.net/publication/7143554. PDF also here (proof version)
- ↑ Publishing, Harvard Health. «Going off antidepressants». Harvard Health. Αρχειοθετήθηκε από το πρωτότυπο στις 26 Ιουνίου 2019. Ανακτήθηκε στις 26 Σεπτεμβρίου 2020.
- ↑ «A review of the management of antidepressant discontinuation symptoms». Therapeutic Advances in Psychopharmacology 5 (6): 357–68. December 2015. doi:. PMID 26834969.
- ↑ «Recognition and management of antidepressant discontinuation syndrome». J Psychiatry Neurosci 42 (4): 7–8. June 2017. doi:. PMID 28639936.
- ↑ «Antidepressant Discontinuation Syndrome». American Family Physician 74 (3): 449–56. 1 August 2006. PMID 16913164. https://archive.org/details/sim_american-family-physician_2006-08-01_74_3/page/449.
- ↑ «Antidepressant discontinuation syndrome». Canadian Medical Association Journal 189 (21): 747. 29 May 2017. doi:. PMID 28554948.
- ↑ «Antidepressants and Suicidality in Adults: Statistical Evaluation. (Presentation at Psychopharmacologic Drugs Advisory Committee; December 13, 2006)». Αρχειοθετήθηκε από το πρωτότυπο στις 27 Σεπτεμβρίου 2007. Ανακτήθηκε στις 13 Μαΐου 2007.
- ↑ 48,0 48,1 «Clinical Review: Relationship Between Antidepressant Drugs and Suicidality in Adults» (PDF). Overview for December 13 Meeting of Psychopharmacologic Drugs Advisory Committee (PDAC). FDA. 17 Νοεμβρίου 2006. σελίδες 11–74. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 16 Μαρτίου 2007. Ανακτήθηκε στις 22 Σεπτεμβρίου 2007.
- ↑ 49,0 49,1 «Statistical Evaluation of Suicidality in Adults Treated with Antidepressants» (PDF). Overview for December 13 Meeting of Psychopharmacologic Drugs Advisory Committee (PDAC). FDA. 17 Νοεμβρίου 2006. σελίδες 75–140. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 16 Μαρτίου 2007. Ανακτήθηκε στις 22 Σεπτεμβρίου 2007.
- ↑ «The flawed basis for FDA post-marketing safety decisions: the example of anti-depressants and children». Neuropsychopharmacology 31 (4): 689–99. April 2006. doi:. PMID 16395296.
- ↑ Hammad, Tarek A. (13 Σεπτεμβρίου 2004). «Results of the Analysis of Suicidality in Pediatric Trials of Newer Antidepressants». Presentation at the Meeting of Psychopharmacologic Drugs Advisory Committee and the Pediatric Advisory Committee on September 13, 2004. FDA. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 28 Φεβρουαρίου 2008.Pages 25, 28. Retrieved 6 January 2008.
- ↑ Committee on Safety of Medicines Expert Working Group (Δεκεμβρίου 2004). «Report on The Safety of Selective Serotonin Reuptake Inhibitor Antidepressants» (PDF). MHRA. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 28 Φεβρουαρίου 2008. Ανακτήθηκε στις 25 Σεπτεμβρίου 2007.
- ↑ «Selective serotonin reuptake inhibitors (SSRIs) and suicide in adults: meta-analysis of drug company data from placebo controlled, randomised controlled trials submitted to the MHRA's safety review». BMJ 330 (7488): 385. February 2005. doi:. PMID 15718537.
- ↑ Cubeddu, Luigi X. (2016). «Drug-induced Inhibition and Trafficking Disruption of ion Channels: Pathogenesis of QT Abnormalities and Drug-induced Fatal Arrhythmias». Current Cardiology Reviews 12 (2): 141–154. doi:. ISSN 1875-6557. PMID 26926294.
- ↑ Tisdale, James E. (May 2016). «Drug-induced QT interval prolongation and torsades de pointes: Role of the pharmacist in risk assessment, prevention and management». Canadian Pharmacists Journal 149 (3): 139–152. doi:. ISSN 1715-1635. PMID 27212965.
- ↑ «CredibleMeds :: Quicksearch». crediblemeds.org. Ανακτήθηκε στις 2 Σεπτεμβρίου 2019.
- ↑ «Fluoxetine». Fluoxetine. NCBI.
- ↑ Gury, C.; Cousin, F. (September 1999). «[Pharmacokinetics of SSRI antidepressants: half-life and clinical applicability]». L'Encephale 25 (5): 470–476. ISSN 0013-7006. PMID 10598311.
- ↑ Janicak, Philip G.· Marder, Stephen R. (26 Δεκεμβρίου 2011). Principles and Practice of Psychopharmacotherapy (στα Αγγλικά). Lippincott Williams & Wilkins. ISBN 978-1-4511-7877-7.
A 2-week interval is adequate for all of these drugs, with the exception of fluoxetine. Because of the extended half-life of norfluoxetine, a minimum of 5 weeks should lapse between stopping fluoxetine (20mg/day) and starting an MAOI. With higher daily doses, the interval should be longer.
- ↑ «Fluoxetine and ibuprofen Drug Interactions». Drugs.com. Αρχειοθετήθηκε από το πρωτότυπο στις 31 Αυγούστου 2017. Ανακτήθηκε στις 3 Μαρτίου 2017.
- ↑ «Fluoxetine increases norepinephrine release in rat hypothalamus as measured by tissue levels of MHPG-SO4 and microdialysis in conscious rats». Journal of Neural Transmission 104 (8–9): 953–66. 1997. doi:. PMID 9451727.
- ↑ «Fluoxetine, but not other selective serotonin uptake inhibitors, increases norepinephrine and dopamine extracellular levels in prefrontal cortex». Psychopharmacology 160 (4): 353–61. April 2002. doi:. PMID 11919662. https://archive.org/details/sim_psychopharmacology_2002-04_160_4/page/353.
- ↑ «R-fluoxetine increases extracellular DA, NE, as well as 5-HT in rat prefrontal cortex and hypothalamus: an in vivo microdialysis and receptor binding study». Neuropsychopharmacology 27 (6): 949–59. December 2002. doi:. PMID 12464452.
- ↑ 64,0 64,1 «SSRIs act as selective brain steroidogenic stimulants (SBSSs) at low doses that are inactive on 5-HT reuptake». Current Opinion in Pharmacology 9 (1): 24–30. February 2009. doi:. PMID 19157982.
- ↑ «alpha(2)-Adrenoceptors mediate the acute inhibitory effect of fluoxetine on locus coeruleus noradrenergic neurons». Neuropharmacology 56 (6–7): 1068–73. 2009. doi:. PMID 19298831.
- ↑ «Interactions of selective serotonin reuptake inhibitors with the serotonin 5-HT2c receptor». Psychopharmacology 126 (3): 234–40. August 1996. doi:. PMID 8876023. http://link.springer.de/link/service/journals/00213/bibs/6126003/61260234.htm.
- ↑ «Neuroactive steroids and stress axis regulation: Pregnancy and beyond». The Journal of Steroid Biochemistry and Molecular Biology 160: 160–8. June 2016. doi:. PMID 26259885.
- ↑ 68,0 68,1 «Fluoxetine increases GABA(A) receptor activity through a novel modulatory site». The Journal of Pharmacology and Experimental Therapeutics 304 (3): 978–84. March 2003. doi:. PMID 12604672. https://archive.org/details/sim_journal-of-pharmacology-and-experimental-therapeutics_2003-03_304_3/page/978.
- ↑ «Interactions of selective serotonin reuptake inhibitors with subtypes of sigma receptors in rat brain». European Journal of Pharmacology 307 (1): 117–9. June 1996. doi:. PMID 8831113.
- ↑ «Sigma-1 receptors and selective serotonin reuptake inhibitors: clinical implications of their relationship». Central Nervous System Agents in Medicinal Chemistry 9 (3): 197–204. September 2009. doi:. PMID 20021354.
- ↑ «Fluoxetine». IUPHAR Guide to Pharmacology. IUPHAR. Αρχειοθετήθηκε από το πρωτότυπο στις 10 Νοεμβρίου 2014. Ανακτήθηκε στις 10 Νοεμβρίου 2014.
- ↑ «Calcium activated chloride channel». IUPHAR Guide to Pharmacology. IUPHAR. Αρχειοθετήθηκε από το πρωτότυπο στις 10 Νοεμβρίου 2014. Ανακτήθηκε στις 10 Νοεμβρίου 2014.
- ↑ 73,0 73,1 «Prozac Pharmacology, Pharmacokinetics, Studies, Metabolism». RxList.com. 2007. Αρχειοθετήθηκε από το πρωτότυπο στις 10 Απριλίου 2007. Ανακτήθηκε στις 14 Απριλίου 2007.
- ↑ «Fluoxetine metabolism and pharmacological interactions: the role of cytochrome p450». Current Drug Metabolism 7 (2): 127–33. February 2006. doi:. PMID 16472103.
- ↑ «Pharmacokinetics of selective serotonin reuptake inhibitors». Pharmacology & Therapeutics 85 (1): 11–28. January 2000. doi:. PMID 10674711.
- ↑ 76,0 76,1 «Weekly dosing of fluoxetine for the continuation phase of treatment of major depression: results of a placebo-controlled, randomized clinical trial». Journal of Clinical Psychopharmacology 20 (4): 423–7. August 2000. doi:. PMID 10917403.
- ↑ «Drug Treatments in Psychiatry: Antidepressants». Newcastle University School of Neurology, Neurobiology and Psychiatry. 2005. Αρχειοθετήθηκε από το πρωτότυπο στις 17 Απριλίου 2007. Ανακτήθηκε στις 14 Απριλίου 2007.
- ↑ 78,0 78,1 «Augmentation of fluoxetine's antidepressant action by pindolol: analysis of clinical, pharmacokinetic, and methodologic factors». Journal of Clinical Psychopharmacology 21 (1): 36–45. February 2001. doi:. PMID 11199945.
- ↑ «Fluoxetine and norfluoxetine plasma concentrations during relapse-prevention treatment». Journal of Affective Disorders 68 (2–3): 243–9. April 2002. doi:. PMID 12063152.
- ↑ 80,0 80,1 «A comparison of brain and serum pharmacokinetics of R-fluoxetine and racemic fluoxetine: A 19-F MRS study». Neuropsychopharmacology 30 (8): 1576–83. August 2005. doi:. PMID 15886723.
- ↑ «Prozac (fluoxetine, Lilly 110140), the first selective serotonin uptake inhibitor and an antidepressant drug: twenty years since its first publication». Life Sciences 57 (5): 411–41. 1995. doi:. PMID 7623609. https://archive.org/details/sim_life-sciences_1995_57_5/page/411.
- ↑ «A selective inhibitor of serotonin uptake: Lilly 110140, 3-(p-trifluoromethylphenoxy)-N-methyl-3-phenylpropylamine». Life Sciences 15 (3): 471–9. August 1974. doi:. PMID 4549929.
- ↑ 83,0 83,1 Breggin, Peter R.· Breggin, Ginger Ross (1995). Talking Back to Prozac. Macmillan Publishers. σελίδες 1–2. ISBN 978-0-312-95606-6.
- ↑ Swiatek, Jeff (2 August 2001). «Prozac's profitable run coming to an end for Lilly». The Indianapolis Star. Αρχειοθετήθηκε από το πρωτότυπο στις 18 August 2007. https://web.archive.org/web/20070818163109/http://www2.indystar.com/library/factfiles/business/companies/lilly/stories/2001_0802.html.
- ↑ «Electronic Orange Book». Food and Drug Administration. Απριλίου 2007. Αρχειοθετήθηκε από το πρωτότυπο στις 20 Αυγούστου 2007. Ανακτήθηκε στις 24 Μαΐου 2007.
- ↑ Simons, John (28 Ιουνίου 2004). «Lilly Goes Off Prozac The drugmaker bounced back from the loss of its blockbuster, but the recovery had costs». Fortune Magazine. Αρχειοθετήθηκε από το πρωτότυπο στις 26 Απριλίου 2016. Ανακτήθηκε στις 26 Σεπτεμβρίου 2020.
