AIDS: Διαφορά μεταξύ των αναθεωρήσεων
| Γραμμή 227: | Γραμμή 227: | ||
== Πρόληψη == |
== Πρόληψη == |
||
=== Σεξουαλική επαφή === |
=== Σεξουαλική επαφή === |
||
Η |
Η σταθερή χρήση [[προφυλακτικό|προφυλακτικού]] μειώνει τον κίνδυνο μετάδοσης HIV περίπου στο 80% μακροπρόθεσμα.<ref>{{cite journal|last=Crosby|first=R|coauthors=Bounse, S|title=Condom effectiveness: where are we now?|journal=Sexual health|date=2012 Mar|volume=9|issue=1|pages=10–7|pmid=22348628|doi=10.1071/SH11036}}</ref> |
||
Σε περιπτώσεις όπου ο ένας παρτενέρ στο ζευγάρι είναι μολυσμένος η συνεχής χρήση του προφυλακτικού έχει ως αποτέλεσμα ποσοστά μετάδοσης στο μη μολυσμένο σύντροφο κάτω από 1% ανά έτος[ |
Σε περιπτώσεις όπου ο ένας παρτενέρ στο ζευγάρι είναι μολυσμένος η συνεχής χρήση του προφυλακτικού έχει ως αποτέλεσμα ποσοστά μετάδοσης στο μη μολυσμένο σύντροφο κάτω από 1% ανά έτος.<ref name=WHOCondoms>{{cite web| publisher=[[World Health Organization|WHO]]| month=August | year=2003|url=http://www.wpro.who.int/mediacentre/factsheets/fs_200308_Condoms/en/index.html | title=Condom Facts and Figures|accessdate=January 17, 2006 }}</ref> Κάποια δεδομένα υποστηρίζουν την ισοδύναμη αποτελεσματικότητα του [[γυναικείο προφυλακτικό|γυναικείου προφυλακτικού]] σε σχέση με τα (ανδρικά) προφυλακτικά από [[λάτεξ]],<ref>{{cite journal|last=Gallo|first=MF|coauthors=Kilbourne-Brook, M; Coffey, PS|title=A review of the effectiveness and acceptability of the female condom for dual protection|journal=Sexual health|date=2012 Mar|volume=9|issue=1|pages=18–26|pmid=22348629|doi=10.1071/SH11037}}</ref> παρ' όλα αυτά οι μαρτυρίες γι’ αυτό δεν έχουν οριστικοποιηθεί. |
||
Η χρήση [[κολπικό τζελ|κολπικού τζελ]] που περιέχει [[tenofovir]] (έναν [[αναστολέας της αντίστροφης μεταγραφάσης|αναστολέα της αντίστροφης μεταγραφάσης]]) λίγο πριν το σεξ φαίνεται να μειώνει τα ποσοστά μόλυνσης σε 40% στις Αφρικανές γυναίκες.<ref name=VagGel2012>{{cite journal|last=Celum|first=C|coauthors=Baeten, JM|title=Tenofovir-based pre-exposure prophylaxis for HIV prevention: evolving evidence|journal=Current opinion in infectious diseases|date=2012 Feb|volume=25|issue=1|pages=51–7|pmid=22156901|doi=10.1097/QCO.0b013e32834ef5ef|pmc=3266126}}</ref> Αντίθετα, η χρήση του [[σπερματοκτόνο|σπερματοκτόνου]] [[nonoxynol-9]] μπορεί να αυξήσει τον κίνδυνο μετάδοσης λόγω του γεγονότος ότι προκαλεί κολπικό και πρωκτικό ερεθισμό.<ref>{{cite journal|last=Baptista|first=M|coauthors=Ramalho-Santos, J|title=Spermicides, microbicides and antiviral agents: recent advances in the development of novel multi-functional compounds|journal=Mini reviews in medicinal chemistry|date=2009-11-01|volume=9|issue=13|pages=1556–67|pmid=20205637|doi=10.2174/138955709790361548}}</ref> |
|||
Η χρήση του σπερματοκτόνου nonoxynol-9 μπορεί να αυξήσει τον κίνδυνο μετάδοσης λόγω του γεγονότος ότι προκαλεί κολπικό και λοίμωξης σε ετεροφυλόφιλους άνδρες σε ένα ποσοστό ανάμεσα στο 38 και 66% σε διάστημα 2 ετών (από άλλες μελέτες) [75]. |
|||
Η [[περιτομή]] στην Υποσαχάρια Αφρική μειώνει την μόλυνση από HIV σε ετεροφυλόφιλους άνδρες σε ένα ποσοστό ανάμεσα στο 38 και 66% σε διάστημα 2 ετών.<ref>{{cite journal|last=Siegfried|first=N|coauthors=Muller, M; Deeks, JJ; Volmink, J|title=Male circumcision for prevention of heterosexual acquisition of HIV in men|journal=Cochrane database of systematic reviews (Online)|date=2009-04-15|issue=2|pages=CD003362|pmid=19370585|doi=10.1002/14651858.CD003362.pub2|editor1-last=Siegfried|editor1-first=Nandi}}</ref> Με βάση αυτές τις μελέτες, το 2007 ο Παγκόσμιος Οργανισμός Υγείας και ο UNAIDS (Οργανισμός των Ηνωμένων Εθνών για το AIDS) συνέστησαν την ανδρική περιτομή σαν μέσο πρόληψης της μετάδοσης από γυναίκα σε άνδρα μέσα στο 2007.<ref>{{cite web |title=WHO and UNAIDS announce recommendations from expert consultation on male circumcision for HIV prevention |publisher=World Health Organization |date=Mar 28, 2007|url=http://www.who.int/mediacentre/news/releases/2007/pr10/en/index.html}}</ref> Το αν η περιτομή προστατεύει και από τη μετάδοση από άνδρα σε γυναίκα είναι αμφισβητήσιμο,<ref>{{cite journal|last=Larke|first=N|title=Male circumcision, HIV and sexually transmitted infections: a review|journal=British journal of nursing (Mark Allen Publishing)|date=2010 May 27 – Jun 9|volume=19|issue=10|pages=629–34|pmid=20622758}}</ref><ref>{{cite journal|last=Eaton|first=L|coauthors=Kalichman, SC|title=Behavioral aspects of male circumcision for the prevention of HIV infection|journal=Current HIV/AIDS reports|date=2009 Nov|volume=6|issue=4|pages=187–93|pmid=19849961|doi=10.1007/s11904-009-0025-9}}(subscription required)</ref> και επίσης το αν είναι προς όφελος των ανδρών που κάνουν σεξ με άνδρες στις ανεπτυγμένες χώρες δεν έχει καθοριστεί. <ref>{{cite journal|last=Kim|first=HH|coauthors=Li, PS, Goldstein, M|title=Male circumcision: Africa and beyond?|journal=Current opinion in urology|date=2010 Nov|volume=20|issue=6|pages=515–9|pmid=20844437|doi=10.1097/MOU.0b013e32833f1b21}}</ref><ref>{{cite journal|last=Templeton|first=DJ|coauthors=Millett, GA, Grulich, AE|title=Male circumcision to reduce the risk of HIV and sexually transmitted infections among men who have sex with men|journal=Current opinion in infectious diseases|date=2010 Feb|volume=23|issue=1|pages=45–52|pmid=19935420|doi=10.1097/QCO.0b013e328334e54d}}</ref><ref>{{Cite journal | last1 = Wiysonge | first1 = CS. | last2 = Kongnyuy | first2 = EJ. | last3 = Shey | first3 = M. | last4 = Muula | first4 = AS.|last5 = Navti | first5 = OB. | last6 = Akl | first6 = EA. | last7 = Lo | first7 = YR. | title = Male circumcision for prevention of homosexual acquisition of HIV in men | journal = Cochrane Database Syst Rev | volume = | issue = 6 | pages = CD007496 | month = | year = 2011 | doi = 10.1002/14651858.CD007496.pub2 | pmid = 21678366 | editor1-last = Wiysonge |editor1-first = Charles Shey }}</ref> Women who have undergone [[female genital cutting]] have an increased risk of HIV.<ref>{{Cite journal|author=Utz-Billing I, Kentenich H|title=Female genital mutilation: an injury, physical and mental harm |journal=J Psychosom Obstet Gynaecol |volume=29|issue=4 |pages=225–9|year=2008 |month=December |pmid=19065392 |doi=10.1080/01674820802547087 |url=}}</ref> |
|||
| ⚫ | Μερικοί ειδικοί πιστεύουν ότι η μειωμένη αντίληψη ευπάθειας (δηλαδή κινδύνου μόλυνσης) που μπορεί να έχουν οι περιτετμημένοι άνδρες, μπορεί να τους οδηγήσει σε υψηλότερου κινδύνου σεξουαλική συμπεριφορά και έτσι να ακυρώσει τα προληπτικά αποτελέσματα της περιτομής τους.<ref>{{Cite journal|author=Eaton LA, Kalichman S |title=Risk compensation in HIV prevention: implications for vaccines, microbicides, and other biomedical HIV prevention technologies |journal=Curr HIV/AIDS Rep |volume=4 |issue=4 |pages=165–72 |year=2007|month=December|pmid=18366947|pmc=2937204 |doi=10.1007/s11904-007-0024-7}}</ref> Γυναίκες που έχουν υποστεί [[ακρωτηριασμός των γυναικείων γεννητικών οργάνων|ακρωτηριασμό των εξωτερικών γεννητικών τους οργάνων]], όπως [[κλειτοριδεκτομή]], διατρέχουν αυξημένο κίνδυνο να μολυνθούν με HIV.<ref>{{Cite journal|author=Utz-Billing I, Kentenich H|title=Female genital mutilation: an injury, physical and mental harm |journal=J Psychosom Obstet Gynaecol |volume=29|issue=4 |pages=225–9|year=2008 |month=December |pmid=19065392 |doi=10.1080/01674820802547087 |url=}}</ref> |
||
| ⚫ | Μερικοί ειδικοί πιστεύουν ότι |
||
=== Πρόληψη πριν από την έκθεση === |
=== Πρόληψη πριν από την έκθεση === |
||
Έκδοση από την 22:31, 13 Δεκεμβρίου 2012
| Αυτό το λήμμα χρειάζεται επιμέλεια ώστε να ανταποκρίνεται σε υψηλότερες προδιαγραφές ορθογραφικής και συντακτικής ποιότητας ή μορφοποίησης. Αίτιο: εσωτερικοί σύνδεσμοι, παραπομπές Για περαιτέρω βοήθεια, δείτε τα λήμματα πώς να επεξεργαστείτε μια σελίδα και τον οδηγό μορφοποίησης λημμάτων. |
| AIDS | |
|---|---|
 Η κόκκινη κορδέλα, σύμβολο αλληλεγγύης με τους φορείς και αυτούς που νοσούν από AIDS | |
| Ειδικότητα | λοιμωξιολογία |
| Συμπτώματα | πυρετός[1], αδενοπάθεια[1], διάρροια[1], λήθαργος[1], απώλεια σωματικού βάρους[1], εξάνθημα[2], Ευκαιριακή λοίμωξη, Σάρκωμα Καπόσι, λέμφωμα, peripheral neuropathy, night sweats[2], μυαλγία[2], Πονόλαιμος[2], κόπωση[2], λεμφαδενική διόγκωση[2], στοματικό έλκος[2] και ρίγος[2] |
| Ταξινόμηση | |
| ICD-10 | B20 – B24 |
| ICD-9 | 042-044 |
| OMIM | 609423 |
| DiseasesDB | 5938 |
| MedlinePlus | 000594 |
| eMedicine | emerg/253 |
| MeSH | D000163 |
Η λοίμωξη με τον Ιό Ανθρώπινης Ανοσοανεπάρκειας (Human Immunodeficiency Virus Infection) και το Σύνδρομο Επίκτητης Ανοσοανεπάρκειας (AIDS) είναι μια νόσος του ανθρώπινου ανοσοποιητικού συστήματος που προκαλείται από τον ιό της ανθρώπινης ανοσοανεπάρκειας (HIV).[3] Η νόσος παρεμβαίνει στο ανοσοποιητικό σύστημα και παρεμποδίζει τη λειτουργία του, κάνοντας τα άτομα με AIDS περισσότερο πιθανά να αποκτήσουν λοιμώξεις, όπως ευκαιριακές λοιμώξεις και όγκους που συνήθως δεν προσβάλουν τα άτομα με λειτουργικά ανοσοποιητικά συστήματα. Αυτή η ευπάθεια χειροτερεύει με την εξέλιξη της νόσου.
Ο HIV μεταδίδεται πρωταρχικά με τη σεξουαλική επαφή, όπως με το πρωκτικό, κολπικό ή στοματικό σεξ, τη μετάγγιση αίματος, τις μολυσμένες υποδερμικές βελόνες, και από τη μητέρα στο παιδί κατά την εγκυμοσύνη, τον τοκετό και τον θηλασμό.[4] Ορισμένα σωματικά υγρά όπως το σάλιο, τα δάκρυα, τα ούρα και ο ιδρώτας δεν μεταδίδουν τον HIV εκτός εάν περιέχουν μικροποσότητες αίματος.[5] Ο ιός μπορεί να μεταδοθεί επίσης από επαφή ενός βλεννογόνου (δηλ. μιας βλεννώδους μεμβράνης που επικαλύπτει κάποιες κοιλότητες του σώματος, όπως ο βλεννογόνος του στόματος ή του εντέρου) με ένα σωματικό υγρό που περιέχει τον ιό, όπως αίμα, σπέρμα, κολπικά υγρά, προσπερματικά υγρά ή γάλα θηλασμού ενός μολυσμένου ατόμου.
Η προφύλαξη από την HIV λοίμωξη, πρωταρχικά μέσω του ασφαλούς σεξ και των προγραμμάτων ανταλλαγής συρίγγων και βελονών, αποτελεί στρατηγική κλειδί για τον έλεγχο της νόσου. Δεν υπάρχει θεραπεία ίασης ή προληπτικό εμβόλιο. Παρόλα αυτά η αντιρετροϊκή θεραπεία μπορεί να επιβραδύνει την εξέλιξη της νόσου και να οδηγήσει σε ένα προσδόκιμο ζωής κοντά στο φυσιολογικό. Παρότι η θεραπεία αυτή μειώνει τον κίνδυνο θανάτου και επιπλοκών από τη νόσο, τα φάρμακα αυτά είναι υψηλού κόστους και σχετίζονται με παρενέργειες οφειλόμενες αποκλειστικά σε αυτά (οι οποίες πολλές φορές συνδυάζονται με τις παρενέργειες που προκαλεί η χρόνια HIV λοίμωξη).
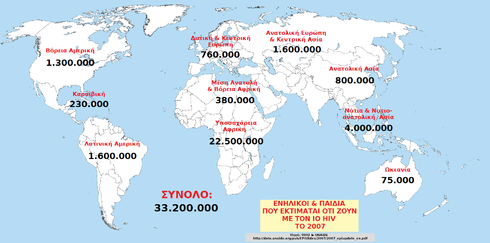
Ο ιός και η νόσος αναφέρονται συχνά μαζί ως HIV/AIDS. Η νόσος είναι τεράστιο πρόβλημα υγείας σε πολλά μέρη του κόσμου, και θεωρείται πανδημία, δηλαδή μία έκρηξη της ασθένειας που επηρεάζει μια ευρεία περιοχή και εξαπλώνεται ενεργά.[6] Το 2010 περίπου 34 εκατομμύρια άνθρωποι είχαν HIV λοίμωξη παγκοσμίως.[7] Από αυτούς περίπου 16,8 εκατομμύρια είναι γυναίκες και 3,4 εκατομμύρια είναι κάτω από 15 ετών.[7] Το αποτέλεσμα είναι περίπου 1,8 εκατομμύρια θάνατοι από AIDS το 2010, χαμηλότερα σε σχέση με τα 3,1 εκατομμύρια θανάτους του 2001.[7] Από το 1981, που το AIDS αναγνωρίστηκε για πρώτη φορά, έως το 2009 προκάλεσε σχεδόν 30 εκατομμύρια θανάτους.[8]
Η γενετική έρευνα δείχνει ότι ο HIV προήλθε από την Κεντροδυτική Αφρική κατά τη διάρκεια των αρχών του 20ου αιώνα.[9] Το AIDS αναγνωρίστηκε για πρώτη φορά από τα Κέντρα Ελέγχου και Πρόληψης Νοσημάτων των Ηνωμένων Πολιτειών το 1981 και η αιτία του, ο HIV, αναγνωρίστηκε στις αρχές τις δεκαετίας του 1980.[10]
Γενική περιγραφή
Ο ιός HIV προσκολλάται στο δέκτη CD4 που βρίσκεται στα Τ-λεμφοκύτταρα καθώς και στα μακροφάγα. Το RNA του ιού αυτού μπαίνει στο κύτταρο του ξενιστή όπου και αντιγράφεται με τη βοήθεια της αντίστροφης μεταγραφάσης σε DNA. Αυτό πλέον το DNA του ιού ενσωματώνεται με το DNA των χρωμοσωμάτων του ξενιστή. Από εκεί και πέρα μπορεί πλέον ο ιός να ελέγξει τη παραγωγή νέων σωματίων HIV που εξέρχονται από το αρχικά προσβαλλόμενο κύτταρο του ξενιστή. Εναλλακτικά το ενσωματωμένο DNA μπορεί ακόμα να μείνει αδρανές και να μην εντοπιστεί από το ανοσοποιητικό σύστημα. Ο HIV αποφεύγει σταθερά την ανοσοαπόκριση παραμένοντας στα κενοτόπια μέσα στα μακροφάγα. Σημειώνεται επίσης ότι ο HIV μπορεί να δεχθεί υψηλά ποσοστά αντιγονικής ποικιλότητας επειδή σφάλματα κατά την αντιγραφή του RNA του ιού σε DNA προκαλούν μεγάλες αλλαγές στη φύση των περιβαλλουσών πρωτεϊνών του ιού. Αν και ένα μικρό ποσοστό φορέων του HIV (περίπου 1 στους 500) δεν αναπτύσσουν AIDS,[11] όλοι οι φορείς του HIV μπορούν να μεταδώσουν τον ιό. Ο μέσος χρόνος από της προσβολής από τον ιό και της εμφάνισης του AIDS είναι περίπου 10 χρόνια.
Τελικά το προσβληθέν άτομο υποκύπτει σε διάφορες λοιμώξεις, επειδή ακριβώς η σταδιακή μείωση του αριθμού των CD4 Τ-λεμφοκυττάρων έχει ως αποτέλεσμα την αστοχία του ανοσοποιητικού συστήματος. Μέχρι σήμερα δεν έχει ανακαλυφθεί εμβόλιο κυρίως επειδή ο ιός παρουσιάζει μεγάλη ικανότητα να μεταλλάσσεται ραγδαία και συνεπώς μεγάλη ικανότητα αποφυγής του ανοσοποιητικού συστήματος. Οι έρευνες δημιουργίας ενός τέτοιου εμβολίου συνεχίζονται από πλήθος επιστημονικών εργαστηρίων. Μέχρι τελευταία (2005) έχει χρησιμοποιηθεί η αζινοθυμιδίνη (ΑΖΤ) που ως αντιρετροϊκό φάρμακο εμποδίζει την αντιγραφή του ιού και επομένως τον πολλαπλασιαμσό του, πλην όμως παρουσιάζει πολλές παρενέργειες. Παράλληλα έχει χρησιμοποιηθεί και η ακτινοθεραπεία που επίσης δημιουργεί πολλές παρενέργειες.
Σημεία και συμπτώματα
Υπάρχουν 3 κύρια στάδια της HIV λοίμωξης: η οξεία λοίμωξη, η κλινική λανθάνουσα περίοδος και το AIDS.[12][13]
Οξεία λοίμωξη

Η αρχική περίοδος μετά τη μόλυνση με HIV ονομάζεται οξεία HIV λοίμωξη ή πρώιμη HIV λοίμωξη ή οξύ ρετροϊκό σύνδρομο.[12][14] Πολλά άτομα αναπτύσσουν ένα σύνδρομο παρόμοιο με γρίπη ή με λοιμώδη μονοπυρήνωση 2-4 εβδομάδες μετά την έκθεσή τους στον ιό, ενώ άλλα άτομα δεν έχουν κάποια αξιοσημείωτα συμπτώματα.[15][16] Πάντως στο 40-90% των περιπτώσεων παρουσιάζονται συμπτώματα που συνηθέστατα περιλαμβάνουν: πυρετό, διογκωμένους και ευαίσθητους (με πόνο) λεμφαδένες, φλεγμονή στο λαιμό (φαρυγγίτιδα, οισοφαγίτιδα), εξάνθημα στο δέρμα, πονοκέφαλο και έλκη (πληγές) στο στόμα και τα γεννητικά όργανα.[14][16] Δεν σημαίνει βέβαια ότι όποιος παρουσιάσει συμπτώματα θα παρουσιάσει όλα αυτά μαζί. Μπορεί να έχει μόνο ένα από αυτά ή κάποια από αυτά.
Το εξάνθημα εμφανίζεται στο 20-50% των περιπτώσεων και κλασσικά είναι κηλιδοβλατιδώδες (με κηλίδες και βλατίδες, που είναι βλάβες του δέρματος συνήθως κόκκινης απόχρωσης) και παρουσιάζεται στον κορμό.[17] Μερικοί άνθρωποι αναπτύσσουν επίσης ευκαιριακές λοιμώξεις σε αυτό το στάδιο.[14]
Άλλα συμπτώματα μπορεί να περιλαμβάνουν: ναυτία, εμετό, διάρροια και νευρολογικά προβλήματα όπως περιφερική νευροπάθεια και σύνδρομο Guillain-Barre (σπάνια νόσος με παράλυση περιφερικών νεύρων από λανθασμένη επίθεση του ανοσοποιητικού στο νευρικό σύστημα).[16] H διάρκεια των συμπτωμάτων ποικίλλει, αλλά συνήθως είναι 1 με 2 εβδομάδες.[16]
Λόγω της μη ειδικής φύσεως αυτών των συμπτωμάτων, συχνά δεν αναγνωρίζονται ως σημάδια μιας HIV λοίμωξης. Ακόμη κι αν το άτομο πάει στο γιατρό του ή σε νοσοκομείο, συχνά θα του γίνει η λάθος διάγνωση ότι πρόκειται για κάποια από τις κοινές λοιμώξεις που παρουσιάζουν ίδια συμπτώματα. Έτσι συνιστάται να εξετάζεται και η HIV λοίμωξη σαν ενδεχόμενο σε όσους παρουσιάζουν ανεξήγητο πυρετό και έχουν παράγοντες κινδύνου για HIV λοίμωξη.[16]
Κλινική λανθάνουσα περίοδος
Μετά από τα αρχικά συμπτώματα της οξείας φάσης η HIV λοίμωξη μπαίνει σε ένα στάδιο που ονομάζεται κλινική λανθάνουσα περίοδος ή ασυμπτωματική HIV λοίμωξη ή χρόνια HIV λοίμωξη.[13] Χωρίς αντιρετροϊκή αγωγή το δεύτερο αυτό στάδιο διαρκεί κατά μέσο όρο 8 χρόνια[18], όμως μπορεί να κυμανθεί από 3 χρόνια[19] έως και περισσότερα από 20.[20] Ενώ τυπικά σε αυτή τη φάση δεν υπάρχουν συμπτώματα ή υπάρχουν ελάχιστα, κατά το τέλος αυτής της περιόδου πολλά άτομα αναπτύσσουν πυρετό, απώλεια βάρους, γαστρεντερικά συμπτώματα και πόνο στους μύες.[13]
Ένα ποσοστό 50-70% των ατόμων αναπτύσσουν επίσης επίμονη γενικευμένη λεμφαδενοπάθεια με διογκωμένους αλλά χωρίς πόνο λεμφαδένες που εμφανίζονται σε δύο διαφορετικές περιοχές του σώματος και για περισσότερο από 3-6 μήνες, χωρίς να μπορεί να βρεθεί κάποια άλλη αιτία για την παρουσία τους.[12]
Ένα μικρό ποσοστό (περίπου 5%) ατόμων που έχουν μολυνθεί με τον HIV-1 διατηρούν υψηλά επίπεδα CD4 χωρίς αντιρετροϊκή θεραπεία για περισσότερα από 5 χρόνια.[16][21] Παρόλα αυτά οι περισσότεροι από αυτούς έχουν ανιχνεύσιμο ιικό φορτίο και τελικά θα αναπτύξουν AIDS χωρίς την αντιρετροϊκή αγωγή.[21] Αυτά τα άτομα κατατάσσονται στην κατηγορία που ονομάζεται HIV ελεγκτές (HIV controllers) ή μακροχρόνια μη-εξελισσόμενοι (long term nonprogressors – LTNP).[21] Άνθρωποι που χωρίς αντιρετροϊκή θεραπεία διατηρούν υψηλά επίπεδα CD4 και ταυτόχρονα χαμηλό ή μη ανιχνεύσιμο ιικό φορτίο, είναι γνωστοί ως εξέχοντες ελεγκτές (elite controllers) ή εξέχοντες καταστολείς (elite suppressors).[21]
AIDS

Ορίζεται ότι κάποιος έχει αναπτύξει AIDS είτε όταν τα CD4 κύτταρά του είναι σε αριθμό λιγότερα από 200/μL (μικρολίτρο) αίματος, είτε όταν εκδηλωθεί η παρουσία συγκεκριμένων νόσων που συσχετίζονται με την προχωρημένη HIV λοίμωξη.[16] Περίπου οι μισοί από τους ανθρώπους που έχουν μολυνθεί με HIV θα αναπτύξουν AIDS σε 10 χρόνια αν δεν λάβουν θεραπεία.[16] Οι πιο κοινές αρχικές καταστάσεις που σημαίνουν συναγερμό για την εμφάνιση AIDS είναι η πνευμονία από πνευμονοκύστη (PCP) σε ποσοστό 40%, το σύνδρομο απίσχνασης (αδυνατίσματος) από HIV και η οισοφαγική καντιντίαση (μυκητίαση από το μύκητα candida).[16] Άλλες κοινές εκδηλώσεις AIDS περιλαμβάνουν τις υποτροπιάζουσες λοιμώξεις του αναπνευστικού[16] (όπως η πνευμονία).
Οι ευκαιριακές λοιμώξεις στις οποίες περιλαμβάνονται οι παραπάνω καταστάσεις μπορεί να προκαλούνται από βακτηρίδια, ιούς, μύκητες και παράσιτα, που σε φυσιολογικές συνθήκες ελέγχονται από ένα υγιές ανοσοποιητικό σύστημα.[22] Ποιες ακριβώς λοιμώξεις θα εμφανιστούν εξαρτάται εν μέρει από το ποιοι από αυτούς τους μικροοργανισμούς είναι περισσότερο κοινοί και διαδεδομένοι στο περιβάλλον του ατόμου.[16] Οι λοιμώξεις αυτές μπορούν να επηρεάσουν σχεδόν όλα τα συστήματα του οργανισμού.[23]
Τα άτομα με AIDS διατρέχουν αυξημένο κίνδυνο να αναπτύξουν διάφορους καρκίνους που προκαλούνται από ιούς. Σε αυτούς συμπεριλαμβάνονται το σάρκωμα Kaposi, το λέμφωμα Burkitt, το πρωτοπαθές λέμφωμα εγκεφάλου και ο καρκίνος του τραχήλου της μήτρας.[17] Το σάρκωμα Kaposi είναι ο πιο κοινός καρκίνος και εμφανίζεται στο 10-20% των ανθρώπων με HIV λοίμωξη.[24] Ο δεύτερος πιο κοινός καρκίνος είναι το λέμφωμα και ευθύνεται σχεδόν για το 16% των θανάτων στα άτομα που αναπτύσσουν AIDS ενώ αποτελεί το πρώτο εμφανιζόμενο σημείο AIDS στο 3-4% των περιπτώσεων αυτών.ref name=M169/> Και οι δύο αυτοί καρκίνοι συσχετίζονται με τον ανθρώπινο ερπητοϊό 8.[24]
Ο καρκίνος του τραχήλου της μήτρας παρουσιάζεται συχνότερα στις γυναίκες με AIDS λόγω της σχέσης του με τον ιό των ανθρωπίνων θηλωμάτων (HPV) που ανάλογα με τον υπότυπο προκαλεί κονδυλώματα, μυρμηκίες κλπ. Όταν μια γυναίκα έχει μολυνθεί κάποια στιγμή στη ζωή της με τον υπότυπο του HPV που προκαλεί κονδυλώματα στον τράχηλο της μήτρας, αυτά μπορεί να εξελιχθούν σε καρκίνο αν δεν θεραπευτούν, αλλά μετά από πολλά χρόνια. Αν όμως συνυπάρχει στη γυναίκα HIV λοίμωξη για την οποία δεν λαμβάνεται θεραπεία, η εξέλιξη αυτή επιταχύνεται και αν αναπτυχθεί AIDS είναι πολύ πιθανή.
Ο HPV είναι ένας κατεξοχήν σεξουαλικά μεταδιδόμενος ιός και υπάρχει στο 95% των σεξουαλικά ενεργών ανθρώπων, αφού μεταδίδεται πολύ εύκολα, ακόμη και με την τριβή των γεννητικών οργάνων ή της περιοχής του πρωκτού. Ο υπότυπος του HPV που προκαλεί τα κονδυλώματα προσβάλλει πολλές φορές και την περιοχή του πρωκτού και του ορθού εντέρου (του τελευταίου τμήματος του παχέος εντέρου) και έτσι αυτά μπορεί να εμφανιστούν και σε άντρες ή γυναίκες που έχουν πρωκτικές σεξουαλικές επαφές. Σε αυτές της περιπτώσεις ισχύει η ίδια εξέλιξη: αν δεν θεραπευτούν αποτελεσματικά μπορεί μελλοντικά να προκαλέσουν καρκίνο του πρωκτού ή του ορθού, αλλά σε συνύπαρξη HIV λοίμωξης αυτό είναι πολύ πιο πιθανό αν δεν λαμβάνεται θεραπεία όπως επίσης και αν αναπτυχθεί AIDS.
Το ίδιο σενάριο βέβαια ισχύει και για τους άλλους όγκους που περιγράφηκαν παραπάνω και συσχετίζονται αιτιολογικά με ιούς. Σε ασθενείς με συλλοίμωξη HIV και ιών ηπατίτιδας B ή C (HBV, HCV) που παραμένουν στον οργανισμό και προκαλούν χρόνια ηπατίτιδα B ή C, η πιθανότητα ανάπτυξης καρκίνου του ήπατος είναι 20 και παραπάνω φορές μεγαλύτερη από ότι αν ένα άτομο έχει μόνο χρόνια ηπατίτιδα B ή C χωρίς την παρουσία HIV λοίμωξης.
Εδώ θα πρέπει να τονιστεί ότι το πόσο πιθανή θα είναι μια επικίνδυνη εξέλιξη σε καρκίνο των παραπάνω λοιμώξεων από καρκινογόνους ιούς με τη συνύπαρξη του HIV, εξαρτάται πολύ από τους εξής παράγοντες :
- Από το αν οι λοιμώξεις αυτές λαμβάνουν αποτελεσματική θεραπεία από τη στιγμή της διάγνωσής τους, ή αν έχουν διαγνωστεί αργά και έχουν μείνει χωρίς θεραπεία για καιρό (πολύ μεγαλύτερος κίνδυνος)
- Από το αν η HIV λοίμωξη διαγιγνώσκεται και θεραπεύεται από νωρίς και αποτελεσματικά με αντιρετροϊκή αγωγή και διατηρείται μη ανιχνεύσιμο το ιικό φορτίο του HIV και φυσιολογικά τα επίπεδα των CD4
- Από το αν έχει αναπτυχθεί AIDS (μεγαλύτερος κίνδυνος)
- Από το αν γίνεται κατάχρηση άλλων επικίνδυνων ή καρκινογόνων ουσιών, όπως ο καπνός του τσιγάρου ή της μαριχουάνας ή η χρήση ναρκωτικών ουσιών που εξασθενούν το ανοσοποιητικό (ηρωίνη, κοκαΐνη κλπ) ή και χρόνια κακή διατροφή και γενικότερα ανθυγιεινός τρόπος ζωής.
Στα συμπτώματα του AIDS μπορεί τέλος να περιλαμβάνονται παρατεταμένος πυρετός (για πάνω από ένα μήνα), πολλοί ιδρώτες (ιδιαίτερα τη νύχτα), πρησμένοι λεμφαδένες, ρίγη, αδυναμία και απώλεια βάρους.[25] Η διάρροια είναι ένα επίσης κοινό σύμπτωμα του AIDS, είναι παρατεταμένη (για περισσότερο από ένα μήνα) και εμφανίζεται περίπου στο 90% των ατόμων με AIDS.[26]
Μετάδοση
Τρόποι μετάδοσης
Ο HIV μεταδίδεται μέσω τριών κυρίων οδών:
- τη σεξουαλική επαφή
- την έκθεση σε μολυσμένα σωματικά υγρά, ιστούς, σύριγγες και μετάγγιση
- από τη μητέρα στο παιδί (γνωστή ως κάθετη μετάδοση) κατά τη διάρκεια της εγκυμοσύνης, του τοκετού και του θηλασμού.[4] Είναι δυνατή επίσης η μόλυνση με περισσότερα του ενός στελέχη του HIV, κάτι που είναι γνωστό ως HIV υπερλοίμωξη.[27]
Σεξουαλική επαφή
Η πλειονότητα των HIV λοιμώξεων αποκτούνται διαμέσου σεξουαλικών επαφών που γίνονται χωρίς τη χρήση προφυλακτικού.[4] Σε παγκόσμιο επίπεδο οι επαφές που στις περισσότερες περιπτώσεις οδηγούν σε μετάδοση είναι οι ετεροσεξουαλικές επαφές, μεταξύ ατόμων του αντίθετου φύλου, παρά μεταξύ αυτών του ιδίου φύλου.[4] Στις ΗΠΑ, όσο αφορά το 2009, οι περισσότερες περιπτώσεις σεξουαλικής μετάδοσης συνέβησαν μεταξύ ανδρών που κάνουν σεξ με άνδρες,[4] με το ποσοστό του πληθυσμού αυτού να αναλογεί στο 64% όλων των νέων μεταδόσεων.[28]
Σε χώρες με υψηλό κατά κεφαλήν εισόδημα ο κίνδυνος μετάδοσης από γυναίκες σε άνδρες είναι περίπου 0,04 % ανά σεξουαλική πράξη ενώ ο κίνδυνος από άνδρα σε γυναίκα είναι 0,08% ανά επαφή αντίστοιχα.[29] Για διάφορους λόγους αυτά τα ποσοστά είναι κατά 4-10 φορές υψηλότερα σε χώρες με χαμηλά κατά κεφαλήν εισοδήματα με τη μετάδοση από γυναίκα σε άνδρα στο περίπου 0,38% ανά επαφή και από άνδρα σε γυναίκα στο 0,30 % ανά επαφή. [29] Ο κίνδυνος από πρωκτική συνουσία είναι ιδιαίτερα υψηλός και εκτιμάται περίπου 1,7% ανά επαφή[29][30] τόσο για τις ετεροσεξουαλικές όσο και για τις ομοφυλοφιλικές επαφές. Αν και ο κίνδυνος μετάδοσης με το στοματικό σεξ είναι μικρότερος, είναι ακόμη παρών (υπαρκτός)..[31] Αυτός ο κίνδυνος υπολογίζεται στο 0-0,04% ανά επαφή για την παθητική στοματική επαφή. [32]
Ο κίνδυνος αυξάνει με την παρουσία πολλαπλών σεξουαλικά μεταδιδόμενων νοσημάτων[33] και την ύπαρξη γεννητικά όργανα.[29] Τα γεννητικά έλκη κάνουν τον κίνδυνο περίπου πενταπλάσιο[29] ενώ υπάρχει μία μικρότερη αύξηση του κινδύνου από ΣΜΝ (Σεξουαλικώς Μεταδιδόμενα Νοσήματα) όπως γονόρροια (βλεννόροια), χλαμύδια, τριχομονάδωση και βακτηριακή κολπίτιδα.[32] Το βίαιο σεξ φαίνεται επίσης ότι αυξάνει τον κίνδυνο.[34]
Το ιικό φορτίο του ατόμου είναι σημαντικό και στην ετεροφυλοφιλική και στην κάθετη μετάδοση (μητέρα-παιδί).[35] Κατά τους πρώτους 2,5 μήνες της λοίμωξης με HIV η μολυσματικότητα ενός ατόμου είναι 12 φορές υψηλότερη λόγω αυτού του υψηλού ιικού φορτίου.[32] Όταν το άτομο είναι στα τελευταία στάδια της νόσου ο βαθμός μετάδοσης είναι περίπου 8 φορές μεγαλύτερος.[29]
Το επαγγελματικό (αγοραίο) σεξ ενέχει έναν κίνδυνο με μετάδοση από γυναίκα σε άνδρα στο περίπου 2,4 % ανά επαφή ενώ από άνδρα σε γυναίκα στο περίπου 0,08 % ανά επαφή.[29]
Η σεξουαλική επίθεση (βιασμός) πιστεύεται ότι έχει αυξημένο κίνδυνο μετάδοσης καθώς σπάνια χρησιμοποιούνται προφυλακτικά, είναι πιθανό να προκληθεί τραυματισμός στον κόλπο ή τον πρωκτό και μπορεί να υπάρχει μεγαλύτερος κίνδυνος ταυτόχρονης μετάδοσης και σεξουαλικά μεταδιδόμενων νοσημάτων.[36] Το ποσοστό ατόμων στις ΗΠΑ που είναι HIV θετικοί και φυλακισμένοι για σεξουαλικές επιθέσεις, περίπου είναι στο 1%[40].
Σωματικά υγρά - Σύριγγες
Ο δεύτερος πιο συχνός τρόπος μετάδοσης είναι διαμέσου του αίματος και των παραγώγων του.[4] Παρ' όλα αυτά η λοίμωξη δεν είναι δυνατόν να μεταδοθεί μέσω κουνουπιών ή άλλων εντόμων[2] [41]. Ο κίνδυνος από το μοίρασμα βελόνας κατά την ενέσιμη χρήση ναρκωτικών είναι από 0,63 έως 2,4% (κατά μέσο όρο 0,8%).[37] Ο κίνδυνος μόλυνσης με HIV από ένα μόνο τσίμπημα βελόνας που έχει χρησιμοποιηθεί από ένα HIV-θετικό άτομο είναι περίπου 0,3% (1 στις 333 τέτοιες περιπτώσεις) και ο κίνδυνος μετά από έκθεση των βλεννογόνων σε μολυσμένο αίμα είναι 0,09% (περίπου 1 στις 1000 περιπτώσεις).[38] Στις ΗΠΑ οι χρήστες ενδοφλέβιων ναρκωτικών αποτέλεσαν 12% των νέων περιπτώσεων HIV για στο 2009[28] και σε μερικές περιοχές περισσότερα από 80% των ατόμων που κάνουν ενέσιμη χρήση ναρκωτικών είναι HIV θετικοί.[4]
Οι μεταγγίσεις μολυσμένου αίματος καταλήγουν σε μετάδοση της λοίμωξης στο περίπου 93% των περιπτώσεων.[37] Στις αναπτυγμένες χώρες ο κίνδυνος μετάδοσης HIV από μετάγγιση αίματος είναι εξαιρετικά χαμηλός (λιγότερο από 1 στο μισό εκατομμύριο) όταν εκτελείται εξελιγμένη επιλογή δοτών αίματος και έλεγχος για HIV.[4] Στο Ηνωμένο Βασίλειο ο κίνδυνος αναφέρεται να είναι στο 1 στα 5 εκατομμύρια. [39] Παρ' όλα αυτά στις φτωχές χώρες μόνο η μισή ποσότητα αίματος που μεταγγίζεται ελέγχεται κατάλληλα (όπως αναφέρεται το 2008).[40] Εκτιμάται ότι σε αυτές τις χώρες έως και 15% των νέων μολύνσεων προέρχεται από μετάγγιση αίματος και παραγώγων του, που αντιπροσωπεύει μεταξύ 5% και 10% του συνόλου παγκοσμίως.[4][41]
Η επαναχρησιμοποίηση των συριγγών σε ιατρικές και νοσηλευτικές διαδικασίες παίζει σημαντικό ρόλο στην εξάπλωση του HIV στην Υποσαχάρια Αφρική, με το ποσοστό των μολύνσεων που αποδίδεται στην πρακτική αυτή να κυμαίνεται από 12 έως 17% σύμφωνα με στοιχεία του 2009.[42] Ο κίνδυνος από μία μόνο μη ασφαλή φαρμακευτική ένεση στην Αφρική υπολογίζεται από τον ΠΟΥ στο περίπου 1,2%.[42] Αξιοσημείωτοι κίνδυνοι σχετίζονται επίσης με τις επεμβατικές ιατρικές πράξεις, τον υποβοηθούμενο τοκετό και την οδοντιατρική περίθαλψη στις περιοχές αυτές.[42]
Άτομα που εκτελούν ή δέχονται τατουάζ, piercing ή εγχάραξη δέρματος έχουν θεωρητικά ένα κίνδυνο λοίμωξης αλλά δεν έχουν καταγραφεί επιβεβαιωμένες περιπτώσεις.[43] It is not possible for mosquitoes or other insects to transmit HIV.[44]
Από μητέρα σε παιδί (κάθετη μετάδοση)
Ο HIV μπορεί να μεταδοθεί από τη μητέρα στο παιδί στη διάρκεια της εγκυμοσύνης, του τοκετού και μετά τον τοκετό διαμέσου του θηλασμού.[45][46] Είναι ο τρίτος πιο κοινός τρόπος μετάδοσης παγκοσμίως.[4]
Όταν η μητέρα δεν λαμβάνει αγωγή ο κίνδυνος μετάδοσης στην περιγεννητική περίοδο (λίγο πριν και κατά τη διάρκεια της γέννησης) είναι γύρω στο 20% και για τα νεογνά που θηλάζουν στο 35%.[45] Το 2008 η κάθετη μετάδοση αποτέλεσε την οδό μόλυνσης στο 90% των παιδιών που μολύνθηκαν.[45] Με την κατάλληλη αγωγή ο κίνδυνος μόλυνσης από τη μητέρα στο παιδί μπορεί να μειωθεί στο περίπου 1%.[45] Για να γίνει αυτό, χρειάζεται η μητέρα να παίρνει αντιρετροϊκά στη διάρκεια της εγκυμοσύνης και του τοκετού, να γίνει προαιρετικά καισαρική τομή και να μη γίνει θηλασμός, καθώς επίσης και η λήψη αντιρετροϊκών από το βρέφος μετά τη γέννηση.[47] Παρ'όλα αυτά πολλά από αυτά τα μέτρα δεν είναι διαθέσιμα στον αναπτυσσόμενο κόσμο.[47]
Αν αίμα μολύνει το φαγητό στην προμάσηση (πρακτική που κάνουν κάποιες μητέρες ή συγγενείς για δώσουν προμασημένο φαγητό στο παιδί την περίοδο του απογαλακτισμού του), αυτό μπορεί να αποτελεί έναν κίνδυνο μετάδοσης.[43]
Μη μετάδοση
Ο HIV δεν μεταδίδεται:
- Από την καθημερινή, κοινωνική επαφή, τη χειραψία, το αγκάλιασμα, το απλό φιλί, τη συνάθροιση ατόμων
- Από την συγκατοίκηση με κάποιον/α οροθετικό, την κοινή χρήση ρούχων, σκεπασμάτων, πιάτων, ποτηριών και μαχαιροπήρουνων, τηλεφώνων
- Από την τουαλέτα
- Από τον ιδρώτα ή τα δάκρυα
- Από πισίνες ή τη θάλασσα
- Από κουνούπια ή άλλα έντομα
- Δεν υπάρχει κίνδυνος μετάδοσης από έκθεση σε κόπρανα, ρινικές εκκρίσεις, φλέματα, σάλιο ή εμετό από ένα μολυσμένο άτομο, εκτός εάν αυτά τα υλικά περιέχουν αίμα.[38]
Ιολογία

Ο ιός HIV είναι το αίτιο του φάσματος (εκδηλώσεων) της ασθένειας που είναι γνωστή ως HIV/AIDS. Ο HIV είναι ένας ρετροϊός που πρωταρχικά επιμολύνει τμήματα του ανθρώπινου ανοσοποιητικού συστήματος όπως τα CD4 T κύτταρα (μια υποομάδα των Τ λεμφοκυττάρων ή Τ4 λεμφοκύτταρα), τα μακροφάγα και τα δενδριτικά κύτταρα. Άμεσα και έμμεσα καταστρέφει τα CD4 T κύτταρα.[48]
Ο HIV είναι μέλος του γένους των Φακοϊών (Lentiviridae)[49] που αποτελεί μέρος της οικογένειας των Ρετροϊών (Retroviridae).[50] Οι φακοϊοί μοιράζονται πολλές κοινές μορφολογικές και βιολογικές ιδιότητες. Πολλά είδη θηλαστικών μολύνονται από φακοϊούς, οι οποίοι είναι υπεύθυνοι για μακράς διάρκειας ασθένειες με μακρά περίοδο επώασης.[51] Οι φακοϊοί μεταδίδονται ως (μοριακά) μονοκλωνικοί, περιτυλιγμένοι RNA ιοί θετικής πολικότητας.
Κατά την είσοδο στο κύτταρο-στόχο το ιικό RNA μονόκλωνο γονιδίωμα μετασχηματίζεται (μεταγράφεται αντιστρόφως) σε διπλού κλώνου DNA από μια κωδικοποιημένη από τον ιό αντίστροφη μεταγραφάση (ή αντίστροφη τρανσκριπτάση - ένζυμο μεταγραφής) η οποία μεταφέρεται μαζί με το ιικό γονιδίωμα μέσα στο σωματίδιο του ιού. Το παραγόμενο ιικό DNA εισάγεται τότε στον πυρήνα του κυττάρου και ενσωματώνεται στο κυτταρικό DNA με τη δράση μιας κωδικοποιημένης από τον ιό ιντεγκράσης (ένζυμο ενσωμάτωσης) και συμπαραγόντων του (κυττάρου) ξενιστή.[52] Αφού ενσωματωθεί ο ιός μπορεί να παραμείνει σε λανθάνουσα μορφή επιτρέποντας στον εαυτό του και στο κύτταρο ξενιστή (που τον φιλοξενεί) να αποφύγουν την ανίχνευση από το ανοσοποιητικό σύστημα.[53]
Εναλλακτικά ο ιός μπορεί να αντιγράφεται, παράγοντας έτσι νέο ιικό RNA γονιδίωμα και ιικές πρωτεΐνες που πακετάρονται και απελευθερώνονται από το κύτταρο ως νέα ιικά σωματίδια (με τη δράση μιας ιικής πρωτεάσης – ένζυμο κοπής μιας αρχικής ανενεργούς ιικής μεγαπρωτεΐνης σε μικρότερες λειτουργικές) και κατόπιν τα νέα αυτά ιικά σωματίδια αρχίζουν εκ νέου τον κύκλο αντιγραφής.[54]
Έχουν ταυτοποιηθεί δυο υπότυποι του HIV: ο HIV-1 και ο HIV-2. Ο HIV-1 ήταν ο ιός που αρχικά ανακαλύφθηκε και ονομάστηκε τότε με δύο ονομασίες : LAV και HTLV-III HIV. Είναι περισσότερο παθογόνος (λοιμογόνος), περισσότερο μεταδοτικός[55] και η αιτία της πλειοψηφίας των μολύνσεων παγκοσμίως. Η χαμηλότερη μεταδοτικότητα του HIV-2 συγκρινόμενη με αυτή του HIV-1 υποδηλώνει ότι λιγότερα άτομα από αυτά που εκτέθηκαν στον HIV-2 θα μολυνθούν τελικά από την έκθεση αυτή. Λόγω της σχετικά χαμηλής ικανότητάς του για μετάδοση ο HIV-2 είναι σε μεγάλο βαθμό περιορισμένος στη Δυτική Αφρική.[56]
Παθοφυσιολογία

Αφότου ο ιός εισέλθει στο σώμα υπάρχει μια περίοδος ταχείας αντιγραφής του που οδηγεί σε αφθονία του ιού στο περιφερικό αίμα. Κατά την πρωτολοίμωξη τα επίπεδα του ιού μπορεί να φτάσουν σε αρκετά εκατομμύρια ιικά σωματίδια ανά μικρολίτρο (μl – 1 εκατομμυριοστό του λίτρου ) αίματος,[57] σε επίπεδα υψηλότερα και από αυτά του τέλους της νόσου, όταν το ανοσοποιητικό σύστημα έχει πια «νικηθεί».
Αυτή η αντίδραση συνοδεύεται από μια αξιοσημείωτη πτώση του αριθμού των κυκλοφορούντων CD4 T κυττάρων. Αυτή η οξεία ιαιμία συσχετίζεται κατ’ ουσίαν σε όλους τους ανθρώπους με την ενεργοποίηση των CD8 T κυττάρων (φονικά κύτταρα - killer cells) τα οποία σκοτώνουν τα μολυσμένα με HIV κύτταρα, και ακολούθως με την παραγωγή αντισωμάτων ή ορομετατροπή. Από αυτό το σημείο και μετά κάποιος χαρακτηρίζεται τυπικά ως HIV «οροθετικός».
H απάντηση αυτή των CD8 Τ-κυττάρων πιστεύεται ότι είναι σημαντική στον έλεγχο των επιπέδων του ιού, τα οποία φτάνουν σε μία αιχμή και κατόπιν πέφτουν, καθώς τα CD4 Τ κύτταρα ανακάμπτουν. Μια καλή απάντηση από τα CD8 T κύτταρα έχει συνδεθεί με βραδύτερη πρόοδο της νόσου και καλύτερη πρόγνωση, παρότι δεν εξαλείφει τον ιό.[58]
Η παθοφυσιολογία του AIDS είναι περίπλοκη.[59] Τελικά ο HIV προκαλεί AIDS εξαλείφοντας τα CD4 T βοηθητικά λεμφοκύτταρα. Αυτό εξασθενεί το ανοσοποιητικό σύστημα και επιτρέπει ευκαιριακές λοιμώξεις. Τα Τ κύτταρα είναι θεμελιώδη για την ανοσολογική απάντηση και χωρίς αυτά το σώμα δεν μπορεί να πολεμήσει τις λοιμώξεις ή να σκοτώσει τα καρκινικά κύτταρα. Ο μηχανισμός της ελάττωσης των Τ4 κυττάρων είναι διαφορετικός στην οξεία φάση από τη χρόνια φάση.[60] Κατά τη διάρκεια της οξείας φάσης η προκαλούμενη από τον HIV κυτταρική λύση και η καταστροφή των μολυσμένων κυττάρων από κυτταροτοξικά Τ κύτταρα εξηγούν την εξάλειψη των Τ4 κυττάρων αν και ένας παράγοντας γι’ αυτό μπορεί να είναι και η κυτταρική απόπτωση (η φυσιολογικά προγραμματισμένη διαδικασία κυτταρικού θανάτου των πολυκύτταρων οργανισμών). Στη διάρκεια της χρόνιας φάσης οι συνέπειες της γενικευμένης ανοσολογικής ενεργοποίησης σε συνδυασμό με τη σταδιακή απώλεια της ικανότητας του ανοσοποιητικού συστήματος να παράγει καινούργια Τ κύτταρα φαίνεται να ερμηνεύουν τη βραδεία ελάττωση του αριθμού των Τ4 κυττάρων.[61]
Αν και τα συμπτώματα της ανεπάρκειας του ανοσοποιητικού που είναι χαρακτηριστικά του ΑIDS δεν εμφανίζονται για χρόνια από τη στιγμή που ένα άτομο έχει μολυνθεί, το μεγάλο μέρος της απώλειας των CD4 συμβαίνει κατά τις πρώτες εβδομάδες της λοίμωξης, ιδιαίτερα στον εντερικό βλεννογόνο, που φιλοξενεί το μεγαλύτερο μέρος των λεμφοκυττάρων του σώματος.[62] Η αιτία αυτής της κατά προτίμηση απώλειας των Τ4 κυττάρων του βλεννογόνου είναι ότι η πλειοψηφία των CD4 κυττάρων του βλεννογόνου μεταφέρουν τον συνυποδοχέα CCR5 (κυτταρική πρωτεΐνη με σημαντικό ρόλο στη σύνδεση του HIV με το κύτταρο), ενώ μόνο ένα μικρό κλάσμα (τμήμα) των CD4 του αίματος έχει αυτή την ιδιαιτερότητα.[63]
Κατά τη διάρκεια της οξείας φάσης της λοίμωξης, ο HIV αναζητά και καταστρέφει αυτά ακριβώς τα CD4 κύτταρα που εκφράζονται με το συνυποδοχέα CCR5.[64] Στο τέλος μια ισχυρή αντίδραση του ανοσοποιητικού ελέγχει τη λοίμωξη και ξεκινά την κλινικά λανθάνουσα φάση. Τα CD4 κύτταρα στους βλεννογόνους ιστούς συνεχίζουν να είναι ιδιαίτερα επηρεασμένα[64] καθώς οι αριθμοί τους δεν επανακάμποτυν ποτέ στα προ της λοίμωξης επίπεδα.
Η συνεχής αντιγραφή του HIV έχει ως αποτέλεσμα μια κατάσταση γενικευμένης ανοσολογικής ενεργοποίησης που επιμένει κατά τη διάρκεια της χρόνιας φάσης.[65] Η ανοσολογική αυτή ενεργοποίηση η οποία αντανακλάται από την κατάσταση αυξημένης ενεργοποίησης των ανοσοκυττάρων και την έκλυση προφλεγμονωδών κυτταροκινών, είναι το αποτέλεσμα της δραστηριότητας αρκετών προϊόντων του HIV γονιδιώματος και της ανοσολογικής αντίδρασης στη συνεχιζόμενη αντιγραφή του HIV. Μία ακόμη αιτία της ανοσολογικής ενεργοποίησης είναι η διάσπαση του ανοσολογικού συστήματος επίβλεψης – παρακολούθησης που υπάρχει στον βλεννογόνο φραγμό που προκαλείται από τη (μαζική) απώλεια των CD4 T κυττάρων του βλεννογόνου κατά την οξεία φάση της νόσου.[66]
Διάγνωση
Το HIV/AIDS διαγιγνώσκεται μέσω εργαστηριακών εξετάσεων και κατόπιν σταδιοποιείται στη βάση της παρουσίας συγκεκριμένων κλινικών σημείων και συμπτωμάτων.[14] Η εξέταση για HIV συνιστάται σε όλους όσους είναι σε υψηλό κίνδυνο συμπεριλαμβανομένων και όλων όσων έχουν διαγνωστεί με σεξουαλικά μεταδιδόμενο νόσημα.[17]
Σε πολλές περιοχές του κόσμου το ένα τρίτο των ανθρώπων με HIV το ανακαλύπτουν μόνο όταν η νόσος είναι ήδη προχωρημένη.[17] Στις αναπτυσσόμενες χώρες χρησιμοποιείται πρωταρχικά το σύστημα σταδιοποίησης του Παγκόσμιου Οργανισμού Υγείας, ενώ στις ανεπτυγμένες χώρες χρησιμοποιείται συχνότερα το σύστημα ταξινόμησης της μόλυνσης με HIV κατά CDC (Center for Disease Control – Κέντρο Ελέγχου Νοσημάτων των Ηνωμένων Πολιτειών).[67]
Το τεστ για HIV
Οι περισσότεροι άνθρωποι που μολύνονται με HIV αναπτύσσουν αντισώματα (κάνουν ορομετατροπή) μέσα σε 3 έως 12 εβδομάδες από τη στιγμή που θα μπει ο ιός στο αίμα.[16]
Η διάγνωση της πρώιμης HIV λοίμωξης πριν συμβεί η ορομετατροπή γίνεται με τη μέτρηση του HIV RNA (γονιδίωμα ή γενετικό υλικό του HIV ή ιικό φορτίο του HIV) με τη μέθοδο PCR (Polymerase Chain Reaction) ή του αντιγόνου p24 (πρωτεϊκό συστατικό της επιφάνειας του σωματιδίου του HIV, βλ. διάγραμμα).[16] Θετικά αποτελέσματα που λαμβάνονται είτε με μέτρηση αντισωμάτων είτε με ΡCR, επιβεβαιώνονται είτε με δεύτερη εξέταση για διαφορετικό αντίσωμα είτε με δεύτερη PCR.[14]
Τα τεστ αντισωμάτων σε παιδιά κάτω των 18 μηνών είναι τυπικά ανακριβή λόγω της παρουσίας μητρικών αντισωμάτων.[68] Έτσι σε αυτή την περίπτωση η διάγνωση της λοίμωξης μπορεί να γίνει μόνο με PCR για HIV RNA ή DNA (μεταγραμμένο HIV RNA) ή μέσω εξέτασης για το αντιγόνο p24.[14]
Μεγάλο μέρος του πληθυσμού παγκοσμίως έχει έλλειψη πρόσβασης σε αξιόπιστες εξετάσεις PCR και σε πολλά μέρη απλώς περιμένουν μέχρι το παιδί να αναπτύξει συμπτώματα ή να γίνει αρκετά μεγάλο για κάνει εξέταση αντισωμάτων με ακρίβεια διάγνωσης.[68] Στην υπο-Σαχάρια Αφρική για τα έτη 2007-2009 ένα 30-70 % του πληθυσμού ήταν ενήμερο για το HIV status του.[69] Το 2009 εξετάστηκε ένα ποσοστό ανάμεσα σε 4% και 42% του πληθυσμού.[69] Αυτά τα ποσοστά αντιπροσωπεύουν ουσιώδη αύξηση σε σχέση με ότι επικρατούσε δέκα χρόνια πιο πριν.[69]
Στάδια Ασθένειας
Ο παγκόσμιος Οργανισμός Υγείας πρότεινε για πρώτη φορά έναν ορισμό του AIDS το 1986.[14] Από τότε υπήρξε ένας αριθμός αναβαθμίσεων και επεκτάσεων του ορισμού, μέχρι την πιο πρόσφατη εκδοχή (ταξινόμηση) του 2007.[14]
- Πρώιμη HIV λοίμωξη : μπορεί να είναι είτε ασυμπτωματική είτε σχετιζόμενη με οξύ ρετροϊκό σύνδρομο.[14]
- Στάδιο Ι : ασυμπτωματική HIV λοίμωξη με αριθμό CD4 μεγαλύτερο από (>) 500/μl (ανά μικρόλιτρο ή κυβικό χιλιοστό αίματος).[14] Μπορεί να περιλαμβάνει γενικευμένη διόγκωση λεμφαδένων.[14]
- Στάδιο ΙΙ: ήπια συμπτώματα που μπορεί να περιλαμβάνουν χαμηλής βαρύτητας βλεννογονοδερματικές εκδηλώσεις και υποτροπιάζουσες λοιμώξεις του ανώτερου αναπνευστικού. Αριθμός CD4 μικρότερος από (<) 500/μl.[14]
- Στάδιο ΙΙΙ: Προχωρημένα συμπτώματα που μπορεί να περιλαμβάνουν ανεξήγητη χρόνια διάρροια για περισσότερο από 1 μήνα, σοβαρές βακτηριακές λοιμώξεις συμπεριλαμβανομένης της πνευμονικής φυματίωσης και αριθμό CD4 < 350/μl.[14]
- Στάδιο ΙV ή AIDS : σοβαρά συμπτώματα που περιλαμβάνουν τοξοπλάσμωση εγκεφάλου, καντιντίαση (ευκαιριακή μυκητίαση) οισοφάγου, τραχείας, βρόγχων ή πνευμόνων και σάρκωμα Kaposi. Αριθμός CD4 <200/μl.[14]
Ταξινόμηση κατά CDC (Κέντρο ελέγχου Νοσημάτων) Ηνωμένων Πολιτειών
Το Κέντρο Ελέγχου και Πρόληψης Νοσημάτων των Ηνωμένων Πολιτειών αναβάθμισε το δικό του σύστημα ταξινόμησης για το HIV/AIDS το 2008.[67] Στο σύστημα αυτό η λοίμωξη κατατάσσεται βάσει αριθμού CD4 και κλινικών συμπτωμάτων.
- Στάδιο 1: αριθμός CD4 > 500/μl και μη ύπαρξη καταστάσεων που ορίζουν το AIDS.
- Στάδιο 2: αριθμός CD4 200-500/μl και μη ύπαρξη καταστάσεων που ορίζουν το AIDS.
- Στάδιο 3: αριθμός CD4 <200/μl και παρουσία καταστάσεων που ορίζουν το AIDS.
- Άγνωστο: όταν δεν υπάρχει επαρκής πληροφόρηση για την κατάταξη σε κάποιο από τα παραπάνω στάδια.
Η διάγνωση του AIDS (στάδιο 3) εξακολουθεί να ισχύει ακόμη και αν μετά τη θεραπεία ο αριθμός των CD4 ανέβει πάνω από τα 200/μl ή θεραπευτούν άλλες ασθένειες που ορίζουν το ΑIDS.
Πρόληψη
Σεξουαλική επαφή
Η σταθερή χρήση προφυλακτικού μειώνει τον κίνδυνο μετάδοσης HIV περίπου στο 80% μακροπρόθεσμα.[70]
Σε περιπτώσεις όπου ο ένας παρτενέρ στο ζευγάρι είναι μολυσμένος η συνεχής χρήση του προφυλακτικού έχει ως αποτέλεσμα ποσοστά μετάδοσης στο μη μολυσμένο σύντροφο κάτω από 1% ανά έτος.[71] Κάποια δεδομένα υποστηρίζουν την ισοδύναμη αποτελεσματικότητα του γυναικείου προφυλακτικού σε σχέση με τα (ανδρικά) προφυλακτικά από λάτεξ,[72] παρ' όλα αυτά οι μαρτυρίες γι’ αυτό δεν έχουν οριστικοποιηθεί.
Η χρήση κολπικού τζελ που περιέχει tenofovir (έναν αναστολέα της αντίστροφης μεταγραφάσης) λίγο πριν το σεξ φαίνεται να μειώνει τα ποσοστά μόλυνσης σε 40% στις Αφρικανές γυναίκες.[73] Αντίθετα, η χρήση του σπερματοκτόνου nonoxynol-9 μπορεί να αυξήσει τον κίνδυνο μετάδοσης λόγω του γεγονότος ότι προκαλεί κολπικό και πρωκτικό ερεθισμό.[74]
Η περιτομή στην Υποσαχάρια Αφρική μειώνει την μόλυνση από HIV σε ετεροφυλόφιλους άνδρες σε ένα ποσοστό ανάμεσα στο 38 και 66% σε διάστημα 2 ετών.[75] Με βάση αυτές τις μελέτες, το 2007 ο Παγκόσμιος Οργανισμός Υγείας και ο UNAIDS (Οργανισμός των Ηνωμένων Εθνών για το AIDS) συνέστησαν την ανδρική περιτομή σαν μέσο πρόληψης της μετάδοσης από γυναίκα σε άνδρα μέσα στο 2007.[76] Το αν η περιτομή προστατεύει και από τη μετάδοση από άνδρα σε γυναίκα είναι αμφισβητήσιμο,[77][78] και επίσης το αν είναι προς όφελος των ανδρών που κάνουν σεξ με άνδρες στις ανεπτυγμένες χώρες δεν έχει καθοριστεί. [79][80][81] Women who have undergone female genital cutting have an increased risk of HIV.[82]
Μερικοί ειδικοί πιστεύουν ότι η μειωμένη αντίληψη ευπάθειας (δηλαδή κινδύνου μόλυνσης) που μπορεί να έχουν οι περιτετμημένοι άνδρες, μπορεί να τους οδηγήσει σε υψηλότερου κινδύνου σεξουαλική συμπεριφορά και έτσι να ακυρώσει τα προληπτικά αποτελέσματα της περιτομής τους.[83] Γυναίκες που έχουν υποστεί ακρωτηριασμό των εξωτερικών γεννητικών τους οργάνων, όπως κλειτοριδεκτομή, διατρέχουν αυξημένο κίνδυνο να μολυνθούν με HIV.[84]
Πρόληψη πριν από την έκθεση
Η πρώιμη θεραπεία οροθετικών ατόμων με αντιρετροϊκά έχει προστατέψει το 96% των συντρόφων τους (σύμφωνα με μελέτες) [88] [89]. Προφύλαξη προ της έκθεσης (στη λοίμωξη) με ημερήσια δόση των φαρμάκων τενοφοβίρη (tenofovir – Viread) με ή χωρίς εμτρισιταβίνη (emtricitabine-Emtriva) είναι αποτελεσματική σε ορισμένες ομάδες που περιλαμβάνουν: άνδρες που κάνουν σεξ με άνδρες, ζευγάρια όπου ο ένας από τους δύο είναι HIV οροθετικός και νεαροί ετεροφυλόφιλοι στην Αφρική[74].
Προφυλάξεις σε παγκόσμιο επίπεδο μέσα στο πλαίσιο του περιβάλλοντος υγειονομικής περίθαλψης θεωρούνται αποτελεσματικές στη μείωση του κινδύνου για HIV[90]. Η ενδοφλέβια χρήση ναρκωτικών είναι ένας σημαντικός παράγοντας κινδύνου και οι στρατηγικές μείωσης βλάβης όπως προγράμματα ανταλλαγής βελονών (και συριγγών) και η θεραπεία υποκατάστασης οπιοειδών φαίνονται να είναι αποτελεσματικά στη μείωση αυτού του κινδύνου[91].
Πρόληψη (προφύλαξη) μετά την έκθεση
Μια σειρά αντιρετροϊκών που χορηγούνται εντός 48 έως 72 ωρών μετά από έκθεση σε HIV μολυσμένο αίμα ή γεννητικές εκκρίσεις αναφέρονται ως προφύλαξη μετά από έκθεση[92]. Η χρήση μόνο του παράγοντα ζιδοβουδίνη (zidovudine-Retrovir) μειώνει 5 φορές τον κίνδυνο που ακολουθεί έναν τραυματισμό από τρύπημα βελόνας[92]. Η θεραπεία προφύλαξης συνιστάται μετά από μία σεξουαλική επίθεση όταν οι δράστες είναι γνωστό ότι είναι οροθετικοί αλλά είναι αμφιλεγόμενη σε περίπτωση που το HIV status των δραστών είναι άγνωστο[40].
Τα σύγχρονα θεραπευτικά σχήματα προφύλαξης χρησιμοποιούν λοπιναβίρη/ριτοναβίρη (lopinavir/Ritonavir-Kaletra) μαζί με λαμιβουδίνη/ζιδοβουδίνη (Combivir) ή με εμτρισιταβίνη/τενοφοβίρη (Truvada) και μπορούν να μειώσουν περαιτέρω τον κίνδυνο[92]. Η διάρκεια της (προφυλακτικής) αγωγής είναι συνήθως 4 εβδομάδες[93] και σχετίζεται με σημαντικά ποσοστά ανεπιθύμητων ενεργειών ( πχ, για τη ζιδοβουδίνη περίπου 70% που περιλαμβάνουν ναυτία 24%, κόπωση 22%, συναισθηματική κατάπτωση 13%, πονοκεφάλους 9% κλπ) [26].
Πρόληψη από μητέρα στο παιδί
Προγράμματα που εμποδίζουν τη μετάδοση από μητέρα σε παιδί μπορούν να μειώσουν τον κίνδυνο σε ποσοστά από 92-99%[48] [91]. Τα προγράμματα αυτά περιλαμβάνουν πρωταρχικά τη χρήση ενός συνδυασμού αντιρετροϊκών στη διάρκεια της εγκυμοσύνης και μετά τη γέννηση στο βρέφος, αλλά επίσης δυνητικά περιλαμβάνουν τη διατροφή του με μπουκάλι αντί του θηλασμού[48] [94].
Αν αυτή η αντικατάσταση στη διατροφή του βρέφους είναι αποδεκτή, εφικτή, οικονομικά ανεκτή, διατηρήσιμη και ασφαλής, οι μητέρες θα πρέπει να αποφεύγουν το θηλασμό των βρεφών τους, παρόλα αυτά αν δεν συντρέχουν τα παραπάνω, τότε συνιστάται αποκλειστικά η διατροφή μέσω θηλασμού κατά τη διάρκεια των πρώτων μηνών της ζωής[95]. Αν εφαρμοστεί αυτή η αποκλειστική διατροφή μέσω θηλασμού, τότε η παροχή παρατεταμένης αντιρετροϊκής προφύλαξης στο βρέφος μειώνει τον κίνδυνο μετάδοσης[96].
Εμβολιασμός
Μέσα στο 2012 δεν υπάρχει αποτελεσματικό (προληπτικό) εμβόλιο για το HIV/AIDS[97]. Μια απλή μελέτη (δοκιμή) του εμβολίου RV 144 που δημοσιεύτηκε το 2009 αποκάλυψε μια μερική αποτελεσματικότητα σε ποσοστό περίπου 30% και προκάλεσε αισιοδοξία στην ερευνητική κοινότητα για την προοπτική ανάπτυξης ενός πραγματικά αποτελεσματικού εμβολίου[98]. Περαιτέρω κλινικές δοκιμές για το εμβόλιο συνεχίζονται[99] [100].
Αντιμετώπιση
Αυτή τη στιγμή δεν υπάρχει ίαση ή αποτελεσματικό εμβόλιο για τον HIV. Η αγωγή αποτελείται από την υψηλής δραστικότητας αντιρετροϊκή θεραπεία (HAART-Highly Active Antiretroviral Therapy) η οποία επιβραδύνει την εξέλιξη της νόσου[101] και με στοιχεία για το 2010 περισσότεροι από 6,6 εκατομμύρια άνθρωποι τη λαμβάνουν σε χώρες με χαμηλό ή μεσαίο εισόδημα[5]. Η αγωγή επίσης περιλαμβάνει προληπτική αλλά και ενεργό θεραπεία των ευκαιριακών λοιμώξεων.
Αντιυική θεραπεία
Οι σύγχρονες επιλογές της HAART περιλαμβάνουν συνδυασμούς (ή κοκτέιλ) αποτελούμενους από τουλάχιστον 3 φάρμακα τα οποία ανήκουν σε τουλάχιστον 2 τύπους ή κατηγορίες αντιρετροϊκών παραγόντων[102]. Αρχικά η θεραπεία αποτελείται τυπικά από δύο νουκλεοσιδικoύς-νουκλεοτιδικούς αναστολείς της αντίστροφης μεταγραφάσης (τρανσκριπτάσης) του ιού (νουκλεοσιδικά -νουκλεοτιδικά ανάλογα -NRTIs) και έναν μη-νουκλεοσιδικό αναστολέα της αντίστροφης τρανσκριπτάσης του ιού (NNRTIs) [102].
Στους τυπικούς νουκλεοσιδικούς αναστολείς αντίστροφης μεταγραφάσης (NRTIs) περιλαμβάνεται η ζιδοβουδίνη (AZT), η λαμιβουδίνη (3TC- Epivir), η εμτρισιταβίνη (FTC-Emtriva), η αμπακαβίρη (abacavir-Ziagen) και σε αυτή την κατηγορία συμπεριλαμβάνεται και ο νουκλεοτιδικός αναστολέας τενοφοβίρη (TDF-Viread). Αυτά μπορούν να δοθούν και συχνά δίνονται σε συνδυασμό ως ένα φάρμακο (ένα χάπι μια φορά τη μέρα) όπως για παράδειγμα τα ζιδοβουδίνη/λαμιβουδίνη (Combivir), αμπακαβίρη/λαμιβουδίνη (Kivexa) και τενοφοβίρη/εμτρισιταβίνη (Truvada).
Στους μη νουκλεοσιδικούς αναστολείς της αντίστροφης μεταγραφάσης περιλαμβάνονται φάρμακα όπως η εφαβιρένζη (Efavirenz-Stocrin), η νεβιραπίνη (nevirapine-Viramune) και τα νεώτερα ετραβιρίνη (Intelence) και ριλπιβιρίνη (Edurant).
Τα τελευταία χρόνια χρησιμοποιούνται και συνδυασμοί δύο νουκλεοσιδικών-νουκλεοτιδικών αναστολέων με έναν μη-νουκλεοσιδικό αναστολέα σε ένα μόνο φάρμακο (ένα χάπι μια φορά τη μέρα) όπως τα : τενοφοβίρη/εμτρισιταβίνη + εφαβιρένζη (Atripla) και το πλέον πρόσφατο τενοφοβίρη/εμτρισιταβίνη + ριλπιβιρίνη (Complera, Eviplera).
Αν κάποιο από τα παραπάνω συνδυαστικά σχήματα χάσει την αποτελεσματικότητά του, τότε χρησιμοποιούνται συνδυασμοί παραγόντων που περιλαμβάνουν τους αναστολείς πρωτεάσης του HIV. Στην κατηγορία αυτή περιλαμβάνονται φάρμακα όπως η αταζαναβίρη (Atazanavir-Reyataz), η νταρουναβίρη (Darunavir-Prezista), η τιπραναβίρη (tipranavir-Aptivus), η φοζαμπρεναβίρη (Fosamprenavir-Telzir) και η ριτοναβίρη (ritonavir-Norvir) που χορηγείται πάντοτε σε χαμηλή δόση μαζί με κάθε ένα από τους παραπάνω αναστολείς πρωτεάσης. Επίσης ο συνδυασμός λοπιναβίρη/ριτοναβίρη δίνεται πλέον σε ένα φάρμακο (lopinavir/ritonavir-Kaletra) διευκολύνοντας έτσι τους ασθενείς που τον λαμβάνουν.
Οι νεώτερες κατηγορίες αντιρετροϊκών παραγόντων που χρησιμοποιούνται εναλλακτικά στους συνδυασμούς των φαρμάκων αυτών περιλαμβάνουν : τους αναστολείς ιντεγκράσης (integrase inhibitors) του HIV με κυριότερο εκπρόσωπο τη ραλτεγκραβίρη (raltegravir-Isentress) και τους αναστολείς του CCR5 συνυποδοχέα (πρωτεΐνη του CD4 κυττάρου με σημαντικό ρόλο στη σύνδεση του ιού με το κύτταρο) (Maraviroc-Selcentri). Μια ακόμη κατηγορία αντιρετροϊκών που χρησιμοποιείται λιγότερο και σε αποτυχία των παραπάνω συνδυασμών περιλαμβάνει τους αναστολείς σύντηξης (ένωσης του σωματιδίου του ιού με το σωματίδιο του κυττάρου) με εκπρόσωπο το ενέσιμο φάρμακο Fuzeon ή T-20.
Το πότε ξεκινάει η αντιρετροϊκή θεραπεία είναι αντικείμενο διένεξης[14] [103]. Ο Παγκόσμιος Οργανισμός Υγείας, οι Ευρωπαϊκές οδηγίες και οι Ηνωμένες Πολιτείες συνιστούν αντιρετροϊκή αγωγή σε όλους τους έφηβους, ενήλικες και έγκυες γυναίκες που έχουν αριθμό CD4<350 (λιγότερο από 350) κύτταρα ανά μl αίματος ή έχουν συμπτώματα ανεξαρτήτως του αριθμού των CD4[14] [102]. Η άποψη αυτή υποστηρίζεται από το γεγονός ότι η έναρξη της θεραπείας στο επίπεδο αυτό μειώνει τον κίνδυνο θανάτου[104]. Οι Ηνωμένες Πολιτείες επιπρόσθετα συνιστούν την αγωγή σε όλα τα HIV οροθετικά άτομα, ασχέτως αριθμού CD4 ή συμπτωμάτων αλλά πάραυτα κάνει τη σύσταση με επιφύλαξη στα άτομα με υψηλότερους (των 350) αριθμούς CD4[105]. Επίσης ο Π.Ο.Υ συνιστά θεραπεία σε όσους έχουν συλλοίμωξη με φυματίωση και στα άτομα που έχουν ταυτόχρονα χρόνια ενεργό ηπατίτιδα Β[102]. Από τη στιγμή που η θεραπεία ξεκινήσει συνιστάται να συνεχίζεται χωρίς διαλλείματα ή ‘’διακοπές’’ [14]. Πολλοί άνθρωποι διαγιγνώσκονται μόνο αφότου παρέλθει ο χρόνος που η θεραπεία θα έπρεπε ιδανικά να είχε ξεκινήσει[14].
Το επιθυμητό αποτέλεσμα της θεραπείας είναι μία μακροχρόνια τιμή HIV-RNA στο πλάσμα του αίματος μικρότερη από 50 αντίγραφα ανά ml[14]. Επίπεδα (τιμών HIV-RNA) για να αποφασιστεί αν η θεραπεία έχει αποτέλεσμα συνιστάται να λαμβάνονται μετά 4 εβδομάδες (από την έναρξη) και μόλις πέσουν κάτω από τα 50 αντίγραφα είναι τυπικά επαρκείς οι έλεγχοι κάθε 3 έως 6 μήνες[14]. Ανεπαρκής έλεγχος (του ιού) θεωρείται η τιμή (HIV-RNA) που είναι μεγαλύτερη από 400 κόπιες (αντίγραφα) ανά μl. Βασισμένη σε αυτά τα κριτήρια η αγωγή είναι αποτελεσματική σε περισσότερους από το 95% των ανθρώπων που τη λαμβάνουν κατά τον πρώτο χρόνο[14].
Τα πλεονεκτήματα της αγωγής περιλαμβάνουν μειωμένο κίνδυνο εξέλιξης της λοίμωξης σε AIDS και μειωμένο κίνδυνο θανάτου[106]. Στον αναπτυσσόμενο κόσμο η αγωγή βελτιώνει επίσης τη σωματική και πνευματική-ψυχική υγεία[107]. Με τη θεραπεία επιτυγχάνεται ένας κατά 70% μειωμένος κίνδυνος απόκτησης φυματίωσης[102]. Επιπρόσθετα οφέλη περιλαμβάνουν μειωμένο κίνδυνο μετάδοσης της ασθένειας στους σεξουαλικούς παρτενέρ και μείωση της μετάδοσης από μητέρα σε παιδί[102].
Η αποτελεσματικότητα της αγωγής εξαρτάται κατά μεγάλο μέρος στη συμμόρφωση[14]. Λόγοι μη-συμμόρφωσης περιλαμβάνουν φτωχή πρόσβαση σε ιατρική φροντίδα[108], ανεπαρκή κοινωνική υποστήριξη, ψυχική νόσο και κατάχρηση ναρκωτικών[109]. Επίσης η πολυπλοκότητα των θεραπευτικών σχημάτων (λόγω του αριθμού χαπιών και της συχνότητας των δόσεων), αλλά και οι παρενέργειες των φαρμάκων είναι λόγοι που μπορεί να οδηγήσουν σε σκόπιμη μη-συμμόρφωση[110]. Παρόλα αυτά η συμμόρφωση είναι το ίδιο καλή (ή κακή) και στις χώρες χαμηλού εισοδήματος αλλά και σε αυτές υψηλού εισοδήματος[111].
Ιδιαίτερες ανεπιθύμητες ενέργειες (παρενέργειες) σχετίζονται κάθε φορά με το (φαρμακευτικό) παράγοντα που λαμβάνεται[112]. Μερικές σχετικά κοινές (για τα διάφορα φάρμακα) περιλαμβάνουν : σύνδρομο λιποδυστροφίας, δυσλιπιδαιμία και σακχαρώδη διαβήτη, ειδικά με τους αναστολείς πρωτεάσης[9]. Άλλα κοινά συμπτώματα περιλαμβάνουν διάρροια[12] [113] και επίσης υπάρχει ένας αυξημένος κίνδυνος καρδιαγγειακής νόσου[114], αλλά και άλλων σοβαρών καταστάσεων όπως εγκεφαλικών επεισοδίων, εξελισσόμενης - μη αναστρέψιμης ηπατικής νόσου (ίνωση-κίρρωση-καρκίνος ήπατος), τελικής νεφρικής νόσου, άλλων καρκίνων μη οφειλόμενων σε AIDS, οστεοπενίας-οστεοπόρωσης και καταγμάτων κλπ. Ο αυξημένος κίνδυνος για όλες αυτές τις σοβαρές καταστάσεις οφείλεται στη συνεργική δράση των φαρμάκων αλλά και της ίδιας της μακροχρόνιας HIV λοίμωξης και των βλαβών που προκαλεί στο ανοσοποιητικό σύστημα σε χρόνια βάση.
Εντούτοις οι παρενέργειες είναι λιγότερες με μερικές από τις νεότερες θεραπείες που συνιστώνται[14]. Το κόστος μερικών (κυρίως νεώτερων φαρμάκων) μπορεί να αποτελεί ένα ζήτημα[115] , παρόλα αυτά φαίνεται το 2010 ότι το 47% αυτών που τα χρειάζονταν τα έπαιρναν στις χώρες με χαμηλό και μεσαίο εισόδημα[5]. Μερικά φάρμακα μπορεί να σχετίζονται με ανωμαλίες κατά τη γέννηση γι’ αυτό και δεν είναι κατάλληλα για (οροθετικές) γυναίκες που σχεδιάζουν να αποκτήσουν παιδιά[14].
Στα οροθετικά παιδιά οι συστάσεις θεραπείας διαφέρουν σε κάποια πράγματα σε σχέση με τους ενήλικες. Για το 2010 στον αναπτυσσόμενο κόσμο, το 23% των παιδιών που βρίσκονταν σε ανάγκη για θεραπεία είχαν πρόσβαση σε αυτήν[116]. Ο Παγκόσμιος Οργανισμός Υγείας αλλά και οι Ηνωμένες Πολιτείες συνιστούν θεραπεία για όλα τα παιδιά μικρότερα της ηλικίας των 12 μηνών[117] [118]. Για αυτά που έχουν ηλικία ανάμεσα στα 1 και 5 έτη οι Ηνωμένες πολιτείες συνιστούν θεραπεία σε όσα έχουν τιμές HIV-RNA μεγαλύτερες από 100000 αντίγραφα ανά ml, ενώ στα μεγαλύτερα από 5 ετών συνιστούν αγωγή σε όσα έχουν αριθμό CD4<500[117].
Ευκαιριακές και άλλες λοιμώξεις
Τα μέτρα για την πρόληψη των ευκαιριακών λοιμώξεων είναι αποτελεσματικά σε πολλά άτομα με HIV/AIDS. Η θεραπεία με αντιιικά φάρμακα συχνά βελτιώνει τις παρούσες ευκαιριακές λοιμώξεις και επίσης μειώνει τον κίνδυνο για μελλοντικές[112]. Ο εμβολιασμός για ηπατίτιδες Α και Β συνιστάται σε όλους τους ανθρώπους που είναι ευάλωτοι στον HIV πριν μολυνθούν, παρόλα αυτά μπορεί να τους δοθεί και μετά τη μόλυνση[119].
Σε βρέφη γεννημένα από οροθετικές μητέρες, συνιστάται προφύλαξη με τριμεθοπρίμη/σουλφαμεθοξαζόλη στην ηλικία ανάμεσα στις 4 έως 6 εβδομάδες της ζωής και το τελείωμα του θηλασμού, όταν το περιβάλλον τους έχει περιορισμένους πόρους[116]. Επίσης η προφύλαξη αυτή συνιστάται για την πρόληψη της PCP (πνευμονία από πνευμονοκύστη) στα άτομα με αριθμό CD4<200 κύτταρα καθώς και σε εκείνους που ήδη έχουν ή είχαν παλαιότερα PCP[120]. Σε ανθρώπους με σημαντική ανοσοκαταστολή συνιστάται επίσης να λαμβάνουν προφυλακτική θεραπεία για τοξοπλάσμωση και κρυπτοκοκκική μηνιγγίτιδα[121]. Τα κατάλληλα προληπτικά μέτρα έχουν μειώσει τα ποσοστά αυτών των λοιμώξεων κατά 50% ανάμεσα στα έτη 1992 και 1997[122].
Εναλλακτικές θεραπείες
Στις ΗΠΑ περίπου το 60% των ανθρώπων με HIV χρησιμοποιούν διάφορες μορφές συμπληρωματικών ή εναλλακτικών θεραπειών[123]. Εντούτοις η αποτελεσματικότητα των περισσότερων από αυτές τις θεραπείες δεν έχει εδραιωθεί[124]. Αναφορικά με τις διατροφικές συμβουλές στο AIDS κάποιες μαρτυρίες έχουν δείξει ένα όφελος από τη λήψη ιχνοστοιχείων σε συμπληρώματα[125]. Οι μαρτυρίες για συμπληρώματα με σελήνιο είναι ανάμεικτες με αβέβαιες αποδείξεις περί σχετικού οφέλους[126]. Υπάρχουν κάποιες μαρτυρίες ότι τα συμπληρώματα βιταμίνης Α σε παιδιά μειώνουν τον κίνδυνο θανάτου και βελτιώνουν την ανάπτυξη[125]. Στην Αφρική σε περιπτώσεις διατροφικά στερημένων εγκύων αλλά και θηλαζουσών γυναικών μια συμπληρωματική δίαιτα με πολυβιταμίνες βελτίωσε την έκβαση και για τις μητέρες και για τα παιδιά[125]. Η διατροφική λήψη των ιχνοστοιχείων στη Συνιστώμενη Ημερήσια Δόση από HIV ενήλικες συνιστάται από τον Παγκόσμιο Οργανισμό Υγείας[127] [128]. Ο Π.Ο.Υ. επιπλέον δηλώνει ότι αρκετές μελέτες υποδεικνύουν ότι τα συμπληρώματα βιταμίνης Α, ψευδαργύρου και σιδήρου μπορούν να προκαλέσουν παρενέργειες σε ενήλικες με HIV λοίμωξη[128]. Επίσης δεν υπάρχουν αρκετές μαρτυρίες για την υποστήριξη της χρήσης βοτανολογικών θεραπειών[129].
Πρόγνωση
Το HIV/AIDS έχει πλέον γίνει σε πολλές περιοχές του κόσμου μια χρόνια ασθένεια παρά μια οξεία θανατηφόρος νόσος[130]. Η πρόγνωση της νόσου ποικίλλει και για τα προβλεπόμενα αποτελέσματα αποτελούν χρήσιμα μεγέθη ο αριθμός CD4 και το ιικό φορτίο[13]. Χωρίς θεραπεία ο μέσος όρος επιβίωσης μετά τη λοίμωξη με HIV εκτιμάται από 9 έως 11 έτη εξαρτώμενος από τον υπότυπο του ιού[131]. Μετά μία διάγνωση AIDS, αν δεν είναι διαθέσιμη η θεραπεία, η επιβίωση κυμαίνεται από 6 έως 19 μήνες[132] [133]. Η HAART και η κατάλληλη πρόληψη των ευκαιριακών λοιμώξεων μειώνουν το ποσοστό θανάτου κατά 80% και ανεβάζουν το προσδόκιμο επιβίωσης (εναπομείναντα έτη ζωής) για ένα νεοδιαγνωσμένο νεαρό ενήλικα στα 20 έως 50 χρόνια[130] [134] [135]. Αυτό σημαίνει περίπου τα δύο τρίτα έως σχεδόν το προσδόκιμο ζωής του γενικού πληθυσμού[134]. Αν η θεραπεία ξεκινήσει αργά στη διάρκεια της λοίμωξης, η πρόγνωση δεν είναι τόσο καλή[14], για παράδειγμα αν ξεκινήσει μετά τη διάγνωση AIDS το προσδόκιμο επιβίωσης είναι περίπου 10-40 χρόνια[14] [130]. Χωρίς θεραπεία τα μισά από τα βρέφη που γεννιούνται με HIV πεθαίνουν πριν την ηλικία των δύο χρόνων[116].
Οι πρωταρχικές αιτίες θανάτου από HIV/AIDS είναι οι ευκαιριακές λοιμώξεις και ο καρκίνος, συχνά αποτελώντας και οι δύο αιτίες αποτέλεσμα της προοδευτικής ανεπάρκειας του ανοσοποιητικού συστήματος[122] [137]. Ο κίνδυνος για καρκίνο φαίνεται να αυξάνει από τη στιγμή που ο αριθμός των CD4 πέσει κάτω από τα 500/μl[14]. Ο βαθμός της εξέλιξης της νόσου κλινικά διαφέρει ανάμεσα στα άτομα και έχει φανεί ότι επηρεάζεται από έναν αριθμό παραγόντων όπως η ευπάθεια του ατόμου και η λειτουργία του ανοσοποιητικού του συστήματος[138], η πρόσβασή του σε ιατρική φροντίδα και οι συλλοιμώξεις[132] [139], καθώς επίσης και το συγκεκριμένο στέλεχος (γένος) του ιού που εμπλέκεται στη λοίμωξη[140] [141].
Η συλλοίμωξη με φυματίωση είναι μια από τις κύριες αιτίες νόσου και θανάτου στα άτομα με HIV/AIDS, συμβαίνει στα 2/3 όλων των HIV οροθετικών ατόμων και οδηγεί στο 25% των θανάτων που σχετίζονται με το HIV/AIDS[142]. Επίσης ο ίδιος ο HIV είναι ο πιο σημαντικός παράγοντας κινδύνου για φυματίωση[143]. Η ηπατίτιδα C είναι άλλη μία πολύ κοινή συλλοίμωξη και αποτελεί επίσης περίπτωση όπου η μία νόσος επιταχύνει την εξέλιξη της άλλης[144]. Οι δύο πιο κοινοί καρκίνοι που σχετίζονται με το HIV/AIDS είναι το σάρκωμα Kaposi και το σχετιζόμενο με AIDS μη-Hogkin λέμφωμα[137]. Το προσδόκιμο επιβίωσης έχει πέσει στις χώρες που πλήττονται χειρότερα από το HIV/AIDS. Για παράδειγμα το 2006 εκτιμάται πως στη Μποτσουάνα έπεσε από τα 65 στα 35 χρόνια ζωής[4].
Ακόμη πάντως και με την αντιρετροϊκή αγωγή, μακροχρόνια τα άτομα με ΗΙV μπορεί να αντιμετωπίσουν νευρογνωσιακές διαταραχές[145], νευροπάθεια[147], οστεοπόρωση[146], καρκίνο[148] [149], ηπατική νόσο, νεφρική νόσο[150] και καρδιαγγειακή νόσο[113] και μάλιστα νωρίτερα και με χειρότερη πρόγνωση σε σχέση με τα αντίστοιχα νοσήματα του υπόλοιπου πληθυσμού. Τα νεώτερα δεδομένα δείχνουν ότι αυτές οι σοβαρές συν-νοσηρότητες οφείλονται στη μακροχρόνια HIV φλεγμονή αλλά ενισχύονται και από τις παρενέργειες της αντιρετροϊκής αγωγής.
Επιδημιολογία
Ο πρώτος βεβαιωμένος θάνατος από AIDS σημειώθηκε στα 1959 στην Αφρική (διαγνώστηκε αναδρομικά με εξέταση ιστών του θύματος), ενώ υπάρχει και ένας δεύτερος που υποστηρίζεται ότι προκλήθηκε από τη νόσο την ίδια χρονιά στην Αγγλία. Ακολούθησαν σποραδικοί θάνατοι στην Αφρική και τη Νορβηγία, όμως η μικρή συχνότητα δεν προκάλεσε ενδιαφέρον για περαιτέρω μελέτη. Γύρω στα τέλη της δεκαετίας του '60, ο ιός πέρασε στην Αϊτή κι από εκεί στις Ηνωμένες Πολιτείες.
Η πρώτη επίσημη ανακοίνωση για τη νόσο εκδόθηκε το 1981 από τις υπηρεσίες υγείας των ΗΠΑ και αφορούσε πέντε περιστατικά ομοφυλόφιλων ανδρών στο Λος Άντζελες. Λόγω του αρχικού περιορισμού της λοίμωξης στην πληθυσμιακή αυτή ομάδα, το AIDS χαρακτηρίστηκε ως περίεργη «νόσος των ομοφυλόφιλων», «καρκίνος των ομοφυλόφιλων» ή «πανούκλα των ομοφυλόφιλων», επειδή οι πρώτοι διαγνωσμένοι ασθενείς ανήκαν σε αυτή την πληθυσμιακή ομάδα. Αργότερα όμως επηρέασε και άλλες από τις λεγόμενες ομάδες υψηλού κινδύνου, όπως οι ναρκομανείς ή οι αιμορροφιλικοί, μολύνοντας τελικά και άτομα που δεν ανήκαν σε αυτές τις ομάδες. Σήμερα η ετεροσεξουαλική επαφή είναι ο κύριος τρόπος μετάδοσης. Μέχρι σήμερα έχουν πεθάνει λόγω του AIDS περίπου 25 εκατομμύρια άνθρωποι, ενώ περίπου 40 επιπλέον εκατομμύρια νοσούν. Στα πρώτα χρόνια εξάπλωσης του ιού αίσθηση προκάλεσαν οι θάνατοι του Φρέντι Μέρκιουρι, του Άντονι Πέρκινς, του Ροκ Χάντσον και άλλων διάσημων.
Μέχρι στιγμής έχουν αναγνωριστεί δυο είδη του ιού HIV, ο HIV-1 και ο HIV-2. Ο HIV-1 είναι αυτός που ευθύνεται για τη μεγάλη πλειοψηφία των μολύνσεων παγκόσμια (περίπου 90%), και επίσης είναι αυτός με τις περισσότερες μεταλλάξεις και υποτύπους. Ο HIV-2, που αναγνωρίστηκε το 1986 και θεωρείται προγενέστερος τύπος από τον HIV-1, εντοπίζεται σχεδόν αποκλειστικά στη Δυτική Αφρική, με λίγα περιστατικά σε χώρες που έχουν συχνή επικοινωνία με την περιοχή αυτή (όπως π.χ. η Γαλλία). Ο HIV-2 τείνει να μεταδίδεται σχετικά δυσκολότερα σε σχέση με το άλλο είδος, ενώ η εξέλιξη της νόσου στους φορείς HIV-2 είναι πιο αργή.
Στην Ελλάδα στα τέλη Οκτωβρίου του 2007 ο συνολικός αριθμός οροθετικών HIV ατόμων ήταν 8.584 από τους οποίους είχαν νοσήσει με AIDS οι 2.829, ενώ κατέληξαν στο θάνατο οι 1.552[85]. Ο αριθμός των κρουσμάτων που δηλώνονται κάθε χρόνο κορυφώθηκε το 1996, για να ακολουθήσει πτωτική πορεία στη συνέχεια μέχρι και το 2002, οπότε και παρουσιάστηκε μικρή σταθεροποίηση με ελαφρά αυξητικές τάσεις. Έρευνες που έγιναν κατά την τριετία 2005 ως 2007 έδειξαν ρυθμό αύξησης των περιστατικών μόλυνσης από AIDS περίπου 23%. Σύμφωνα με έρευνες, η εισαγωγή του υποτύπου Α του ιού του AIDS —του περισσότερο και ταχύτερα διαδεδομένου στην ελλαδική επικράτεια— έφτασε στη χώρα από την Αφρική το 1978 και σήμερα όχι μόνο έχει μεταδοθεί σε διαφορετικές πληθυσμιακές ομάδες αλλά διέσχισε και τα ελληνικά σύνορα προς την Αλβανία.
Ιστορία
Ανακάλυψη
Το AIDS παρατηρήθηκε κλινικά για πρώτη φορά το 1981 στις Ηνωμένες Πολιτείες[21]. Οι αρχικές περιπτώσεις ήταν ένα σύνολο από χρήστες ενέσιμων ναρκωτικών και ομοφυλόφιλους άνδρες που δεν είχαν κάποια γνωστή βλάβη ανοσοποιητικού και παρουσίαζαν συμπτώματα πνευμονίας από πνευμονοκύστη carinii (PCP), μια σπάνια ευκαιριακή λοίμωξη που ήταν γνωστό ότι συνέβαινε σε ανθρώπους με πολύ εκτεθειμένο ανοσοποιητικό σύστημα[158]. Σύντομα κατόπιν ένας επιπρόσθετος αριθμός ομοφυλόφιλων ανδρών ανέπτυξε έναν παλαιότερα σπάνιο καρκίνο του δέρματος, το σάρκωμα Kaposi (KS) [159] [160]. Πολλές ακόμη περιπτώσεις PCP και KS εμφανίστηκαν, θέτοντας σε συναγερμό τα αμερικανικά Κέντρα Ελέγχου και Πρόληψης Νοσημάτων (CDC) και δημιουργήθηκε μια ομάδα κρούσης από τα CDC προκειμένου να παρακολουθήσει και να ελέγξει το ξέσπασμα (της νόσου) [161].
Αρχικά το CDC δεν είχε κάποια επίσημη ονομασία για την ασθένεια και συχνά αναφερόταν σε αυτήν εν είδει των (επιμέρους) ασθενειών που συνδέονταν με τη νόσο, πχ. ως ‘’λεμφαδενοπάθεια’’ , μια ασθένεια που τελικά με βάση αυτήν οι εξερευνητές του HIV ονόμασαν πρωτότυπα τον ιό[162] [163]. Επίσης χρησιμοποιούσαν τον όρο ‘’σάρκωμα Kaposi και Ευκαιριακές Λοιμώξεις’’ με βάση τον οποίο είχε δημιουργηθεί και μια ομάδα κρούσης το 1981[164]. Στον τύπο είχα επινοηθεί ο όρος GRID που σήμαινε ’’gay related immune deficiency’’ (’’ανοσοανεπάρκεια συνδεόμενη με ομοφυλόφιλους’’) [165]. Το CDC ψάχνοντας ένα όνομα και ερευνώντας τις κοινότητες αυτών που είχαν μολυνθεί, επινόησε την ’’ασθένεια με τα 4H’’ καθώς φαινόταν ότι αφορούσε τους Αϊτινούς (Haitians), ομοφυλόφιλους (Homosexuals), αιμοφιλικούς (Hemophiliacs) και τους χρήστες ηρωίνης (Heroin users) [166]. Εντούτοις αφότου αποφασίστηκε ότι το AIDS δεν περιοριζόταν μόνο στην κοινότητα των ομοφυλόφιλων[164], έγινε συνειδητό ότι ο όρος GRID ήταν παραπλανητικός και τότε εισήχθη ο όρος AIDS σε μία συνεδρίαση τον Ιούλιο του 1982[167]. Τον όρο αυτό ξεκίνησε να χρησιμοποιεί το CDC από τον Σεπτέμβριο του 1982[168].
Το 1983 δύο χωριστές ερευνητικές ομάδες, μια αμερικανική με επικεφαλής το Robert Gallo και μια γαλλική με επικεφαλής τον κορυφαίο Γάλλο ερευνητή του ινστιτούτου Παστέρ στο Παρίσι Luc Montagnier, δήλωσαν η μία ανεξάρτητα από την άλλη, ότι ένας καινοφανής (νεοεμφανιζόμενος) ιός μπορεί να έχει προσβάλλει τους ασθενείς του AIDS. Δημοσίευσαν τα ευρήματά τους στην ίδια έκδοση του επιστημονικού περιοδικού Science[169] [170]. Ο Gallo ισχυρίστηκε πως ένας ιός που η ομάδα του είχε απομονώσει από έναν ασθενή του AIDS, είχε σχηματικά εκπληκτική ομοιότητα με ανθρώπινους Τ-λεμφοτροπικούς ιούς (HTLVs) μία κατηγορία ιών που η δική του ομάδα πρώτη είχε απομονώσει. Η ομάδα του Gallo έδωσε στον καινούργιο ιό που είχε απομονώσει την ονομασία HTLV-III.
Την ίδια περίοδο η ομάδα του Montagnier απομόνωσε έναν ιό από έναν ασθενή που παρουσίαζε οίδημα (πρήξιμο) των λεμφαδένων του λαιμού και σωματική εξασθένηση, δύο κλασσικά συμπτώματα του AIDS. Αντικρούοντας την έκθεση της ομάδας του Gallo, ο Montagnier και οι συνεργάτες του έδειξαν ότι οι πρωτεΐνες του πυρήνα του νέου ιού, ήταν ανοσολογικά διαφορετικές από τις αντίστοιχες του HTLV-I. Η ομάδα του Montagnier έδωσε στον ιό που είχε απομονώσει την ονομασία LAV (Lymphadenopathy-associated Virus - Ιό σχετιζόμενο με λεμφαδενοπάθεια) [161]. Η ονομασία HIV επιλέχθηκε συμβιβαστικά ανάμεσα στους δύο ισχυρισμούς (HTLV-III και LAV).
Προέλευση
Και οι δύο υπότυποι του ιού, οι HIV-1 και HIV-2 πιστεύεται ότι προέρχονται από μη-ανθρώπινα πρωτεύοντα θηλαστικά της Κεντροδυτικής Αφρικής και ότι μεταφέρθηκαν στους ανθρώπους (διαδικασία γνωστή ως ζωονοσία) στις αρχές του 20ού αιώνα[7]. Ο HIV-1 φαίνεται να έχει πρωτοεμφανιστεί στο νότιο Καμερούν μέσω εξέλιξης του SIV(cpz) (Simian Immunodeficiency Virus (chimpanzee) - πιθηκοειδής ιός ανοσοανεπάρκειας ο υπότυπος που μολύνει τους άγριους χιμπατζήδες. O HIV-1 κατάγεται από την ενδημία του SIVcpz στο υποείδος χιμπατζήδων που ονομάζεται Pan troglodytes troglodytes[171] [172]. Αντίστοιχα ο στενότερος συγγενής του HIV-2 είναι ο SIV(smm) δηλαδή ο υπότυπος του SIV που μολύνει το είδος πιθήκου sooty mangabey (Cercosebus alys alys) που είναι ένας πίθηκος του Παλαιού Κόσμου που ζει στη Δυτική Αφρική (από τη Νότια Σενεγάλη έως τη Δυτική Ακτή Ελεφαντοστού) [56].
Οι πίθηκοι του Νέου Κόσμου (δηλ. της Αμερικανικής ηπείρου) όπως ο πίθηκος-κουκουβάγια (είδος που δραστηριοποιείται τη νύχτα) είναι ανθεκτικοί στη λοίμωξη από HIV-1, πιθανώς λόγω γονιδιακής συγχώνευσης δύο ιικών ανθεκτικών γενών[173]. Ο HIV-1 εικάζεται ότι έχει υπερπηδήσει το (γενετικό) φραγμό των (ζωικών) ειδών σε τουλάχιστον 3 χωριστές περιπτώσεις, δίνοντας έτσι ύπαρξη στις 3 (γονιδιακές) ομάδες του ιού: Μ, Ν και Ο[174].
Υπάρχουν μαρτυρίες ότι άνθρωποι που συμμετέχουν σε δραστηριότητες σχετικές με τη χρήση του κρέατος αγρίων ζώων, είτε ως κυνηγοί είτε ως πωλητές του κρέατος, συχνά αποκτούν SIV[175]. Παρόλα αυτά ο SIV είναι ασθενής ιός, που τυπικά καταστέλλεται από το ανθρώπινο ανοσοποιητικό σύστημα μέσα σε μερικές εβδομάδες από τη λοίμωξη. Πιστεύεται πως χρειάζονται αρκετές μεταδόσεις του SIV, από άτομο σε άτομο με γρήγορη αλληλουχία, ώστε να του επιτραπεί να έχει ικανό χρόνο για να μεταλλαχθεί σε HIV[176]. Επιπλέον λόγω του σχετικά αργού ρυθμού μετάδοσης του ιού από άτομο σε άτομο, αυτός μπορεί να εξαπλωθεί στον ευρύτερο πληθυσμό μόνο με την παρουσία των οδών (καναλιών) υψηλού κινδύνου μετάδοσης οι οποίες πιστεύεται ότι δεν υπήρχαν στην Αφρική πριν τον 20ο αιώνα.
Τέτοια εξειδικευμένα υποδεικνυόμενα κανάλια υψηλού κινδύνου μετάδοσης, που επιτρέπουν στον ιό να προσαρμοστεί προς το ανθρώπινο είδος και να εξαπλωθεί, εξαρτώνται από τον υποδεικνυόμενο συγχρονισμό της διασταύρωσης από ζώο σε άνθρωπο. Γενετικές μελέτες του ιού υποδηλώνουν ότι ο πιο πρόσφατος κοινός πρόγονος της ομάδας Μ του HIV-1 κατάγεται χρονικά πίσω γύρω στο 1910[178]. Υποστηρικτές αυτής της χρονολογίας συνδέουν την επιδημία του HIV με την εμφάνιση της αποικιοκρατίας και την ανάπτυξη μεγάλων αποικιοκρατικών αφρικανικών πόλεων. Το γεγονός αυτό οδήγησε σε κοινωνικές μεταβολές, μέσα στις οποίες συμπεριλαμβάνονται ένας υψηλότερος βαθμός σεξουαλικής ασυδοσίας, η διάδοση της πορνείας, καθώς και η συνεπακόλουθη υψηλής συχνότητας εμφάνιση ασθενειών που προκαλούν έλκη στα γεννητικά όργανα (όπως η σύφιλη) στις αναδυόμενες αποικιοκρατικές πόλεις. Ενώ ο βαθμός μετάδοσης του HIV διαμέσου της κολπικής συνεύρεσης είναι χαμηλός υπό κανονικές συνθήκες, αυξάνει πολλαπλάσια αν ένας από τους παρτενέρ υποφέρει από μια σεξουαλικά μεταδιδόμενη λοίμωξη που προκαλεί έλκη στα γεννητικά όργανα. Οι πρώτες αποικιοκρατικές πόλεις του 1900 ήταν γνωστές λόγω της υψηλής διάδοσης της πορνείας και των γεννητικών ελκών, σε βαθμό που το 1928 το 45% των γυναικών κατοίκων της ανατολικής Κινσάσα πιστεύεται ότι ήταν πόρνες και το 1933 περίπου το 15% όλων των κατοίκων της ίδιας πόλης ήταν μολυσμένοι από κάποιο τύπο σύφιλης[178].
Μια εναλλακτική άποψη θεωρεί πως μη ασφαλείς ιατρικές πρακτικές στην Αφρική κατά τα χρόνια που ακολούθησαν το Β’ Παγκόσμιο πόλεμο, όπως η επαναχρησιμοποίηση μη αποστειρωμένων συριγγών στη διάρκεια μαζικών εμβολιασμών ή οι εκστρατείες για την αντιμετώπιση της ελονοσίας και άλλων λοιμώξεων με αντιβιοτικά, αποτέλεσαν την εναρκτήρια οδό που επέτρεψε στον ιό να προσαρμοστεί προς τους ανθρώπους και να εξαπλωθεί[176] [179] [180].
Η παλαιότερη καλά τεκμηριωμένη περίπτωση HIV σε άνθρωπο, χρονολογείται πίσω στο 1959 στο Κονγκό[181]. Ο ιός μπορεί ήδη να είχε κάνει την παρουσία του στις Ηνωμένες Πολιτείες από το 1966[182], όμως η προέλευση της μεγάλης πλειονότητας των μολύνσεων που συνέβησαν εκτός υπο-Σαχάριας Αφρικής (συμπεριλαμβανομένων και των ΗΠΑ) μπορεί να αποδοθεί σε ένα άγνωστο άτομο το οποίο μολύνθηκε από HIV στην Αϊτή και μετά έφερε τη λοίμωξη στις ΗΠΑ κάποια στιγμή γύρω στο 1969[183].
Κατόπιν η επιδημία εξαπλώθηκε γρήγορα ανάμεσα στις ομάδες υψηλού κινδύνου (αρχικά σε σεξουαλικά ασύδοτους άνδρες από το γκρουπ των ανδρών που κάνουν σεξ με άνδρες). Κατά το 1978 η εξάπλωση του HIV στους ομοφυλόφιλους αρσενικούς κατοίκους της Νέας Υόρκης και του Σαν Φρανσίσκο υπολογίστηκε σε ποσοστό 5%, υποδηλώνοντας ότι αρκετές χιλιάδες ατόμων στη χώρα είχαν ήδη μολυνθεί[183].
Κοινωνικά και πολιτιστικά δεδομένα
Στίγμα
Το στίγμα του AIDS υπάρχει στον κόσμο με διάφορους τρόπους που περιλαμβάνουν τον (κοινωνικό) εξοστρακισμό και απόρριψη, τη διακριτική συμπεριφορά (διακρίσεις) και την αποφυγή των ανθρώπων με HIV λοίμωξη.
Ακόμη συναντά κανείς περιπτώσεις όπως υποχρεωτικό τεστ για HIV χωρίς προηγούμενη συναίνεση ή προστασία της εμπιστευτικότητας (του απορρήτου), πράξεις βίας εναντίον ατόμων που είτε έχουν HIV λοίμωξη είτε εκλαμβάνεται ότι έχουν, καθώς και καραντίνα των οροθετικών στον HIV ατόμων[184]. Η βία που συνδέεται με το στιγματισμό ή ο φόβος για τη βία αυτή, εμποδίζει πολλά άτομα να αναζητήσουν να εξεταστούν για HIV[185], ή να επιστρέψουν για να πάρουν τα αποτελέσματα της εξέτασης ή να εξασφαλίσουν τη θεραπεία τους. Κατ’ αυτό τον τρόπο, αυτό που θα μπορούσε να είναι μια διαχειρίσιμη χρόνια ασθένεια γι’ αυτούς το μετατρέπουν πιθανώς σε θανατική καταδίκη και ταυτόχρονα διαιωνίζουν την εξάπλωση της λοίμωξης.
Ο στιγματισμός του AIDS διαιρείται περαιτέρω στις παρακάτω 3 κατηγορίες :
- Οργανικό στίγμα AIDS – μία αντανάκλαση του φόβου και της αντίληψης που πιθανά μπορεί να υπάρχει συνδεόμενη με μια θανατηφόρο και μεταδιδόμενη ασθένεια[186].
- Συμβολικό στίγμα AIDS – η χρήση του HIV/AIDS για την έκφραση συμπεριφορών προς τις κοινωνικές ομάδες ή τους τρόπους ζωής (lifestyle) που εκλαμβάνεται ότι συνδέονται με τη νόσο[186].
- Στίγμα ’’αβροφροσύνης’’ - στιγματισμός των ανθρώπων που είναι HIV-οροθετικοί ή αυτών που συνδέονται με το ζήτημα του HIV/AIDS[186].
Συχνά το στίγμα του AIDS εκφράζεται σε σύνδεση με ένα ή περισσότερα άλλα στίγματα, ιδιαίτερα αυτά που συνδέονται με την ομοφυλοφιλία, αμφιφυλοφιλία, τον σεξουαλικό υπερκαταναλωτισμό, την πορνεία και την ενδοφλέβια χρήση ναρκωτικών.
Σε πολλές ανεπτυγμένες χώρες υπάρχει μα συσχέτιση του AIDS με την ομοφυλοφιλία ή την αμφιφυλοφιλία και αυτή η συσχέτιση συνδέεται με υψηλά επίπεδα σεξουαλικών προκαταλήψεων, όπως συμπεριφορές εναντίον των ομοφυλόφιλων/ αμφιφυλόφιλων ατόμων[188]. Υπάρχει επίσης και μια εκλαμβανόμενη συσχέτιση ανάμεσα στο AIDS και όλες τις σεξουαλικές συμπεριφορές μεταξύ ανδρών, συμπεριλαμβανομένου και του σεξ μεταξύ μη μολυσμένων ανδρών[186].
Οικονομικός αντίκτυπος
Το HIV/AIDS επιδρά στα οικονομικά και των ατόμων και των χωρών[154]. Το ακαθάριστο εθνικό προϊόν των χωρών που έχουν επηρεαστεί έχει μειωθεί λόγω της έλλειψης ανθρώπινου δυναμικού[154] [189]. Χωρίς την κατάλληλη διατροφή, υγειονομική φροντίδα και φαρμακευτική αγωγή, μεγάλος αριθμός ανθρώπων πεθαίνει από επιπλοκές σχετιζόμενες με το AIDS. Στη διάρκεια της ασθένειάς τους οι άνθρωποι αυτοί, όχι μόνο δεν θα μπορούν να δουλέψουν, αλλά θα χρειαστεί να λάβουν σημαντική ιατρική φροντίδα. Για το έτος 2007 υπολογίζεται ότι υπήρχαν 12 εκατομμύρια ορφανά παιδιά λόγω AIDS[154]. Πολλά από αυτά δέχονται φροντίδα από τους ηλικιωμένους παππούδες και γιαγιάδες[190].
Πλήττοντας πολλούς νεαρούς ενήλικες, το AIDS μειώνει το φορολογούμενο πληθυσμό, ελαττώνοντας κατά συνέπεια τους διαθέσιμους πόρους για τις δημόσιες δαπάνες, όπως η εκπαίδευση και οι υπηρεσίες υγείας που δεν συνδέονται με το AIDS. Σαν αποτέλεσμα υπάρχει αυξημένη πίεση στα οικονομικά των κρατών και επιβράδυνση της ανάπτυξης των οικονομιών. Αυτό περαιτέρω καταλήγει σε βραδύτερη ανάπτυξη της φορολογικής βάσης, ένα αποτέλεσμα που ενισχύεται όταν υπάρχουν αυξημένες δαπάνες για την περίθαλψη των αρρώστων, την εργασιακή εκπαίδευση (προκειμένου να αντικαθιστώνται οι άρρωστοι εργάτες) αλλά και την περίθαλψη και φροντίδα των ορφανών του AIDS. Αυτό είναι ιδιαιτέρως αλήθεια όταν η απότομη αύξηση της θνητότητας των ενηλίκων μεταφέρει την όλη ευθύνη για τα ορφανά, από την οικογένειά τους στην κυβέρνηση που πρέπει να τα φροντίσει[190].
Στο επίπεδο του νοικοκυριού το AIDS έχει σαν αποτέλεσμα απώλεια εισοδήματος, αλλά και αυξημένες δαπάνες για υγειονομική περίθαλψη. Αυτό αφήνει στην οικογένεια λιγότερο εισόδημα για έξοδα εκπαίδευσης. Μια μελέτη στην Ακτή Ελεφαντοστού έδειξε ότι οικογένειες που είχαν ένα ασθενή του AIDS ξόδεψαν διπλάσια χρήματα σε έξοδα ιατρικής περίθαλψης σε σχέση με άλλα νοικοκυριά[191].
Θρησκεία και AIDS
Το ζήτημα της σχέσης της θρησκείας με το AIDS έχει υπάρξει αντικείμενο μεγάλης αμφισβήτησης στη διάρκεια των τελευταίων 20 ετών, πρωταρχικά λόγω του ότι πολλοί διακεκριμένοι θρησκευτικοί ηγέτες έχουν δημόσια δηλώσει την εναντίωσή τους στη χρήση προφυλακτικών[192] [193]. Σύμφωνα με μια έκθεση ενός αμερικανού ειδικού σε θέματα υγείας του Matthew Hanley που έχει τίτλο ’’The Catholic Church and the Global AIDS Crisis’’ (Η Καθολική Εκκλησία και η παγκόσμια κρίση του AIDS’’ ), η θρησκευτική προσέγγιση για την πρόληψη της εξάπλωσης του AIDS υποστηρίζει ότι είναι αναγκαίες πολιτισμικές αλλαγές, μεταξύ των οποίων μια επαναφορά της έμφασης υπέρ της πίστης μέσα στο γάμο και της σεξουαλικής εγκράτειας έξω απ’ αυτόν[193].
Επιπρόσθετα της πρόληψης κάποιες θρησκευτικές ομάδες έχουν παρεμποδίσει και διακόψει τη θεραπεία για το AIDS ! Σύμφωνα με το Αφρικανικό Δίκτυο Πολιτικής Υγείας κάποιες εκκλησίες στο Λονδίνο ισχυρίζονται ότι το AIDS θα θεραπευτεί με την προσευχή και σύμφωνα με έκθεση του Κέντρου Μελέτης Σεξουαλικής Υγείας και AIDS που εδρεύει στο Hacney( διοικητικός τομέας Βόρειου/Βορειοανατολικού Λονδίνου) αναφέρεται ότι αρκετοί άνθρωποι διέκοψαν την αγωγή τους, μερικές φορές μάλιστα μετά από άμεση προτροπή του πάστορά τους (τοπικού ιερέα) με αποτέλεσμα έναν αριθμό θανάτων[194].
Η εκκλησιαστική οργάνωση ’’The Synagogue Church Of All Nations” (Εκκλησία Συναγωγής όλων των Εθνών) διαφημίζει ένα ’’νερό επάλειψης’’ που προάγει τη θεραπεία από το Θεό, αν και η οργάνωση αρνείται ότι διαφημίζει τη διακοπή της θεραπείας[194]. Επίσης, μια αίτηση ευρεσιτεχνίας στις ΗΠΑ με αριθμό 2001051133 παρομοίως υποδεικνύει ότι καθαρό απεσταγμένο νερό που χορηγείται ενδοφλέβια εξαφανίζει τον HIV διαμέσου του ελέους του Θεού[195].
Η απεικόνιση του HIV/AIDS από τα media
Τα media έχουν απεικονίσει το HIV/AIDS με διάφορους τρόπους ανάλογα με τον τόπο και το χρόνο. Μία τάση της κοινωνικής ενημερότητας του HIV/AIDS είναι ότι παντού τα media ρέπουν στη δυσπιστία και το δισταγμό στο να το παρουσιάσουν αρχικά και ότι γεγονότα ή άνθρωποι – κλειδιά τείνουν στο να προκαλούν ευρεία συζήτηση για την ασθένεια σε διάφορους πληθυσμούς.
Μια από τις πρώτες περιπτώσεις AIDS με υψηλό προφίλ ήταν ο αμερικανός Rock Hudson ένας ομοφυλόφιλος ηθοποιός που ήταν παντρεμένος και διαζευγμένος παλαιότερα στη ζωή του και που πέθανε στις 2 Οκτωβρίου 1985 έχοντας ανακοινώσει ότι πάσχει από τον ιό στις 25 Ιουλίου της ίδιας χρονιάς. Είχε διαγνωστεί το 1984[196]. Μια αξιοσημείωτη απώλεια λόγω AIDS από τη Βρετανία την ίδια χρονιά ήταν ο Nicholas Eden, ομοφυλόφιλος, μέλος του Κοινοβουλίου και γιός του πρώην πρωθυπουργού Anthony Eden[197] [198]. O ιός πάντως αξίωσε ίσως το πιο διάσημο θύμα του στο πρόσωπο του Βρετανού ροκ σταρ Freddie Mercury στις 24 Νοεμβρίου 1991, όταν ο Mercury, επικεφαλής τραγουδιστής του συγκροτήματος Queen, πέθανε από ασθένεια σχετιζόμενη με το AIDS έχοντας ανακοινώσει ότι πάσχει από τη νόσο μόλις την προηγούμενη μέρα[199]. Εντούτοις είχε διαγνωστεί σαν HIV οροθετικός στη διάρκεια του 1987[200].
Μια από τις πρώτες περιπτώσεις προσβολής από τον ιό ενός ετεροφυλόφιλου ατόμου με υψηλό προφίλ ήταν ο Arthur Ashe, αμερικανός τενίστας. Διαγνώστηκε σαν HIV θετικός στις 31 Αυγούστου 1988, έχοντας πάρει τον ιό από μετάγγιση αίματος στη διάρκεια καρδιοχειρουργικής επέμβασης νωρίτερα στη δεκαετία του ’80. Περισσότερες εξετάσεις μέσα στις πρώτες 24 ώρες από την αρχική διάγνωση αποκάλυψαν ότι ο Ashe είχε AIDS, αλλά ο ίδιος δεν το ανακοίνωσε στο κοινό μέχρι τον Απρίλιο του 1992[201]. Πέθανε στις 6 Φεβρουαρίου 1993, σε ηλικία 49 ετών[202].
Άρνηση, συνωμοσία και παρανοήσεις
Μια μικρή ομάδα ατόμων εξακολουθούν να αμφισβητούν τη σύνδεση μεταξύ HIV και AIDS[203], την ύπαρξη του ίδιου του HIV ή ακόμη την εγκυρότητα της εξέτασης για HIV και των μεθόδων θεραπείας[204] [205]. Αυτοί οι ισχυρισμοί, γνωστοί ως απάρνηση του AIDS, έχουν μελετηθεί και απορριφθεί από την επιστημονική κοινότητα[206]. Παρόλα αυτά είχαν σημαντικό πολιτικό αντίκτυπο ιδιαίτερα στη Νότιο Αφρική, όπου ο εναγκαλισμός της επίσημης κυβέρνησης στους αρνητές ήταν υπεύθυνος για την αναποτελεσματική απάντηση στην επιδημία του AIDS σε αυτή τη χώρα και η κυβέρνηση κατηγορήθηκε για εκατοντάδες χιλιάδες μολύνσεις με HIV και θανάτους, που θα μπορούσαν να αποφευχθούν[207] [208] [209].
Το ’’Operation INFEKTION’’ (Επιχείρηση ΜΟΛΥΝΣΗ) ήταν μια παγκόσμιας εμβέλειας Σοβιετική επιχείρηση ενεργών μέτρων, με σκοπό τη διάδοση της πληροφορίας ότι οι ΗΠΑ είχαν δημιουργήσει το HIV/AIDS. Οι μελέτες δείχνουν ότι αρκετοί άνθρωποι πίστεψαν –και εξακολουθούν να πιστεύουν- τέτοιους ισχυρισμούς[210].
Υπάρχουν πολλές παρανοήσεις σχετικά με το HIV/AIDS. Τρεις από τις πιο κοινές είναι ότι το AIDS μπορεί να εξαπλωθεί με την καθημερινή επαφή, ότι η σεξουαλική επαφή με παρθένα μπορεί να θεραπεύσει το AIDS και ότι ο HIV μπορεί να μολύνει μόνο ομοφυλόφιλους άντρες και χρήστες ναρκωτικών. Άλλες παρανοήσεις είναι ότι κάθε πράξη πρωκτικής σεξουαλικής επαφής μεταξύ δύο μη μολυνθέντων ομοφυλόφιλων ανδρών μπορεί να οδηγήσει σε HIV λοίμωξη και ότι η ανοιχτή συζήτηση για την ομοφυλοφιλία και τον HIV στα σχολεία θα οδηγήσει σε αυξημένα ποσοστά ομοφυλοφιλίας και AIDS[211] [212].
Έρευνα
Η έρευνα για τη βελτίωση των τρεχουσών θεραπειών περιλαμβάνει τη μείωση των παρενεργειών των τωρινών φαρμάκων, περαιτέρω απλοποίηση των φαρμακευτικών σχημάτων για τη βελτίωση της συμμόρφωσης και τον καθορισμό της καλύτερης αλληλουχίας των σχημάτων για την αντιμετώπιση της φαρμακευτικής αντοχής του ιού. Εντούτοις μόνο ένα (προληπτικό) εμβόλιο πιστεύεται ότι είναι ικανό να σταματήσει την επιδημία. Και αυτό γιατί ένα εμβόλιο θα κόστιζε λιγότερο και έτσι θα γινόταν οικονομικά ανεκτό στις αναπτυσσόμενες χώρες και δεν θα απαιτούσε καθημερινή θεραπεία[213]. Όμως μετά από περισσότερο από 20 χρόνια έρευνας, ο HIV-1 παραμένει ένας δύσκολος στόχος για την παρασκευή ενός εμβολίου[213] [214].
Μεταμόσχευση εμβρυονικών κυττάρων (βλαστοκυττάρων)
Το 2007 ο Timothy Ray Brown[215] ένας 40χρονος HIV οροθετικός έκανε μεταμόσχευση βλαστοκυττάρων ως μέρος της θεραπείας του για οξεία μυελογενή λευχαιμία (AML - ΟΜΛ) [216] και μια δεύτερη μεταμόσχευση του έγινε ένα χρόνο αργότερα μετά από μια υποτροπή της νόσου. Ο δότης επιλέχτηκε όχι μόνο για την γενετική συμβατότητά του, αλλά και γιατί ήταν ομοζυγώτης (είχε πλήρη επικράτηση στο DNA του) μιας μετάλλαξης του CCR5-Δ32 (πρωτεΐνη-συνυποδοχέας του CD4 κυττάρου για τη σύνδεση του ιού με το κύτταρο). Η μετάλλαξη αυτή είναι γνωστό ότι προκαλεί αντίσταση στη λοίμωξη με HIV[217] [218]. Μετά από 20 μήνες χωρίς αντιρετροϊκή θεραπεία αναφέρθηκε ότι τα επίπεδα του HIV στο αίμα, το μυελό των οστών και το έντερο του Brown ήταν κάτω από το όριο ανίχνευσης[218]. Ο ιός παρέμεινε μη ανιχνεύσιμος για πάνω από 3 χρόνια από την πρώτη μεταμόσχευση[216]. Παρότι οι ερευνητές και μερικοί σχολιαστές έχουν χαρακτηρίσει αυτό το αποτέλεσμα ως ίαση, άλλοι προτείνουν ότι ο ιός μπορεί να παραμένει κρυμμένος σε ιστούς[220] όπως ο εγκέφαλος (δηλ. μια ιική δεξαμενή). Η θεραπεία με βλαστοκύτταρα παραμένει ερευνητική εξαιτίας της μη τεκμηρίωσής της, της νοσηρότητας και του κινδύνου θνητότητας που συνδέεται με τη μεταμόσχευση βλαστοκυττάρων και της δυσκολίας εύρεσης κατάλληλων δοτών[219] [221].
Ανοσοτροποποιητικοί παράγοντες
Συμπληρώνοντας τις προσπάθειες για τον έλεγχο της υιικής αντιγραφής, εξετάστηκαν σε δοκιμές στο παρελθόν αλλά και σε δοκιμές που συνεχίζονται ακόμη, οι ανοσοθεραπείες, που ενδέχεται να βοηθήσουν στην ανάκαμψη του ανοσοποιητικού συστήματος. Σε αυτές συμπεριλαμβάνονται η ιντερλευκίνη-2 και η ιντερλευκίνη-7[222].
Η αποτυχία των υποψήφιων εμβολίων να προστατεύσουν από την HIV λοίμωξη και την εξέλιξη σε AIDS, έχει οδηγήσει σε μία ανανεωμένη στόχευση πάνω στους βιολογικούς μηχανισμούς που ευθύνονται για τη λανθάνουσα περίοδο της HIV λοίμωξης. Μια περιορισμένη περίοδος θεραπείας που θα συνδυάζει αντιρετροϊκά μαζί με φάρμακα που στοχεύουν τη δεξαμενή λανθάνουσας λοίμωξης, μπορεί κάποια μέρα να επιτρέψει την πλήρη εξάλειψη της HIV λοίμωξης[223]. Οι ερευνητές έχουν ανακαλύψει ένα αντίσωμα-ένζυμο (αντίσωμα με δράση καταλύτη, όπως τα ένζυμα) που μπορεί να καταστρέψει τη θέση πρόσδεσης με το CD4 κύτταρο στην πρωτεΐνη gp120. Η πρωτεΐνη αυτή του ιού είναι κοινή σε όλες τις παραλλαγές του HIV καθώς αποτελεί το σημείο σύνδεσης για το Β λεμφοκύτταρο, με την επακόλουθη έκθεση του ανοσοποιητικού συστήματος[224].
Υποσημειώσεις
- ↑ 1,0 1,1 1,2 1,3 1,4 (Τσεχικά, Σλοβακικά) WikiSkripta.
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 2,7 www
.hiv .gov /hiv-basics /overview /about-hiv-and-aids /symptoms-of-hiv. Ανακτήθηκε στις 31 Δεκεμβρίου 2021. - ↑ Sepkowitz KA (June 2001). «AIDS—the first 20 years». N. Engl. J. Med. 344 (23): 1764–72. doi:. PMID 11396444.
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 Markowitz, edited by William N. Rom ; associate editor, Steven B. (2007). Environmental and occupational medicine (4th έκδοση). Philadelphia: Wolters Kluwer/Lippincott Williams & Wilkins. σελ. 745. ISBN 978-0-7817-6299-1.
- ↑ «HIV and Its Transmission». Centers for Disease Control and Prevention. 2003. Αρχειοθετήθηκε από το πρωτότυπο στις 4 Φεβρουαρίου 2005. Ανακτήθηκε στις 23 Μαΐου 2006.
- ↑ Kallings LO (2008). «The first postmodern pandemic: 25 years of HIV/AIDS». J Intern Med 263 (3): 218–43. doi:. PMID 18205765. http://www.blackwell-synergy.com/doi/full/10.1111/j.1365-2796.2007.01910.x.(subscription required)
- ↑ 7,0 7,1 7,2 UNAIDS 2011 pg. 1–10
- ↑ «Global Report Fact Sheet» (PDF). UNAIDS. 2010.
- ↑ Sharp, PM; Hahn, BH (2011 Sep). «Origins of HIV and the AIDS Pandemic». Cold Spring Harbor perspectives in medicine 1 (1): a006841. doi:. PMID 22229120.
- ↑ Gallo RC (2006). «A reflection on HIV/AIDS research after 25 years». Retrovirology 3: 72. doi:. PMID 17054781. PMC 1629027. http://www.retrovirology.com/content/3//72.
- ↑ National Institute of Allergy and Infectious Diseases, http://www.niaid.nih.gov/volunteer/hivlongterm/Pages/default.aspx, accessed July 5, 2011
- ↑ 12,0 12,1 12,2 Mandell, Bennett, and Dolan (2010). Chapter 121.
- ↑ 13,0 13,1 13,2 «Stages of HIV». U.S. Department of Health & Human Services. Δεκ. 2010. Ανακτήθηκε στις 13 Ιουνίου 2012.
- ↑ 14,00 14,01 14,02 14,03 14,04 14,05 14,06 14,07 14,08 14,09 14,10 14,11 14,12 14,13 WHO case definitions of HIV for surveillance and revised clinical staging and immunological classification of HIV-related disease in adults and children (PDF). Geneva: World Health Organization. 2007. σελίδες 6–16. ISBN 978-92-4-159562-9.
- ↑ Diseases and disorders. Tarrytown, NY: Marshall Cavendish. 2008. σελ. 25. ISBN 978-0-7614-7771-6.
- ↑ 16,00 16,01 16,02 16,03 16,04 16,05 16,06 16,07 16,08 16,09 16,10 16,11 16,12 Mandell, Bennett, and Dolan (2010). Chapter 118.
- ↑ 17,0 17,1 17,2 17,3 Σφάλμα αναφοράς: Σφάλμα παραπομπής: Λανθασμένο
<ref>. Δεν υπάρχει κείμενο για τις παραπομπές με όνομαDeut2010. - ↑ Elliott, Tom (2012). Lecture Notes: Medical Microbiology and Infection. John Wiley & Sons. σελ. 273. ISBN 978-1-118-37226-5.
- ↑ Evian, Clive (2006). Primary HIV/AIDS care: a practical guide for primary health care personnel in a clinical and supportive setting (Updated 4th έκδοση). Houghton [South Africa]: Jacana. σελ. 29. ISBN 978-1-77009-198-6.
- ↑ Radiology of AIDS. Berlin [u.a.]: Springer. 2001. σελ. 19. ISBN 978-3-540-66510-6.
|first1=missing|last1=in Authors list (βοήθεια) - ↑ 21,0 21,1 21,2 21,3 Blankson, JN (2010 Mar). «Control of HIV-1 replication in elite suppressors». Discovery medicine 9 (46): 261–6. PMID 20350494.
- ↑ Holmes CB, Losina E, Walensky RP, Yazdanpanah Y, Freedberg KA (2003). «Review of human immunodeficiency virus type 1-related opportunistic infections in sub-Saharan Africa». Clin. Infect. Dis. 36 (5): 656–662. doi:. PMID 12594648.
- ↑ Chu, C; Selwyn, PA (2011-02-15). «Complications of HIV infection: a systems-based approach». American family physician 83 (4): 395–406. PMID 21322514.
- ↑ 24,0 24,1 Mandell, Bennett, and Dolan (2010). Chapter 169.
- ↑ «AIDS». MedlinePlus. A.D.A.M. Ανακτήθηκε στις 14 Ιουνίου 2012.
- ↑ Sestak K (July 2005). «Chronic diarrhea and AIDS: insights into studies with non-human primates». Curr. HIV Res. 3 (3): 199–205. doi:. PMID 16022653.
- ↑ van der Kuyl, AC; Cornelissen, M (2007-09-24). «Identifying HIV-1 dual infections». Retrovirology 4: 67. doi:. PMID 17892568.
- ↑ 28,0 28,1 «HIV in the United States: An Overview». Center for Disease Control and Prevention. Μαρτίου 2012.
- ↑ 29,0 29,1 29,2 29,3 29,4 29,5 29,6 Boily MC, Baggaley RF, Wang L, Masse B, White RG, Hayes RJ, Alary M (February 2009). «Heterosexual risk of HIV-1 infection per sexual act: systematic review and meta-analysis of observational studies». The Lancet Infectious Diseases 9 (2): 118–129. doi:. PMID 19179227.
- ↑ Beyrer, C; Baral, SD; van Griensven, F; Goodreau, SM; Chariyalertsak, S; Wirtz, AL; Brookmeyer, R (2012 Jul 28). «Global epidemiology of HIV infection in men who have sex with men.». Lancet 380 (9839): 367-77. doi:. PMID 22819660.
- ↑ Yu, M; Vajdy, M (2010 Aug). «Mucosal HIV transmission and vaccination strategies through oral compared with vaginal and rectal routes». Expert opinion on biological therapy 10 (8): 1181–95. doi:. PMID 20624114.
- ↑ 32,0 32,1 32,2 Dosekun, O; Fox, J (2010 Jul). «An overview of the relative risks of different sexual behaviours on HIV transmission». Current opinion in HIV and AIDS 5 (4): 291–7. doi:. PMID 20543603.
- ↑ Ng, BE; Butler, LM; Horvath, T; Rutherford, GW (2011-03-16). Butler, Lisa M, επιμ. «Population-based biomedical sexually transmitted infection control interventions for reducing HIV infection». Cochrane database of systematic reviews (Online) (3): CD001220. doi:. PMID 21412869.
- ↑ Klimas, N; Koneru, AO; Fletcher, MA (2008 Jun). «Overview of HIV». Psychosomatic Medicine 70 (5): 523–30. doi:. PMID 18541903.
- ↑ Anderson, J (2012 Feb). «Women and HIV: motherhood and more». Current opinion in infectious diseases 25 (1): 58–65. doi:. PMID 22156896.
- ↑ Draughon, JE; Sheridan, DJ (2012). «Nonoccupational post exposure prophylaxis following sexual assault in industrialized low-HIV-prevalence countries: a review». Psychology, health & medicine 17 (2): 235–54. doi:. PMID 22372741.
- ↑ 37,0 37,1 Baggaley, RF; Boily, MC; White, RG; Alary, M (2006-04-04). «Risk of HIV-1 transmission for parenteral exposure and blood transfusion: a systematic review and meta-analysis». AIDS (London, England) 20 (6): 805–12. doi:. PMID 16549963.
- ↑ 38,0 38,1 Kripke, C (2007-08-01). «Antiretroviral prophylaxis for occupational exposure to HIV». American family physician 76 (3): 375–6. PMID 17708137.
- ↑ «Will I need a blood transfusion?» (PDF). NHS patient information. National Health Services. 2011. Ανακτήθηκε στις 29 Αυγούστου 2012.
- ↑ UNAIDS 2011 pg. 60–70
- ↑ «Blood safety ... for too few». WHO. 2001. Ανακτήθηκε στις 17 Ιανουαρίου 2006.
- ↑ 42,0 42,1 42,2 Reid, SR (2009-08-28). «Injection drug use, unsafe medical injections, and HIV in Africa: a systematic review». Harm reduction journal 6: 24. doi:. PMID 19715601.
- ↑ 43,0 43,1 «Basic Information about HIV and AIDS». Center for Disease Control and Prevention. Απριλίου 2012.
- ↑ «Why Mosquitoes Cannot Transmit AIDS [HIV virus]». Rci.rutgers.edu. Ανακτήθηκε στις 28 Ιουλίου 2010.
- ↑ 45,0 45,1 45,2 45,3 Σφάλμα αναφοράς: Σφάλμα παραπομπής: Λανθασμένο
<ref>. Δεν υπάρχει κείμενο για τις παραπομπές με όνομαMother2010. - ↑ «Fluids of transmission». AIDS.gov. United States Department of Health and Human Services. 1 Νοεμβρίου 2011. Ανακτήθηκε στις 14 Σεπτεμβρίου 2012.
- ↑ 47,0 47,1 Thorne, C; Newell, ML (2007 Jun). «HIV». Seminars in fetal & neonatal medicine 12 (3): 174–81. doi:. PMID 17321814.
- ↑ Alimonti JB, Ball TB, Fowke KR (2003). «Mechanisms of CD4+ T lymphocyte cell death in human immunodeficiency virus infection and AIDS». J. Gen. Virol. 84 (7): 1649–1661. doi:. PMID 12810858.
- ↑ International Committee on Taxonomy of Viruses (2002). «61.0.6. Lentivirus». National Institutes of Health. Αρχειοθετήθηκε από το πρωτότυπο στις 18 Απριλίου 2006. Ανακτήθηκε στις 25 Ιουνίου 2012.
- ↑ International Committee on Taxonomy of Viruses (2002). «61. Retroviridae». National Institutes of Health. Αρχειοθετήθηκε από το πρωτότυπο στις 29 Ιουνίου 2006. Ανακτήθηκε στις 25 Ιουνίου 2012.
- ↑ Lévy, J. A. (1993). «HIV pathogenesis and long-term survival». AIDS 7 (11): 1401–10. doi:. PMID 8280406.
- ↑ Smith, Johanna A.; Daniel, René (Division of Infectious Diseases, Center for Human Virology, Thomas Jefferson University, Philadelphia) (2006). «Following the path of the virus: the exploitation of host DNA repair mechanisms by retroviruses». ACS Chem Biol 1 (4): 217–26. doi:. PMID 17163676.
- ↑ Martínez, edited by Miguel Angel (2010). RNA interference and viruses : current innovations and future trends. Norfolk: Caister Academic Press. σελ. 73. ISBN 9781904455561.
- ↑ Immunology, infection, and immunity. Washington, D.C.: ASM Press. 2004. σελ. 550. ISBN 9781555812461.
|first1=missing|last1=in Authors list (βοήθεια) - ↑ Gilbert, PB και άλλοι. (28 February 2003). «Comparison of HIV-1 and HIV-2 infectivity from a prospective cohort study in Senegal». Statistics in Medicine 22 (4): 573–593. doi:. PMID 12590415.
- ↑ Reeves, J. D. and Doms, R. W (2002). «Human Immunodeficiency Virus Type 2». J. Gen. Virol. 83 (Pt 6): 1253–65. doi:. PMID 12029140.
- ↑ Piatak, M., Jr, Saag, M. S., Yang, L. C., Clark, S. J., Kappes, J. C., Luk, K. C., Hahn, B. H., Shaw, G. M. and Lifson, J.D. (1993). «High levels of HIV-1 in plasma during all stages of infection determined by competitive PCR». Science 259 (5102): 1749–1754. doi:. PMID 8096089. Bibcode: 1993Sci...259.1749P.
- ↑ Pantaleo G, Demarest JF, Schacker T, Vaccarezza M, Cohen OJ, Daucher M, Graziosi C, Schnittman SS, Quinn TC, Shaw GM, Perrin L, Tambussi G, Lazzarin A, Sekaly RP, Soudeyns H, Corey L, Fauci AS. (1997). «The qualitative nature of the primary immune response to HIV infection is a prognosticator of disease progression independent of the initial level of plasma viremia». Proc Natl Acad Sci U S A. 94 (1): 254–258. doi:. PMID 8990195. Bibcode: 1997PNAS...94..254P.
- ↑ Guss DA (1994). «The acquired immune deficiency syndrome: an overview for the emergency physician, Part 1». J Emerg Med 12 (3): 375–84. doi:. PMID 8040596.
- ↑ Hel Z, McGhee JR, Mestecky J (June 2006). «HIV infection: first battle decides the war». Trends Immunol. 27 (6): 274–81. doi:. PMID 16679064.
- ↑ Arie J. Zuckerman et al. (eds) (2007). Principles and practice of clinical virology (6th έκδοση). Hoboken, N.J.: Wiley. σελ. 905. ISBN 978-0-470-51799-4.
- ↑ Mehandru S, Poles MA, Tenner-Racz K, Horowitz A, Hurley A, Hogan C, Boden D, Racz P, Markowitz M (September 2004). «Primary HIV-1 infection is associated with preferential depletion of CD4+ T cells from effector sites in the gastrointestinal tract». J. Exp. Med. 200 (6): 761–70. doi:. PMID 15365095.
- ↑ Brenchley JM, Schacker TW, Ruff LE, Price DA, Taylor JH, Beilman GJ, Nguyen PL, Khoruts A, Larson M, Haase AT, Douek DC (September 2004). «CD4+ T cell depletion during all stages of HIV disease occurs predominantly in the gastrointestinal tract». J. Exp. Med. 200 (6): 749–59. doi:. PMID 15365096.
- ↑ 64,0 64,1 editor, Julio Aliberti, (2011). Control of Innate and Adaptive Immune Responses During Infectious Diseases. New York, NY: Springer Verlag. σελ. 145. ISBN 978-1-4614-0483-5.
- ↑ Appay V, Sauce D (January 2008). «Immune activation and inflammation in HIV-1 infection: causes and consequences». J. Pathol. 214 (2): 231–41. doi:. PMID 18161758.
- ↑ Brenchley JM, Price DA, Schacker TW, Asher TE, Silvestri G, Rao S, Kazzaz Z, Bornstein E, Lambotte O, Altmann D, Blazar BR, Rodriguez B, Teixeira-Johnson L, Landay A, Martin JN, Hecht FM, Picker LJ, Lederman MM, Deeks SG, Douek DC (December 2006). «Microbial translocation is a cause of systemic immune activation in chronic HIV infection». Nat. Med. 12 (12): 1365–71. doi:. PMID 17115046.
- ↑ 67,0 67,1 Schneider, E; Whitmore, S; Glynn, KM; Dominguez, K; Mitsch, A; McKenna, MT; Centers for Disease Control and Prevention, (CDC) (2008-12-05). «Revised surveillance case definitions for HIV infection among adults, adolescents, and children aged <18 months and for HIV infection and AIDS among children aged 18 months to <13 years--United States, 2008». MMWR. Recommendations and reports : Morbidity and mortality weekly report. Recommendations and reports / Centers for Disease Control 57 (RR–10): 1–12. PMID 19052530.
- ↑ 68,0 68,1 Kellerman, S; Essajee, S (2010 Jul 20). «HIV testing for children in resource-limited settings: what are we waiting for?». PLoS medicine 7 (7): e1000285. doi:. PMID 20652012.
- ↑ 69,0 69,1 69,2 UNAIDS 2011 pg. 70–80
- ↑ Crosby, R; Bounse, S (2012 Mar). «Condom effectiveness: where are we now?». Sexual health 9 (1): 10–7. doi:. PMID 22348628.
- ↑ «Condom Facts and Figures». WHO. 2003. Ανακτήθηκε στις 17 Ιανουαρίου 2006. Unknown parameter
|month=ignored (βοήθεια) - ↑ Gallo, MF; Kilbourne-Brook, M; Coffey, PS (2012 Mar). «A review of the effectiveness and acceptability of the female condom for dual protection». Sexual health 9 (1): 18–26. doi:. PMID 22348629.
- ↑ Celum, C; Baeten, JM (2012 Feb). «Tenofovir-based pre-exposure prophylaxis for HIV prevention: evolving evidence». Current opinion in infectious diseases 25 (1): 51–7. doi:. PMID 22156901.
- ↑ Baptista, M; Ramalho-Santos, J (2009-11-01). «Spermicides, microbicides and antiviral agents: recent advances in the development of novel multi-functional compounds». Mini reviews in medicinal chemistry 9 (13): 1556–67. doi:. PMID 20205637.
- ↑ Siegfried, N; Muller, M; Deeks, JJ; Volmink, J (2009-04-15). Siegfried, Nandi, επιμ. «Male circumcision for prevention of heterosexual acquisition of HIV in men». Cochrane database of systematic reviews (Online) (2): CD003362. doi:. PMID 19370585.
- ↑ «WHO and UNAIDS announce recommendations from expert consultation on male circumcision for HIV prevention». World Health Organization. 28 Μαρτίου 2007.
- ↑ Larke, N (2010 May 27 – Jun 9). «Male circumcision, HIV and sexually transmitted infections: a review». British journal of nursing (Mark Allen Publishing) 19 (10): 629–34. PMID 20622758.
- ↑ Eaton, L; Kalichman, SC (2009 Nov). «Behavioral aspects of male circumcision for the prevention of HIV infection». Current HIV/AIDS reports 6 (4): 187–93. doi:. PMID 19849961.(subscription required)
- ↑ Kim, HH; Li, PS, Goldstein, M (2010 Nov). «Male circumcision: Africa and beyond?». Current opinion in urology 20 (6): 515–9. doi:. PMID 20844437.
- ↑ Templeton, DJ; Millett, GA, Grulich, AE (2010 Feb). «Male circumcision to reduce the risk of HIV and sexually transmitted infections among men who have sex with men». Current opinion in infectious diseases 23 (1): 45–52. doi:. PMID 19935420.
- ↑ Wiysonge, CS.; Kongnyuy, EJ.; Shey, M.; Muula, AS.; Navti, OB.; Akl, EA.; Lo, YR. (2011). Wiysonge, Charles Shey, επιμ. «Male circumcision for prevention of homosexual acquisition of HIV in men». Cochrane Database Syst Rev (6): CD007496. doi:. PMID 21678366.
- ↑ Utz-Billing I, Kentenich H (December 2008). «Female genital mutilation: an injury, physical and mental harm». J Psychosom Obstet Gynaecol 29 (4): 225–9. doi:. PMID 19065392.
- ↑ Eaton LA, Kalichman S (December 2007). «Risk compensation in HIV prevention: implications for vaccines, microbicides, and other biomedical HIV prevention technologies». Curr HIV/AIDS Rep 4 (4): 165–72. doi:. PMID 18366947.
- ↑ Utz-Billing I, Kentenich H (December 2008). «Female genital mutilation: an injury, physical and mental harm». J Psychosom Obstet Gynaecol 29 (4): 225–9. doi:. PMID 19065392.
- ↑ Η Καθημερινή, 2 Δεκεμβρίου 2007, «Οι νέοι «κλείνουν» τα μάτια στον ενδεχόμενο κίνδυνο για έιτζ».
Πηγές
- Μακεδονία, 29 Νοεμβρίου 2007, «AIDS. Ανησυχητική έξαρση των περιστατικών στη Θεσσαλονίκη».
- Ελευθεροτυπία, 30 Νοεμβρίου 2007, «AIDS: 25.000 «κρυφοί» φορείς στην Ελλάδα».
- Ελεύθερος Τύπος, 30 Νοεμβρίου 2007, «AIDS: Με δέκα μορφές ο ιός στην Ελλάδα».
- Γκούβας Χαράλαμπος: "ΑIDS, ερωτήματα και αλήθειες", εκδόσεις "Ωκεανίδα", Αθήνα 1985
Εξωτερικοί σύνδεσμοι
- Συμβουλευτική για τη Λοίμωξη και Νόσο HIV.
- Hiv.gr, σελίδα ενημέρωσης για οροθετικούς ή μη.
- Νέοι άνθρωποι και AIDS από την UNICEF.
- HIV/AIDS από την Ευρωπαϊκή Επιτροπή.
 AIDS, ασθένεια και ίαση (Αρχείο ντοκιμαντέρ της ΕΡΤ)
AIDS, ασθένεια και ίαση (Αρχείο ντοκιμαντέρ της ΕΡΤ) AIDS, η άλλη πραγματικότητα (Αρχείο ντοκιμαντέρ της ΕΡΤ)
AIDS, η άλλη πραγματικότητα (Αρχείο ντοκιμαντέρ της ΕΡΤ)
—
Πρότυπο:Link FA Πρότυπο:Link FA Πρότυπο:Link FA Πρότυπο:Link FA Πρότυπο:Link FA Πρότυπο:Link FA Πρότυπο:Link FA

