Χημική κινητική
| Το λήμμα δεν περιέχει πηγές ή αυτές που περιέχει δεν επαρκούν. |
| Αυτό το λήμμα χρειάζεται επιμέλεια ώστε να ανταποκρίνεται σε υψηλότερες προδιαγραφές ορθογραφικής και συντακτικής ποιότητας ή μορφοποίησης. Αίτιο: μορφοποίηση, σύνδεσμοι, βιβλιογραφία Για περαιτέρω βοήθεια, δείτε τα λήμματα πώς να επεξεργαστείτε μια σελίδα και τον οδηγό μορφοποίησης λημμάτων. |
| Μέρος σειράς στη |
| Χημική μηχανική |
|---|
| Βασικές αρχές |
| Μονάδα διεργασιών |
| Πτυχές |
|
|
Η χημική κινητική, που είναι επίσης γνωστή και ως κινητική των χημικών αντιδράσεων, είναι η μελέτη της ταχύτητας των χημικών διεργασιών. Η Χημική κινητική διερευνά για το πώς διαφορετικές πειραματικές συνθήκες μπορούν να επηρεάσουν την ταχύτητα μιας χημικής αντίδρασης και δινει πληροφορίες σχετικά με το μηχανισμό της αντίδρασης και τις μεταβατικές καταστάσεις, όπως και μαθηματικά μοντέλα που μπορούν να περιγράψουν τα χαρακτηριστικά μιας χημικής αντίδρασης. Το 1864 , ο Πέτερ Βέγκε και ο Cato Guldberg πρωτοστάτησαν στην ανάπτυξη της χημικής κινητικής δίνοντας το νόμο δράσεως των μαζών, ο οποίος ορίζει ότι η ταχύτητα μιας χημικής αντίδρασης είναι ανάλογη με την ποσότητα των αντιδρώντων ουσιών .[1][2][3]
Η Χημική κινητική ασχολείται με τον πειραματικό προσδιορισμό της ταχύτητας της αντίδρασης από τον οποίο προέρχονται οι νόμοι της ταχύτητας και οι σταθερές ταχύτητας. Σχετικά απλοί νόμοι ταχύτητας υπάρχουν για τις αντιδράσεις μηδενικής τάξης (για τις οποίες οι ταχύτητες αντίδρασης είναι ανεξάρτητες από τη συγκέντρωση). Διαφορετικοί νόμοι ταχύτητας προκύπτουν για τις αντιδράσεις πρωτης τάξης, και αντιδράσεις δεύτερης τάξης. Οι απλές αντιδράσεις, δηλαδή οι αντιδράσεις που γίνονται σε ένα βήμα, ακολουθούν το νόμο δράσης της μάζας. Αλλά ο νόμος για τις πολύπλοκες αντιδράσεις που γίνονται σε πολλά στάδια πρέπει να προέρχεται από το συνδυασμό των νόμων των επιμέρους στοιχειωδών βημάτων, και μπορεί να γίνει αρκετά πολύπλοκος. Σε διαδοχικές αντιδράσεις, η ταχύτητα του πιο αργού σταδίου καθορίζει συχνά την ταχύτητα της αντίδρασης. Η ενέργεια ενεργοποίησης για μια αντίδραση προσδιορίζεται πειραματικά μέσω της εξίσωσης Arrhenius και της εξίσωσης Eyring. Οι κύριοι παράγοντες που επηρεάζουν την ταχύτητα της αντίδρασης περιλαμβάνουν: την φυσική κατάσταση των αντιδρώντων, την συγκέντρωση των αντιδραστηρίων,την θερμοκρασία στην οποία λαμβάνει χώρα η αντίδραση, και κατά πόσον ή όχι κάποιοι καταλύτες είναι παρόντες στην αντίδραση.
Παράγοντες που επηρεάζουν την ταχύτητα αντίδρασης[Επεξεργασία | επεξεργασία κώδικα]
Φύση των αντιδρώντων[Επεξεργασία | επεξεργασία κώδικα]
Ανάλογα με τις ουσίες που αντιδρούν, ο ρυθμός αντίδρασης ποικίλλει. Οι αντιδράσεις οξέος βάσεως (εξουδετέρωση), ο σχηματισμός αλάτων και ανταλλαγή ιόντων (αντιδράσεις διπλής αντικατάστασης) είναι γρήγορες αντιδράσεις. Όταν σχηματίζονται ομοιοπολικοί δεσμοί μεταξύ των μορίων τότε σχηματίζονται μεγάλα μόρια και οι αντιδράσεις τείνουν να είναι πολύ αργές. Η φύση των αντιδρώντων μορίων επηρεάζουν σε μεγάλο βαθμό το ρυθμό της μετατροπής τους σε προϊόντα.
Φυσική κατάσταση[Επεξεργασία | επεξεργασία κώδικα]
Η φυσική κατάσταση (στερεού, υγρού, ή αερίου) ενός αντιδραστηρίου είναι επίσης σημαντικός παράγοντας του ρυθμού της αλλαγής. Όταν τα αντιδρώντα βρίσκονται στην ίδια φάση (ομογενείς αντιδράσεις), όπως στο υδατικό διάλυμα, η θερμική κίνηση τους φέρνει σε επαφή. Ωστόσο, όταν βρίσκονται σε διαφορετικές φάσεις (ετερογενείς αντιδράσεις), η αντίδραση περιορίζεται στην επιφάνεια επαφής μεταξύ των αντιδρώντων φάσεων. Στην περίπτωση ενός υγρού και ενός αερίου, η αντίδραση μπορεί να συμβεί μόνο στην περιοχή επαφής τους, δηλαδή στην επιφάνεια του υγρού. Τότε χρειάζεται έντονη ανακίνηση και ανάδευση για να φέρει την αντίδραση σε ολοκλήρωση. Αυτό οφείλεται στο ότι όσο πιο λεπτοδιαμερισμένο είναι το στερεό ή υγρό αντιδραστήριο (μεγαλύτερο εμβαδόν επιφανείας ανά μονάδα όγκου) τόσο μεγαλύτερη είναι η επαφή με το άλλο αντιδραστήριο, έτσι επιτυνχάνεται η ταχύτερη αντίδραση.
Για να δείτε μια αναλογία, για παράδειγμα: μια πυρκαγιά εξελίσσεται ταχύτατα, σχεδόν εκρηκτικά, όταν κάποιος χρησιμοποιεί ροκανίδια και μικρά κλαδιά και δεν ξεκινά σχεδόν καθόλου με μεγάλους κορμούς. Στην οργανική χημεία ο διαλύτης μέσα στον οποίο διαλύονται τα αντιδρώντα παίζει σημαντικό ρόλο, και οι ομογενείς αντιδράσεις λαμβάνουν χώρα ταχύτερα από τις ετερογενείς αντιδράσεις.
Συγκέντρωση[Επεξεργασία | επεξεργασία κώδικα]
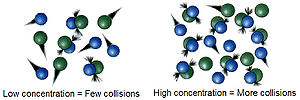
Οι αντιδράσεις οφείλονται σε επιτυχείς συγκρούσεις των αντιδρώντων ειδών, μορίων ή ιόντων. Η συχνότητα με την οποία τα μόρια ή ιόντα συγκρούονται εξαρτάται απο τις συγκεντρώσεις τους. Όσο πιο πολυσύχναστη είναι η μοριακή φάση, τόσο πιο πιθανό είναι τα μόρια να συγκρουστούν και να αντιδράσουν μεταξύ τους. Έτσι, η αύξηση στις συγκεντρώσεις των αντιδρώντων θα οδηγήσει συνήθως στην αντίστοιχη αύξηση της ταχύτητας της αντίδρασης, ενώ η μείωση των συγκεντρώσεων θα έχει συνήθως αντίστροφη επίδραση. Για παράδειγμα, η καύση που λαμβάνει χώρα στον αέρα (με 21% οξυγόνο) θα συμβεί πολύ ταχύτερα σε καθαρό οξυγόνο.
Θερμοκρασία[Επεξεργασία | επεξεργασία κώδικα]
Η θερμοκρασία συνήθως έχει σημαντική επίδραση στο ρυθμό μιας χημικής αντίδρασης. Μόρια σε υψηλότερη θερμοκρασία έχουν περισσότερη θερμική ενέργεια και τα μόρια κινούνται με μεγαλύτερες ταχύτητες. Παρά το γεγονός ότι η συχνότητα των συγκρούσεων είναι μεγαλύτερη σε υψηλότερες θερμοκρασίες, αυτό από μόνο του συμβάλλει μόνο κατά ένα πολύ μικρό ποσοστό στην αύξηση της ταχύτητας της αντίδρασης. Τον καθοριστικό ρόλο παίζει η σφοδρότητα της σύγκρουσης, δηλαδή το κατά πόσον τα συγκρουόμενα μόρια θα συγκρουστούν με επαρκή σφοδρότητα ώστε οι δεσμοί μεταξύ των ατόμων τους να σπάσουν και τα άτομα να μείνουν ελεύθερα ή χαλαρά ενωμένα ώστε να δημιουργήσουν νέους δεσμούς. Η ενέργεια που πρέπει να έχουν ονομάζεται ενέργεια ενεργοποίησης Εα. Οι περισσότερες από τις μοριακές συγκρούσεις δεν είναι αποτελεσματικές. Συνεπώς το πολύ σημαντικό είναι η αναλογία των αντιδρώντων μορίων με επαρκή ενέργεια για να αντιδράσουν (ενέργεια μεγαλύτερη από την ενέργεια ενεργοποίησης: E> Εα). Η αναλογία αυτή αυξάνεται με την αύξηση της θερμοκρασίας όπως εξηγείται λεπτομερώς από την κατανομή Maxwell-Boltzmann της θερμικής μοριακής ενέργειας.
Ο «κανόνας» που το ποσοστό των χημικών αντιδράσεων διπλασιάζεται για κάθε 10°C αύξησης της θερμοκρασίας είναι μια κοινή παρερμηνεία. Αυτό είναι μια διασταλτική γενίκευση της ειδικής περίπτωσης των βιολογικών συστημάτων, όπου το α (συντελεστής θερμοκρασίας στην εξίσωση του Arrhenius) είναι συχνά μεταξύ 1,5 και 2,5.
Η επίδραση της θερμοκρασίας στην κινητική μιας αντίδρασης μπορεί επίσης να μελετηθεί με την τεχνική "άλμα θερμοκρασίας". Αυτό περιλαμβάνει τη χρήση μιας απότομης αύξηση της θερμοκρασίας και μετρώντας το χρόνο χαλάρωσης που χρειάζεται μέχρι να επέλθει η ισορροπία. Μια ιδιαίτερα χρήσιμη συσκευή για το "άλμα θερμοκρασίας" είναι ένας σωλήνας μέσα στον οποίο η θερμοκρασία ενός αερίου μπορεί γρήγορα να πηδήξει κατά περισσότερο από 1000 βαθμούς.
Καταλύτες[Επεξεργασία | επεξεργασία κώδικα]

Ένας καταλύτης είναι μια ουσία που επιταχύνει την ταχύτητα μιας χημικής αντίδρασης αλλά παραμένει χημικά αμετάβλητος μετά την αντίδραση. Ο καταλύτης αυξάνει την ταχύτητα της αντίδρασης, παρέχοντας έναν διαφορετικό μηχανισμό αντίδρασης που μπορεί να συμβεί με χαμηλότερη ενέργεια ενεργοποίησης. Στην αυτοκατάλυση, ένα προϊόν της αντίδρασης είναι από μόνο του καταλύτης για την εν λόγω αντίδραση και οδηγεί σε θετική ανατροφοδότηση. Οι πρωτεΐνες που δρουν ως καταλύτες σε αντιδράσεις που ονομάζονται βιοχημικα ένζυμα. Κινητικές Michaelis-Menten περιγράφουν την ταχύτητα αντιδράσεων μέσω των ενζύμων που διαμεσολαβούν. Ένας καταλύτης δεν επηρεάζει τη θέση της χημικής ισορροπίας, καθώς ο καταλύτης επιταχύνει τις αντιδράσεις εξίσου και προς τις δύο κατευθύνσεις.
Σε ορισμένα οργανικά μόρια, ειδικοί υποκαταστάτες μπορεί να έχουν επίδραση στην ταχύτητα αντίδρασης που περιλαμβάνει γειτονικές ομάδες και όχι τους ίδιους τους υποκαταστάτες.
Πίεση[Επεξεργασία | επεξεργασία κώδικα]
Η αύξηση της πίεσης σε ένα αέριο που αντιδρά θα αυξήσει τον αριθμό των συγκρούσεων μεταξύ αντιδρώντων, αυξάνοντας την ταχύτητα της αντίδρασης. Αυτό συμβαίνει επειδή η συγκέντρωση ενός αερίου είναι ευθέως ανάλογη με την μερική πίεση του αερίου. Είναι παρόμοιο με το αποτέλεσμα της αύξησης της συγκέντρωσης του διαλύματος.
Εκτός από αυτή την απλή επίδραση λόγω της μεταβολής της συγκέντρωση στο "νόμο δράσεως των μαζών", όπου ο συντελεστής της ταχύτητας παραμένει ο ίδιος, υπάρχει και η περίπτωση όπου αυτός μπορεί να αλλάξει λόγω της πίεσης. Οι συντελεστές ταχύτητας πολλών αντιδράσεων που βρίσκονται σε αέρια φάση υψηλής θερμοκρασίας μπορεί να αλλάξουν αν στο αέριο αντιδρών μείγμα προστεθεί ένα αδρανές αέριο. Αυτό το φαινόμενο που ονομάζεται και χημική ενεργοποίηση. Τα φαινόμενα αυτά οφείλονται σε εξώθερμες ή ενδόθερμες αντιδράσεις που συμβαίνουν πιο γρήγορα από ό,τι η μεταφορά θερμότητας, εξαναγκάζοντας τα μόρια να έχουν μη κανονικές κατανομές θερμικής ενέργειας (non-Boltzmann distribution). Η αύξηση της πίεσης αυξάνει τον ρυθμό μεταφοράς θερμότητας μεταξύ των μορίων που αντέδρασαν και ελευθέρωσαν θερμική ενέργεια και του υπόλοιπου συστήματος της αντίδρασης, μειώνοντας το φαινόμενο αυτό.
Η Κινητική μιας αντίδρασης μπορεί επίσης να μελετηθεί με την τεχνική του άλματος πίεσης. Αυτό συνεπάγεται γρήγορες αλλαγές στην πίεση και παρατήρηση του χρόνου χαλάρωσης που χρειάζεται μέχρι να επέλθει η ισορροπία.
Πειραματικές μέθοδοι[Επεξεργασία | επεξεργασία κώδικα]
Ο πειραματικός προσδιορισμός των ταχυτήτων αντίδρασης περιλαμβάνει τη μέτρηση του πως οι συγκεντρώσεις των αντιδρώντων ή των προϊόντων αλλάζουν με την πάροδο του χρόνου. Για παράδειγμα, η συγκέντρωση ενός αντιδρώντος μπορεί να μετρηθεί με φασματοφωτομετρία σε ένα μήκος κύματος όπου κανένα άλλο αντιδρών ή προϊόν του σύστηματος δεν απορροφά το φως.
Για αντιδράσεις οι οποίες διαρκούν αρκετά λεπτά, είναι δυνατόν να αρχίσουν οι μετρήσεις όταν τα αντιδραστήρια έχουν αναμιχθεί σε κατάλληλη θερμοκρασία.
Γρήγορες αντιδράσεις[Επεξεργασία | επεξεργασία κώδικα]
Για ταχύτερες αντιδράσεις, όπου ο χρόνος που απαιτείται για την ανάμιξη των σωμάτων που αντιδρούν ή/και για να έρθουν σε μια καθορισμένη θερμοκρασία είναι συγκρίσιμος ή μεγαλύτερος από την ημίσεια ζωή της αντίδρασης χρησιμοποιούνται ειδικές μέθοδοι για να ξεκινήσει γρήγορα χωρίς αντιδράσεις το αργό βήμα της ανάμιξης. [4] Αυτές περιλαμβάνουν:
Μεθόδους διακοπής ροής, οι οποίες μπορούν να μειώσουν το χρόνο ανάμιξης σε ένα χιλιοστό του δευτερολέπτου.[4][5][6]
Μεθόδους Χημικής διαταραχής όπως το άλμα θερμοκρασίας και το άλμα πίεσης, στις οποίες ένα προ-αναμεμιγμένο σύστημα αρχικά σε ισορροπία διαταράσσεται από την ταχεία θέρμανση ή αποσυμπίεση έτσι ώστε να μην υπάρχει πλέον ισορροπία, και παρατηρείται η επαναφορά πίσω στην ισορροπία.[4][7][8][9] Για παράδειγμα, αυτή η μέθοδος έχει χρησιμοποιηθεί για να μελετηθεί η εξουδετέρωση H3O+ + OH− με χρόνο ημιζωής του 1 μικροδευτερολέπτου ή λιγότερο κάτω από συνήθεις συνθήκες.[4][9]
Η φλάς-φωτόλυση (Flash photolysis), στην οποία ένας παλμός φωτός ή παλμός λέιζερ παράγει εξαιρετικά διεγερμένα μόρια ή συγκροτήματα ατόμων όπως ελεύθερες ρίζες, των οποίων οι αντιδράσεις προκειται να μελετηθούν.
Ισορροπία[Επεξεργασία | επεξεργασία κώδικα]
Ενώ η χημική κινητική ασχολείται με τη ταχύτητα μιας χημικής αντίδρασης, η θερμοδυναμική καθορίζει το βαθμό στον οποίο ολοκληρώνεται η αντιδράση. Σε μία αμφίδρομη αντίδραση, η χημική ισορροπία επιτυγχάνεται όταν οι ταχύτητες της αντίδρασης προς τα δεξιά και προς τα αριστερά γίνουν ίσες οπότε και οι συγκεντρώσεις των αντιδρώντων και προϊόντων παραμένουν σταθερές.
Ελευθερη ενέργεια[Επεξεργασία | επεξεργασία κώδικα]
Σε γενικές γραμμές, η ελεύθερη ενέργεια και η μεταβολή εντροπίας μιας αντίδρασης καθορίζει αν μια χημική μεταβολή θα λάβει χώρα, αλλά η κινητική περιγράφει πόσο γρήγορα η αντίδραση αυτή θα γίνει. Μια αντίδραση μπορεί να είναι εξώθερμη και έχει μια πολύ θετική μεταβολή εντροπίας, αλλά δεν θα συμβεί στην πράξη, αν η αντίδραση είναι πολύ αργή. Εάν ένα αντιδραστήριο μπορεί να παράγει δύο διαφορετικά προϊόντα,το θερμοδυναμικά πιο σταθερό θα είναι το κύριο προϊόν, εκτός από ειδικές περιπτώσεις, όπου η αντίδραση λέγεται ότι είναι υπό κινητικό έλεγχο. Σε τέτοιες περιπτώσεις το θερμοδυναμικά σταθερώτερο προϊόν δεν είναι το κύριο προϊόν λόγω του ότι το ασταθέστερο παράγεται με μεγαλύτερη ταχύτητα.
Η κινητική δράση ισοτόπων είναι η διαφορά στο ρυθμό μιας χημικής αντίδρασης όταν ένα άτομο σε ένα από τα αντιδραστήρια, αντικατασταθεί από ένα ισότοπο.
Η χημική κινητική παρέχει πληροφορίες σχετικά με το χρόνο παραμονής και μεταφοράς θερμότητας σε ένα χημικό αντιδραστήρα στη χημική μηχανική και τη μοριακή κατανομή της μάζας στην χημεία πολυμερών.
Οι Εφαρμογές και τα μοντέλα[Επεξεργασία | επεξεργασία κώδικα]
Τα μαθηματικά μοντέλα που περιγράφουν την χημική κινητική των αντιδράσεων τα χρησιμοποιούν οι χημικοί και οι χημικοι μηχανικοι σαν εργαλεία για να κατανοήσουν καλύτερα και να περιγράψουν χημικές διεργασίες όπως η αποσύνθεση των τροφίμων, η ανάπτυξη μικροοργανισμών, η αποσύνθεση του στρατοσφαιρικού όζοντος, και το σύνολο της χημείας των βιολογικών συστημάτων. Τα μοντέλα αυτά μπορούν επίσης να χρησιμοποιηθούν στον σχεδιασμό ή την τροποποίηση των χημικών αντιδραστήρων για τη βελτιστοποίηση της απόδοσης του προϊόντος, για πιο αποτελεσματικά ξεχωριστά προϊόντα, και για να εξαλειφθούν τα επιβλαβή για το περιβάλλον παραπροϊόντα. Κατά την εκτέλεση καταλυτικής πυρόλυσης βαρέων υδρογονανθράκων σε βενζίνη και ελαφρού αέριο, για παράδειγμα, τα κινητικά μοντέλα μπορούν να χρησιμοποιηθούν για να βρεθεί η θερμοκρασία και η πίεση στην οποία θα προκύψει η υψηλότερη απόδοση της παραγωγής της βενζίνης.
Η χημική κινητική μιας αντίδρασης συχνά διερευνάται και επικυρώνεται μέσω μοντελοποίησης με εξειδικευμένα μαθηματικά πακέτα συνήθων διαφορικών εξισώσεων.[10]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ C.M. Guldberg and P. Waage,"Studies Concerning Affinity" C. M. Forhandlinger: Videnskabs-Selskabet i Christiana (1864), 35
- ↑ P. Waage, "Experiments for Determining the Affinity Law" ,Forhandlinger i Videnskabs-Selskabet i Christiania, (1864) 92.
- ↑ C.M. Guldberg, "Concerning the Laws of Chemical Affinity", C. M. Forhandlinger i Videnskabs-Selskabet i Christiania (1864) 111
- ↑ 4,0 4,1 4,2 4,3 Laidler, K. J. Chemical Kinetics (3rd ed., Harper and Row 1987) p.33-39 ISBN 0-06-043862-2
- ↑ Espenson, J.H. Chemical Kinetics and Reaction Mechanisms (2nd ed., McGraw-Hill 2002), p.254-256 ISBN 0-07-288362-6
- ↑ Atkins P. and de Paula J., Physical Chemistry (8th ed., W.H. Freeman 2006) p.793 ISBN 0-7167-8759-8
- ↑ Espenson,J.H. Chemical Kinetics and Reaction Mechanisms (2nd ed., McGraw-Hill 2002), p.256-8 ISBN 0-07-288362-6
- ↑ Steinfeld J.I., Francisco J.S. and Hase W.L. Chemical Kinetics and Dynamics (2nd ed., Prentice-Hall 1999) p.140-3 ISBN 0-13-737123-3
- ↑ 9,0 9,1 Atkins P. and de Paula J., Physical Chemistry (8th ed., W.H. Freeman 2006) pp.805-7 ISBN 0-7167-8759-8
- ↑ «Chemical Kinetics: Simple Binding: F + G ? B» (PDF). Civilized Software, Inc. Ανακτήθηκε στις 1 Σεπτεμβρίου 2015.

