Σύνδρομο Γουλφ-Πάρκινσον-Γουάιτ
| Σύνδρομο Γουλφ-Πάρκινσον-Γουάιτ | |
|---|---|
 Χαρακτηριστικό κύμα δέλτα (με το βέλος) σε άτομο με σύνδρομο Wolff–Parkinson–White. Παρατηρήστε το βραχύ διάστημα PR. | |
| Ειδικότητα | Καρδιολογία |
| Συμπτώματα | Μη φυσιολογικός ταχύς καρδιακός ρυθμός, αίσθημα παλμών, δύσπνοια, ζάλη, απώλεια αισθήσεων[1][2] |
| Συνήθης έναρξη | Εκ γενετής[1] |
| Αίτια | πρόσθετος αγωγός ηλεκτρικών ώσεων στην καρδιά[1] |
| Διαγνωστική μέθοδος | Το Ηλεκτροκαρδιογράφημα εμφανίζει βραχύ διάστημα PR και ευρύ σύμπλεγμα QRS κύματος δέλτα[3] |
| Θεραπεία | Παρακολούθηση, φαρμακευτική αγωγή, ablation ραδιοσυχνοτήτων[4][5] |
| Πρόγνωση | Ασυμπτωματικό με κίνδυνο θανάτου το 0,5% (παιδιά), 0,1% (ενήλικες[5] |
| Νοσηρότητα | 0,2%[1] |
| Ταξινόμηση | |
Το σύνδρομο Wolff – Parkinson – White ( WPWS ) είναι διαταραχή που οφείλεται σε συγκεκριμένο τύπο προβλήματος με το ηλεκτρικό σύστημα της καρδιάς που οδηγεί σε συμπτώματα. [2] [3] Περίπου το 40% των ατόμων με ηλεκτρικό πρόβλημα δεν εμφανίζουν ποτέ συμπτώματα. [5] Τα συμπτώματα μπορεί να περιλαμβάνουν ασυνήθιστα γρήγορο καρδιακό παλμό, αίσθημα παλμών, δύσπνοια, ζάλη ή συγκοπή . [1] Σπανιότερα μπορεί να εμφανιστεί καρδιακή ανακοπή. Ο πιο κοινός τύπος ακανόνιστου καρδιακού παλμού που εμφανίζεται είναι γνωστός ως παροξυσμική υπερκοιλιακή ταχυκαρδία .
Η αιτία του WPW είναι συνήθως άγνωστη και πιθανότατα οφείλεται σε συνδυασμό τυχαίων και γενετικών παραγόντων. [2] Μικρός αριθμός περιπτώσεων οφείλεται σε μετάλλαξη του γονιδίου PRKAG2 που μπορεί να κληρονομηθεί από τους γονείς ενός ατόμου με αυτοσωμικό επικρατή τρόπο. Ο υποκείμενος μηχανισμός περιλαμβάνει βοηθητικό "μονοπάτι" ηλεκτρικής αγωγιμότητας μεταξύ των κόλπων και των κοιλιών. [1] Συνδέεται με άλλες καταστάσεις όπως η ανωμαλία του Ebstein και η υποκαλιαιμική περιοδική παράλυση . Η διάγνωση του WPW πραγματοποιείται με συνδυασμό αισθήματος παλμών και όταν το ηλεκτροκαρδιογράφημα (ΗΚΓ) εμφανίζει ένα μικρό διάστημα PR και ένα κύμα δέλτα. [3] Είναι τύπος συνδρόμου προ-διέγερσης .
Το σύνδρομο WPW μπορεί να παρακολουθείται ή να θεραπευθεί είτε με φάρμακα είτε με ablation (καταστρέφοντας τους ιστούς) όπως με ablation ραδιοσυχνοτήτων . [4] Επηρεάζει μεταξύ 0,1 και 0,3% του πληθυσμού. [1] Ο κίνδυνος θανάτου σε άτομα χωρίς συμπτώματα είναι περίπου 0,5% ετησίως σε παιδιά και 0,1% ετησίως σε ενήλικες. [5] Σε ορισμένες περιπτώσεις, η μη επεμβατική παρακολούθηση μπορεί να βοηθήσει σε πιο προσεκτικη διαστρωμάτωση κινδύνου των ασθενών σε μια κατηγορία χαμηλότερου κινδύνου. [6] Στα άτομα χωρίς συμπτώματα, η συνεχής παρακολούθηση μπορεί να είναι αιτιολογημένη. Σε άτομα με WPW που περιπλέκονται από κολπική μαρμαρυγή, μπορεί να χρησιμοποιηθεί καρδιομετατροπή ή το φάρμακο προκαϊναμίδη. [7] Η κατάσταση πήρε το όνομά της από τους Λούις Γουλφ (Louis Wolff), Τζον Πάρκινσον (John Parkinson) και Πωλ Ντάντλεϊ Γουάιτ (Paul Dudley White) που περιέγραψαν τα ευρήματα στο ΗΚΓ το 1930. [3]
Σημεία και συμπτώματα[Επεξεργασία | επεξεργασία κώδικα]
Τα άτομα με WPW είναι συνήθως ασυμπτωματικά όταν δεν έχουν γρήγορο καρδιακό ρυθμό. Ωστόσο, τα άτομααυτά μπορεί να παρουσιάσουν αίσθημα παλμών, ζάλη, δύσπνοια ή σπάνια συγκοπή (λιποθυμία ή σχεδόν λιποθυμία) κατά τη διάρκεια επεισοδίων υπερκοιλιακής ταχυκαρδίας . Το WPW σχετίζεται επίσης με πολύ μικρό κίνδυνο ξαφνικού θανάτου λόγω πιο επικίνδυνων διαταραχών του καρδιακού ρυθμού. [8]
Παθοφυσιολογία[Επεξεργασία | επεξεργασία κώδικα]

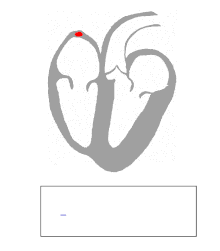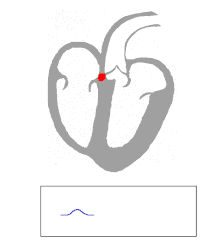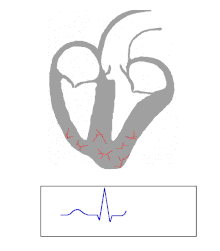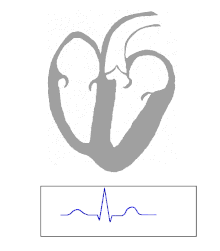
Η ηλεκτρική δραστηριότητα στη φυσιολογική ανθρώπινη καρδιά ξεκινά όταν προκύπτει δυναμικό καρδιακής δράσης στον σινοκολπικό κόμβο (SA), που βρίσκεται στο δεξιό κόλπο . Από εκεί, το ηλεκτρικό ερέθισμα μεταδίδεται μέσω εσωτερικών οδών στον κολποκοιλιακό κόμβο (AV). Μετά από μια σύντομη καθυστέρηση στον κόμβο AV, το ερέθισμα κινειται μέσω της δέσμης His προς τους αριστερούς και δεξιούς κλάδους δέσμης και στη συνέχεια προς τις ίνες Purkinje και στο ενδοκάρδιο στην κορυφή της καρδιάς, και τέλος στο κοιλιακό μυοκάρδιο .
Ο κόμβος AV εξυπηρετεί τη σημαντική λειτουργία ως "φύλακας πυλών", περιορίζοντας την ηλεκτρική δραστηριότητα που φθάνει στις κοιλίες. Σε περιπτώσεις όπου ο κόλπος δημιουργεί υπερβολικά ταχεία ηλεκτρική δραστηριότητα (όπως κολπική μαρμαρυγή ή κολπικό πτερυγισμός, ο κόμβος AV περιορίζει τον αριθμό των σημάτων που άγονται προς τις κοιλίες. Για παράδειγμα, εάν οι κόλποι ενεργοποιούνται ηλεκτρικά με 300 παλμούς ανά λεπτό, οι μισοί από αυτούς τους ηλεκτρικούς παλμύς μπορεί να μπλοκαριστούν από τον κόμβο AV, έτσι ώστε οι κοιλίες να διεγείρονται μόνο με 150 παλμούς ανά λεπτό, με αποτέλεσμα παλμό 150 σφύξεις ανά λεπτό. Μια άλλη σημαντική ιδιότητα του κόμβου AV είναι ότι επιβραδύνει μεμονωμένους ηλεκτρικούς παλμούς. Αυτό παρατηρείται στο ηλεκτροκαρδιογράφημα ως διάστημα PR (ο χρόνος που μεσολαβεί από την ηλεκτρική ενεργοποίηση του κόλπου έως την ηλεκτρική ενεργοποίηση των κοιλιών ), ο οποίος συνήθως μειώνεται σε διάρκεια σε λιγότερο από 120 χιλιοστά του δευτερολέπτου.
Τα άτομα με WPW διαθέτουν ένα βοηθητικό μονοπάτι που επικοινωνεί μεταξύ των κόλπων και των κοιλιών, εκτός από τον κόμβο AV. [9] Αυτό το πρόσθετο μονοπάτι είναι γνωστό ως "πακέτο του Κεντ". Αυτή η βοηθητική διαδρομή δεν μοιράζεται τις ιδιότητες επιβράδυνσης του ρυθμού του κόμβου AV και μπορεί να διεξαγάγει ηλεκτρική δραστηριότητα με σημαντικά υψηλότερο ρυθμό από τον κόμβο AV. Για παράδειγμα, στο παραπάνω παράδειγμα, εάν ένα άτομο είχε κολπικό ρυθμό 300 παλμών ανά λεπτό, η βοηθητική δέσμη μπορεί να άγει όλες τις ηλεκτρικές ώσεις από τον κόλπο έως τις κοιλίες, κάνοντας τις κοιλίες να συστέλλονται με 300 παλμούς ανά λεπτό. Εξαιρετικά ταχείς καρδιακοί παλμοί όπως αυτοί μπορούν να οδηγήσουν σε αιμοδυναμική αστάθεια ή καρδιογενές σοκ . Σε ορισμένες περιπτώσεις, ο συνδυασμός μιας βοηθητικής οδού και μη φυσιολογικών καρδιακών ρυθμών μπορεί να προκαλέσει κοιλιακή μαρμαρυγή, μια κύρια αιτία ξαφνικού καρδιακού θανάτου.
Το WPW μπορεί να σχετίζεται με PRKAG2, ένα ένζυμο πρωτεϊνικής κινάσης που κωδικοποιείται από το γονίδιο PRKAG2 . [10]
Δέσμη του Κεντ[Επεξεργασία | επεξεργασία κώδικα]

Η δέσμη του Κεντ είναι μια μη φυσιολογική έξοδος ή βοηθητική αγωγιμότητα μεταξύ των κόλπων και των κοιλιών που υπάρχει σε ένα μικρό ποσοστό (μεταξύ 0,1 και 0,3%) του γενικού πληθυσμού. [11] [12] [13] Αυτή η οδός μπορεί να επικοινωνεί μεταξύ του αριστερού κόλπου και της αριστερής κοιλίας, οπότε ορίζεται ως «προ-διέγερση τύπου Α», ή μεταξύ του δεξιού κόλπου και της δεξιάς κοιλίας, στην οποία περίπτωση ονομάζεται «προ- διέγερση τύπου Β ". Προβλήματα προκύπτουν όταν αυτή η διαδρομή δημιουργεί ηλεκτρικό κύκλωμα που παρακάμπτει τον κόμβο AV. Ο κόμβος AV είναι ικανός να επιβραδύνει το ρυθμό αγωγής ηλεκτρικών παλμών στις κοιλίες, ενώ η δέσμη του Κεντ στερείται αυτής της ικανότητας. Όταν πραγματοποιείται παρεκκλίνουσα ηλεκτρική σύνδεση μέσω της δέσμης του Κεντ, μπορεί να προκύψουν ταχυαρρυθμίες.
Διάγνωση[Επεξεργασία | επεξεργασία κώδικα]

Το WPW διαγιγνώσκεται συνήθως με βάση το ηλεκτροκαρδιογράφημα σε ασυμπτωματικό άτομο. Σε αυτήν την περίπτωση, εκδηλώνεται ως κύμα δέλτα, το οποίο είναι μια αδρανής ανοδική πορεία στο σύμπλεγμα QRS που σχετίζεται με σύντομο διάστημα PR. Το μικρό διάστημα PR και η συνένωση του συμπλέγματος QRS αντικατοπτρίζουν την ώθηση που φθάνει στις κοιλίες νωρίς (μέσω της βοηθητικής οδού) χωρίς τη συνήθη καθυστέρηση που παρατηρείται στον κόμβο AV.
Εάν ένα άτομο με WPW εμφανίσει επεισόδια κολπικής μαρμαρυγής, το ΗΚΓ εμφανίζει μια ταχεία πολυμορφική ταχυκαρδία ευρέως συμπλόκου (χωρίς torsades de pointes, συστροφή κορυφών). Αυτός ο συνδυασμός κολπικής μαρμαρυγής και WPW θεωρείται επικίνδυνος και τα περισσότερα αντιαρρυθμικά φάρμακα αντενδείκνυνται.
Όταν ένα άτομο έχει φυσιολογικό φλεβοκομβικό ρυθμό, τα χαρακτηριστικά του ΗΚΓ του WPW είναι μικρό διάστημα PR (λιγότερο από 120 χιλιοστά του δευτερολέπτου σε διάρκεια), το διευρυμένο σύμπλεγμα QRS (διάρκεια μεγαλύτερη από 120 χιλιοστά του δευτερολέπτου) με την ανοδική κίνηση του συμπλέγματος QRS και δευτερογενή επαναπόλωση αλλαγές (αντικατοπτρίζονται στο τμήμα ST - αλλαγές κυμάτων T ).
Σε άτομα με WPW, η ηλεκτρική δραστηριότητα που ξεκινά στον κόμβο SA κινείται μέσω της βοηθητικής οδού, καθώς και μέσω του κόμβου AV για την ενεργοποίηση των κοιλιών και από τις δύο οδούς. Δεδομένου ότι η βοηθητική διαδρομή δεν έχει τις ιδιότητες επιβράδυνσης ώθησης του κόμβου AV, η ηλεκτρική ώθηση ενεργοποιεί πρώτα τις κοιλίες μέσω της βοηθητικής οδού και αμέσως μετά μέσω του κόμβου AV. Αυτό δίνει το σύντομο διάστημα PR και την ανοδική κίνηση του συμπλέγματος QRS που είναι γνωστό ως κύμα δέλτα.
Σε περίπτωση προ-διέγερσης τύπου Α (αριστερές κολποκοιλιακές συνδέσεις), θετικό κύμα R εμφανίζεται στο V1 ("θετικό δέλτα") στους προκαταρκτικούς αγωγούς του ηλεκτροκαρδιογραφήματος, ενώ στον προ-διέγερσης τύπο Β (δεξιές κολποκοιλιακές συνδέσεις), κυρίως το αρνητικό κύμα δέλτα φαίνεται στο πρόσθιο τμήμα του V1 ("αρνητικό δέλτα").
Τα άτομα με WPW μπορεί να έχουν περισσότερες από μία βοηθητική οδό – σε ορισμένες περιπτώσεις, έχουν βρεθεί οκτώ ανώμαλες βοηθητικές οδοί. Αυτό έχει παρατηρηθεί σε άτομα με ανωμαλία του Ebstein .
Το σύνδρομο Wolff – Parkinson – White συνδέεται μερικές φορές με την κληρονομική οπτική νευροπάθεια του Leber, μορφή μιτοχονδριακής νόσου . [14]
Στρωματοποίηση κινδύνου[Επεξεργασία | επεξεργασία κώδικα]

Το WPW ενέχει μικρό κίνδυνο ξαφνικού θανάτου, πιθανώς λόγω της ταχείας διεξαγωγής κολπικής μαρμαρυγής που προκαλεί κοιλιακή μαρμαρυγή. Ενώ ο συνολικός κίνδυνος είναι περίπου 2,4 ανά 1000 άτομα έτη, ο κίνδυνος σε ένα άτομο εξαρτάται από τις ιδιότητες της βοηθητικής οδού που προκαλεί προ-διέγερση. [8]
Μπορεί να προταθεί μια διαδρομή αξεσουάρ υψηλότερου κινδύνου από ένα ιστορικό συγκοπής, αλλά η διαστρωμάτωση του κινδύνου πραγματοποιείται καλύτερα με την αξιολόγηση του πόσο συχνά μια διαδρομή μπορεί να προκαλέσει ώθηση στις κοιλίες, συνήθως μέσω προγραμματισμένης ηλεκτρικής διέγερσης (PES) στο εργαστήριο καρδιακής ηλεκτροφυσιολογίας. Αυτή είναι μια επεμβατική αλλά γενικά χαμηλού κινδύνου διαδικασία κατά την οποία οι κόλποι διεγείρονται για να προσπαθήσουν να προκαλέσουν ταχυκαρδία. Εάν μπορεί να προκληθεί ταχυκαρδία που περιλαμβάνει το βοηθητικό μονοπάτι, ο καρδιολόγος μπορεί στη συνέχεια να αξιολογήσει πόσο γρήγορα μπορεί να διεξαχθεί η βοηθητική οδός. Όσο γρηγορότερα μπορεί να διεξαχθεί, τόσο μεγαλύτερη είναι η πιθανότητα το εναλλακτικό μονοπάτι να μπορεί να οδηγήσει αρκετά γρήγορα ώστε να προκαλέσει θανατηφόρα ταχυκαρδία.
Τα χαρακτηριστικά υψηλού κινδύνου που μπορεί να υπάρχουν κατά τη διάρκεια της PES περιλαμβάνουν μια αποτελεσματική ανθεκτική περίοδο της βοηθητικής οδού μικρότερη από 250 ms, πολλαπλές διαδρομές, διάφραγμα τοποθεσίας της οδού και επαγώγιμη υπερκοιλιακής ταχυκαρδίας ( AVRT, κολπική μαρμαρυγή). Άτομα με οποιοδήποτε από αυτά τα χαρακτηριστικά υψηλού κινδύνου θεωρούνται γενικά σε αυξημένο κίνδυνο για SCD ή συμπτωματική ταχυκαρδία και θα πρέπει να αντιμετωπίζονται ανάλογα (π.χ.: ablation). [15]
Δεν είναι σαφές εάν η διεισδυτική διαστρωμάτωση του κινδύνου (με PES) είναι απαραίτητη στο ασυμπτωματικό άτομο. [16] Ενώ ορισμένες ομάδες υποστηρίζουν το PES για διαστρωμάτωση του κινδύνου σε όλα τα άτομα κάτω των 35 ετών, άλλες το προσφέρουν μόνο σε άτομα που έχουν ιστορικό που υποδηλώνει ταχυδυσρυθμία, καθώς η συχνότητα αιφνίδιου καρδιακού θανάτου είναι τόσο χαμηλή (λιγότερο από 0,6% σε ορισμένες αναφορές). [13] [17] [18]
Άλλες μέθοδοι διαστρωμάτωσης του κινδύνου περιλαμβάνουν την παρακολούθηση του κοιλιακού ρυθμού κατά τη διάρκεια της αυθόρμητης κολπικής μαρμαρυγής σε ένα ΗΚΓ 12 μολύβδου. Τα διαστήματα RR μικρότερα από 250 ms υποδηλώνουν υψηλότερη οδό κινδύνου. Κατά τη διάρκεια των δοκιμών άσκησης, η απότομη απώλεια προ-διέγερσης καθώς αυξάνεται ο καρδιακός ρυθμός υποδηλώνει επίσης μια διαδρομή χαμηλού κινδύνου. [8] Ωστόσο, αυτή η προσέγγιση παρεμποδίζεται από τη φυσιολογική βελτίωση στην αγωγή του κόμβου AV κατά τη διάρκεια της άσκησης, η οποία μπορεί επίσης να καλύψει την προ-διέγερση παρά τη συνεχιζόμενη αγωγή κάτω από το αξεσουάρ.
Θεραπευτική αγωγή[Επεξεργασία | επεξεργασία κώδικα]
Άτομα με WPW που αντιμετωπίζουν γρήγορους μη φυσιολογικούς καρδιακούς ρυθμούς ( ταχυδυσρυθμίες ) μπορεί να απαιτούν συγχρονισμένη ηλεκτρική καρδιομετατροπή εάν παρουσιάζουν σοβαρά σημεία ή συμπτώματα (για παράδειγμα, χαμηλή αρτηριακή πίεση ή λήθαργος με αλλοιωμένη ψυχική κατάσταση ). Εάν είναι σχετικά σταθερά, μπορεί να χρησιμοποιηθεί φάρμακο.
Φαρμακευτική αγωγή[Επεξεργασία | επεξεργασία κώδικα]
Τα άτομα με κολπική μαρμαρυγή και ταχεία κοιλιακή απόκριση μπορούν να υποβληθούν σε αγωγή με αμιωδαρόνη [19] ή προκαϊναμίδη [20] για τη σταθεροποίηση του καρδιακού ρυθμού τους. Η προκαϊναμίδη και η καρδιομετατροπή είναι αποδεκτές θεραπείες για τη μετατροπή της ταχυκαρδίας που βρέθηκαν με το WPW. [21] Η αμιωδαρόνη στην κολπική μαρμαρυγή με WPW, συνδέεται με κοιλιακή μαρμαρυγή και συνεπώς μπορεί να είναι χειρότερη από την προκαϊναμίδη.
Οι αποκλειστές κόμβων AV πρέπει να αποφεύγονται σε κολπική μαρμαρυγή και κολπικό πτερυγισμό με WPW ή ιστορικό αυτού. Αυτό περιλαμβάνει αδενοσίνη, διλτιαζέμη, βεραπαμίλη, άλλους αποκλειστές διαύλων ασβεστίου και βήτα αναστολείς . [22] Μπορούν να επιδεινώσουν το σύνδρομο μπλοκάροντας την κανονική ηλεκτρική οδό της καρδιάς (επομένως ευνοώντας την αγωγή κολπικής προς κοιλία 1: 1 μέσω της οδού προ-διέγερσης, πιθανώς οδηγώντας σε ασταθείς κοιλιακές αρρυθμίες).
Ablation με καθετήρα[Επεξεργασία | επεξεργασία κώδικα]
Η οριστική αντιμετώπιση του WPW είναι η καταστροφή της ανώμαλης ηλεκτρικής οδού με ablation . Δύο κύριοι τύποι ablation περιλαμβάνουν ablation με ψύχος ή της ραδιοσυχνότητας (θερμική). [23] Αυτή η διαδικασία πραγματοποιείται από καρδιο ηλεκτροφυσιολόγους. Όταν εκτελείται από έμπειρο ηλεκτροφυσιολόγο, η ablation ραδιοσυχνοτήτων έχει υψηλό ποσοστό επιτυχίας. [24] Τα ευρήματα από το 1994 δείχνουν ποσοστά επιτυχίας έως και 95% σε άτομα που έλαβαν αφαίρεση ablation ραδιοσυχνοτήτων για WPW. [25] Εάν η κατάλυση του ablation ραδιοσυχνοτήτων εκτελείται επιτυχώς, η κατάσταση θεωρείται γενικά θεραπευμένη. Τα ποσοστά υποτροπής είναι συνήθως λιγότερο από 5% μετά από μια επιτυχημένη ablation. Η μόνη προειδοποίηση είναι ότι τα άτομα με υποκείμενη ανωμαλία του Ebstein μπορεί να έχουν πολλαπλές βοηθητικές οδούς λόγω της υποκείμενης συγγενής καρδιακής νόσου.
Ιστορία[Επεξεργασία | επεξεργασία κώδικα]
Η δέσμη του Κεντ ονομάστηκε επώνυμα για τον Βρετανό φυσιολόγο Άλμπερτ Φρανκ Στάνλεϊ Κεντ (1863 – 1958), ο οποίος περιέγραψε πλευρικά κλαδιά στην κολποκοιλιακή αυλάκωση της καρδιάς των πιθήκων (εσφαλμένα πιστεύοντας ότι αυτά αποτελούσαν το κανονικό σύστημα κολποκοιλιακής αγωγής). [26] [27]
Το 1915, ο Φρανκ Νόρμαν Γουίλσον (1890 – 1952) έγινε ο πρώτος που περιέγραψε την κατάσταση που αργότερα ονομάστηκε σύνδρομο Βολφ – Πάρκινσον – Ουάιτ. [28] Ο Άλφρεντ Μ. Ουέντ (1887 – 1967) ήταν ο επόμενος που περιέγραψε την κατάσταση το 1921. [29] Οι καρδιολόγοι Λούις Βολφ (1898 – 1972), Τζον Πάρκινσον (1885 – 1976) και Πωλ Ντούντλεϊ Ουάιτ (1886 – 1973) πιστώνονται με την οριστική περιγραφή της διαταραχής το 1930. [30]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 Reference, Genetics Home (Μαρτίου 2017). «Wolff-Parkinson-White syndrome». Genetics Home Reference (στα Αγγλικά). Αρχειοθετήθηκε από το πρωτότυπο στις 27 Απριλίου 2017. Ανακτήθηκε στις 30 Απριλίου 2017.
- ↑ 2,0 2,1 2,2 «Wolff-Parkinson-White syndrome». rarediseases.info.nih.gov (στα Αγγλικά). 31 Δεκεμβρίου 2012. Αρχειοθετήθηκε από το πρωτότυπο στις 21 Απριλίου 2017. Ανακτήθηκε στις 30 Απριλίου 2017.
- ↑ 3,0 3,1 3,2 3,3 Bhatia, A; Sra, J; Akhtar, M (March 2016). «Preexcitation Syndromes». Current Problems in Cardiology 41 (3): 99–137. doi:. PMID 26897561.
- ↑ 4,0 4,1 Liu, A; Pusalkar, P (29 June 2011). «Asymptomatic Wolff-Parkinson-White syndrome: incidental ECG diagnosis and a review of literature regarding current treatment». BMJ Case Reports 2011: bcr0520114192. doi:. PMID 22693197.
- ↑ 5,0 5,1 5,2 5,3 Kim, SS; Knight, BP (May 2017). «Long term risk of Wolff-Parkinson-White pattern and syndrome». Trends in Cardiovascular Medicine 27 (4): 260–68. doi:. PMID 28108086.
- ↑ Authority, University of Wisconsin Hospitals and Clinics. «Wolff-Parkinson-White Syndrome Clinic». UWHealthkids.org. Ανακτήθηκε στις 22 Μαρτίου 2021.
- ↑ Simonian, SM; Lotfipour, S; Wall, C; Langdorf, MI (October 2010). «Challenging the superiority of amiodarone for rate control in Wolff-Parkinson-White and atrial fibrillation». Internal and Emergency Medicine 5 (5): 421–26. doi:. PMID 20437113. http://www.escholarship.org/uc/item/0tv7016q.
- ↑ 8,0 8,1 8,2 Brugada, Josep; Katritsis, Demosthenes G.; Arbelo, Elena; Arribas, Fernando; Bax, Jeroen J.; Blomström-Lundqvist, Carina; Calkins, Hugh; Corrado, Domenico και άλλοι. (2019-08-31). «2019 ESC Guidelines for the management of patients with supraventricular tachycardiaThe Task Force for the management of patients with supraventricular tachycardia of the European Society of Cardiology (ESC)». European Heart Journal 41 (5): 655–720. doi:. ISSN 1522-9645. PMID 31504425.
- ↑ Authority, University of Wisconsin Hospitals and Clinics. «Wolff-Parkinson-White Syndrome Clinic». UWHealthkids.org. Ανακτήθηκε στις 22 Μαρτίου 2021.
- ↑ Gollob MH (January 2008). «Modulating phenotypic expression of the PRKAG2 cardiac syndrome». Circulation 117 (2): 134–35. doi:. PMID 18195183. http://circ.ahajournals.org/cgi/pmidlookup?view=long&pmid=18195183.
- ↑ «Electrocardiography in the patient with the Wolff–Parkinson–White syndrome: diagnostic and initial therapeutic issues». American Journal of Emergency Medicine 17 (7): 705–14. 1999. doi:. PMID 10597097. https://archive.org/details/sim_american-journal-of-emergency-medicine_1999-11_17_7/page/705.
- ↑ «The prevalence of the Wolff–Parkinson–White syndrome in a population of 116,542 young males» (στα it). Giornale Italiano di Cardiologia 25 (6): 681–87. 1995. PMID 7649416.
- ↑ 13,0 13,1 «A population study of the natural history of Wolff–Parkinson–White syndrome in Olmsted County, Minnesota, 1953–1989». Circulation 87 (3): 866–73. 1993. doi:. PMID 8443907. https://archive.org/details/sim_circulation_1993-03_87_3/page/866.
- ↑ «High incidence of pre-excitation syndrome in Japanese families with Leber's hereditary optic neuropathy». Clinical Genetics 50 (6): 535–37. 1996. doi:. PMID 9147893. http://gateway.ovid.com/ovidweb.cgi?T=JS&PAGE=linkout&SEARCH=9147893.ui.
- ↑ «A randomized study of prophylactic catheter ablation in asymptomatic patients with the Wolff–Parkinson–White syndrome». New England Journal of Medicine 349 (19): 1803–11. 2003. doi:. PMID 14602878.
- ↑ «Survey of current practice of pediatric electrophysiologists for asymptomatic Wolff–Parkinson–White syndrome». Pediatrics 111 (3): e245–47. 2003. doi:. PMID 12612279. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-01-30. https://web.archive.org/web/20110130032458/http://pediatrics.aappublications.org/cgi/content/full/111/3/e245.
- ↑ «The natural history of Wolff–Parkinson–White syndrome in 228 military aviators: a long-term follow-up of 22 years». American Heart Journal 142 (3): 530–36. 2001. doi:. PMID 11526369. https://zenodo.org/record/1236036.
- ↑ John Kenyon. Wolff–Parkinson–White Syndrome and the Risk of Sudden Cardiac Death. Doctors Lounge Website. Available at: «Wolff-Parkinson-White Syndrome and the Risk of Sudden Cardiac Death». Αρχειοθετήθηκε από το πρωτότυπο στις 10 Οκτωβρίου 2010. Ανακτήθηκε στις 7 Οκτωβρίου 2010..
- ↑ Simonian, SM; Lotfipour, S; Wall, C; Langdorf, MI (October 2010). «Challenging the superiority of amiodarone for rate control in Wolff-Parkinson-White and atrial fibrillation.». Internal and Emergency Medicine 5 (5): 421–26. doi:. PMID 20437113. https://escholarship.org/uc/item/0tv7016q.
- ↑ «Atrial fibrillation in the Wolff–Parkinson–White syndrome: ECG recognition and treatment in the ED». Am J Emerg Med 25 (5): 576–83. June 2007. doi:. PMID 17543664. https://archive.org/details/sim_american-journal-of-emergency-medicine_2007-06_25_5/page/576.
- ↑ «23: ECG Abnormalities». The Atlas of Emergency Medicine, 3e.
- ↑ Wald DA (2009). «Resuscitation». Στο: Lex J. Emergency Medicine Q&A (3rd έκδοση). McGraw–Hill. σελ. 4. ISBN 978-0-7216-5944-2.
- ↑ Authority, University of Wisconsin Hospitals and Clinics. «Wolff-Parkinson-White Syndrome Clinic». UWHealthkids.org. Ανακτήθηκε στις 22 Μαρτίου 2021.
- ↑ «Ablation of paroxysmal tachycardia in Wolff–Parkinson–White syndrome» (στα it). Cardiologia 38 (12 Suppl 1): 189–97. 1993. PMID 8020017.
- ↑ «Radiofrequency catheter ablation in patients with Wolff-Parkinson-White syndrome». CMAJ 151 (6): 771–76. September 1994. PMID 8087753.
- ↑ Kent AFS (1893). «Researches on the structure and function of the mammalian heart». Journal of Physiology 14 (4–5): 233–54. doi:. PMID 16992052.
- ↑ Kent AFS (1914). «A conducting path between the right auricle and the external wall of the right ventricle in the heart of the mammal». Journal of Physiology 48: 57.
- ↑ Wilson FN (1915). «A case in which the vagus influenced the form of the ventricular complex of the electrocardiogram». Archives of Internal Medicine 16 (6): 1008–27. doi:. http://archinte.ama-assn.org/cgi/content/summary/XVI/6/1008.
- ↑ Wedd AM (1921). «Paroxysmal tachycardia, with reference to nomotropic tachycardia and the role of the extrinsic cardiac nerves». Archives of Internal Medicine 27 (5): 571–90. doi:.
- ↑ «Bundle-branch block with short P-R interval in healthy young people prone to paroxysmal tachyardia». American Heart Journal 5 (6): 685–704. 1930. doi:. https://archive.org/details/sim_american-heart-journal_1930-08_5_6/page/685.
Εξωτερικοί σύνδεσμοι[Επεξεργασία | επεξεργασία κώδικα]
- Σύνδρομο Γουλφ-Πάρκινσον-Γουάιτ στο Curlie
- Home Genetics Reference: Wolff-Parkinson-White σύνδρομο ( Εθνική Βιβλιοθήκη Ιατρικής των Ηνωμένων Πολιτειών, Bethesda, Maryland)
- Κλινική Wolff-Parkinson-White Syndrome, Πανεπιστήμιο του Ουισκόνσιν - Μάντισον
