Οξικός ανυδρίτης
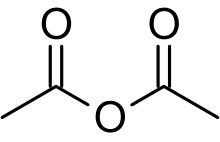
Ο οξικός ανυδρίτης (Acetic anhydride), ή αιθανοϊκός ανυδρίτης[1], είναι η χημική ένωση με το μοριακό τύπο, (CH3CO)2O. Συνήθως, συντομογραφικά αναφέρεται ως Ac2O.
Χαρακτηριστικά[Επεξεργασία | επεξεργασία κώδικα]
Είναι ο απλούστερος απομονωμένος ανυδρίτης που υπάρχει. Είναι ουσιαστικά ανυδρίτης του καρβοξυλικού οξέος και χρησιμοποιείται ευρέως ως αντιδραστήριο στην οργανική σύνθεση.[2] Είναι άχρωμο υγρό, σε κανονικές συνθήκες πίεσης και θερμοκρασίας. Έχει την έντονη οσμή του ξυδιού, παρόμοια με αυτή του οξικού οξέος. Ως χημικό, είναι εξαιρετικά διαβρωτικό για το ανθρώπινο δέρμα και επικίνδυνοι – ερεθιστικοί οι ατμοί του. Διαβρώνει επίσης και τα μέταλλα.
Δομή και ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Ο οξικός ανυδρίτης, όπως όλοι οι ανυδρίτες, είναι ένα πολυδιάστατο και χρήσιμο αντιδραστήριο, με μία μη επίπεδη, τρισδιάστατη χημική δομή.[3] Η σύνδεση δεσμού Pi μέσω του κεντρικού οξυγόνου, προσφέρει πολύ ασθενή σταθεροποίηση συντονισμού, σε σύγκριση με την απώθηση διπόλου-διπόλου μεταξύ των δύο καρβονυλικών οξυγόνων. Τα ενεργειακά εμπόδια στην περιστροφή των δεσμών μεταξύ καθεμιάς από τις επίπεδες διαμορφώσεις είναι αρκετά χαμηλά.[4]

Όπως συμβαίνει με τους οξικούς ανυδρίτες, το καρβονυλικό άτομο άνθρακα στον οξικό ανυδρίτη έχει ηλεκτρονιόφιλο χαρακτήρα.
Πρώτη σύνθεση[Επεξεργασία | επεξεργασία κώδικα]
Η πρώτη σύνθεση οξικού ανυδρίτη έγινε πειραματικά, και τυχαία, το έτος 1852, από τον Γάλλο χημικό Τσάρλς Φρεντερίκ Γκέρχαρντ (Charles Frédéric Gerhardt)[5] (1816-1856), ο οποίος θέρμανε οξικό νάτριο μαζί με βενζοϋλοχλωρίδιο[6]
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
Εργαστηριακά, δύναται να παραχθεί μετά από αντίδραση κονιοποιημένης ποσότητας άνυδρου οξικού νατρίου με ακετυλοχλωρίδιο, με αργή θέρμανση, με λυχνία Bunsen.[7] Βιομηχανικά, ο οξικός ανυδρίτης παρασκευάζεται μετά από καρβονυλίωση του μεθυλεστέρα.[8]
- CH3CO2CH3 + CO → (CH3CO)2O
Ετησίως, περίπου 2,8 εκατομμύρια μετρικοί τόνοι παράγονται σε παγκόσμια κλίμακα.[9]
Τελικές χρήσεις[Επεξεργασία | επεξεργασία κώδικα]
Οι χρήσεις του είναι ποικίλες. Η μεγαλύτερη εφαρμογή του ανυδρίτη αυτού είναι σε αντιδράσεις ακετυλίωσης, ιδίως για ορισμένα σημαντικά χημικά προϊόντα. Λ.χ. βοηθά στη μετατροπή της κυτταρίνης σε οξική κυτταρίνη η οποία αξιοποιείται πολύ σε φωτογραφικά φιλμ και άλλα επικαλυμμένα υλικά. Επίσης, χρησιμοποιείται και για την παραγωγή φίλτρων τσιγάρων.[10] Επίσης, έχει εφαρμογές στη βιομηχανική παραγωγή αγροτικών χημικών ενώσεων, αρωματικών και ορισμένων ποτών.

Στη φαρμακευτική χημεία, είναι σημαντική πρώτη ύλη, ώστε με χημική ακετυλίωση του σαλικυλικού οξέος να παραχθεί η ασπιρίνη. Τα τελευταία χρόνια, ο οξικός ανυδρίτης είναι σημαντικό χημικό αντιδραστήριο σε νέες τεχνολογίες προστασίας του ξύλου και ορισμένων εκ των προϊόντων ξυλείας, μέσω αντίδρασης σε αυτόκλειστο, γνωστές ως ακετυλίωση του ξύλου.[11]
Στη βιομηχανία αμύλου, είναι επίσης ένα συνηθισμένο μέσο ακετυλίωσης και χρησιμοποιείται για την παραγωγή των λεγόμενων, «τροποποιημένων αμύλων» E1414, E1420 και E1422.
Ωστόσο, τόσο στις Ηνωμένες Πολιτείες Αμερικής όσο και σε άλλες χώρες, ο οξικός ανυδρίτης έχει κατηγοριοποιηθεί ως χημικό αντιδραστήριο της λίστας DEA List II, και είναι υπό περιορισμό και αυστηρό έλεγχο, εξαιτίας της συχνής και (συνήθως) παράνομης χρήσης του στη σύνθεση της ηρωίνης (μέσω της χημικής διακετυλίωσης της μορφίνης).[12]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ https://www.britannica.com/science/anhydride
- ↑ https://pubchem.ncbi.nlm.nih.gov/compound/Acetic-anhydride
- ↑ Seidel, R. W.; Goddard, R.; Nöthling, N.; Lehmann, C. W. (2016), «Acetic anhydride at 100 K: the first crystal structure determination», Acta Crystallographica Section C 72 (10): 753–757, doi:, PMID 27703123
- ↑ Wu, Guang; Van Alsenoy, C.; Geise, H. J.; Sluyts, E.; Van Der Veken, B. J.; Shishkov, I. F.; Khristenko (2000), «Acetic Anhydride in the Gas Phase, Studied by Electron Diffraction and Infrared Spectroscopy, Supplemented with ab Initio Calculations of Geometries and Force Fields», The Journal of Physical Chemistry A 104 (7): 1576–1587, doi:
- ↑ https://www.britannica.com/biography/Charles-Gerhardt
- ↑ Charles Gerhardt (1852) “Recherches sur les acides organiques anhydres” (Investigations into the anhydrides of organic acids), Comptes rendus … , 34 : 755-758.
- ↑ http://jupiter.chem.uoa.gr/thanost/zervas/OrgPrep_V.pdf[νεκρός σύνδεσμος]
- ↑ Zoeller, J. R.; Agreda, V. H.; Cook, S. L.; Lafferty, N. L.; Polichnowski, S. W.; Pond, D. M. (1992), «Eastman Chemical Company Acetic Anhydride Process», Catal. Today 13 (1): 73–91, doi:
- ↑ https://www.expertmarketresearch.com/pressrelease/global-acetic-anhydride-market
- ↑ https://www.transparencymarketresearch.com/acetic-anhydride-market.html
- ↑ https://cen.acs.org/articles/90/i32/Making-Wood-Last-Forever-Acetylation.html
- ↑ UN Intercepts Taliban's Heroin Chemical in Rare Afghan Victory, Bloomberg, https://www.bloomberg.com/apps/news?pid=20670001&refer=home&sid=aY1eg_RtBNNU, ανακτήθηκε στις 2008-10-07.
